常见的酸性质
中考化学考点常见酸的主要性质和用途

中考化学考点常见酸的主要性质和用途酸是化学中重要的一类物质,常见的酸有无机酸和有机酸,它们在日常生活和工业生产中都有广泛的应用。
下面将介绍一些常见酸的主要性质和用途。
1.硫酸(H2SO4):硫酸是常用的无机酸之一、它是一种无色、稠密的液体,具有强酸性,具有极强的腐蚀作用。
硫酸广泛用于电池、化肥、制药、纺织等行业。
此外,硫酸还用于水处理、金属清洗和催化反应等。
2.盐酸(HCl):盐酸是无机酸中最常见的一种。
盐酸是一种无色、具有刺激性气味的液体,具有强酸性。
盐酸广泛应用于金属清洗、水处理、酸洗和制备氯化物等。
3.硝酸(HNO3):硝酸是一种强氧化性的无机酸。
它通常是无色或黄色的液体,具有刺激性气味。
硝酸用于制造爆炸品、合成化合物和制造肥料。
此外,硝酸还用于金属清洗、催化剂和溶剂等。
4.醋酸(CH3COOH):醋酸是一种有机酸,也是最常见的有机酸之一、醋酸是无色、具有刺激性气味的液体。
醋酸主要用于食品加工、制药、染料和溶剂等。
5.氯化氢(HCl):氯化氢是无机酸之一、它是一种无色气体,具有刺激性气味和强酸性。
氯化氢主要用于金属清洗、水处理、合成氯化物和酸洗等。
6.磷酸(H3PO4):磷酸是一种无色液体,具有强酸性。
磷酸主要用于制药、农业和食品加工等。
磷酸也用于制备肥料和清洗金属等。
7.碳酸(H2CO3):碳酸是无色液体,具有中等酸性。
碳酸主要用于制备饮料、食品加工和药品制造等。
除了上述常见酸之外,还有许多酸是由特定物质产生的,如植物中的柠檬酸、苹果酸等。
这些酸主要用于食品加工、药物制造和化妆品等。
总的来说,酸有以下几个主要的性质和用途:1.酸具有酸味和酸性。
它可以与碱发生中和反应,产生相应的盐和水。
2.酸具有腐蚀性。
酸可以腐蚀金属和有机物,导致其破坏或腐蚀。
3.酸具有氧化性。
一些酸具有强氧化性,可以促使其他物质发生氧化反应。
酸在日常生活和工业生产中有广泛的应用,如:1.食品加工:醋酸用于制造醋和腌制食品,柠檬酸用于调味品和果汁的调味。
中学常见酸的性质(全)

酸性表现的是溶液或液体的氢离子浓度;氧化性是物质得到电子的能力;强酸是酸中的氢离子几乎完全电离出来的酸;如盐酸/硝酸/高氯酸弱酸只部分电离。
如碳酸/醋酸/氢氟酸“强酸”与“弱酸”可根据酸在一定浓度下的“酸性”来判断;酸都可表现出“氧化性”,但并不一定就是“氧化性的酸”,酸可表现出“氧化性”是因其中的氢离子具有一定的得电子能力;而“氧化性的酸”一般是指酸中除氢以外的元素体现出较强的氧化性,如浓硫酸、硝酸、高氯酸、次氯酸等。
另外注意:氧化性的酸不一定是强酸,如次氯酸;非氧化性的酸不一定是弱酸,如盐酸;强腐蚀性的酸也不一定是强酸,如氢氟酸;但强酸通常都会有强腐蚀性(主要是酸性起的作用)酸中主要元素的非金属性越强,对应的酸的酸性越强。
中学常见弱酸强弱记诵口诀(从前到后酸性逐渐变弱,只考虑第一级电离的比较)亚硫酸>磷酸>氢氟酸,亚硝酸>甲酸>冰醋酸,碳酸>氢硫酸>氢氰酸。
即H2SO3>H3PO4>HF>HNO2>HCOOH>CH3COOH>H2CO3>H2S>HCN其他常见酸如HClO4, H2SO4,HNO3,HI,HBr都是强酸,强酸在水里视作酸性等同(水的拉平效应,使得强酸一级电离完全)碱性:Fe(OH)2>Fe(OH)3>Cu(OH)2规律:0。
总原则——根据碱的电离常数的大小:碱的电离常数越大,该碱的碱性越强。
推论:金属阳离子的水解常数越大,由该金属原子在该价态组成的氢氧化物的碱性越弱。
1。
金属元素的电负性越小,该金属的最高价氧化物对应的水化物(即氢氧化物)的碱性越强。
推论(更具操作性):A)一般金属活动性越大(即金属活动性顺序表中排位越靠前),该金属的最高价氧化物对应的水化物(即氢氧化物)的碱性越强。
可得出:Fe(OH)3>Cu(OH)2B)元素周期表中,同周期的金属{主族}元素随着原子序数的递增,该金属的最高价氧化物对应的水化物(即氢氧化物)的碱性越弱;同周期的金属{副族}元素随着原子序数的递增,该金属的最高价氧化物对应的水化物(即氢氧化物)的碱性越弱;同周期的金属主族与副族元素之间不能应用此规律。
常见的酸(酸的化学性质及通性)

常见的酸(酸的化学性质及通性)一、酸的定义和分类酸:物质溶于水时,形成的阳离子全部是H+的化合物。
由于酸、碱、盐溶于水时会电离出阴、阳离子,所以酸、碱、盐的水溶液具有导电性。
酸的电离:HCl=H++Cl-,H2SO4=2H++SO42-二、常见的酸浓硫酸的特性:吸水性、脱水性、强氧化性、腐蚀性。
盐酸、硝酸、醋酸具有挥发性;碳酸不稳定,容易分解成二氧化碳和水。
硝酸、硝酸银见光易分解,所以它们要放在棕色试剂瓶中。
浓硫酸的稀释操作:酸入水,要搅拌,“杯壁下流”三、酸的化学性质酸有相同的化学性质是因为酸在水中都能电离出H+,有不同的化学性质是因为能电离出的酸根离子不同。
1. 酸溶液能使酸碱指示剂变色:使紫色石蕊溶液变红。
2. 酸+活泼金属→盐+氢气(置换反应)a) 这里不包括浓硫酸和硝酸。
b) Fe+2HCl=FeCl2+H2↑Fe+H2SO4=FeSO4+H2↑【现象】铁表面有气泡产生;溶液由无色逐渐变为浅绿色3. 酸+金属氧化物→盐+水(复分解反应)a) 金属氧化物可以是活泼金属的氧化物和不活泼金属的氧化物。
因为生成物有水,符合复分解反应的发生条件,所以反应一定发生。
b) Fe2O3+6HCl=2FeCl3+3H2O Fe2O3+3H2SO4=Fe2(SO4)3+3H2O【现象】铁锈逐渐溶解消失;溶液由无色逐渐变成黄色c) CuO+2HCl=CuCl2+H2O CuO+H2SO4=CuSO4+H2O【现象】黑色粉末逐渐溶解消失;溶液由无色逐渐变成蓝色4. 酸+碱→盐+水(复分解反应、中和反应)5. 酸+盐→新酸+新盐(复分解反应)a) 反应发生的条件:①新酸是碳酸;②如果新酸不是碳酸,新盐必须是沉淀。
b) 碳酸盐都能与酸反应:CaCO3+2HCl=CaCl2+H2O+CO2↑c) 除硫酸钡以外的钡盐都能与硫酸反应:BaCl2+H2SO4=BaSO4↓+ 2HCld) 硝酸银能与盐酸反应:AgNO3+HCl=HNO3+AgCl↓。
常见的酸的物理性质
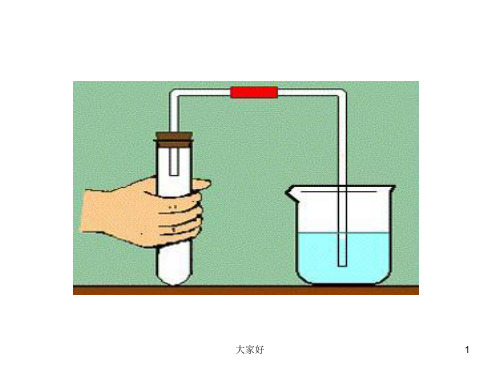
3·打开浓盐酸的试剂瓶,会挥发出有刺
激性气味的气体,在瓶口有白雾形成,
因此浓盐酸具有挥发性.
大家好
10
4.浓盐酸在空气中会生成白雾,是因为 从浓盐酸中挥发出来的氯化氢气体跟空 气中的水蒸气接触,形成盐酸小液滴, 它反映了氯化氢极易溶于水的性质,也 反映了盐酸极易挥发的性质。
5.如果浓盐酸敞口放置,由于浓盐酸具 有挥发性,因而会导致溶液质量和溶液 中溶质的质量分数都减小。
3.下列化学实验操作正确的是( B )
A.稀释浓盐酸时,把水倒入盛有浓盐酸的量筒中
B.用天平称量药品时,药品不能直接放在托盘上
C.用滴管滴加液体时,需将滴管伸入试管内
D.把烧杯放在铁圈上直接加热
4.下列物质在空气中放置一段时间后质量会增加的是
A.浓盐酸 B.浓硝酸 C.浓硫酸 D.碳酸 大家好
(C ) 13
2.盐酸是__H_C_l_气体的水溶液,工业盐酸常呈__黄_ 色, 打开浓盐酸的瓶塞,会在瓶口看见_白__雾__。这是因为
浓盐酸挥发出的_氯__化__氢__与空气中的_水__蒸__气__结合形成 盐酸小液滴的缘故、浓盐酸露置在空气中—段时间后,
溶质质量会_____减_,少溶质的质最分数会___ 减。少
大家好
11
思考:Байду номын сангаас
1.磷在氧气中燃烧会产生 白烟,和白雾有什么区别?
2.若要提高某稀盐酸的浓度,能否采用 蒸发的方法? 因为浓盐酸具有挥发性,
蒸发时氯化氢气体会和水一起蒸发。
3.区分实验室浓盐酸、稀盐酸和工业 盐酸? 颜色和挥发性
大家好
12
1.在空气中打开试剂瓶瓶塞时,瓶口有白雾生成的是
A.浓盐酸 B.浓硫酸, C.酒精, D.蒸馏水 ( A )
常见的酸

、 、
、 、
+
HNO HCl HClO 3 3 一元酸 CH3COOH HF H2S
三元酸 H3PO4
连线题:把相关的内容之间 用短线连接起来;
二元无氧酸 一元含氧酸 氢 硫 酸 二元含氧酸 氢 氯 酸
HNO3 H2SO4 H2S
HCl
现有HCl、HF、H2CO3、H3PO4四 种酸,分别把它们归类并命名。 无 氧 酸 HCl、HF H CO 、 H PO 3 4 含氧酸 2 3
你能试着读出这些酸 的名称吗? 命名 含氧酸 某酸 H2SO4 H2CO3 H3PO4 HClO3 HNO3 命名 氢某酸 无氧酸 HCl H2S HF
酸
H SO HNO HClO 2 4 3 3 含氧酸 H3PO4 CH3COOH 是否 含氧 无氧酸 H S HCl HF
2
H的 二元酸 H2SO4 个数
1.无色、粘稠、油状液体; 2.难挥发;
3.特性:有强烈的吸水性、氧化性、脱水性和腐蚀性。 4.浓硫酸的稀释: 会放出大量的热。
一定要把浓硫酸沿器壁慢慢注入水里,并不断 搅动,使产生的热量迅速的扩散。切不可把水 倒进浓硫酸里。
你想怎样给酸分类?
H2SO4 HNO3 H3PO4 HClO3
HCl H 2S HF CH3COOH
第二节 一、盐酸
酸和碱的性质
(一)浓盐酸的物理性质
1.纯净的浓盐酸是无色液体,有刺激性气味,有 酸味。 2.工业盐酸常因含有杂质带黄色。(Fe3+)
3.浓盐酸有挥发性:在瓶口能形成白雾。 原因:从浓盐酸挥发出来的氯化氢气体跟 空气里的水蒸汽接触,形成盐酸的 小液滴的缘故。
常见酸的性质

解。
几乎所有的硫化物也都可被硝酸溶解,但应先加入盐酸,使硫以H2S的形式挥发出去,以免单质硫将试样裹包,影响分解。
③硫酸(H2SO4)除钙、锶、钡、铅外,其它金属的硫酸盐都溶于水。
热的浓硫酸具有很强的氧化性和脱水性,常用于分解铁、钴、镍等金属和铝、铍、锑、锰、钍、铀、钛等金属合金以及分解土壤等样品中的有机物等。
硫酸的沸点较高(338℃),当硝酸、盐酸、氢氟酸等低沸点酸的阴离子对测定有干扰时,常加硫酸并蒸发至冒白烟(SO3)来驱除。
硫酸能将物质里的H、O元素以2:1脱去。
④磷酸(H3PO4)磷酸根具有很强的配位能力,因此,几乎90%的矿石都能溶于磷酸。
包括许多其它酸不溶的铬铁矿、钛铁矿、铌铁矿、金红石等,对于含有高碳、高铬、高钨的合金也能很好的溶解。
单独使用磷酸溶解时,一般应控制在500~600℃、5min以内。
若温度过高、时间过长,会析出焦磷酸盐难溶物、生成聚硅磷酸粘结于器皿底部,同时也腐蚀了玻璃。
⑤高氯酸(HClO4)热的、浓高氯酸具有很强的氧化性,能迅速溶解钢铁和各种铝合金。
能将Cr、V、S等元素氧化成最高价态。
高氯酸的沸点为203℃,蒸发至冒烟时,可驱除低沸点的酸,残渣易性质:仅知存在于某些溶剂中。
很不稳定,45℃分解,很易快速分解为硫酸、硫、硫化氢、多硫化氢和二氧化硫(混合物)。
硫代硫酸可看成是硫酸分子中的一个氧原子被硫原子所代替的产物。
两个硫原子的平均氧化数为+2。
其中一个硫原子氧化数为+6,另一个硫原子氧化数为-2,因此硫代硫酸及其盐类具有一定的还原性。
硫代硫酸根酸离子在碱性条件下很稳定,有很强的络合能力。
硫代硫酸可在低温(-78℃)下,在乙醚等有机溶剂(-78℃)或无溶剂(10℃以下)中用干燥的氯化氢处理(酸化)无水硫代硫酸钠而得(不能在水溶液中!);或者在0℃和无水条件下,在乙醚中使三氯化硫与硫化氢反应而制得。
由于它很不稳定,故仅用其盐。
主要用作还原剂、定影剂和络合剂等。
对于初中生,只要求掌握盐酸、硝酸、硫酸的一些简单的化学性质,比如酸的通性:使紫色石蕊试液变红、能和碱生成盐和水、能和碱性氧化物生成盐和水。
_酸及其性质

注意:单质的铁和酸反应只 过一会,铁钉表面有气泡冒出
能生成+2价的亚铁
化合物的铁和酸反应,反应 前后铁元素的化合价不变
Fe+ 2HCl =FeCl2 + H2↑
二、酸的化学性质
实验探究
实验内容
将稀盐酸加入 碳酸钠粉末中
在稀盐酸中加 入硝酸银溶液
在稀盐酸中加 入氯化钡溶液
现象与结论 Na2C有O气3+泡2H产C生l=2NaCl+H2O+CO2↑
的存在。
Fe2O3+6HCl=2FeCl3 +3H2O
Na2CO3+2HCl=2 NaCl +H2O+CO2↑
HCl+AgNO3 = AgCl↓+HNO3
复分解 反应
k2CO3+2HCl = 2 KCl +H2O+CO2↑
如果把上述实验中的稀盐酸换成稀硫酸, 你认为是否会产生类似的实验现象?
请试着写出这些反应的化学方程式。
(1)浓盐酸无色、刺激性 (1)浓硫酸无色、粘稠、
气味的液体
油状的液体
(2)浓盐酸有挥发性。 (2)浓硫酸可做气体的干燥剂
浓盐酸需密封保存
浓硫酸需密封保存
(3)浓盐酸有腐蚀性 (3)浓硫酸有强烈的腐蚀性
(4)浓硫酸溶于水放热
除盐酸和硫酸外,
常见的酸还有硝酸( HNO3 )、 醋酸( CH3COOH )
CaCO3+2HCl=CaCl2+CO2↑ +H2O
CaCO3+H2SO4=CaSO4+CO 2↑+H2O
盐酸和稀硫酸为什么具有相似的化学性质?
盐酸 HCl = H+ + Cl硫酸 H2SO4 = 2H+ + SO42硝酸 HNO3 = H+ + NO3-
一常见的酸几种常见的酸物理性质

THANKS FOR WATCHING
感谢您的观看
硝酸具有强腐蚀性,能与多种物质发生反应,如金属、有机物等。
硝酸的化学性质
硝酸具有强氧化性,能与许多物质发 生氧化还原反应。
硝酸能与某些金属反应,生成相应的 金属盐和氮气。
硝酸是一种强酸,能与碱发生中和反 应。
硝酸的应用
硝酸在工业上广泛用于制造化肥、 染料、炸药等。
硝酸在化学实验中常用于制备其 他含氮化合物。
硫酸在金属加工中用于清洗金 属表面的氧化物和杂质。
02 盐酸
盐酸的物理性质
1
盐酸是无色液体,有刺激性气味。
2
盐酸的相对密度为1.188,熔点为-107.5℃,沸 点为108.6℃。
3
盐酸易溶于水,溶解时放出大量的热。
盐酸的化学性质
盐酸是强酸,具有强 腐蚀性,能与金属、 金属氧化物、碱等反 应。
氧化性
磷酸在一定条件下具有氧化性,能与某,能使糖类物质脱水生成单糖或 双糖。
磷酸的应用
肥料生产
磷酸是农业生产中常用的 肥料之一,主要用作磷肥, 能促进植物生长和发育。
食品添加剂
磷酸在食品工业中用作酸 度调节剂、抗氧化剂等, 能延长食品的保质期。
化学工业
磷酸在化学工业中用于生 产各种磷酸盐、磷肥、农 药等,是重要的化工原料。
常见的酸及其物理性质
• 硫酸 • 盐酸 • 硝酸
目录 • 磷酸
01 硫酸
硫酸的物理性质
01
02
03
04
硫酸是无色油状液体, 具有强烈的刺激性气味。
硫酸的沸点很高,不易 挥发。
硫酸的凝固点很低,在 低温下容易结冰。
硫酸的相对密度较大, 约为1.84g/cm³。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
紫色石蕊溶液变红色
无色酚酞溶液不变色
结论:酸能与指示剂反应
金属与盐酸反应的比较
(3)向装了生锈铁钉的两只试管中分别倒入稀盐酸和稀硫酸,观察铁钉表面和 溶液颜色有 什么变化?
现象
化学方程式
铁锈+盐酸
Fe2O3 + 6HCl == 2FeCl3+ 3H2O
铁锈+硫酸
Fe2O3 +3H2SO4==Fe2(SO4)3+3H2O
小木条变黑
将浓硫酸滴到 布变黑甚至烧成洞
一小块布上
浓硫酸能夺取纸张、
木材、皮肤(都由含 碳、氢、氧等元素组 成的化合物)里的 “水分” ( 氢、氧元 素 ), 生成黑色的炭
化学变化
[实验10]稀释浓硫酸的正确操作:
手的感觉 分析
发热 浓硫酸溶于水放热
点拔:水的 密度较小, 浮在浓硫酸 上面,且浓 硫酸溶于水 放出大量热, 使水沸腾。
结论:酸能与某些金属氧化物反应 生成水和盐
小结:酸具有的一些相似化学性质
❖ (1)酸能使紫色石蕊溶液变红,不能使无 色酚酞溶液变色。
❖ (2)酸能与镁、铝、锌、铁等活泼金属反 应,生成氢气和盐
❖
Zn + 2HCl = ZnCl2 + H2↑
❖ (3)酸能与某些金属氧化物反应,生成水
和盐
❖
Fe2O3 + 6HCl = 2FeCl3 + H2O
讨论:
敞口久置于空气中的浓硫酸和浓盐酸,各成分怎样变化?
溶质质量 溶剂质量 溶液质量 溶质质量分数
浓盐酸 减小 浓硫酸 不变
不变 增大
减小 增大
提示: 由于浓硫酸有吸水性,实验室常用来作干燥剂 浓盐酸具有挥发性
减小
减小
如果不慎将浓硫酸沾到皮肤或衣服上,应如何处理?
先用大量的水冲洗,而后涂上碳酸氢钠 稀溶液。
如果将稀硫酸沾到皮肤或衣服上,是否也要进行这样的处理?
用大量的水冲洗。
酸的化学性质
(1)如下图所示,在白色点滴板 上进行实验,并观察现象。
稀盐酸 稀硫酸
加紫色石蕊溶液 加无色酚酞溶液
紫色石蕊溶液变红色
无色酚酞溶液不变色
引入新课
食醋为什么会有酸味? 这些水果为什么都有酸味?
CH3COOH
你已经知道哪些酸?了解
它们的性质吗?它们在生产、
你知道吗
生活中有哪些应用?
1、人的胃液里含有盐酸 2、汽车电瓶里含有硫酸 3、食醋里含有醋酸
第十单元 酸 和 碱
课题1 常见的酸和碱 第二课时
二. 常见的酸
[ 实验10-2]
颜色 状态
浓盐酸
无色液体
打开瓶盖 后的现象
有白雾出现
气味
有刺激性气味
浓硫酸
无色;粘稠、油状、液体
无现象 无气味
白雾产生的原因:浓盐酸挥发出来的 氯化氢气体遇到空气中的水蒸气形成盐酸 小液滴。
[实验10-3]浓硫酸的腐蚀性
实验
放置一会儿后的现象
分析
用玻璃棒蘸 纸上出现黑字
浓硫酸在纸上写字
用小木棍蘸 少量浓硫酸
