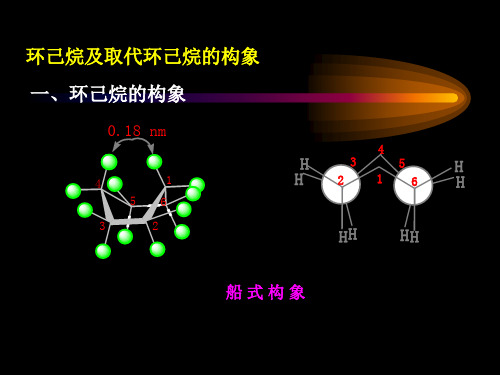
环己烷的构象
环己烷的四种典型构象

环己烷的四种典型构象
环己烷是一种环烷烃,分子式为C6H12,由六个碳原子和十二个氢原子组成。
环己烷具有一个六元环的结构,有许多构象。
其中,四种典型的构象为:
1.船形构象:又称弯曲构象,分子呈现出一个V形的结构,两个碳原子之间的距离较近。
船形构象是环己烷的最不稳定的构象,因为分子内部的张力很大。
2.椅形构象:分子呈现出一个六边形的结构,相邻的两个碳原子之间呈现出一个六角星的形状,分子结构较为稳定。
3.锥形构象:分子呈现出一个尖锥形结构,相邻的两个碳原子之间的距离较远。
锥形构象是一种高能量状态的构象,只在极短的时间内存在。
4.扭曲椅形构象:又称为扭曲构象,分子呈现出一个六边形的结构,其中两个对称的碳原子上的氢原子以对称轴为对称对调位置。
这种构象是中等稳定的,可以保持一段时间。
以上四种典型的构象在环己烷分子中不停地交替出现,其中椅形构象是最稳定的构象,可以用来描述环己烷的大部分化学反应。
环己烷构象
4. 环己烷的半椅式构象
5 4 3 2 6 1
三个全重叠 三个邻交叉
四个全重叠 两个邻交叉
半椅式构象是用分子力学计算过渡态的几何形象时提出的。 构象分布:环己烷椅式构象 : 环己烷扭船式构象 = 10000 : 1
CH3
5
CH3
3
6 2
1
4
பைடு நூலகம்
顺 式 :
H
5 3 2
6 1
CH3 H
CH3 H
4
H
a、a 键
CH3
5
e、e 键
H
3
6 2
1
4
反 式 :
H
5 3 2
6 1
4
H
CH3 H
CH3
CH3 a 、e 键 a 、e 键
环己烷的扭船式构象
4 H H H H H H H H H H H H 5 4 5 3 2 3 6 2 1 4 6 3 6 1 4 5 5 2 2 1 3 6 1
H
1 2
H H
4
2
H
二、取代环己烷的优势构象 1.一取代环己烷
非键张力大 H
5 4
CH3 H
3 6 2 1
H
H
4
5 3 2
6 1
H
CH3 H
5 4
3
CH3
1 2 4 2 3 5 1 6
CH3
6
H
H
结论: 取代 基处 于e 键稳 定。
2.二取代环己烷
(1) 1,2-二取代环己烷
CH3
5 6 3 2 1
18nm123456123456hhhhhhhh船式构象123456hhhhhhhhhhh123456hhhhhhhhhhh183a227a250a锯架式纽曼式ae键键环己烷的六个碳原子构成两个平面六个ae键分别为三上三下同一碳原子若a键在上e键必然在下123456ae键可以相互转化
环己烷构象

环己烷构象本文由南通润丰石油化工整理椅型环己烷分子。
红色为直键氢原子,蓝色为平键氢原子。
历史背景很早就有人提出环己烷可能不是平面型结构。
1890年,德国人赫尔曼·萨克森(Hermann Sachse)提出通过折纸来构建环己烷“对称”和“非对称”结构(即现椅型和船型结构)的方法,从他的文章可以感受出,他已经知晓这些构象有两种不同的氢原子(即现直键氢和平键氢)以及两种椅型结构可能会相互转化,甚至还意识到两种椅型结构的分布可能受环上某些取代基的影响。
不过他的文章没有获得化学家的足够重视,一方面是文章的数学成分太多,难以理解,另一方面则是他的文章没有发表到主要的期刊上。
1893年仅31岁的萨克森去世,他的研究也就此结束。
直到1918年恩斯特·摩尔(Ernst Mohr)用新问世的X射线晶体学技术测定金刚石结构时,才发现所得结构中的基础结构单元正是萨克森预测过的椅型结构,才使环己烷构象研究重新进入焦点之中。
椅型构象sp3杂化的碳原子是四价的,键间角度为109.5°,所以环己烷不是平面的键角120°的正六边形结构,而是采取多种三维的构象。
椅型构象描述的是普通状态环己烷最稳定的构象,25度时99.99%的环己烷分子都是这种构象。
德里克·巴顿和奥德·哈塞尔因对环己烷和其他分子构象的研究而获得诺贝尔化学奖。
能量最低的椅型构象中,12个氢原子中有6个处于竖直方向(红色)——这些碳-氢键互相平行,呈轴向排列,分列环上下,称为直键。
另6个氢处于近似水平方向(蓝色)——这些碳-氢键大致平伏,分别稍向下和向上翘起,称为平键。
对于同一碳原子来说,若与它相连的直键氢是向上的,则平键氢稍向下,反之亦然。
观察可知,对于连有向上直键、稍向下平键的碳原子,与其相邻的两个碳原子必然连有向下直键和稍向上平键。
而且环中相对碳原子所连平键和直键的方向也必然是分别相反的(如H1和H4)。
6.2.3 环己烷的构象翻转

H AH BH AH B123456123456234613456半椅式构象中,1,2,3,4四个C 原子在同一个平面上,另两个C 原子(5,6)分别位于该平面的上方和下方。
半椅式构象是用分子力学计算过渡态的几何形象时提出的,是环己烷分子势能最高、最不稳定的构象;与椅式构象之间的势能差约为46kJ/mol 。
2)半椅式构象(Half-chair conformation )H A H B H A H B 123456123563) 扭船式构象(Twist-boat or skew-boat conformation )AB123561245H AH B扭船式构象中,所有的二面角都是30℃,所有的对边都是交叉的。
由椅式构象转变为扭船式构象,需要经历一个半椅式构象。
H H HHH143256123456扭船式构象比椅式构象不稳定,能量差为23.5kJ/mol 。
A H 123456124A B4)船式构象(Boat conformation )1,3,4,6四个C 原子共平面;另两个C 原子(2,5)在这一平面的同一侧;123456123564123456H HHH HH H H H HH H1456321,6和3,4分别为全重叠;1,2、2,3、4,5、5,6分别为邻位交叉。
因此,船式构象不如椅式构象稳定,两者之间的势能差约为29kJ/mol 。
船式构象中,2、5上两个H 原子(称为“旗杆氢”原子)相距较近(183pm ),存在非键空间张力;无键角张力。
1,6和3,4为全重叠式,存在键扭转张力。
H HHH HH HHHH 1234566.2.3 环己烷的构象翻转扭船式构象中,两个“旗杆”H 原子间的距离相对较远,非键空间张力小,因此比船式构象稳定,两者之间的势能差为5.4kJ/mol 。
H H H H HHH1432566.2.3 环己烷的构象翻转H AH BH AB123456123561245A B6312356235641234561245A B63123456AB12356H AH B6.2.3 环己烷的构象翻转船式椅式椅式扭船式半椅式半椅式扭船式势能23.5kJ/mol 46 kJ/mol6.2.3 环己烷的构象翻转6.2.3 环己烷的构象翻转总结:环己烷的椅式构象可以通过C–C键的旋转变成另一个椅式构象,a键和e键随之转换;此过程称为“构象翻转”(Conformational inversion),相应的两个椅式构象互称为“构象转换体”。
环己烷的构象

环己烷的构象
环己烷是一种六元环有机化合物,化学式为C6H12,它由六个碳原子和十二个氢原子构成,其中每个碳原子都与两个相邻的碳原子和两
个氢原子共形成四个共价键。
环己烷的最稳定的构象为椅形结构,在该结构中,六个碳原子组
成一个六角形,并且在这个六角形的上方和下方各有三个碳原子,这
些碳原子呈现出交错排列的形式。
椅形结构的环己烷分子如同一个椅子,因此称之为“椅状构象”,这种构象下的环己烷稳定性最高,且
相对地容易被取代反应,因此被广泛应用于有机合成中。
另一种环己烷构象是船形结构,其中碳原子按照类似船底的形状
排列。
这种构象相对于椅形结构来说不太稳定,因为其中两个碳原子
太近,容易引起反式构型相互作用的影响。
此外,环己烷还可能形成
扭曲构象,在这种构象下,环己烷分子呈现出扭曲的形状。
环己烷的构象对于它的性质和应用具有重要影响。
例如,在某些
有机化学反应中,需要采用椅形构象才能有效进行反应。
此外,环己
烷还可以作为溶剂、润滑剂、燃料等应用于许多领域。
总之,环己烷所具有的不同构象对它的性质和应用有着重要影响,了解环己烷的构象,有助于研究其在有机合成和其他领域中的应用。
环己烷能量最高的构象

环己烷能量最高的构象说到环己烷,大家首先可能会想到它的分子结构,这个环状的分子是不是看起来有点像个“指环王”?其实它的形态和我们的耳朵或者是手指的戒指差不多,是一个闭合的六角环。
那么问题来了:这个环己烷到底是怎么转动的?是不是永远都保持同一个姿势?嘿嘿,答案可不简单呢。
要知道,环己烷这小子可不是什么老老实实、死气沉沉的家伙。
它的构象(也就是它的立体结构)是可以不停变换的,这也正是它有趣的地方。
环己烷分子就像一辆摩托车,可以“翻转”自己,随时换个姿势。
这是因为环己烷是个非常灵活的分子,它的结构并不固定,总是会调整自己去找到能量最少的“懒人模式”。
它可不像我们天天拖着疲惫的身躯,硬生生呆在同一个地方不动。
环己烷有时候是“椅子”形状,有时候是“船”形状,还有时候是“扭曲”的,反正它从来不会停下动作。
说到环己烷最舒服的姿势,嘿,这就得提到最稳定的构象了,也就是我们常说的“椅子”形态。
想象一下你在沙发上躺着,舒服地伸展身体,完全没有任何压力。
嗯,就是那种“摊着”的感觉。
环己烷的“椅子”形状就是六个碳原子围成一个六边形,而其中两个碳原子会稍微向外“翘”一下,好像在休息时把手脚伸开,整个分子看起来就像一把轻松的椅子。
这个构象的稳定性超强,因为它最大限度地避免了碳原子之间的碰撞,减少了能量,就像我们躺在床上不用担心床板塌了,舒服得不能再舒服。
不过啊,环己烷并不是永远都只呆在这个“椅子”形态。
它是个非常善变的家伙,能不停地从一个构象转换到另一个。
有时候它会变成“船”形。
想象一下你划船时,船的两端高高翘起,形成一个类似于倒V字形的结构。
这时候,环己烷的六个碳原子就会呈现出一个不太稳定的形状。
说实话,虽然船形也能保持一定的结构稳定性,但相较于椅子形,它显得有点“摇摇晃晃”。
就像是你坐船坐得有点不安稳,随时可能被晃到水里一样,能量有点高。
至于环己烷的“扭曲”形态,那就是更为不稳定的一种了。
虽然从化学上看,环己烷的分子在转到这种状态时可以尝试去“躲避”某些物理障碍,但是它的能量还是不低。
环己烷构象环己烷非常稳定

C
环丙烷
C
105.5 。
C
109.5 丙
。 烷
C
香蕉键
C
C
由此可见:
(1) 环丙烷中键的重叠程度小,稳定性减小 。 (2) 电子云分布在两核连线的外侧,增加了试
剂进攻的可能性,故具有不饱和烯烃的性质。
环丙烷的构象
环丁烷的构象
蝶式
环戊烷的构象
信封式
2.环己烷构象
环己烷非常稳定,与溴只发生自由基取代 (与烷烃相似)而不开环 环己烷单元CH2燃烧热与开链烷烃相同, 这与环己烷的构象有关 两种典型的构象:船式构象和椅式构象
8
664
659
单元CH2的燃烧热↑,环的稳定性↓。
◆由小环→大环单元CH2燃烧热逐渐降低, 到环己烷趋于稳定
环的稳定性: 小 环(环丙烷) 依次 普通环(环己烷)
◆为什么小环化合物不稳定? Baeyer理论 —— 张力学说(1885年提出):
。 109.5 。 60 。 24 44'
随着环的扩大,张力ຫໍສະໝຸດ +O2 cat
3.加成反应:小环(C3,C4)特性 (1)催化加氢
Ni 。 80 C + H2 Ni 。 120 C Pt 。 300 C
开 环 加 CH3CH2CH3 氢 的 难 CH3CH2CH2CH3 度 逐 渐 增 CH3CH2CH2CH2CH 3 大
用Ni催化难以反应
2. 加X2
+ Br2 CCl4 室 温 BrCH2CH2CH2Br 可与烷烃区别开来
Drill (练习): 用化学方法鉴别以下五种化合物:
CH3C≡CH A B CH3CH=CH2 D E C
褪色 CH3CH=CH2 Br2/CCl4 CH3C≡CH
环己烷构象翻转 -回复

环己烷构象翻转-回复"环己烷构象翻转"环己烷是一种有机化合物,化学式为C6H12。
它是由六个碳原子和十二个氢原子组成的六元环烷烃,具有多种不同的构象。
当其中一个碳原子周围有两个碳原子时,环己烷就发生了构象翻转。
本文将一步一步回答环己烷构象翻转的过程。
首先,让我们了解一下环己烷的基本结构。
环己烷分子由六个碳原子组成,形成了一个环状结构。
每个碳原子周围都有两个氢原子,总共有十二个氢原子。
环己烷的构象可以用希尔伯特投影式表示,其中每个碳原子以垂直和水平的方式表示。
环己烷的构象翻转是指环状结构中的一个碳原子在平面内旋转180度。
这个过程可以通过两个不同的中间构象进行。
让我们一步一步地了解这个过程。
首先,我们考虑环己烷的正常构象,其中所有的碳原子都处于平面上,氢原子位于平面之上或之下。
这个构象被称为"椅形"构象,因为它看起来像是一个椅子。
接下来,我们需要将其中一个碳原子周围的化学键旋转180度。
这个碳原子通常被称为“轴向碳原子”,因为它的化学键是沿着烷环的轴线延伸的。
在构象翻转过程中,轴向碳原子的化学键需要转到与轴线相反的位置。
为了达到这个目标,我们需要将环己烷分子进行一些旋转和重新排列。
首先,我们将椅形构象的一个氢原子移到轴线的下方。
这个过程导致环烷烃分子发生旋转,直到另一个相邻的碳原子变成新的轴向碳原子。
现在,新的轴向碳原子周围的化学键需要以180度旋转,使其化学键朝向椅形构象中原先的轴向碳原子。
最后,我们将之前下方的氢原子移到轴线上方,使其成为新构象的轴向碳原子的氢原子。
同时,之前的轴向碳原子也成了新构象中周围的碳原子之一。
通过这个过程,环己烷的构象成功发生翻转。
最初处于下方的轴向碳原子现在位于上方,而最初位于上方的轴向碳原子现在位于下方。
这个过程可以转变为另外一种称为"反椅形"构象的构象。
值得注意的是,环己烷的构象翻转只发生在碳原子周围具有特定的取向的情况下,即只有当其中一个碳原子周围正好有两个碳原子时才会发生。
