酮基布洛芬生产工艺研究与改进
酮基布洛芬生产工艺研究与改进

重点研究和改进了甲基化反应和酰化 傅克 反应的生产工艺。甲基化反应以绿色环保的甲基 化试剂( CH 3 O) 2CO 代替了剧毒的 CH 3 ) 2SO2 试剂, 改进后的甲基化反应生产工艺收率 提高了 25% 以上, 同 时改 善了 生产 环 境; 酰 化反 应利 用 苯 SOCl2 共沸除尽酰化物中的 SOCl2 , 避免了傅克反 应中生成副产物二苯亚砜 , 改进的酰化 傅克反应 生产工艺收率提高 6% ~ 10% ; 其他 反应过程也 得到一定优化。通过对生产工艺的改进, 总收率 达 64 2% , 比原有生产工艺的总收率高 28 2% 以上。 参考文献 :
[ 1] 王泽民 . 当代 结构药 物全 集 [ M ] . 北 京 : 北京科 学技 术 出版社 , 1993: 1 069 1 070. [ 2] VENKATARAMAN R, BERRY C B. Preparation of aryl bro moaryl ketones and carboxylic derivatives: WO, 37 052[ P ] . 1998 02 27. [ 3] 永忠 , 李颖 . 酮基布洛芬的合成工艺研究 [ J] . 中国药 物 化学杂志 , 2000, 10( 2 ) : 127 128. [ 4] BORIS Z, MIRKO S. Verfahren zur Horstellung von 2 ( 3 benzoylphenyl propions ure: Ger Offen, 2 914 006[ P] . 1979 10 18. [ 5] 刘志雄 , 程清蓉 , 李 翔 . 酮 洛芬的 合成 [ J] . 中国 新药 杂 志 , 2008, 17( 8) : 673 675. [ 6] 刘鸿 . 一类含亚砜基化合物的合成 [ J] . 惠州 学院学报 , 2004, 24( 3) : 29 33. Study and improvement of the technology for production of ketoprofen LI U Zhi xiong * 1 , CHENG Qing rong2 ( 1. College of Chemistry and Chemical Engineering, Jishou University, Jishou 416000, China; 2. School of Chemical Engineering and Pharma cy , Wuhan Institute of Technology, Wuhan 430074, China ) , Huaxue Shiji, 2009, 31( 12) , 1041~ 1042; 1046 Abstract: The primary technology for production of ketoprofen was analyzed, the reaction process of monomethylation and
布洛芬合成生产实验报告(3篇)

第1篇一、实验目的本实验旨在通过化学合成方法制备布洛芬,并对其合成过程进行详细记录,以了解布洛芬的合成工艺及反应条件。
二、实验原理布洛芬(Ibuprofen)是一种非甾体抗炎药(NSAID),具有解热、镇痛、抗炎作用。
本实验采用芳基1,2-转位重排法合成布洛芬,以异丁基苯为起始原料,经过傅克反应、催化加氢、氧化、酸催化等步骤,最终得到目标产物。
三、实验材料与仪器1. 实验材料:(1)异丁基苯:分析纯(2)三氯化铝:分析纯(3)铁粉:分析纯(4)硝酸:分析纯(5)氢氧化钠:分析纯(6)无水乙醇:分析纯(7)水合肼:分析纯(8)硝酸银:分析纯2. 实验仪器:(1)圆底烧瓶(2)分液漏斗(3)滴液漏斗(4)冷凝管(5)锥形瓶(6)烧杯(7)抽滤瓶(8)干燥器(9)紫外-可见分光光度计(10)红外光谱仪四、实验步骤1. 傅克反应:将50 mL异丁基苯、10 mL三氯化铝和20 mL无水乙醇混合,加入三氯化铝,搅拌溶解。
然后将混合液滴加到装有20 mL三氯化铝和30 mL无水乙醇的圆底烧瓶中,加热回流1小时。
2. 催化加氢:将傅克反应得到的产物冷却至室温,过滤,用无水乙醇洗涤,干燥。
将得到的固体加入装有50 mL无水乙醇的圆底烧瓶中,加入5 g铁粉,加热回流3小时。
3. 氧化:将催化加氢得到的产物冷却至室温,过滤,用无水乙醇洗涤,干燥。
将得到的固体加入装有50 mL硝酸和20 mL水的烧杯中,加热回流2小时。
4. 酸催化:将氧化得到的产物冷却至室温,过滤,用无水乙醇洗涤,干燥。
将得到的固体加入装有50 mL水合肼和20 mL硝酸的烧杯中,加热回流2小时。
5. 纯化:将酸催化得到的产物冷却至室温,过滤,用无水乙醇洗涤,干燥。
将得到的固体加入装有50 mL硝酸银和20 mL水的烧杯中,加热回流2小时。
6. 结晶:将纯化得到的产物加入装有100 mL无水乙醇的烧杯中,冷却至室温,抽滤,干燥,得到布洛芬。
五、实验结果与分析1. 反应条件对产率的影响:(1)三氯化铝的用量:当三氯化铝用量从5 mL增加到10 mL时,产率从40%提高到60%。
碘重排法合成酮基布洛芬
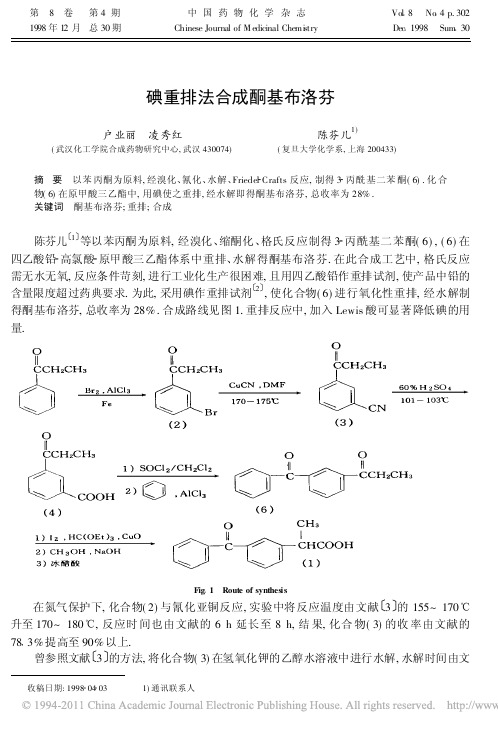
收稿日期:1998 04 03 1)通讯联系人碘重排法合成酮基布洛芬户业丽 凌秀红(武汉化工学院合成药物研究中心,武汉430074) 陈芬儿1)(复旦大学化学系,上海200433)摘 要 以苯丙酮为原料,经溴化、氰化、水解、Friedel Crafts 反应,制得3 丙酰基二苯酮(6).化合物(6)在原甲酸三乙酯中,用碘使之重排,经水解即得酮基布洛芬,总收率为28%.关键词 酮基布洛芬;重排;合成陈芬儿 1 等以苯丙酮为原料,经溴化、缩酮化、格氏反应制得3 丙酰基二苯酮(6),(6)在四乙酸铅 高氯酸 原甲酸三乙酯体系中重排、水解得酮基布洛芬.在此合成工艺中,格氏反应需无水无氧,反应条件苛刻,进行工业化生产很困难,且用四乙酸铅作重排试剂,使产品中铅的含量限度超过药典要求.为此,采用碘作重排试剂 2 ,使化合物(6)进行氧化性重排,经水解制得酮基布洛芬,总收率为28%.合成路线见图1.重排反应中,加入Lewis 酸可显著降低碘的用量.Fig 1 Route of synthes is在氮气保护下,化合物(2)与氰化亚铜反应,实验中将反应温度由文献 3 的155~170!升至170~180!,反应时间也由文献的6h 延长至8h,结果,化合物(3)的收率由文献的78 3%提高至90%以上.曾参照文献 3 的方法,将化合物(3)在氢氧化钾的乙醇水溶液中进行水解,水解时间由文第 8 卷 第4期1998年12月 总30期中国药物化学杂志Chinese Journal of M edicinal Chemi stry Vol 8 No 4p.302Dec 1998 Sum 30献的24h 延长至60h,未得到(4).后改用55%~60%的硫酸在101~103!下水解8h,顺利得到化合物(4),收率达89%.文献 3 用五氯化磷作酰氯化剂,在四氯化碳溶剂中,于40!反应30min 后,经减压蒸馏得化合物(5).实验改用氯化亚砜为酰氯化剂,二氯甲烷作溶剂,回流反应7h,回收溶剂后得(5),可不经减压蒸馏,直接与无水苯在三氯化铝催化下制得化合物(6),两步收率为70 3%.(文献 3 收率:61 2%).化合物(6)与碘、原甲酸三乙酯、催化量的Lew is 酸回流反应15h,再水解即得化合物(1),收率为60%.研究发现,此重排反应中,碘与(6)的摩尔比为2∀1方能发生重排.若在反应体系中加入催化量的Lew is 酸(如溴化亚铜、氧化亚铜等)可显著地使碘与(6)的摩尔比降至1∀1.1 实验部分熔点用毛细管法测定,温度未经校正.3 溴苯丙酮(2)的制备参考文献 1 方法制得.1 1 3 氰基苯丙酮(3)的制备在干燥的四口烧瓶中,加入化合物(2)60g(0 28mol)、氰化亚铜30 4g(0 34mol)、DMF 42 3mL,氮气保护下在170~175!搅拌8h.稍冷,倒入六水三氯化铁112 8g 和水169mL 的溶液中,加入浓盐酸28 2mL,于60~70!搅拌0 5h.冷却后,用甲苯提取(100m L #3),合并有机层,用5%碳酸钠溶液(100mL #2)、水(100mL #3)洗涤,无水硫酸钠干燥,减压回收溶剂,得暗红色油状物39 7g,收率:90%,直接用于下步反应.1 2 3 丙酰基苯甲酸(4)的制备于三口反应瓶中,加入21g (0 13mol)化合物(3)及55%~60%的硫酸65m L,于100~103!搅拌7h.稍冷,用10%氢氧化钠溶液调至pH 9,加活性炭2g,脱色0 5h,抽滤,滤液用4mol/L 盐酸调pH 1~2,有大量浅黄色固体析出.抽滤至干,冷水洗至中性,干燥得浅黄色固体(4)17 0g,收率:78%,mp 121~123!(文献 3 m p 119~124!).1 3 3 丙酰基二苯酮(6)的制备于干燥的三口反应瓶中,加化合物(4)17g(0 1mol)、氯化亚砜23 8g(0 2mol)、二氯甲烷180mL 、无水DMF 一滴,搅拌回流7h.减压回收二氯甲烷和氯化亚砜,得暗红色油状物(冷却后固化),将其溶于36mL 无水苯中备用.在另一干燥的反应瓶中,加入无水三氯化铝27 0g (0 2mol)、无水苯90mL,室温搅拌15min,滴加上述酰氯的苯溶液,滴毕,于75~80!搅拌回流2h.冷却,倒入270g 碎冰和27m L 浓盐酸中搅拌2h.分出有机层,水层用苯提取(50mL,35mL,35mL),合并有机层,用温水洗(100mL #2)至pH 6,无水硫酸钠干燥.常压回收尽苯,减压蒸馏,收集158~165!/400Pa 馏分,得浅黄色液体17g,收率:75%(文献 3 m p 28~33!).1 4 酮基布洛芬(1)的合成于干燥的三口反应瓶中加(6)11 9g(0 05mol)、碘25 4g(0 05mol)、原甲酸三乙酯35 8g 、氧化亚铜0 576g (0 004mol),搅拌回流15h.稍冷,加入10%连二亚硫酸钠60mL,搅拌10min,抽滤,滤液分出有机层,水层用三氯甲烷提取(20mL #3),合并有机层,用10%连二亚硫酸钠(50mL #1)、饱和氯化钠(50mL #2)、水(50mL #2)洗涤,无水硫酸钠干燥,减压回收溶剂,得棕褐色油状物.3033期户业丽等:碘重非法合成酮基布洛芬304中国药物化学杂志8卷将上述油状物与40mL甲醇及30mL30%氢氧化钠搅拌回流4h.补加水35m L、活性炭1g,回流脱色0 5h.抽滤,水洗,合并碱水层,用4mol/L盐酸调pH1~2,苯萃取(20mL# 3),合并有机层,水洗(50mL#3),无水硫酸钠干燥,回收苯,得黄色油状物.上述油状物与6mol/L盐酸30m L搅拌回流4h.冷却,分出有机层,水层用苯提取(20mL#2),合并有机层,加8%氢氧化钠调pH8,搅拌15m in,分出碱水层,有机层用8%氢氧化钠洗(20mL#2),合并碱水层,加活性炭(0 5g)脱色0 5h.抽滤,水洗,滤液用冰醋酸调pH1~2,有油状物析出.静置过夜,倾出水层,用丙酮溶解油状物,无水硫酸钠干燥,减压回收溶剂,得黄棕色油状物,放置固化,用苯 石油醚重结晶,得白色晶体(1)7 6g,收率:60%,m p 94~96!.1H NMR(D2O) :1 56(3H,d),3 78(1H,q),4 65(1H,s),7 2~7 8(9H,m).参 考 文 献1 陈芬儿,张文文.酮基布洛芬的合成.中国医药工业杂志,1991,22(8):344~3452 Huggins SD,Thomas CB.Conversi on of aromatic ketones into arylpropionic acids.J Chem Soc,Perkin T rans,I1983,(7):1483~14883 Zupancis Boris,Jenko Branko.The preparation of2 (3 benzoylph enyl)propionic acid.Ger Off.2913770.11,Oct.1979Synthesis of Ketoprofen via RearrangementUsing Iodine as the CatalystH u Yeli,Ling Xiuhong(Research Centre of Sy nthetic Dr ugs,Wuhan I nstitute ofChemical T echnology,Wuhan430074)Chen Fener(Dep ar tment of Chemistry,Fudan University,Shanghai200433)Abstract An efficient preparation of ketoprofen w as described.Propiophenone was used as the material via bromination,cyanation,hydrolysis,the Friedel Crafts∃reaction to give3 propionyl benzophenone,which w as converted to ketoprofen by rearrangement w ith iodine.The overall yield w as28%from propiophenone.Key words ketoprofen;rearrangement;synthesis。
酮基布洛芬的合成方法改进

收稿日期:2002-10-31作者简介:余红霞(1968-),女(汉族),湖北武汉人,讲师,硕士,主要从事药物及中间体的合成研究工作,Tel :(027)88025421,E 2mail :tree -2001-11@1631com 。
文章编号:1005-0108(2003)02-0097-02酮基布洛芬的合成方法改进余红霞1,郭峰2,陈芬儿3(11武汉化工学院制药系,湖北武汉430073;21中国药科大学药学院,江苏南京210009;31复旦大学化学系,上海200433)摘 要:目的合成酮基布洛芬,提高产品纯度。
方法以32苄基苯乙酮为原料,通过Darzens 缩合,氧化合成目标物。
结果与结论以32苄基苯乙酮计算,总收率约64%,产品纯度为9918%。
并通过红外吸收光谱(IR )、质谱(MS )确证了目标物的结构。
该合成工艺简单,产品质量好。
关键词:药物化学;工艺改进;Darzens 缩合;酮基布洛芬中图分类号:R914 文献标识码:A 酮基布洛芬是优良的非甾体消炎药,具有抗炎作用强、副作用小等特点,临床上用于治疗慢性类风湿关节炎、变形性关节炎、外伤和手术后疼痛。
自1973年上市以来,人们对其进行了大量研究,其合成方法很多,其中以Darzens 缩合法引人瞩目。
我国西南合成药厂首次采用此法实现了酮基布洛芬的生产,但生产实践表明,32苄基苯乙酮在进行Darzens 缩合过程中,除获得32苄基2α2甲基苯乙醛(3)外,尚有约10%~12%的反应物32苄基苯乙酮,难以用常规减压蒸馏的方法除去,当用高锰酸钾氧化3时,不可避免地使32苄基苯乙酮氧化成32苯甲酰基苯甲酸,该副产物与酮基布洛芬难以通过重结晶的方法加以分离,致使酮基布洛芬的质量不能达到英国药典1993年1995增补版标准。
为此在用Darzens 缩合反应来制备32苄基2α2甲基苯乙醛时,本文作者采用在磷酸二氢钠和过氧化氢体系中,用亚氯酸钠选择性将3氧化为4,而该物质为固体,从而除去32苄基苯乙酮,再氧化制得较纯的目标物1。
布洛芬剂型研究进展

布洛芬剂型研究进展作者:李晓洁王崇静梁月琴王珩李仲昆来源:《中国实用医药》2014年第18期布洛芬的化学名为2-(4-异丁基苯基)丙酸,属丙酸衍生物,是一个已使用多年的老药。
其临床应用主要是解热,镇痛,抗炎。
但其长期口服可产生一些不良反应。
周晓梅等[1]收集了2000~2012年国内医药期刊报道的有关布洛芬的不良反应。
据统计,布洛芬致胃肠道不良反应居多;在治疗类风湿性关节炎、关节疼痛时引起不良反应的较多;老年人使用布洛芬出现不良反应的情况较多;在使用时间上,超时使用致不良反应的达23.53%;连续用药出现不良反应的占到52.94%。
针对这些不良反应,人们一直致力于其制剂和技术方面的研究,本文拟就布洛芬的制剂及剂型的研究进展作一综述。
1 ;片剂布洛芬原料药为白色结晶粉末,因其熔点低,与辅料混合后极易产生低共熔现象。
陈晓刚[2]以HPMC为粘合剂制粒,胶态SiO2和MS 混合物外配以解决上冲粘冲现象,外配滑石粉因重下沉以解决下冲粘冲情况,同时处方中加入了聚山梨酯80可确保布洛芬片溶出度达到国外药典的高标准要求。
2 ;乳膏布洛芬局部给药2~4 h,血药浓度达到峰值,在皮下脂肪、肌肉和关节滑液中的药物浓度远远超过血药浓度有利于局部炎症和疼痛的治疗。
符棘玉等[3]研究了氮酮对布洛芬乳膏体外透皮吸收的影响,发现当氮酮的浓度为3%时,布洛芬乳膏的透皮吸收率最高,可以选择氮酮作为布洛芬乳膏的促透剂。
3 ;滴眼液布洛芬难溶于水,因此很难配制成溶液剂型。
韩华等[4]利用布洛芬与聚乙二醇-20000形成低聚共熔混合物的方法,制备了0.2%的布洛芬滴眼液。
对168 例患各种类型结膜炎及内眼手术后患者的临床总有效率为97.0%,未发现明显的毒副作用。
4 ;巴布剂布洛芬的适合局部给药,国外已经成功将布洛芬开发成多种透皮制剂。
王霞等[5]将布洛芬制成药量为5%的巴布剂,所得布洛芬巴布剂含量稳定,渗透速率小于释放速率。
酮洛芬的合成方法研究

酮苯丙酸,化学名为 α甲基3苯甲酰基苯乙酸,是
一种强效的 2芳基丙酸类非甾体镇痛药[1],能与
药物直接作用于膜电位[2],耐受性好、用量少、见
效快、口服吸收好、安全性高,临床也用于治疗口
腔科疼痛、原发性痛经[3,4]。由法国 RhonePoulenc
公司化学家 、 和 开发研制 Farge Messer Moutounier
北迅达药业股份有限公司。已有合成路径主要以
3甲基苯甲酸[6]为起始原料,五氯化磷为酰化试
C剂ra,f经ts 路酰化易反斯应酸制Al得Cl33
催化作用与苯发生 Friedel 甲基二苯酮,经过光照、三
氯化磷催化等条件使其侧链甲基发生溴代反应制
得 3溴甲基二苯酮,之后加入微量对苯二酚催化
制得 3苯甲酰基苯乙腈后水解制得酮洛芬。以 3
968
化学研究与应用
第 30 卷
下,用相转移催化剂催化硫酸二甲酯为甲基化试 剂甲基化反应,后水解制得酮洛芬;以苯甲酸[8]为 起始原料,经过溴化、酰氯化,后与苯发生 Friedel Crafts 酰化反应制得 溴3 二苯甲酮,经过 CuBr 催 化,3溴二苯甲酮与丙二酸二乙酯钠发生偶合得 2(3苯甲酰苯基)丙二酸二乙酯,再经甲基化、水 解、脱羧制得酮洛芬;以对硝基苯乙酮[9]为起始原 料,经缩酮保护,再与苯乙腈缩合生成 5(2甲基 1,3二烷2基)7苯基苯并[c]异唑,之后经
easy to operate and suitable for the industrial production.
: ; ; ; Key words ketoprofen nonsteroidal analgesics methylation synthesis
酮洛芬(Ketoprofen,KP):又名酮基布洛芬、苯
布洛芬新工艺研究

布洛芬新工艺研究引言布洛芬是一种具有解热、镇痛和抗炎作用的药物,被广泛应用于临床医学中。
随着科技的不断进步,对布洛芬生产工艺的研究也在不断深入。
传统的布洛芬生产工艺存在着一些不足之处,如生产效率低下、能耗高等。
因此,研究一种高效、环保的布洛芬新工艺具有重要意义。
本文将介绍布洛芬新工艺研究的现状、方法、结果与展望。
研究现状布洛芬新工艺研究的发展迅速,国内外研究者不断探索新的生产方法。
在国内外学者的共同努力下,一些新型的布洛芬生产工艺逐渐被开发出来。
例如,有学者采用生物酶法合成布洛芬,这种方法具有高效、环保等优点,但生物酶的来源和稳定性仍是亟待解决的问题。
另外,还有学者尝试采用有机合成的方法生产布洛芬,但这种方法生产过程较长,成本较高。
因此,针对现有布洛芬生产工艺存在的问题,本文将重点研究一种新型的布洛芬生产工艺。
研究方法本研究将采用文献调研和实验研究相结合的方法,首先通过文献调研了解布洛芬生产工艺的研究现状和进展,然后通过实验研究探索新型布洛芬生产工艺的可行性。
具体实验方案如下:1、材料:准备布洛芬原料、催化剂、溶剂等实验材料。
2、方法:采用液相催化氢化法合成布洛芬,通过调节反应温度、压力、催化剂用量等参数,探究最佳反应条件。
3、实验设计:进行不同条件下催化剂的活性评价实验,采用正交试验设计方法优选最佳反应条件。
4、数据处理:对实验数据进行整理和分析,采用表格和图表记录数据。
研究结果通过实验研究,我们发现新型布洛芬生产工艺具有以下优点:1、反应条件温和,催化剂活性高,可有效提高布洛芬的产率;2、反应过程易于控制,产品质量稳定,可实现工业化生产;3、催化剂可循环使用,减少了对环境的影响。
然而,新型布洛芬生产工艺也存在一些不足之处:1、催化剂成本较高,可能会增加生产成本;2、工艺流程仍较长,需要进一步优化简化。
结论与展望通过对布洛芬新工艺的研究,我们发现新型生产工艺具有较高的生产效率和环保性能。
虽然新型生产工艺仍存在一些不足之处,但可以通过进一步优化催化剂、简化工艺流程等措施加以改进。
酮基布洛芬生产工艺研究与改进措施分析

酮基布洛芬生产工艺研究与改进措施分析【摘要】酮基布洛芬是一种非甾体消炎、镇痛药物,为了提高药物生产的安全性和有效性,必须对原有的生产工艺进行优化和改进。
下面本文就对酮基布洛芬生产工艺进行研究,并对其优化和改进措施进行了分析。
【关键词】酮基布洛芬生产工艺改进措施酮基布洛芬是一种非甾体类药物,就有消炎、镇痛以及解热的功效,并且具有高效低毒、口服吸收快以及消除快的优点。
为能够提高药物的安全性以及有效性,就需要对之前的生产工艺不断进行优化和改进。
1 原有的生产工艺改进之前的工艺流程如图一所示。
其技术指标为:甲基化反应收率为50%~55%,其中间产物即3-氰乙基苯甲酸甲酯的纯度为93%~94.5%;酰化-傅克反应其收率为75%~80%,这一反应的中间产物,也就是3-苯甲酰基-α-甲基苯乙腈的纯度要>93.4%;脂水解反应的收率要>94%,其中间产物,也就是3-氰乙基苯甲酸的纯度为95%~96%;氰水解反应的收率为83%~87%,其产物酮洛芬的纯度即为98.39%~99.4%(如图1所示)。
2 存在的问题采用以上生产工艺生产酮基布洛芬,如果采用的是间氰甲基苯甲酸甲酯作为原料进行生产,在经过了一系列的反应之后,其酮基布洛芬的收率仅为32%~39%。
经过分析,出现这一问题的原因主要是在甲基化反应以及酰化-傅克反应上,主要是因为这两个环节的反应收率比较低引起的。
其中在甲基化反应中,其单甲基化试剂采用的是硫酸二甲酯,那么就会造成双甲基化产物的出现,从而对单甲基化的选择率产生影响;另外在酰化-傅克反应环节的问题主要是因为酰氯物中的SOCl2没有蒸馏完毕,因而造成了二苯亚砜副产物的产生。
所以对于原有生产工艺的改进,改进重点应该放在对这两个反应环节上。
3 改进措施(1)对于甲基化反应的改进和优化。
如果是在强碱和相转移催化剂共同存在下,采用(CH3)2SO2作为甲基化的试剂,然后在芳基乙腈的侧链-CH2CN 上把甲基和α-单甲基化的时候,会有双甲基化副产物的出现,并且很难和双甲基化进行纯化分离。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
重点研究和改进了甲基化反应和酰化 傅克 反应的生产工艺。甲基化反应以绿色环保的甲基 化试剂( CH 3 O) 2CO 代替了剧毒的 CH 3 ) 2SO2 试剂, 改进后的甲基化反应生产工艺收率 提高了 25% 以上, 同 时改 善了 生产 环 境; 酰 化反 应利 用 苯 SOCl2 共沸除尽酰化物中的 SOCl2 , 避免了傅克反 应中生成副产物二苯亚砜 , 改进的酰化 傅克反应 生产工艺收率提高 6% ~ 10% ; 其他 反应过程也 得到一定优化。通过对生产工艺的改进, 总收率 达 64 2% , 比原有生产工艺的总收率高 28 2% 以上。 参考文献 :
( 下转第 1046 页)
1046
化
学
试
剂
2009 年 12 月
法, 具备能够正确地使用仪器设备、 准确地采集处 理实验数据和表达实验结果的能力; 认真观察实 验现象进行 分析判断、 逻辑处理、 做出结论的能 力; 正确设计实验( 选择实验方法、 实验条件、 仪器 和试剂等) , 并通过查阅手册、 工具书及其他信息 源获得信息以解决实际问题的能力。 2) 基础化学实验中心教学效果得到了各方面 的好评 后继专业课教师的评价 : 通过 3 年基础化学 实验的训练 , 学生基础知识扎实, 动手能力强 ; 学 校督导组教师的评价 : 教师指导严格, 学生实验态 度认真 , 考核方法科学合理[ 6] , 教学效果优良; 学 生的评价 : 基础化学实验可独立操作, 把实践和理 论联系在一起, 激发同学们浓厚的学习兴趣, 培养 在实践中解决问题的习惯 ; 在上海市教委组织的 学士学位评估和上海 市实验示范中 心资格审查 中, 校外同行专家对基础化学实验中心给予高度 的评价: 受益面宽、 影响面大。基础化学实验中心 是应用型本科人才培养的重要基础实验基地; 以 学生为本、 课程体系先进 ; 在创建高水平的应用型 大学和培养高素质应用技术型人才中作用重大; 重视学生实验硬件建设 , 并将先进的贵重仪器全 部投入到学生基础化学实验教学中; 安全环境配 置到位, 符合国家安全规范; 基础化学实验教学与 理论教学队伍互通, 教学、 科研、 实验技术兼容体 现了教学科研相长, 组织结构先进, 师资水平 ; 管 理制度健全面; 利用现代化学实验技术充实实验 教学内容 , 具备创新人才培养的多元化教学环境。 3 结语 1) 构建了包括基础、 综合性、 设计性等实验、 科技创新小发明等内容, 形成从低到高、 基础到前 沿、 接授知识到培养综合应用能力 , 逐级提高的 ( 上接第 1042 页)
在强碱 ( NaOH 、 NaNH 2 等 ) 及相转移催化剂的 存在下用( CH3 ) 2 SO2 作甲基化试在芳基乙腈的侧 链 CH 2 CN 上引 入甲基引入
[ 4]
单甲 基化的同时
产生的双甲 基化副产物 , 二者 难以分离 纯化。 通过质谱 仪分析 改进前 的甲 基化产 物, 其 中有 5% ~ 10% 的双甲基化产物 , 因此如何提高单甲基 化的 选 择 性 成 为 甲 基 化 反 应 的 关 键。 而 ( CH 3O) 2CO 是 一种 对芳 基乙 腈的 侧 链 CH2 CN 上 单 甲 基化 的 高 选 择 性 的试 剂 。 通过 以 ( CH3 O) 2CO 代替 ( CH 3 ) 2SO2 试剂的 研究, 实现了 对甲基化反应的优化。具体操作如下。 在 高 压 反 应 釜 内 按 原 料 2 K2CO3 ( CH 3O) 2 CO 为 18 25 40 质量配比加入高压反应 釜中, 同时加入为原 料 2 质量的 0 5% 的抗氧化 剂, 在 180 搅拌反应 6 h, 逐渐降至室温, 放出反 应产生的二氧化碳, 开釜后 , 将反应液取出过滤, 滤饼回收; 滤液减压回收( CH 3O) 2 CO, 得无色黏稠 液体 , 放 置 固化 粗 品产 物 3, HPLC 测 定 纯度 > 93 5% , 重结晶一次后的产物 3 纯度 > 98 0% , 收 率> 80% 。 以( CH 3O) 2 CO 代 替 ( CH 3 ) 2 SO2 作 甲 基化 试 剂, 实现了高选择性的单甲基化反应, 甲基化产物 经质谱分析仪测定未见有双甲基化副产物生成, 产物粗品 3 纯度提高 , 重结晶次数减少, 所得合格 的产品比 改进前 的产品 纯度 要高, 同时催 化剂 K2 CO3 可循环使用 , 降低了生产成本。 2 2 酰化 傅克工艺分析与优化 对改进前的傅克反应产物进行质谱仪分析,
产物中 含有二苯亚砜。文献 [ 7] 报导 苯与 SOCl2 在 AlCl3 催化作用生成二苯亚砜, 因此傅克反应中 的副产物生成是酰化反应中的 SOCl2 没有蒸馏除 尽所引起的, 因此酰化 傅克反应过程的关键是把 酰化反应完成后除尽酰化物中的 SOCl2 。为此利 用加入苯与 SOCl2 形成共沸物蒸馏除尽酰化物中 的 SOCl2。 按原工艺原料配比进行酰化反应 , 对酰化反 应中除尽 SOCl2 进行了改进 , 当蒸发回收 SOCl2 快 尽之时 , 加入适量的苯 , 让 SOCl2 与苯共沸, 得以 除尽酰化物中的 SOCl2 。傅克反应按原有生产工 艺条件反应, 所得粗品 5 HPLC 测定纯度 93 7% , 重结晶一次得合格产物 5, HPLC 测定产品纯度 > 99 0% 。经改进后 的酰化 傅克 反应的总 收率提
图 1 改进前的工艺流程 Fig. 1 The primary production technology
1 2
技术指标
度> 93 4% 。氰水解反应: 收率 83% ~ 87% , 酮洛 芬( 1) 纯度 98 9% ~ 99 3% 。
甲基化反应: 收率 50% ~ 55% , 中间产物 3 氰乙基苯甲酸甲酯( 3) 纯度 93% ~ 94 5% ; 酯水解 反应: 收率 > 94% , 中间产物 3 氰乙基苯甲酸 ( 4) 纯度 95% ~ 96 0% ; 酰化 傅克反应 : 收率 75% ~ 80% , 中间产物 3 苯甲酰基 甲基 苯乙腈 ( 5) 纯
第 31 卷第 12 期
刘志雄等 : 酮基布洛芬生产工艺研 究与改进
1041
化学试剂 , 2009, 31( 12) , 1041~ 1042; 1046
酮基布洛芬生产工艺研究与改进
刘志雄* 1 , 程清蓉2
( 1. 吉首大学 化学化工学院 , 湖南 吉首 416000; 2. 武汉工程大学 化 学与制药学院 , 湖北 武汉 430074)
5 CO Cl 2 CH 3 CHCN
AlC l3
CH 3 CHCN
1) NaOH 2) HCl S OCl2
CHCN
COO CH 3 3
COOCH 3 4 CH 3 O CHCN
H+பைடு நூலகம்
COOH CH 3 O CHCOOH
6
1
具体合成路线 The synthetical route
改进前工艺流程和技术指标 工艺流程
收稿日期 : 2008 11 11 作者简介 : 刘志 雄 ( 1973 ) , 男 , 湖 南新 化人 , 硕士 , 讲师 , 研 究方向为药物中间体工艺研究和天然产物开发。
1042
化
学
试
剂
2009 年 12 月
2 2 1
生产工艺分析与优化 甲基化工艺分析及优化
高到 90% 。 2 3 其他反应过程工艺的优化 由于甲基化产物纯度的的提高 , 对酯水解反 应过程有优化作用 , 酯水解产物纯度和收率都有 所提高 , 收 率 > 95 6% 、 纯度 > 98 3% ; 傅克反应 的优化使氰水解的反应 原料纯度提高 5 6% , 因 此氰水解反应过程所得产物收率 > 93% , 比改进 前的反应过程的收率高了 6% ~ 10% , 纯度> 99 3% 。 3 结论
[ 1] 王泽民 . 当代 结构药 物全 集 [ M ] . 北 京 : 北京科 学技 术 出版社 , 1993: 1 069 1 070. [ 2] VENKATARAMAN R, BERRY C B. Preparation of aryl bro moaryl ketones and carboxylic derivatives: WO, 37 052[ P ] . 1998 02 27. [ 3] 永忠 , 李颖 . 酮基布洛芬的合成工艺研究 [ J] . 中国药 物 化学杂志 , 2000, 10( 2 ) : 127 128. [ 4] BORIS Z, MIRKO S. Verfahren zur Horstellung von 2 ( 3 benzoylphenyl propions ure: Ger Offen, 2 914 006[ P] . 1979 10 18. [ 5] 刘志雄 , 程清蓉 , 李 翔 . 酮 洛芬的 合成 [ J] . 中国 新药 杂 志 , 2008, 17( 8) : 673 675. [ 6] 刘鸿 . 一类含亚砜基化合物的合成 [ J] . 惠州 学院学报 , 2004, 24( 3) : 29 33. Study and improvement of the technology for production of ketoprofen LI U Zhi xiong * 1 , CHENG Qing rong2 ( 1. College of Chemistry and Chemical Engineering, Jishou University, Jishou 416000, China; 2. School of Chemical Engineering and Pharma cy , Wuhan Institute of Technology, Wuhan 430074, China ) , Huaxue Shiji, 2009, 31( 12) , 1041~ 1042; 1046 Abstract: The primary technology for production of ketoprofen was analyzed, the reaction process of monomethylation and
