高一化学离子方程式书写练习含答案
高一化学第二章离子反应方程式知识点及练习题(含答案)
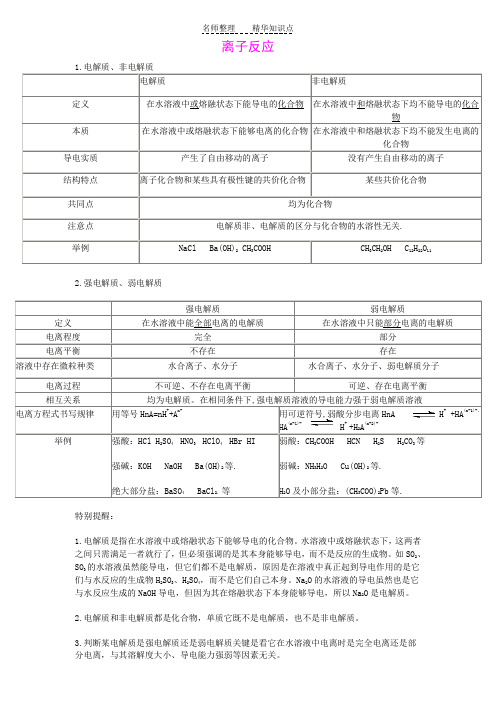
离子反应2.强电解质、弱电解质特别提醒:1.电解质是指在水溶液中或熔融状态下能够导电的化合物。
水溶液中或熔融状态下,这两者之间只需满足一者就行了,但必须强调的是其本身能够导电,而不是反应的生成物。
如SO2、SO3的水溶液虽然能导电,但它们都不是电解质,原因是在溶液中真正起到导电作用的是它们与水反应的生成物H2SO3、H2SO4,而不是它们自己本身。
Na2O的水溶液的导电虽然也是它与水反应生成的NaOH导电,但因为其在熔融状态下本身能够导电,所以Na2O是电解质。
2.电解质和非电解质都是化合物,单质它既不是电解质,也不是非电解质。
3.判断某电解质是强电解质还是弱电解质关键是看它在水溶液中电离时是完全电离还是部分电离,与其溶解度大小、导电能力强弱等因素无关。
离子方程式的书写1.离子反应:指在溶液中(或熔化状态下)有离子参加或离子生成的反应。
2.离子方程式:用实际参加反应的离子符号表示化学反应的式子。
3.离子方程式的书写: (1)书写规则:①单质、氧化物、不溶物、难电离的物质(弱酸、弱碱及水等)不能拆开来写。
如Cl 2、Na 2O等不可以拆开写成Cl -、Na +、O 2-;BaSO 4不可以拆开写成Ba 2+、SO 42-形式。
②易溶于水,易电离的物质的离子符号的改写同电离方程式中的离子形式。
如NaHCO 3改写Na +、HCO 3-;NaHSO 4应改写Na +,H +,SO 42-③微溶物,若出现在反应物中一般改写成离子符号(悬浊液除外);若出现在生成物中一般不改写。
④固体与固体物质反应不写离子方程式。
如实验室制取NH 3的离子方程式为: 2NH 4Cl+Ca(OH)2CaCl 2+2NH 3↑+2H 2O⑤浓H 2SO 4、浓H 3PO 4一般不拆开写成离子形式;HCl 、HNO 3无论浓稀,均应改写成离子符号。
如Cu 片与浓H 2SO 4反应的离子方程式为:Cu+2H 2SO 4(浓)CuSO 4+SO 2↑+2H 2O(2)书写步骤(以CuSO 4溶液与BaCl 2 溶液反应为) ①写出反应的化学方程式:CuSO 4+BaCl 2==CuCl 2+BaSO 4↓ ②把易溶于水、易电离的物质拆开写成离子形式,难溶的物质或难电离的物质以及气体等仍用化学式来表示。
离子方程式试题及答案

高考化学热点知识训练离子方程式1、下列反应的离子方程式书写正确的是()A、铁和稀硫酸反应:2Fe+6H+ = 2Fe3++3H2↑B、氯化亚铁溶中通入氯气:Fe2++Cl2=Fe3++Cl—C、往水中投入一小块金属钠:Na+2H2O=Na++2OH—+H2个D、铝粉溶于NaOH溶液中:2Al +2OH—+2H2O=2AlO2—+3H2↑2、下列反应的离子方程式书写正确的是()A、苛性钾溶液中加入稀醋酸:H++OH—= H2OB、碳酸钠加入稀盐酸:Na2CO3+2H+ = 2Na+ +CO2↑+H2OC、氧化钠溶于盐酸中: Na2O+2H+ = 2Na++H2OD、氯气通入冷水中: Cl2+H2O = 2H++Cl—+ ClO—3、下列反应的离子方程式错误的是()A、澄清石灰水跟稀硝酸反应:H++OH—= H2OB、磷酸与氢氧化钾溶液反应:H++OH—= H2OC、醋酸铵和盐酸反应:CH3COO—+ H+ = CH3COOHD、碳酸钙溶于硝酸中:CaCO3 + 2H+ = Ca2+ + H2O + CO2↑4、下列反应的离子方程式书写正确的是( )A、CuSO4溶液加入过量氢氧化钡溶液:Ba2+ + SO42—= BaSO4↓B、碳酸氢铵溶液与过量氢氧化钠溶液混合:HCO3—+ OH—= CO32—+ H2OC、稀硫酸中滴加氢氧化钡溶液:H++OH—=H2OD、硫酸氢钠溶液中加入碳酸氢钠溶液:H+ + HCO3—= CO2↑+H2O5、下列能正确表示反应的离子方程式的是():Cu + 4H++SO42—=Cu2++SO2↑+2H2OA、铜与浓硫酸反应放出SO2B、浓硫酸与食盐共热制HCl写成:Cl—+ H+= HCl↑C、浓盐酸与二氧化锰反应制氯气:MnO2 + 4H+ +2Cl— = Mn2+ + 2H2O + Cl2↑D、加热NH4Cl和氢氧化钠固体混合物:NH4+ + OH—= NH3↑ + H2O6、下列能正确表示反应的离子方程式的是()A、FeCl3溶液的水解:Fe3+ + 3H2O = Fe(OH)3↓+ 3H+B、氯化钡溶液与碳酸钠溶液反应:Ba2++CO32— =BaCO3C、硫化亚铁与盐酸反应:FeS+2H+=Fe2+ +H2SD、氯气通入碘化钾溶液中:Cl2 + 2I—=I2 + 2Cl—7、下列能正确表示反应的离子方程式的是()A、Na2S溶液水解:S2—+ 2H2O H2S+2OH—B、硫氢化钾溶液水解:HS—+ H2O H2S↑ + OH—C、氯化铝溶液与碳酸钠溶液反应:2Al3+ +3CO32—+3H2O=2Al(OH)3↓+3CO2↑D、用FeCl3溶液制氢氧化铁胶体: Fe3+ + 3H2O Fe(OH)3 (胶体) +3H+8、下列反应的离子方程式正确的是()A、Ba(OH)2溶液不断滴加稀H2SO4:Ba2+ + H+ + OH—+ SO42— = BaSO4↓+ H2OB、Al2(SO4)3溶液中加氨水:2Al3+ + 6NH3·H2O = 2Al(OH)3↓+6NH4+C、稀硫酸中滴加烧碱溶液:2H++2OH—= 2H2OD、氨气通入稀硫酸中:NH3 + H+ = NH4+9、下列反应的离子方程式正确的是()A、用惰性电极电解饱和食盐水2Cl—+2H2O 电解2OH—+ H2↑ + Cl2↑B、往氯化铁溶液中通入硫化氢气体: 2Fe3++S2—= 2Fe2++S↓C、乙醛做银镜反应:CH3CHO+2[Ag(NH3)2]OH→CH3COO—+NH4++2Ag↓+3NH3+H2OD、在硫化钠溶液中加入足量稀硝酸: S2—+ 2H+ = H2S↑10、下列反应的离子方程式错误的的是()A、二氧化碳通入碳酸钠溶液中:CO2 + CO32— + H2O= 2HCO3—B、硫酸铝溶液跟偏铝酸钠溶液反应:Al3+ + 3AlO2—+ 6H2O = 4Al(OH)3↓C、碳酸氢钙溶液跟稀硝酸反应: HCO3— + H+ = H2O + CO2↑D、氢氧化钠稀溶液与氯化铵稀溶液混合:NH4+ + OH—= NH3↑+H2O11、下列反应的离子方程式书写正确的是()A、标准状况下2.24L CO2通入1mol/L 100mL NaOH溶液中:CO2+OH—= HCO3—B、氢氧化亚铁在空气中被氧化:4Fe2+ + O2 + 2H2O = 4Fe3+ + 4OH—C、向漂白粉溶液中通入SO2气体:Ca2++2ClO—+ SO2+H2O = CaSO3↓+2HClOD、等物质的量的NH4HCO3与NaOH在溶液中反应:NH4++HCO3—+2OH—= CO32—+ NH3↑ +2H2O12、下列反应的离子方程式正确的是()A、偏铝酸钠溶液中通入过量的CO2:AlO2—+ 2H2O+CO2=Al(OH)3↓+CO32—B、小苏打溶液中加入过量石灰水:2HCO3—+Ca2++2OH—=CaCO3↓+CO32—+2H2OC、向硝酸镁溶液中加过量氨水:Mg2++2NH3·H2O=Mg(OH)2↓+2NH4+D、NaHSO4溶液中滴入少量Ba(OH)2溶液:H++ SO42—+ Ba2+ + OH—= BaSO4↓+H2O。
高一离子方程式书写专题训练及答案

高一离子方程式书写专题训练写出下列化学反应的离子方程式(写离子方程式先写化学方程式然后拆、删、整理,注意一定要写完之后马上看看电荷守恒原子守恒是否符合)1. 盐酸与氢氧化钠溶液的反应2. 氢氧化钡溶液与硝酸溶液的反应3. 氢氧化钠溶液与硫酸溶液的反应4. 氢氧化钡溶液与硫酸溶液的反应5. 醋酸与氢氧化钠溶液的反应6. 盐酸与氨水的反应7. 氢氧化镁与盐酸的反应8. 醋酸与氨水溶液的反应9. 硫酸铜溶液与氢氧化钡的反应10. 氯化镁与氢氧化钠溶液的反应11. 氯化铝与氨水的反应12.. 氯化镁溶液和硝酸银溶液的反应13. 盐酸溶液和硝酸银溶液的反应14. 硫酸溶液与氯化钡溶液的反应15. 硫酸钠溶液与氯化钡溶液的反应16.碳酸钠溶液与氯化钡溶液的反应17.亚硫酸钠溶液与氯化钡溶液的反应18.氢氧化钠中通入少量二氧化碳19澄清石灰水中通入少量二氧化碳20.铁片投入盐酸溶液中 21.铝片投入盐酸溶液中21.碳酸钠溶液与氢氧化钡溶液反应23. 钠和水的反应(2Na + 2H2O == 2NaOH + H2↑)24. 钠和硫酸的反应25.碳酸氢钠溶液和稀盐酸26. 碳酸氢钙溶液和稀盐酸27. 硫酸氢钠溶液和氢氧化钠溶液28. 碳酸钙中加入稀盐酸29. 碳酸钠溶液中加稀盐酸30. 碳酸钠溶液和石灰水的反应31.碳酸钙中加入醋酸32.碳酸氢钙溶液和氢氧化钙溶液33. 氧化铜中加稀硫酸溶液34. 氧化钠中加稀硫酸溶液35. 铁加入CuSO4溶液中36 碳酸氢钠溶液与氢氧化钠溶液:NaHCO3+NaOH=Na2CO3+H2O37. 亚硫酸钠与盐酸反应38. 铜片插入硝酸银溶液中39. 石灰石与硝酸反应40. MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O41. 2Na2O2+ 2H2O = 4NaOH + O2↑42 Cl2+SO2+2H2O=H2SO4+2HCl43. Cl2+ H2O = HCl + HClO44. SiO2+ 2NaOH = Na2SiO3+ H2O45. 3NO2+ H2O 错误!未找到引用源。
高一化学离子方程式的书写及正误判断试题答案及解析

高一化学离子方程式的书写及正误判断试题答案及解析1.某混合溶液中可能含有HCl、MgCl2、AlCl3、NH4Cl、Na2CO3、KCl中的一种或几种物质,往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入的NaOH溶液体积(V)的关系如图所示。
回答下列问题:(1)溶液中一定含有的溶质是,一定不含有的溶质是(填化学式)。
(2)溶液中可能含有的溶质是(填名称),判断该物质是否存在的实验方法是,现象是。
(3)分别写出AB段、BC段发生反应的离子方程式:①AB段为;②BC段为。
【答案】(1)HCl、AlCl3、NH4Cl MgCl2、Na2CO3(2)氯化钾焰色反应透过蓝色钴玻璃观察焰色反应为紫色(3)①Al3++3OH-====Al(OH)3↓②N+OH-====NH3·H2O【解析】首先分析图像中的拐点、斜线及水平线所表示的化学意义。
OA段是NaOH溶液中和HCl;加入过量NaOH溶液,沉淀全部溶解,说明无MgCl2,所以沉淀只有Al(OH)3;BC段是NaOH溶液与NH4Cl反应,故原溶液中一定含有HCl、AlCl3、NH4Cl,一定无MgCl2;又因为AlCl3、HCl与Na2CO3不能大量共存,所以一定无Na2CO3;可能含有KCl,可用焰色反应进行确定。
【考点】铝的氧化物与氢氧化物从铝土矿中提取铝2.与离子方程式H++OH-====H2O相对应的化学方程式是()A.Ba(OH)2+2HCl====BaCl2+2H2OB.NaOH+NaHSO4====Na2SO4+H2OC.Ba(OH)2+H2SO4====BaSO4↓+2H2OD.NaOH+CH3COOH====CH3COONa+H2O【答案】A、B【解析】离子方程式H++OH-====H2O所表示的含义是可溶性强碱和强酸反应生成可溶性盐和水的反应。
NaHSO4是强酸的酸式盐,在水溶液中完全电离出H+,相当于强酸,A和B选项都正确;Ba(OH)2溶液和H2SO4溶液反应生成的BaSO4是难溶性物质,C选项错误;醋酸属于弱酸,不能拆成离子的形式,D选项错误。
离子方程式练习(含答案)

离子方程式练习姓名:___________班级:___________成绩:___________一、单选题1.下列指定反应的离子方程式正确的是A. 电解熔融NaCl:2Cl-+2H2O 2OH-+Cl2↑+H2↑B. 用氨水溶解AgCl沉淀:Ag++2NH3·H2O=[Ag(NH3)2]++2H2OC. Na2CO3溶液吸收溴蒸气:3CO32-+Br2=Br-+BrO3-+3CO2D. 金属钠与水反应:2Na+2H2O=2Na++2OH-+H2↑2.下列反应的离子方程式表示正确的是A. 用足量的氨水处理工业制硫酸的尾气:SO2+2NH3⋅H2O=2NH4++SO32-+H2OB. 向Fe(NO3)2和KI混合溶液中加入少量稀盐酸:3Fe2++4H++NO3-=3Fe3++2H2O+NO↑C. 漂白粉溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O===CaSO3↓+2HClOD. NH4HCO3溶液中加足量的Ba(OH)2溶液:NH4++ HCO3-+2OH-===CO32-+ NH3⋅H2O +H2O 3.下列化学反应的离子方程式正确的是( )A. 用稀HNO3溶解FeS固体:FeS+2H+===Fe2++H2S↑B. 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-===CaSO3↓+2HClOC. 在稀氨水中通入过量CO2:NH3·H2O+CO2===NH4++HCO3-D. 氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO42-===CaSO4↓+H2O 4.下列离子方程式书写正确的是A. 碘化亚铁中通入过量氯气:2Fe2++ 2I-+ 2Cl2= 2Fe3++ I2+ 4Cl-B. 碳酸钠溶液中通入过量氯气:CO32-+Cl2 = CO2↑+Cl-+ClO-C. NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42-+Ba2+ +OH-=BaSO4↓+H2OD. 金属钠投入硫酸镁溶液中:2Na + 2H2O + Mg2+ = 2Na+ + H2↑ + Mg(OH)2↓5.下列反应的离了方程式正确的是A. 碳酸钙与盐酸的反应:CO32-+2H+=CO2↑+H2OB. 硫酸溶液与氢氧化钡溶液的反应: H++OH-=H2OC. 硝酸银与氯化钠溶液的反应:AgNO3+Cl-=AgCl↓+NO3-D. 铝与硫酸铜溶液的反应:2Al+3Cu2+=2A13++3Cu6.下列表示对应化学反应的离子方程式正确的是本卷由系统自动生成,请仔细校对后使用,答案仅供参考。
高一化学离子方程式书写及判断练习题(附答案)

高一化学离子方程式书写及判断练习题一、多选题1.离子方程式2Ca 2+ + 3-3HCO + 3OH – → 2CaCO 3↓ + 2-3CO + 3H 2O 可以表示( ) A .Ca(HCO 3)2与NaOH 溶液反应B .NaHCO 3与澄清石灰水反应C .Ca(HCO 3)2与澄清石灰水反应D .NH 4HCO 3与澄清石灰水反应2、下列反应的离子方程式书写正确的是A .钠和水反应2Na +2H 2O =2Na ++2OH -+H 2↑ B .盐酸与氢氧化钠溶液反应H ++OH -=H 2O C .三氯化铁腐蚀印刷线路板Fe 3++Cu =Fe 2++Cu 2+D .盐酸与碳酸钙反应制备二氧化碳CO 32-+2H +=CO 2↑+H 23.下列反应的离子书写正确的是( ) A.钠和冷水反应:Na+2H 2O=Na ++2OH -+H 2↑B.金属铝溶于氢氧化钠溶液:Al+20H -=-2AIO +H 2↑ C.金属铝溶于盐酸中:2Al+6H +=2Al 3++3H 2↑ D.铁跟稀硫酸反应:Fe+2H +=Fe 2++H 2↑ 4.下列离子方程式不正确的是( )A.NaHSO 4溶液中滴加NaHCO 3溶液:H ++HCO 3-=H 2O+CO 2↑ B.NH 4HCO 3和过量NaOH 溶液相混合:HCO 3-+OH -=CO 32-+H 2O C.过量CO 2通入BaCl 2溶液反应:CO 2+H 2O+Ba 2+=BaCO 3↓+2H +D.用NaOH 吸收少量的H 2S:H 2S+2OH -=S 2-+2H 2O 5.能正确表示下列反应的离子方程式为( ) A.碳酸氢钠溶液中滴入氢氧化钙溶液: 3HCO OH --+232CO H O -+ B.二氧化硫通入次氯酸钠溶液: 22SO ClO OH --++242SO Cl H O --++ C.硫化钡加入稀硫酸: 2BaS H ++22H S Ba +↑+D.新制的氧化铝可溶于氢氧化钠溶液: 232Al O OH -+222AlO H O -+6.在复盐()442NH Fe SO 溶液中逐滴加入()2Ba OH 溶液,可能发生的反应的离子方程式是( )A. 22242FeSO Ba OH +-+-+++()42BaSO Fe OH ↓+↓B. 32244224NH Fe SO Ba OH++-+-++++ ()43232?BaSO Fe OH NH H O ↓+↓+ C. 32242336FeSO Ba OH +-+-+++ ()4332BaSO Fe OH ↓+↓D. 322443336NH Fe SO Ba OH++-+-++++ ()432333?BaSO Fe OH NH H O ↓+↓+7.下列反应的离子方程式书写正确的是( ) A.铁溶于盐酸中26Fe H++223Fe H ++↑B.澄清石灰水跟稀盐酸反应H OH+-+2H OC.碳酸氢钠与氢氧化纳溶液反应3HCO OH--+223H O CO -+D.硫酸镁溶液中加入氢氧化钡溶液224BaSO +-+4BaSO ↓8、下列离子方程式不正确的是A.Cl 2与稀NaOH 溶液反应:Cl 2+2OH -=Cl -+ClO -+ H 2O B.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H +=Fe 3++3H 2OC.烧碱溶液中加入铝片:Al + OH - + H 2O = AlO 2-+ H 2↑ D.Ba(OH)2溶液中加入过量Al 2(SO 4)3溶液:3Ba 2++6OH -+2Al 3++3SO 42-=3BaSO 4↓+2Al(OH)3↓9、下列反应能用离子方程式:CO 3 2 - + 2H +="==" CO 2 ↑ + H 2O 表示的是A.Na 2CO 3 + 2HCl="=" 2NaCl+ CO 2 ↑ + H 2OB.CaCO 3 + 2HCl ==CaCl 2 + H 2O + CO 2 ↑C.K 2CO 3 + H 2SO 4 ="=" K 2SO 4 + CO 2 ↑ + H 2OD.BaCO 3 + 2HNO 3 ==Ba(NO 3 )2+ CO 2 ↑ + H 2O10.下列各组离子反应可用H ++OH -=H 2O 表示的是( )A.氢氧化钡和硫酸B.氢氧化铁和盐酸C.硝酸和氢氧化钠D.硫酸氢钠和氢氧化钠 11.能正确表示下列反应的离子方程式是( ) A.将Cl 2通人氯化亚铁溶液:Fe 2+ +Cl 2 Fe 3++2Cl-B.氯气通入水中:Cl 2 + H 2O2H ++Cl - +ClO-C.AlCl 3溶液中加入过量的氨水:Al 3++ 3NH 3 • H 2OAl(OH)3 ↓ +3NH 4+D.Cl 2通入烧碱溶液中:Cl 2 + 2OH - Cl -+ ClO -+H 2O 二、不定项选择题12.下列离子方程式正确的有( )A.硫酸镁溶液跟氢氧化钡溶液反应: 224SO Ba-++4BaSO ↓B.稀硫酸滴在锌片上: 2Zn H ++22Zn H ++↑C. 3NaHCO 溶液与稀24H SO 反应: 232CO H-++22H O CO +↑D.氢氧化铜与稀盐酸混合: OH H -++2H O13、下列反应的离子方程式正确的是[ ]A.铝粉投入到NaOH 溶液中:2Al +2OH -= 2AlO 2-+ H 2↑ B.铁粉加入三氯化铁溶液中:2Fe +Fe 3+= 3Fe 2+C.AlCl 3溶液中加入足量的氨水:Al 3++ 3OH - = Al(OH)3↓ D.FeCl 2溶液中加入氯水:Cl 2 +2 Fe14、下列反应的离子方程式正确的是[ ]A.向碳酸氢钙溶液中加入少量氢氧化钠:Ca 2+ +2HCO 3-+2OH -→CaCO 3↓+2H 2O+CO 32-B.等体积、等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:Ba 2++2OH -+NH 4++HCO 3-→BaCO 3↓+NH 3·H 2O+H 2OC.碳酸钠溶液中通入少量二氧化碳气体:CO 32-+CO 2+H 2O→2HCO 3-D.Fe 2+、NaI 混合溶液中加入足量氯水:2I -15.下列反应的离子方程式正确的是( ) A.铜跟浓3HNO 反应: 342Cu H NO +-++ 22222Cu NO H O ++↑+ B.向氯化铝溶液中加入过量氨水: 33Al OH +-+ 222AlO H O -+C.向水通入中2NO :223NO H O + 322?H NO NO +-++ D.4NH Cl 溶液和3AgNO 溶液混合: 4 NH Cl Ag ++ 4 AgCl NH +↓+三、填空题16.下图是无机物A 到M 在一定条件下的转化关系(部分产物及反应条件未列出)。
高一化学《离子反应、离子方程式》分层练习含答案解析
第二节 离子反应第2课时 离子反应(分层练习)1.下列不属于离子反应的是A .氢气在氧气中燃烧B .盐酸和氢氧化钠溶液反应C .铁和硫酸铜溶液反应D .大理石和稀盐酸反应2.下列反应中,不属于离子反应的是A .H 2和O 2的反应B .铁与CuSO 4溶液的反应C .Ba(OH)2溶液和H 2SO 4溶液的反应D .Zn 和稀H 2SO 4反应3.下列物质间的反应不属于离子反应的是A .BaCO 3+ HClB .HCl + AgNO 3C .CO+ Fe 2O 3D .BaCl 2+ H 2SO 44.下列各组物质间的反应不属于离子反应的是A .盐酸+NaOH 溶液B .CaCl 2溶液+AgNO 3溶液C .Fe+CuSO 4溶液D .C+O 25.能用H + + OH - = H 2O 表示的是A .Ba(OH)2溶液和稀硫酸的反应B .NaOH 溶液和稀硫酸的反应C .Cu(OH)2和稀HNO 3的反应D .Ba(OH)2溶液NaHSO 4溶液的反应6.能用+2H +OH H O 表示的反应是A .氢氧化钡溶液与硫酸反应B .氢氧化铜与稀硝酸反应C .氢氧化钾与硫酸反应D .氢氧化钠与醋酸反应7.在离子方程式2Fe 3++Fe=3Fe 2+中,Fe 3 +可能代表的物质是A .FeSO 4B .FeCl 3C .Fe 2O 3D .Fe(OH)38.离子方程式CO 32-+2H +=H 2O+CO 2↑中CO 32-的代表的物质可以是A .CaCO 3B .NaHCO 3C .Na 2CO 3D .BaCO 39.关于离子方程式Cu 2++2OH -=Cu(OH)2↓的说法正确的是A .可表示所有铜盐和强碱的反应B .可表示某一个具体的反应,也可以表示一类反应C .离子方程式中的OH -可代表弱碱或强碱D .该反应可看到Cu(OH)2白色沉淀10.下列选项中的两个反应可用同一离子方程式表示的是A .HCl+Na 2CO 3,HCl+CaCO 3B .HNO 3(足量)+Na 2CO 3,NaHSO 4(足量)+K 2CO 3C .HCl+NH 3·H 2O ,H 2S+KOHD .BaCl 2+CuSO 4,Ba(OH)+NaHSO 4(足量)11.下列离子方程式正确的是A .在稀硝酸中滴加少量Na 2SO 3溶液:SO 32-+2H +=SO 2↑+H 2OB .在NH 4HSO 4溶液中滴加少量的Ba(OH)2,溶液:SO 42-+Ba 2+=BaSO 4↓C .磁性氧化铁溶于稀盐酸:Fe 3O 4+8H +=2Fe 3++Fe 2++4H 2OD .在FeCl 3溶液中滴加几滴KSCN 溶液:Fe 3++3SCN -=Fe(SCN)3↓12.下列指定反应的离子方程式书写正确的是A .硫化氢气体通入氯化铁溶液:2Fe 3++S 2-=S↓+2Fe 2+B .向碳酸氢铵溶液中加入足量石灰水:Ca 2++HCO 3-+OH -=CaCO 3↓+H 2OC .向稀硝酸中加入过量铁粉:Fe+NO 3-+4H +=Fe 3++NO↑+2H 2OD .用氨水吸收少量SO 2:2NH 3•H 2O+SO 2=2NH 4++SO 32-+H 2O13.下列离子方程式书写错误的是A .锌与稀硝酸溶液反应:22Zn 2H Zn H +++=+↑B .向氨水中加入盐酸:3242NH H O H NH H O++⋅+=+C .氯气与水反应:22Cl H O H Cl HClO+-+++ D .44NH HSO 溶液和NaOH 溶液(溶质物质的量)1:1反应:2H OH H O+-+=14.下列反应能用离子方程式CO 32-+2H +=CO 2↑+H 2O 表示的是①Na 2CO 3+2HCl=2NaCl+CO 2↑+H 2O②K2CO3+H2SO4=K2SO4+CO2↑+H2O③CaCO3+2HCl=CaCl2+CO2↑+H2O④2CH3COOH+Na2CO3=2CH3COONa+CO2↑+H2OA.①②B.①②③C.①③④D.②④15.下列离子方程式改写成化学方程式正确的是A.Mg2++2OH-=Mg(OH)2↓,MgCO3+2NaOH=Mg(OH)2↓+Na2CO3B.CO32-+2H+=CO2↑+H2O,NaHCO3+HCl=NaCl+CO2↑+H2OC.Fe2O3+6H+=2Fe3++3H2O,Fe2O3+2H2SO4=2FeSO4+2H2OD.H++OH-=H2O,2NaOH+H2SO4=Na2SO4+2H2O16.下列离子方程式改写为化学方程式正确的是选项离子方程式化学方程式A2H++Zn=Zn2++H2↑2CH3COOH+Zn=Zn(CH3COO)2+H2↑B Ba2++SO42-=BaSO4↓H2SO4+Ba(OH)2=BaSO4↓+2H2OC Ag++Cl-=AgCl↓AgNO3+HCl=AgCl↓+HNO3D Ca2++CO32-=CaCO3↓Ca(OH)2+CO2=CaCO3↓+H2O17.下列四组物质,从左至右都能发生化学反应的是(如:a+b-反应 b+c-反应 c+d-反应)a b c d①CO2NaOH溶液CuSO4溶液Fe②稀盐酸Na2CO3溶液CaCl2溶液CO2③AgNO3溶液BaCl2溶液稀硫酸Fe2O3④Zn稀盐酸NH4NO3溶液Ca(OH)2溶液A.①②③B.①③④C.①③D.①②③④18.写出下列指定反应的离子方程式(1)铜与稀硝酸反应________________________________;(2)NaAlO2溶液中通入足量CO2________________________________;(3)NaHSO4加入到Ba(OH)2溶液中至溶液呈中性____________________________________;(4)向NH4Al(SO4)2溶液中加入过量NaOH溶液______________________________________;(5)向一定量的FeBr2溶液中通入等物质的量的Cl2__________________________________________。
高一化学离子方程式的书写及正误判断试题答案及解析
高一化学离子方程式的书写及正误判断试题答案及解析1.胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打(NaHCO3),能治疗胃酸过多,请写出其反应的离子方程式:;如果病人同时患胃溃疡,为防胃壁穿孔,不能服用小苏打,原因是;此时最好用含氢氧化铝的胃药(如胃舒平),写出其反应的离子方程式:。
【答案】HCO3-+H+=CO2↑+H2O;因产生CO2压力增大而加剧胃壁穿孔;Al(OH)3+3H+=Al3++3H2O。
【解析】小苏打NaHCO3与胃酸HCl反应的化学方程式为NaHCO3+HCl=NaCl+H2O+ CO2↑,离子方程式为HCO3-+H+=CO2↑+H2O。
如果病人同时患胃溃疡,为防胃壁穿孔,不能服用小苏打是因为小苏打与胃酸反应产生的CO2压力增大,导致胃壁变大、变薄而加剧胃壁穿孔,使胃穿孔加剧。
此时最好用含氢氧化铝的胃药。
该反应的离子方程式Al(OH)3+3H+=Al3++3H2O。
【考点】考查治疗胃酸过多的药物的选择及应用的知识。
2.下列离子方程式正确的是A.碳酸氢钠与稀盐酸反应:HCO3—+H+=CO2↑+H2OB.铝溶于NaOH溶液:Al+2OH—=AlO2—+H2↑C.碳酸镁中滴加稀盐酸:CO32—+2H+=CO2↑+H2OD.硫酸铜溶液中滴加氢氧化钡溶液:Cu2++2OH—=Cu(OH)2↓【答案】A【解析】A、碳酸是弱酸,碳酸氢根离子不能改写,正确;B、电子、电荷不守恒,正确的是2Al+2OH—+2H2O=2AlO2—+3H2↑,错误;C、MgCO3难溶于水,不能拆写,正确的是MgCO3+2H+=Mg2++CO2↑+H2O,错误;D、漏写SO42—和Ba2+的离子反应,正确的是Cu2++SO42—+Ba2++2OH—=Cu(OH)2↓+BaSO4↓,错误。
【考点】考查离子方程式的书写等相关知识。
3.表示下列反应的离子方程式正确的是()A.金属钠加入到CuSO4溶液中:2Na+Cu2+=Cu+2Na+B.金属铝加入到NaOH溶液中:Al+2OH-+H2O=AlO2—+2H2↑C.铁粉加入到FeCl3溶液中:Fe+2Fe3+=3Fe2+D.铜片插入到AgNO3溶液中:Cu+Ag+=Cu2++Ag 【答案】C【解析】A、金属钠加入到CuSO4溶液中:2Na+2H2O+ Cu2+═2Na++Cu(OH)2↓+H2↑;B、金属铝加入到NaOH溶液中: 2Al+2OH-+2H2O=2AlO2— +3H2↑;C、铁粉加入到FeCl3溶液中:Fe+2Fe3+=3Fe2+;D、铜片插入到AgNO3溶液中:Cu+2Ag+=Cu2++2Ag。
高一化学离子方程式的书写.doc
专题一、离子方程式的书写和正误判断【例1】(1)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式。
(2)在以上中性溶液中,继续滴加Ba(OH)2溶液,请写出此步反应的离子方程式。
答案(1)SO2-4+2H++2OH-+Ba2+===BaSO4↓+2H2O(2)Ba2++SO2-4===BaSO4↓解析(1)Na+不参加反应,溶液呈中性时,HSO-4中的H+与Ba(OH)2中的OH-皆无剩余:2H++SO2-4+Ba2++2OH-===2H2O+BaSO4↓。
(2)上面所得中性溶液,实为Na2SO4(aq),继续滴加Ba(OH)2(aq)发生以下反应:Ba2++SO2-4===BaSO4↓。
该题类型为给定条件的离子方程式的书写,NaHSO4===Na++H++SO2-4、Ba(OH)2===Ba2++2OH-。
欲使NaHSO4溶液呈中性,只需将其中H+恰好中和即可。
而此时溶液中SO2-4显然过量,反应的离子方程式为:2H++SO2-4+Ba2++2OH-===BaSO4↓+2H2O。
由这一离子方程式可见,溶液中的SO2-4只反应了一半,当继续滴加Ba(OH)2时,发生以下反应:SO2-4+Ba2+===BaSO4↓。
【变式训练】(1)思考下列反应的离子方程式:①在NaHSO4溶液中加过量的Ba(OH)2溶液②Ba(OH)2溶液中加入过量的NaHSO4溶液提示①两溶液混合后,H+与OH-、SO2-4与Ba2+反应,由于NaHSO4少量,所以参与反应的H+与SO2-4的化学计量数之比为1∶1,故参与反应的OH-与Ba2+个数比也为1∶1:H++SO2-4+OH-+Ba2+===H2O+BaSO4↓。
②Ba(OH)2溶液不足时,Ba2+与OH-按物质的量之比为1∶2参加反应:Ba2++2OH-+2H++SO2-4===BaSO4↓+2H2O。
(2)①NaHCO3和Ba(OH)2两种固体中,________属于盐类,________属于碱类,将二者分别溶于水,其电离方程式分别为____________________,____________________。
高一化学离子方程式的书写及正误判断试题答案及解析
高一化学离子方程式的书写及正误判断试题答案及解析1.下列离子方程式书写错误的是()A.Na投入到水中:2Na+2H2O====2Na++2OH-+H2↑B.Al(OH)3溶于NaOH溶液中:Al(OH)3+OH-====Al+2H2OC.NaAlO2溶液中通入足量的CO2:2Al+CO2+3H2O====2Al(OH)3↓+CD.Al2O3粉末溶于NaOH溶液中:Al2O3+2OH-====2Al+H2O【答案】C【解析】 NaAlO2溶液中通入足量的CO2应该生成碳酸氢钠。
【考点】铝的氧化物与氢氧化物从铝土矿中提取铝2.下列有关镁及其化合物的离子方程式书写正确的是A.MgCO3与盐酸反应:C+2H+====CO2↑+H2OB.Mg(OH)2与H2SO4反应:Mg2++2OH-+2H++S====MgSO4↓+2H2OC.镁与醋酸反应:Mg+2H+====Mg2++H2↑D.工业上以海水为原料制取Mg(OH)2:Ca(OH)2+Mg2+====Mg(OH)2↓+Ca2+【答案】D【解析】 MgCO3和Mg(OH)2都是难溶性物质,醋酸为弱电解质,在写离子方程式时不能拆成离子形式,MgSO4是可溶性的盐,在写离子方程式时要拆成Mg2+和S的形式,A、B、C选项中的方程式都错误;工业上以海水为原料制取Mg(OH)2时,要在海水中加入石灰乳,而不是石灰水,所以Ca(OH)2不能拆成离子的形式。
【考点】镁的提取及应用3.(12分)我国有广阔的海岸线,海水综合利用大有可为。
海水中溴含量为65 mg·L-1,从海水中提取溴的工业流程如下:(1)以上步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将之转变成化合态的溴,其目的是:________________________________________________________________________。
(2)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用了溴的________。
