检验科酶联免疫实验原始记录
定性酶免疫测定的室内质控、数据处理及结果报告

浓度范围
质控品应覆盖待测样本可 能出现的浓度范围,以便 更好地监控测定系统的性 能。
质控规则制定
警戒限
用于早期发现测定系统可能存在 的问题,警戒限通常设定为质控
品预期浓度的±3σ。
失控限
用于判断测定结果是否可接受,失 控限通常设定为质控品预期浓度的 ±5σ。
反应时间
记录每个质控品的反应时间,以评 估测定系统的反应速度和灵敏度。
持续优化数据处理流程
数据清洗
对原始数据进行清洗,去除异常值和离群点,确保数据质量 。
算法优化
对数据处理算法进行持续优化,提高数据处理效率和准确性 。
提高结果报告的可读性与准确性
标准化报告格式
采用标准化的报告格式,使结果报告 更加清晰易读。
审核机制
建立结果报告审核机制,确保报告的 准确性。
感谢您的观看
确保数据格式统一,以便进行后续的 数据处理和分析。
异常值识别
通过统计学方法(如Z分数)或经验 阈值识别异常值,并对其进行处理, 如删除或替换。
异常值处理
识别异常值
通过统计学方法(如四分位数范 围、Z分数等)或专业经验识别
异常值。
异常值处理
根据实际情况选择合适的处理方 法,如删除、替换或进行进一步
的验证。
定性酶免疫测定的室内 质控、数据处理及结果 报告
目录 CONTENT
• 室内质控 • 数据处理 • 结果报告 • 数据分析与解读 • 质量控制改进措施
01
室内质控
质控品选择
01
02
03
稳定性
质控品应具有较好的稳定 性,以保证在长时间内保 持一致的浓度和性能。
基质匹配
质控品应与待测样本具有 相似的基质背景,以减少 误差和偏差。
HIV抗体检测试验原始记录(英科新创试剂)

HIV抗体检测试验原始记录(英科新创试剂)HIV抗体检测试验(ELISA法)原始记录编号:(张疾控)字(原始记录)第()号第页共页试剂名称:(英科新创)试剂批号:试剂效期:样品状态:样品来源:送检人群:环境温度:检测仪器:1.北京普朗DNM-9602型酶酶标仪 2.北京普朗DNM-9620型洗板机3. 电热恒溫水浴箱4. 移液器检测地点:检测日期:检测份数:检测依据:《全国艾滋病检测技术规范》(2009年修订版)实验步骤:1.实验准备:样品、试剂、酶标条置室温(18-25℃),平衡时间_30_分钟。
按实验室SOP做好试剂准备。
2.温育期间配制洗涤液:按1:19稀释,取20×洗涤液 ml,加蒸馏水 ml。
()3. 将酶联反应板从密封袋中取出,取下孔板条,放在板架上。
按顺序编号,设一个空白对照孔,两个阳性(1)对照孔,两个阳性(2)对照孔,两个阴性对照孔。
()4.取阳性对照和阴性对照分别充分混匀后各50μl加入对照孔中,空白孔不加,其余每个孔加待检血清50μl,轻轻振荡,充分混匀。
并填写加样顺序表(见下表)。
()5.用不干胶封片封盖反应板,置37℃温育60分钟。
()6.撕去贴膜,用洗涤液洗5次(洗板机洗,程序已编好),然后在吸水纸上拍干。
()7.除空白孔外每孔加酶标抗原100μl,用不干胶片封盖反应板。
37℃温育30分钟。
()8. 撕去贴膜,用洗涤液洗5次(洗板机洗,程序已编好),然后在吸水纸上拍干。
()9.每孔加显色剂A 50μl ,显色剂B 50μl,轻轻振荡后置37℃避光暗处显色30分钟。
()10. 每孔加终止剂50μl。
混匀。
()11.选择酶标仪450nm或630 nm双波长测定,空白孔调零点,测定各孔的吸光度。
并打印结果。
()12. 加样顺序表:ABCDEFGH1314.判定公式:Cut off值=阴性对照平均值+0.10 当阴性对照平均值≤0.05时,按0.05计算。
本次检测临界值为:____________。
酶联免疫吸附试验检测乙肝表面抗体阴性而电化学发光法检测阳性二例报告

疗 和 防治 有 重 要 的参 考 价 值 。 大 多 数 医 院 测 定 HB Ab均 s 采 用 E IA 法 , 是 E IA 法 在 操 作 中 受 到 影 响 的 因 素 LS 但 LS
很多 , 比如 溶 血 、 自身抗 体 、 体 和 易 发 生 交 叉 反 应 的 内 源 补
清 购 自中 国 卫 生 部 临 床 检 验 中心 。 1 3 方 法 : E IA 法 : 用 双 抗 原 夹 心 法 : 苯 乙烯 板 . ① LS 采 聚 包 被 HB Ag 与 标本 中 标 记 的 HB Ab结 合 , 入 辣 根 过 氧 s , s 加 化 物 酶 培 育 , 去 游 离 的酶 标 抗 原 , 四 甲基 联 苯 胺 为 底 物 洗 以 显 色 , 酸 终 止 后 4 0 6 0n 处 读 取 吸 光 度 值 ( ) 阴 经 5 / 3 m A 。 性 对 照 平 均 A 值 ×2 1为 临 界 值 。检 测 孔 A 值 大 于 临 界 值 .
液 吸 入 流 动 室 , 微 粒 由磁 铁 吸 附 到 电 极 表 面 , 入 三 丙 磁 加
优 于 E IA 法 , 能 准确 地进 行 定 量 检 测 , s LS 且 HB Ab只 有 定
量 值 在 1 0U/ 以 上 时 才 具 有 抵 抗 HB 入 侵 的 作 用 ] 0 L V ,
( s ) 性 而 电化 学 发 光 法 ( C I 法 ) 测 阳 性 , 分 HB Ab 阴 E LA 检 现 析 如下 。 1 资 料 与 方 法
表 2 患 者 2E IA 法 和 E LI 法 检 测 结 果 LS C A
1 1 临 床 资 料 :0 0年 1 . 21 1月 前 来 我 院 就 诊 的 患 者 2例 , 例 l女性 , , 5岁 , 出 生 时 注 射 乙 肝 三 联 疫 苗 ; 2 男 性 , 于 例 , 3 岁 , 出 生 时 注 射 乙肝 三联 疫 苗 。患 者 静 脉 取 血 , 心 分 离 于 离
001酶免检测过程及关键控制点检查记录清样
是□否□
是□否□
是□否□
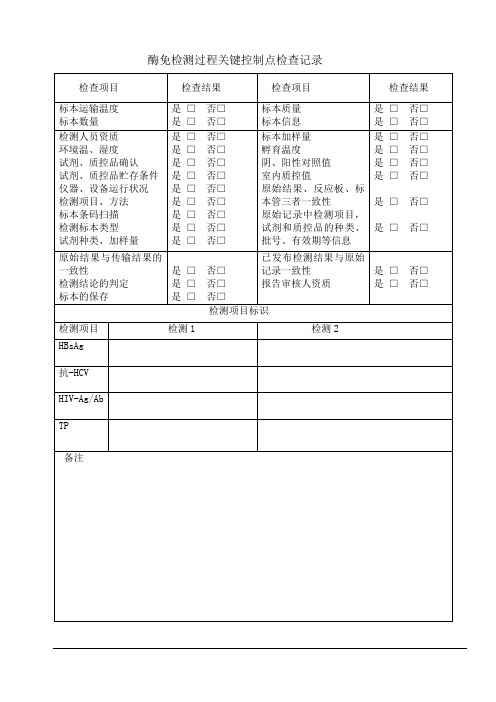
标本加样量
孵育温度
阴、阳性对照值
室内质控值
原始结果、反应板、标本管三者一致性
原始记录中检测项目,试剂和质控品的种类、批号、有效期等信息
是□否□
是□否□
是□否□
是□否□
是□否□
是□否□
原始结果与传输结果的一致性
ห้องสมุดไป่ตู้检测结论的判定
标本的保存
是□否□
是□否□
是□否□
已发布检测结果与原始记录一致性
报告审核人资质
是□否□
是□否□
检测项目标识
检测项目
检测1
检测2
HBsAg
抗-HCV
HIV-Ag/Ab
TP
备注
检查人
复核人
“是”表示符合要求或与实际相符“否”表示不符合要求或与实际不符发现不符项目将具体内容填写在“备注”中
酶免检测过程关键控制点检查记录
检查项目
检查结果
检查项目
检查结果
标本运输温度
标本数量
是□否□
是□否□
标本质量
标本信息
是□否□
是□否□
检测人员资质
环境温、湿度
试剂、质控品确认
试剂、质控品贮存条件
仪器、设备运行状况
检测项目、方法
标本条码扫描
检测标本类型
试剂种类、加样量
是□否□
是□否□
是□否□
是□否□
是□否□
酶标仪定性检测原始记录

1
定
性
结
果
2
3
4
5
6
7
8
9
10
11
12
备注
分析人:校核人:审核人:
qnjqrd24382014酶标仪定性检测原始记录样品名称样品编号检测日期样品状态检测方法温度试剂盒检测项目湿度检测步骤程序参数工作波长振板方式检测方式定性公式定性方向阴性对照值阳性对照值无效性判断孔位设置定性对照值临界值阴性n阳性p弱阳性l灰色区吸光度101112备注分析人
QNJQRD2438-2014
酶标仪定性检测原始记录
No:第页共页
样品名称
样品编号
检测日期
样品状态
检测方法
温度
℃
试剂盒
检测项目
湿度
%
检测步骤
程序参数
工作波长
单双孔位
振板方式
检测方式
定性公式
定性方向
阴性对照值
阳性对照值
无效性判断
孔位设置
检测结果
定性对照值
临界值
阴性N
阳性P
弱阳性L
灰色区
吸Байду номын сангаас度
A
B
C
D
E
F
G
H
A
B
C
D
E
F
G
H
样
品
吸
光
检验科常见免疫学检测方法介绍

检验科常见免疫学检测方法介绍免疫学检测是一种通过测试体内免疫系统的反应来评估病理状况的方法。
它在临床医学中具有广泛的应用,可以用于诊断、预防和监测疾病。
本文将介绍检验科中常见的免疫学检测方法,并从原理、应用范围和优缺点等方面进行分析。
一、酶联免疫吸附试验(Enzyme-Linked Immunosorbent Assay, ELISA)酶联免疫吸附试验是一种常用的免疫学检测方法,它通过检测抗原和抗体之间的特异性结合来确定目标物的存在与否。
ELISA的原理简单,操作方便,并且可以高通量地检测多个样本。
只需少量的样品,即可进行大规模的检测。
然而,ELISA也存在一些限制,如交叉反应较高、灵敏度较低等。
二、免疫荧光检测(Immunofluorescence Assay, IFA)免疫荧光检测是一种利用荧光染料标记抗体来检测样本中特定抗原的方法。
它在病毒感染、自身免疫性疾病等方面有着广泛的应用。
通过观察样本中荧光的分布和强度,可以确定目标物的存在和定量分析。
与ELISA相比,IFA在特异性和检测灵敏度上都有较大的优势。
三、流式细胞术(Fluorescence-Activated Cell Sorting, FACS)流式细胞术是一种基于细胞表面标记物的免疫学分析技术。
它可以用于分离和鉴定不同类型的细胞,并研究它们的功能和活性。
流式细胞术结合了免疫学、生物物理学和细胞生物学的原理,可以对单个细胞进行多参数分析。
因此,它在肿瘤科研和免疫监测中得到了广泛应用。
四、免疫印迹(Western Blotting)免疫印迹是一种检测特定蛋白质的方法,它可以通过分析细胞和组织中的蛋白质表达来诊断疾病。
免疫印迹通过将蛋白质分离和转移至膜上,然后通过特异性抗体与目标蛋白质结合,并通过酶反应可视化目标蛋白质的位置和数量。
免疫印迹的优势是可以同时检测多个蛋白质,但也存在一些局限性,如对蛋白质大小和亲和性的依赖。
五、免疫组织化学(Immunohistochemistry, IHC)免疫组织化学是一种通过免疫染色来定位和分析细胞或组织中目标蛋白质的方法。
HIV抗体筛查实验原始记录
HIV抗体筛查实验原始记录(ELISA)
1 样本来源:
2 检测日期:标本数量:实验室温/湿度:℃ %
3 试剂厂家:试剂批号:试剂效期:
4 洗板机型号:酶标仪型号:
5 实验步骤:
(1)将试剂盒恢复至室温,准备相应的数目反应板(条)。
(2)在相应孔中加入待测样品 ul,阴性对照 ul,阳性对照ul,外部质控 ul,37℃孵育分钟,时分至时
分。
(3)每孔加入酶标试剂100ul,空白孔除外。
(4)用封板膜封板后,置37±1℃温育60±2分钟。
(5)小心揭掉封板膜,用洗板机洗板次,拍干,加入显色剂ul,℃闭光显色分钟,时分至时
分。
(6)加入反应终止液 ul,置波长450nm(参考波长630nm)测OD值。
6 实验蓝图:
7.检测结果:(酶标打印结果)
检测者:复核者:。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
陕西省结核病防治院检验科酶联免疫实验
原始记录
检验项目: HIV-抗体筛查试验 实验日期: 2014-12-1 使用仪器机器编号:洗板机KHB ST-36W 型 酶标仪ST-360型 恒温水浴箱 实验室温度、湿度: 26 ℃ 65 %RH 试验依据: GB/6000—1995 试剂厂家名称: 英科新创(厦门)科技有限公司 试剂批号: 2014020102 试剂效期: 20150824 检验步骤:
将样本、试剂盒置室温平衡30分钟,严格按照试剂盒说明书操作,设置S 、N 、P 各孔位置,S 、N 、P 各加50ul 与相对应的孔中,封板 ,洗板 5遍拍
干,每孔加入酶标试剂100ul ,封板 , 洗板5遍拍干,每孔加入显色剂A 、B 各50ul ,封板混匀, ,每孔加入终止液50ul ,混匀,即可于酶标仪比
色,测定各孔吸光度值(450nm/630nm ,10分钟内测定) 样本编号及酶标板对应关系
注: N 阴性对照 P 代表阳性对照 B 代表空白 Q 代表质控
实验结果附页酶标图谱
37 ℃
60分钟 37 ℃ 30分钟
37 ℃
30分钟
原始记录
检验项目: HIV-抗体筛查试验 实验日期: 2014-12-1 使用仪器机器编号:洗板机KHB ST-36W 型 酶标仪ST-360型 恒温水浴箱 实验室温度、湿度: 26 ℃ 65 %RH 试验依据: GB/6000—1995 试剂厂家名称: 英科新创(厦门)科技有限公司 试剂批号: 2014020102 试剂效期: 20150824 检验步骤:
将样本、试剂盒置室温平衡30分钟,严格按照试剂盒说明书操作,设置S 、N 、P 各孔位置,S 、N 、P 各加50ul 与相对应的孔中,封板 ,洗板 5遍拍
干,每孔加入酶标试剂100ul ,封板 , 洗板5遍拍干,每孔加入显色剂A 、B 各50ul ,封板混匀, ,每孔加入终止液50ul ,混匀,即可于酶标仪比
色,测定各孔吸光度值(450nm/630nm ,10分钟内测定) 样本编号及酶标板对应关系
注: N 阴性对照 P 代表阳性对照 B 代表空白 Q 代表质控
实验结果附页酶标图谱
37 ℃
60分钟 37 ℃ 30分钟
37 ℃
30分钟
原始记录
检验项目:HIV-抗体筛查试验实验日期:2014-12-1 实验室温度、湿度:26℃68 %RH 试验依据:胶体金免疫技术和层析原理试剂厂家名称:珠海丽珠试剂股份有限公司
试剂批号:2014070702 试剂效期:20160106
检测记录
检验步骤:
1.将带测样品及所需试剂从贮存条件下取出,平衡至室温。
2.打开铝箔袋,取出试纸卡平置于工作台面。
3.将50微升(1滴)样品加在加样区,然后加1滴样品稀释液。
4.等待红色条带的出现,在15分钟时读取测试结果。
阳性:在检测线和质控线位置上各出现一条紫红色条带。
阴性:仅在质控线位置上出现一条紫红色条带。
无效:在检测线和质控线位置上均未出现紫红色条带,或仅在检测线位置出现紫红色条带。
5.测试结果应在15分钟时读取,30分钟后判读无效。
检验者:审核者:时间:2014.12.1。
