烃的衍生物的化学反应归纳与整理
烃的衍生物知识总结

Na2CO3 反应生成硝 酸钠、水和 CO2
NaHCO3 反应生成硝 酸钠、水和 CO2
反应生成 反应生成酚
CH3COONa、 钠C6H5ONa
水和CO2
和NaHCO3
反应生成 CH3COONa、 水和CO2
不反应
不反应 不反应
PPT文档演模板
烃的衍生物知识总结
•几种物质与高锰酸钾和溴水的作用:
PPT文档演模板
烃的衍生物知识总结
•卤代烃
•烃的衍生物知识总结
•醇类
•烃的衍生物
•醛类
•羧酸
•酯(油脂)
•酚
•通式:CnH2n-6O(n≥6)
•(1)易被氧化变质(氧化反应)
•酚
•代表
物•OH
•化性•(2)与Br2发生取代(取代反应) •(3)与FeCl3显紫色(显色反应) •(4)弱酸性(比碳酸的酸性弱)
• 卤代烃的水解
• 酯化反应
• 酯的水解
PPT文档演模板
烃的衍生物知识总结
PPT文档演模板
2.加成反应:
烯(C=C)、 炔烃(加H2、HX、H2O), 苯(加H2)、 醛(加H2)、酮 油脂氢化(加H2)。
烃的衍生物知识总结
PPT文档演模板
3.消去反应:
乙醇(分子内脱H2O)
•卤代烃(脱HX)
烃的衍生物知识总结
• 例5.已知乙炔(C2H2)、苯 (C6H6)、乙醛(C2H4O)的混 合气体中含氧元素的质量分数为 8%,则混合气体中碳元素的质 量分数为( )
•A.84%
B.
60%
•C.91%
D.
42%
PPT文档演模板
烃的衍生物知识总结
• 例6、下列各组混合物中,总质量一定时,
烃的衍生物重要知识点总结
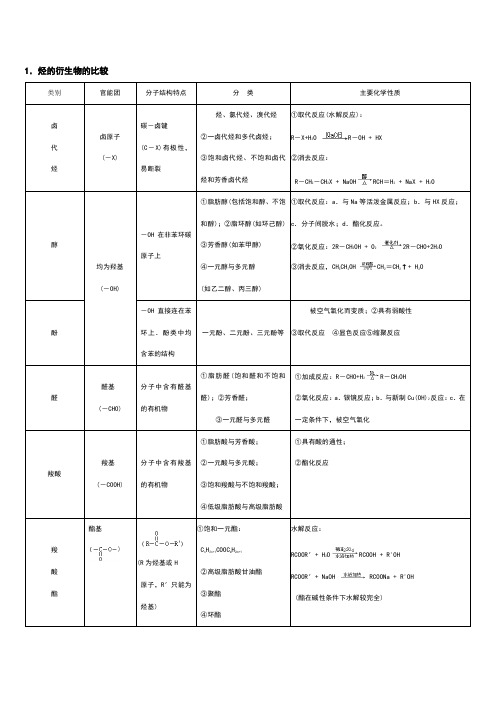
1.烃的衍生物的比较类别官能团分子结构特点分类主要化学性质卤代烃卤原子(-X)碳-卤键(C-X)有极性,易断裂烃、氯代烃、溴代烃②一卤代烃和多代卤烃;③饱和卤代烃、不饱和卤代烃和芳香卤代烃①取代反应(水解反应):R-X+H2O R-OH + HX②消去反应:R-CH2-CH2X + NaOH RCH=H2 + NaX + H2O醇均为羟基(-OH)-OH在非苯环碳原子上①脂肪醇(包括饱和醇、不饱和醇);②脂环醇(如环己醇)③芳香醇(如苯甲醇)④一元醇与多元醇(如乙二醇、丙三醇)①取代反应:a.与Na等活泼金属反应;b.与HX反应;c.分子间脱水;d.酯化反应。
②氧化反应:2R-CH2OH + O22R-CHO+2H2O③消去反应,CH3CH2OH CH2=CH2↑+ H2O酚-OH直接连在苯环上.酚类中均含苯的结构一元酚、二元酚、三元酚等被空气氧化而变质;②具有弱酸性③取代反应④显色反应⑤缩聚反应醛醛基(-CHO)分子中含有醛基的有机物①脂肪醛(饱和醛和不饱和醛);②芳香醛;③一元醛与多元醛①加成反应:R-CHO+H2R-CH2OH②氧化反应:a.银镜反应;b.与新制Cu(OH)2反应:c.在一定条件下,被空气氧化羧酸羧基(-COOH)分子中含有羧基的有机物①脂肪酸与芳香酸;②一元酸与多元酸;③饱和羧酸与不饱和羧酸;④低级脂肪酸与高级脂肪酸①具有酸的通性;②酯化反应羧酸酯酯基(R为烃基或H原子,R′只能为烃基)①饱和一元酯:C n H2n+1COOC m H2m+1②高级脂肪酸甘油酯③聚酯④环酯水解反应:RCOOR′+ H2O RCOOH + R'OHRCOOR′+ NaOH RCOONa + R'OH(酯在碱性条件下水解较完全)2.有机反应的主要类型反应类型定义举例(反应的化学方程式)消去反应有机物在一定条件下,从一个分子中脱去一个小分子(如H2O、HBr等)而生成不饱和(含双键或叁键)化合物的反应C2H5OH CH2=CH2↑+ H2O苯酚的显色反应苯酚与含Fe3+的溶液作用,使溶液呈现紫色的反应还原反应有机物分子得到氢原子或失去氧原子的反应CH≡CH + H2CH2=CH2 CH2=H2 + H2CH3CH3 R—CHO + H2R-CH2OH氧化反应燃烧或被空气中的O2氧化有机物分子得到氧原子或失去氢原子的反应2CH3CH2OH + O2 2CH3CHO + 2H2O2CH3CHO + O2 2CH3COOH银镜反应CH3CHO + 2Ag(NH3)2OH CH3COONH4+2Ag↓+ 3NH3↑+ H2O红色沉淀反应CH3CHO + 2Cu(OH)2CH3COOH + Cu2O↓+ 2H2O取代反应卤代烃水解NaOH水溶液,卤代烃水解,生成醇和卤化氢的反应R-CH2X + H2O RCH2OH + HX 酯化反应酸(无机含氧酸或羧酸)与醇作用,生成酯和水的反应RCOOH + R'CH2OH RCOOCH2R′+ H2O 酯的水解反应在酸或碱存在的条件下,酯与水作用生成醇与酸的反应RCOOR′+ H2O RCOOH + R'OHRCOOR′+ NaOH → RCOONa + R'OH4.醇、酚、羧酸中羟基的活性比较羟基种类重要代表物与Na反应与NaOH反应与Na2CO3反应醇羟基CH3CH2-OH√××酚羟基HO√√√但不放出气体羧酸羟基CH3-C-OHO√√√放出CO2。
烃的衍生物知识总结精选全文完整版

可编辑修改精选全文完整版烃的衍生物知识总结一、卤代烃(代表物C 2H 5Br ):烃分子中的氢原子被卤素原子取代后的产物。
(卤素原子) 1、通式: C n H 2n+1X 、 R —X 2、化学性质:(1)、取代反应:C 2H 5Br + H 2O C 2H 5OH + HBr (水解反应)C 2H 5Br + NaOH C 2H 5OH + NaBr(2)、消去反应:C 2H 5Br + NaOH CH 2==CH 2↑+ NaBr +H 2O 3、卤代烃中卤素原子的检验:取少量卤代烃,加NaOH 溶液,加热,一段时间后加HNO 3酸化后再加AgNO 3,如有白色沉淀说明有Cl ¯,如有浅黄色沉淀则有Br ¯,如有黄色沉淀则有I ¯。
二、醇(代表物:CH 3CH 2OH )1、通式:R —OH ,饱和一元醇C n H 2n+1OH2、化学性质:(1)非电解质,中性,不电离出H+; (2)与K 、Ca 、Na 等活泼金属反应放出H 2; 2C 2H 5OH + 2Na 2C 2H 5ONa + H 2↑(3)氧化反应:燃烧:C 2H 5OH +3O 2 2CO 2 +3H 2O 催化氧化:2C 2H 5OH + O 2 2CH 3CHO + H 2O(4)脱水生成乙烯或乙醚。
消去反应: C 2H 5OH CH 2==CH 2↑+ H 2O 取代反应:2C 2H 5OH CH3CH 2OCH 2CH 3+ H 2O(5三、酚(代表物:) 1、化学性质:(1)、弱酸性:酸性: + NaOH + H 2O弱酸性: + H 2O + CO 2 + NaHCO 3(强酸制弱酸)(2)、取代反应: + 3Br 2↓ + 3HBr (3)、显色反应:与Fe 3+反应生成紫色物质 四、醛(代表物:CH 3CHO 、HCHO )1、通式:RCHO ,一元饱和醛:C n H 2n+1CHO ,分子式:C n H 2n O2、化学性质:(1)、加成反应:CH 3CHO + H 2催化剂 △CH 3CH 2OH (还原反应)NaOH △醇 △—OH —OH—ONa—ONa —OH —OH —OH BrBrBr点燃Cu 或Ag △浓硫酸170℃浓硫酸 140℃△(2)、氧化反应:①催化氧化:2CH 3CHO + O 2催化剂 △2CH 3COOH②银镜反应:CH 3CHO +2 Ag (NH 3)2OH△2Ag ↓+ CH 3COONH 4 +3 NH 3 + H 2O③与新制Cu (OH )2反应:CH 3CHO + 2Cu (OH )2△Cu 2O + CH 3COOH + 2H 2O3、制法:(1)乙烯氧化法 (2)乙炔水化法 (3)乙醇氧化法 五、羧酸(代表物: CH 3COOH 、HCOOH )1、通式:R —COOH ,一元饱和酸C n H 2n+1COOH ,分子式C n H 2n O 22、化学性质:(1)具有酸的通性(羧酸盐几乎全溶于水):CH 3COOH + NaOH === CH 3COONa + H 2O2CH 3COOH +2 Na → 2CH 3COONa + H 2↑ CH 3COOH + NaHCO 3→ CH 3COONa + H 2O+CO 2↑ (2)与醇酯化成酯(酸脱羟基醇脱氢): CH 3COOH + CH 3CH 2OH浓硫酸 △CH 3COOCH 2CH 3 + H 2O(3)甲酸、甲酸盐、甲酸形成的酯都具有醛基能发生银镜反应。
化学选修五烃的衍生物知识点归纳

苯及苯的同系物: C)化学性质:①取代反应(与液溴、HNO 3、H 2SO 4等)②加成反应(与H 2、Cl 2等)醇类:A) 官能团:—OH (醇羟基); 代表物: CH 3CH 2OH 、HOCH 2CH 2OHB) 结构特点:羟基取代链烃分子(或脂环烃分子、苯环侧链上)的氢原子而得到的产物。
结构与相应的烃类似。
C) 化学性质:①羟基氢原子被活泼金属置换的反应②跟氢卤酸的反应 ③催化氧化(α—H )④酯化反应(跟羧酸或含氧无机酸) 醛酮A) 官能团:(或—CHO)、 (或—CO —) ;代表物:CH 3CHO 、HCHO 、 ①加成反应(加氢、氢化或还原反应)②氧化反应(醛的还原性)羧酸A) 官能团: (或—COOH);代表物:CH 3COOH2CH 3CH 2OH + 2Na2CH 3CH 2ONa + H 2↑ HOCH 2CH 2OH + 2NaNaOCH 2CH 2ONa + H 2↑CH 3CH 2OH + HBr CH 3CH 2Br + H 2O△2CH 3CH 2OH + O 22CH 3CHO + 2H 2O △ Cu 或AgHOCH 3CH 2OH + O 2OHC —CHO+ 2H 2O△Cu 或Ag 2CH 3CHCH 3 + O 22CH 3CCH 3 + 2H 2OOHO△Cu 或AgO—C —H O—C —O CH 3—C—CH 3CH 3CHO + H 2CH 3CH 2OH△催化剂 + H 2CH 33OH OCH 3—C —CH 3 △催化剂 2CH3CHO + 5O24CO 2 + 4H 2O 点燃CH 3CHO + 2[Ag(NH 3)2OH]CH 3COONH 4 + 2Ag ↓ + 3NH3 + H 2O (银镜反应)△CH 3CHO + 2Cu(OH)2CH 3COOH + Cu 2O ↓ + H 2O (费林反应)△2CH 3CHO + O 22CH 3COOH 催化剂OH —C —H + 4[Ag(NH 3)2OH](NH 4)2CO 3 + 4Ag ↓ + 6NH 3 + 2H 2O△O—C —OH + Br 2+ HBr ↑ Br Fe 或FeBr 3+ HNO 3+ H 2O NO 2 浓H 2SO 460℃ + 3H 2Ni △+ 3Cl 2 紫外线C) 化学性质:①具有无机酸的通性 ②酯化反应 酯类A) 官能团:(或—COOR )(R 为烃基); 代表物: CH 3COOCH 2CH 3 C) 化学性质:水解反应(酸性或碱性条件下)与Na 反应的有机物:含有—OH 、—COOH 的有机物.与NaOH 反应的有机物:常温下,易与含有 酚羟基...、—COOH 的有机物反应加热时,能与卤代烃、酯反应(取代反应)与Na 2CO 3反应的有机物:含有酚.羟基的有机物反应生成酚钠和NaHCO 3;含有—COOH 的有机物反应生成羧酸钠,并放出CO 2气体;与NaHCO 3反应的有机物:含有—COOH 、—SO 3H 的有机物反应生成羧酸钠、磺酸钠并放出等物质的量的CO 2气体。
烃的衍生物知识总结

C17H35COOCH
C17H35COOCH2
烃的衍生物知识总结
烃的衍生物
卤代烃 醇类 醛类 通式:CnH2n-6O(n≥6) 化性 代表物 OH (1)易被氧化变质(氧化反应) (2)与Br2发生取代(取代反应) (3)与FeCl3显紫色(显色反应) (4)弱酸性(比碳酸的酸性弱) Cl OH 羧酸 酯(油脂) 酚
红热铜丝插入醇中有刺激性气味
(1)弱酸性 (2)取代反应 (3)显色反应
与FeCl3显紫色
苯、甲苯、苯酚的结构与性质的比较
类别 苯
不被高锰酸钾 溶液氧化 液溴 催化剂 C6H5Br
甲苯
—CH3 可被高锰酸钾溶 液氧化 液溴 催化剂 邻、间、对三种 一溴甲苯
苯酚
—OH
常温下在空气中被氧 化呈红色 溴水 无催化剂 三溴苯酚
化性
代表物 CH3CH2OH
制法 (1)乙烯水化 (2)淀粉发酵
烃的衍生物知识总结
烃的衍生物
卤代烃 醇类 醛类 羧酸 酯(油脂) 酚
通式:RCHO,一元饱和醛CnH2n+1CHO,分子式CnH2nO
醛类
化性
代表物 CH3CHO (1)乙烯氧化法 制法 (2)乙炔水化法 HCHO (3)乙醇氧化法
(1)氧化反应:银镜反应、与新制Cu(OH)2反应 能使溴水、高锰酸钾溶液褪色 (2)还原反应:加氢被还原成乙醇 (3)甲醛与苯酚缩聚成酚醛树脂
结构简式 氧化反应情况
溴 代 反 应 溴状态
条件 产物
结论 原因
苯酚与溴的取代反应比苯、甲苯易进行 酚羟基对苯环的影响使苯环上的氢原子变得活泼,易被 取代
;厂房出租网 厂房出租 厂房出租网 厂房出租 ;
个老家伙气息无比厚叠,似是比那魏振志,实历还要强大の样子.
烃的衍生物知识总结
化性
代表物 CH3CH2OH
制法 (1)乙烯水化 (2)淀粉发酵
烃的衍生物知识总结
烃的衍生物
卤代烃 醇类 醛类 羧酸 酯(油脂) 酚
通式:RCHO,一元饱和醛CnH2n+1CHO,分子式CnH2nO
醛类
化性
代表物 CH3CHO (1)乙烯氧化法 制法 (2)乙炔水化法 HCHO (3)乙醇氧化法
(1)氧化反应:银镜反应、与新制Cu(OH)2反应 能使溴水、高锰酸钾溶液褪色 (2)还原反应:加氢被还原成乙醇 (3)甲醛与苯酚缩聚成酚醛树脂
水解 取代
醇类 R—OH
氧化 加氢
醛类 R—CHO
氧化
羧酸 R—COOH
酯化 水解
酯类 RCOOR`
CH3CH3 CH2=CH2
CH3CH2Br CH3CH2OH CH2Br
CH3COOC2H5 CH3CHO CH2OH CH2OH O=C O=C O CHO CHO O CH2 CH2 CH3COOH COOH COOH
制法
烃的衍生物知识总结
烃的衍生物
卤代烃 醇类 O 通式:R`—C—O—H,油脂的通式 酯(油脂) 代 表 物 CH3COOC2H5 C17H35COOCH2 醛类 羧酸 酯(油脂) R`—COO—CH2 酚
R``—COO—CH
R```—COO—CH2
(1)水解生成酸和醇 性质 (2)油脂发生皂化反应 (3)甲酸某酯具有还原性能发生银镜反应 制法:酸(羧酸或无机含氧酸)与醇反应制得
பைடு நூலகம்
CH=CH
CH2Br [ CH2—CH ]n Cl
CH2=CHCl
醇和酚的比较
类别 实例 官能团 结构 特点 脂肪醇 CH3CH2OH —OH 芳香醇 C6H5CH2OH —OH 酚 C6H5OH —OH
烃的衍生物总结

烃的衍生物-规律•易混点•易错点I.性质•制法•鉴别一.卤代烃:(以饱和一元卤代烃为代表物.通式:C n H2n+1X)化学性质:1.消去反应:⑴.条件:与NaOH醇溶液共热(无水条件下,醇作溶剂)。
⑵.结果:形成碳碳不饱和键。
⑶.反应举例:⑷.特例:*①.扎依采夫定则:当消去反应有两种可能时,卤素原子主要与其所连碳原子邻旁含氢较少的碳原子上的氢原子发生消去反应。
*②.多元卤代烃的消去反应:一般来说,卤代烃分子中有多少个卤原子,经过完全消去就能形成多少碳碳不饱和键。
⑸.不能发生消去反应的卤代烃:①.分子中只有1个碳原子的卤代烃。
如CH3X、CH2X2、CHX3等。
②.卤素原子所连碳原子邻旁碳原子上不含氢原子的卤代烃。
如R-C(CH3)2CHXC(C2H5)CH3、CR3-CH2X.2.水解反应:⑴.条件:与NaOH水溶液共热。
⑵.结果:发生取代反应,生成含羟基的化合物。
⑶.反应举例:CH3CH2Cl+H2O CH3CH2OH+HCl.⑷.特例:多元卤代烃的水解反应:①.当卤原子连在不同碳原子上时:完全水解时生成多元醇。
②.当卤原子连在相同碳原子上时:i.同一碳原子上连两个卤原子:完全水解时生成醛。
R-CHX2+H2O R-CHO+2HX.ii.同一碳原子上连3个卤原子:完全水解时生成羧酸。
R-CX3+H2O R-COOH+3HX.*③.双键碳原子及苯环碳原子上的卤原子不易发生水解反应。
制法:1.卤代反应:⑴.烷烃卤代:属于链锁反应,制得的产物不纯。
一般不用。
例如:CH4+Cl2CH3Cl+HCl.⑵.醇与卤化氢反应:RCH2OH+HX→RCH2X+H2O.*⑶.烯烃α-氢原子的高温卤代:只生成一元卤代物。
CH3-CH=CH2+Cl2Cl-CH2-CH=CH2+HCl.⑷.醛、羧酸α-氢原子的卤代:CH3-CHO+3Cl2→CCl3-CHO+3HCl. CH3-COOH+3Cl2→CCl3-COOH+3HCl.2.加成反应:⑴.加卤素:生成多元卤代物。
烃的衍生物总结

甲烷燃烧CH4+2O2→CO2+2H2O(条件为点燃)甲烷隔绝空气高温分解甲烷分解很复杂,以下是最终分解。
CH4→C+2H2(条件为高温高压,催化剂)甲烷和氯气发生取代反应CH4+Cl2→CH3Cl+HClCH3Cl+Cl2→CH2Cl2+HClCH2Cl2+Cl2→CHCl3+HClCHCl3+Cl2→CCl4+HCl (条件都为光照。
)实验室制甲烷CH3COONa+NaOH→Na2CO3+CH4(条件是CaO 加热)乙烯燃烧CH2=CH2+3O2→2CO2+2H2O(条件为点燃)乙烯和溴水CH2=CH2+Br2→CH2Br-CH2Br乙烯和水CH2=CH2+H20→CH3CH2OH (条件为催化剂)乙烯和氯化氢CH2=CH2+HCl→CH3-CH2Cl乙烯和氢气CH2=CH2+H2→CH3-CH3 (条件为催化剂)乙烯聚合nCH2=CH2→-[-CH2-CH2-]n- (条件为催化剂)氯乙烯聚合nCH2=CHCl→-[-CH2-CHCl-]n- (条件为催化剂)实验室制乙烯CH3CH2OH→CH2=CH2↑+H2O (条件为加热,浓H2SO4)乙炔燃烧C2H2+3O2→2CO2+H2O (条件为点燃)乙炔和溴水C2H2+2Br2→C2H2Br4乙炔和氯化氢两步反应:C2H2+HCl→C2H3Cl--------C2H3Cl+HCl→C2H4Cl2乙炔和氢气两步反应:C2H2+H2→C2H4→C2H2+2H2→C2H6 (条件为催化剂)实验室制乙炔CaC2+2H2O→Ca(OH)2+C2H2↑以食盐、水、石灰石、焦炭为原料合成聚乙烯的方程式。
CaCO3 === CaO + CO2 2CaO+5C===2CaC2+CO2CaC2+2H2O→C2H2+Ca(OH)2C+H2O===CO+H2-----高温C2H2+H2→C2H4 ----乙炔加成生成乙烯C2H4可聚合苯燃烧2C6H6+15O2→12CO2+6H2O (条件为点燃)苯和液溴的取代C6H6+Br2→C6H5Br+HBr苯和浓硫酸浓硝酸C6H6+HNO3→C6H5NO2+H2O (条件为浓硫酸)苯和氢气C6H6+3H2→C6H12 (条件为催化剂)乙醇完全燃烧的方程式C2H5OH+3O2→2CO2+3H2O (条件为点燃)乙醇的催化氧化的方程式2CH3CH2OH+O2→2CH3CHO+2H2O(条件为催化剂)(这是总方程式)乙醇发生消去反应的方程式CH3CH2OH→CH2=CH2+H2O (条件为浓硫酸 170摄氏度)两分子乙醇发生分子间脱水2CH3CH2OH→CH3CH2OCH2CH3+H2O (条件为催化剂浓硫酸 140摄氏度)乙醇和乙酸发生酯化反应的方程式CH3COOH+C2H5OH→CH3COOC2H5+H2O乙酸和镁Mg+2CH3COOH→(CH3COO)2Mg+H2乙酸和氧化钙2CH3COOH+CaO→(CH3CH2)2Ca+H2O乙酸和氢氧化钠CH3COOCH2CH3+NaOH→CH3COONa+CH3CH2OH乙酸和碳酸钠Na2CO3+2CH3COOH→2CH3COONa+H2O+CO2↑甲醛和新制的氢氧化铜HCHO+4Cu(OH)2→2Cu2O+CO2↑+5H2O乙醛和新制的氢氧化铜CH3CH O+2Cu→Cu2O(沉淀)+CH3COOH+2H2O乙醛氧化为乙酸2CH3CHO+O2→2CH3COOH(条件为催化剂或加温)烯烃是指含有C=C键的碳氢化合物。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
反应类型
反应特点
举例
取代反应
等价替换
①烷烃、芳环与X2的反应
②醇与卤代烃反应
③醇的分子间脱水
④羧酸与醇的酯化反应
⑤酯的水解反应
⑥卤代烃在碱的水溶液中水解
加成反应
开键加合
①不饱和烃(烯、炔等)与H2、X2、HX、H2O的反应
②苯环、醛、酮与H2的反应
消去反应
脱水/卤化氢重键式
①某些卤代烃与碱的醇溶液在加热条件下的反应
-OH
乙醇
CH3CH2OH
-OH与链烃基直接相连
C-O键和
O-H键易断裂
-OH与
β-H消去
取代反应:
①与Na反应生成H2
②分子间脱水成醚
③与羧酸发生酯化反应。
④与HX反应生成卤代烃
消去反应:分子内脱水发生消去反应生成烯
氧化反应:①生成醛或酮②被强氧化剂氧化
酚
-OH
-OH(酚羟基)的氢可微弱电离
苯环上的氢(2,4,6位)较活泼
三、有机物的转化关系
四、高分子化合物
加聚反应
缩聚反应
相同
①单体是式量小有机物②产物为高分子
单体可相同,也可不相同
不同
产物中
无小分子
有小分子(H2O,NH3)
高分子与单体
组成相同
组成不相同
高分子式量
是单体式量的整数倍
n个单体式量之和减去缩去分子式量的n倍或2n倍
反应特点
打开不饱和键,相互连成长碳键
官能团与官能团(烃基)间缩去一个小分子,逐步缩合
常见反应情况
(1)均聚反应/自聚反应:一种单体的聚合
①乙烯型
②丁二烯型
③特例:醛类如甲醛
(2)共聚反应:两种或两种以上单体的聚合
①乙烯型+乙烯型
②丁二烯型+丁二烯型
③乙烯型+丁二烯型
nHO-A-COOH
→H[O-A-CO]nOH+(n-1)H2O
五、有机化学实验
1.分离提纯:蒸馏、重结晶、萃取、(色谱)
羧
酸
R-COOH
CnH2nO2
(n≥1)
O
‖
—C—OH
乙酸
O
‖
CH3—C—OH
O-H、C-O易断裂
C=O
不容易加成
酸性
酯化反应:能与醇发生
酯化反应。
酯
RCOOR’
CnH2nO2
(n≥2)
O
‖
—C—O—
乙酸乙酯
O
‖
CH3—C—OC2H5
C-O可断裂
C=O不容易加成
酸性条件下可逆水解,生成羧酸和醇。
碱性条件下彻底水解,生成羧酸盐和醇。
②某些醇在浓H2SO4作用下分子内脱水生成烯烃的反应。
氧化反应
脱氢重键式
氧原子插入式
①任何有机物的燃烧
②烯、炔、甲苯、醇、醛与KMnO4的反应
③醛的银镜、Cu(OH)2
④醇、醛的催化氧化
还原反应
加氢式
碳碳双键、三键、醛基、羰基、苯环与H2的加成反应。
加聚反应
缩聚反应
开键加合式
缩水结链式
含不饱和键的有机物如乙烯、1,3-丁二烯、甲醛等二元醇与二元羧酸、氨基酸、核苷酸等双官能团的物质
2.结构测定:元素分析、质谱、核磁共振氢谱、红外光谱
3.验证性实验:
1)卤代烃在不同溶剂中的反应:产物的差异
2)苯酚的弱酸性:苯酚与NaOH,苯酚钠溶液与CO2
3)醛基的还原性:银镜反应、与新制Cu(OH)2反应
4)葡萄糖的还原性:
4.制备实验:原理、装置(发生、净化、收集、尾气)
1)乙烯:
2)乙炔:
二有机反应主要类型反应类型反应特点举例取代反应等价替换烷烃芳环与x2的反应醇的分子间脱水羧酸与醇的酯化反应酯的水解反应卤代烃在碱的水溶液中水解加成反应不饱和烃烯炔等与h2x2hxh2o的反应苯环醛酮与h2的反应消去反应脱水卤化氢重键式某些卤代烃与碱的醇溶液在加热条件下的反应某些醇在浓h2so4作用下分子内脱水生成烯烃的反氧化反应脱氢重键式氧原子插入式任何有机物的燃烧烯炔甲苯醇醛与kmno4的反应醛的银镜cuoh2醇醛的催化氧化还原反应加氢式碳碳双键三键醛基羰基苯环与h2的加成反应
3)乙酸乙酯:
4)酚醛树脂:
烃的衍生物的化学反应归纳与整理
一、烃的衍生物的性质
类别
饱和一元物的通式
官能团
代表物
分子结构特点
主要化学性质
卤
代
烃
R-X
CnH2n+1X
-X
溴乙烷
CH3CH2Br
C-Br
易断裂
取代反应:与NaOH水溶液发生取代反应,生成醇
消去反应:与强碱的乙醇溶液共热,脱去卤化氢,生成烯烃
醇
R-OH
CnH2n+2O
(n≥1)
弱酸性:ห้องสมุดไป่ตู้NaOH溶液发生中和反应
取代反应:①与浓溴水②硝酸
显色反应:
醛
R-CHO
CnH2nO
(n≥1)
O
‖
—C—H
乙醛
O
‖
CH3—C—H
O
‖
-C—H的C-H键可断裂
C=O键
的π键可
打开,羰基碳显电正性
氧化反应:可被O2、银氨溶液、新制Cu(OH)2悬浊液氧化成羧酸(或羧酸盐)。
还原反应:与H2发生加成反应生成醇
