铁、钴、镍实验报告
无机化学实验铁钴镍实验报告

无机化学实验铁钴镍实验报告今天我们要聊聊一个有点儿“金属味儿”的实验——铁、钴、镍的实验。
想想看,这些元素可都是大人物哦,在化学领域可是有一席之地的。
咱们从实验开始吧!一开始,实验室里的那些试管、烧杯啥的都准备好了,我一站进去,心里想,这不就跟上课听老师讲化学一样吗?只不过今天,咱不是听别人说,而是亲自操作。
你知道那种感觉吗?就是“啊!我也能行!”的瞬间。
不过,话说回来,要搞清楚铁、钴、镍这些金属是怎么回事儿,我们得先搞明白它们的基本性质。
比如铁,大家都知道,特别容易生锈,没错,就那么一碰水就开始腐蚀,大家是不是都知道那种黄色的锈斑?哎呀,咱就从这里开始,往下继续看看。
一开始,铁、钴、镍这三种金属的外观差别不大,乍一看,都是银白色或者稍微带点灰色。
嘿,像不像那些典型的“硬汉”?不过,别被它们的外表骗了,铁的性子可是挺倔强的,尤其在水分和氧气的作用下,它简直就变成了个脆弱的小家伙。
试试把铁片放到水里,几天后你会发现,那上面不知不觉多了一层锈,变成了棕色的老样子。
而钴呢,虽然也有点儿容易生锈,但比铁好一点儿,不那么容易见锈。
再说说镍,它可就稳妥多了,镍就像是“沉得住气”的那种,几乎不生锈。
大家可能会觉得这些金属有啥不一样的地方?其实它们之间的反应性差异,就像是我们每个人的性格一样:有的外向,有的内敛,有的特别急躁,有的则稳重。
实验的时候,咱们要对这三种金属进行一些反应,看看它们在不同条件下会怎么样。
比如把它们分别放进酸里,哎呀,铁在酸中反应得可快了,溶解得很彻底,立马就能见到氢气泡腾腾冒出来。
而钴和镍呢?哎,没那么“热心”,钴的反应没铁那么激烈,但也能看到气体冒出来,慢慢来。
而镍呢?几乎没有什么反应,这可是让我们很惊讶的地方。
镍这家伙真是超稳,跟个不爱吵架的家伙似的。
想想看,镍就像是个“佛系”金属,永远不和你计较,不急不躁,啥都不说,啥都不做,就那么默默地待着。
再往下说,咱们还做了一些还原反应,简单点说,就是让金属变成离子。
实验二十四:第一过渡系元素(二)(铁、钴、镍)
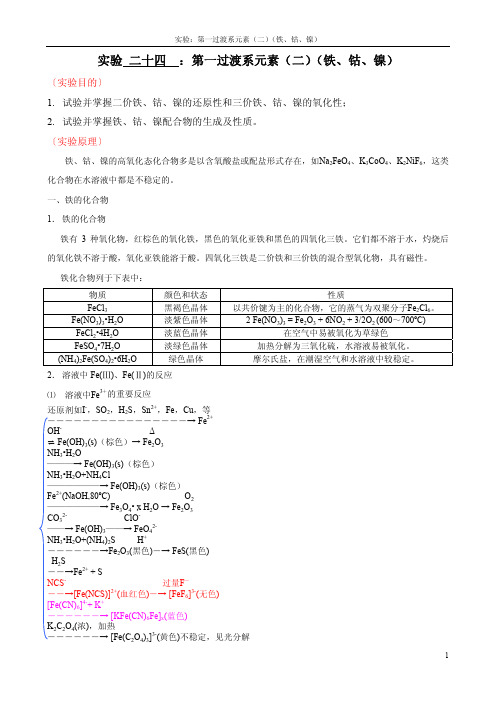
实验二十四:第一过渡系元素(二)(铁、钴、镍)〔实验目的〕1.试验并掌握二价铁、钴、镍的还原性和三价铁、钴、镍的氧化性;2.试验并掌握铁、钴、镍配合物的生成及性质。
〔实验原理〕铁、钴、镍的高氧化态化合物多是以含氧酸盐或配盐形式存在,如Na2FeO4、K3CoO4、K2NiF6,这类化合物在水溶液中都是不稳定的。
一、铁的化合物1.铁的化合物铁有3种氧化物,红棕色的氧化铁,黑色的氧化亚铁和黑色的四氧化三铁。
它们都不溶于水,灼烧后的氧化铁不溶于酸,氧化亚铁能溶于酸。
四氧化三铁是二价铁和三价铁的混合型氧化物,具有磁性。
铁化合物列于下表中:物质颜色和状态性质FeCl3黑褐色晶体以共价键为主的化合物,它的蒸气为双聚分子Fe2Cl6。
Fe(NO3)3 = Fe2O3 + 6NO2 + 3/2O2 (600~700ºC) Fe(NO3)3•H2O 淡紫色晶体 2FeCl2•4H2O 淡蓝色晶体在空气中易被氧化为草绿色FeSO4•7H2O 淡绿色晶体加热分解为三氧化硫,水溶液易被氧化。
(NH4)2Fe(SO4)2•6H2O 绿色晶体摩尔氏盐,在潮湿空气和水溶液中较稳定。
2.溶液中Fe(Ⅲ)、Fe(Ⅱ)的反应⑴溶液中Fe3+的重要反应还原剂如I-,SO2,H2S,Sn2+,Fe,Cu,等――――――――――――――――→ Fe2+OH-Δ⇌ Fe(OH)3(s)(棕色)→ Fe2O3NH3•H2O———→ Fe(OH)3(s)(棕色)NH3•H2O+NH4Cl——————→ Fe(OH)3(s)(棕色)Fe2+(NaOH,80ºC) O2——————→ Fe3O4• x H2O → Fe2O3CO32-ClO-——→ Fe(OH)3——→ FeO42-NH3•H2O+(NH4)2S H+――――――→Fe2O3(黑色)―→ FeS(黑色)H2S――→Fe2+ + SNCS-过量F-――→[Fe(NCS)]2+(血红色)―→ [FeF6]3-(无色)[Fe(CN)6]4-+ K+――――――→ [KFe(CN)6Fe]x(蓝色)K2C2O4(浓),加热――――――→ [Fe(C2O4)3]3-(黄色)不稳定,见光分解⑵溶液中Fe2+的重要反应氧化剂如Cr2O72-,浓HNO3等―――――――――――→ Fe3+OH-O2⇌ Fe(OH)2(s)(纯白色)→Fe(OH)3(s)(棕色)NH3•H2O――→ Fe(OH)2(s)(纯白色)NH3•H2O+NH4Cl――――――→无沉淀CO32-H2O + CO2 O2――→ FeCO3(白色)――→ Fe(HCO3)2―→Fe(OH)3(s)(NH4)2S―――→ FeS(黑色)NO――→[Fe(NO)( H2O)5]2+( 棕色)H2O2 +过量F-―――――→ [FeF6]3-(无色)NCS-――→无溶液、无颜色CN-过量CN-Cl2―→Fe(CN)2(s) (白色) ――→[Fe(CN)6]4-――→[Fe(CN)6]3-[Fe(CN)6]3-+ K+――――――→ [KFe(CN)6Fe]x(蓝色)二、钴的化合物1. 钴的化合物钴的氧化物与铁的氧化物类似,为暗褐色的Co2O3•xH2O和灰绿色的CoO。
下学期实验报告示范
Fe2++ 2OH-= Fe(OH)2(白色)
4Fe(OH)2+ O2+ 2H2O = 4Fe(OH)3
2 钴(II)的还原性
(1)Co2+溶液中加入Cl2水
实验未观察到溶液颜色变化。
Co2+与Cl2水不反应。
(2)CoCl2溶液中加入NaOH。所得沉淀分成两份。一份置于空气中,一份加入Cl2水
a.加入NaOH后首先观察到蓝色沉淀生成,NaOH过量,得到粉红色沉淀。
a.Fe(OH)3溶入浓盐酸,KI-淀粉试纸无变化;
b.Co(OH)3Ni(OH)3加入浓盐酸后,KI-淀粉试纸变蓝;
a.Fe(OH)3与浓盐酸只发生酸碱反应;
b.Co(OH)3和Ni(OH)3溶入浓盐酸后,生成的Co3+和Ni3+在水溶液中由于强氧化性不能存在,与浓盐酸反应释放Cl2气使KI-淀粉试纸变蓝。
b.沉淀放置在空气中慢慢转变为褐色;
c.加入Cl2水,很快转变为褐色。
a.Co2+溶液中加入NaOH后,首先生成蓝色碱式盐
Co(OH)Cl,NaOH过量生成Co(OH)2。
CoCl2+ 2NaOH = Co(OH)2+ 2NaCl
b.Co(OH)2具有一定的还原性,在空气中慢慢被氧化为褐色的Co(OH)2。
2[Fe(CN)6]4-+ I2=2[Fe(CN)6]3-+ 2I-
2[Fe(CN)6]3-+ 3Fe2+= Fe3[Fe(CN)6]2
(2)新配置的(NH4)2Fe(SO4)2溶液中加入碘水,摇荡试管。溶液分成两份,各加入KSCN溶液,向其中一只试管中加入H2O2
铁、钴、镍实验报告
一试管加Br2水
2Co(OH)2+Br2+2OH-=2Co(OH)3↓+2Br-
Ni(Ⅱ)的氢氧化物
三试管各+NiSO4+NaOH
Ni2++2OH-=Ni(OH)2↓
一试管振荡,空气中放置
一试管加H2O2
一试管加Br2水
2Ni(OH)2+Br2+2OH-=2Ni(OH)3↓+2Br-
CoCl2+OH-=Co(OH)Cl↓+Cl-
上述溶液+过量NH3水
Co(OH)Cl+6NH3=[Co(NH3)6]2++OH-+Cl-
4[Co(NH3)6]2++O2+2H2O=4[Co(NH3)6]3++4OH-
NiSO4+适量NH3水
2Ni2++2OH-+SO42-=Ni2(OH)2SO4↓
上述溶液+过量NH3水
Fe(OH)3+3H+=Fe3++3H2O
Co(Ⅲ)的氢氧化物
CoCl2+NaOH
Co2++2OH-=Co(OH)2↓
上述溶液+H2O2
2Co(OH)2+H2O2=2Co(OH)3↓
沉淀+浓HCl,用KI-淀粉试纸检验气体
2Co(OH)3+6HCl=2CoCl2+Cl2↑+6H2O
Cl2+2I-=I2+2Cl-
Ni2(OH)2SO4+12NH3=2[Ni(NH3)6]2++2OH-+SO42↓
铁钴镍实验报告

一、实验目的1. 掌握铁、钴、镍的化学性质及其在反应中的表现。
2. 熟悉铁、钴、镍化合物的制备方法和实验操作技巧。
3. 通过实验观察和分析,培养实验操作能力、观察能力和分析问题的能力。
二、实验原理铁(Fe)、钴(Co)、镍(Ni)是周期表中的过渡金属元素,它们具有相似的化学性质,但在反应中表现出不同的特点。
本实验主要涉及铁、钴、镍的氢氧化物、配合物及其氧化还原性质。
三、实验仪器与试剂1. 仪器:试管、烧杯、酒精灯、滴管、玻璃棒等。
2. 试剂:硫酸亚铁铵、硫酸钴、硫酸镍、氢氧化钠、氨水、溴水、氯水、硫酸等。
四、实验内容1. 铁(II)、钴(II)、镍(II)化合物的还原性(1)铁(II)的还原性- 在酸性介质中,往盛有1毫升溴水的试管中加入3滴1:1 H2SO4的溶液,然后滴加0.2mol/L (NH4)2Fe(SO4)2溶液,观察现象。
反应式:2Fe2+ + Br2 → 2Fe3+ + 2Br-(2)钴(II)的还原性- 往盛有CoCl2和NiSO4的试管中分别滴入氯水,观察现象。
反应式:Co2+ + Cl2 → Co3+ + 2Cl-2. 铁、钴、镍氢氧化物的生成和性质- 将Fe粉3g加入煮沸冷却的NaOH溶液中,观察现象。
反应式:Fe + 2NaOH → Fe(OH)2 + H2↑- 将0.5mL氢氧化钠溶液滴入硫酸亚铁铵溶液中,观察现象。
反应式:Fe2+ + 2OH- → Fe(OH)2↓3. 铁、钴、镍配合物的生成和性质- 将过量的氨水加入Co2+或Ni2+离子的水溶液中,观察现象。
反应式:[Co(NH3)6]2+ + 2OH- → [Co(NH3)6]2+ + 2H2O五、实验现象1. 铁在酸性介质中与溴水反应,溶液由橙红色变为棕黄色。
2. 钴在氯水中反应,溶液由蓝色变为棕黄色。
3. 铁粉与NaOH反应,生成白色沉淀,逐渐变为灰绿色,最后变为红棕色。
4. 硫酸亚铁铵溶液中加入NaOH,生成白色沉淀。
铁骨镍的实验报告

一、实验目的1. 掌握铁、钴、镍三种金属的基本性质。
2. 了解铁、钴、镍在化学反应中的表现。
3. 培养实验操作能力、观察能力和分析问题的能力。
二、实验原理铁(Fe)、钴(Co)、镍(Ni)是周期表中的过渡金属元素,它们在化学反应中表现出不同的性质。
本实验通过观察铁、钴、镍与不同试剂的反应,分析其化学性质。
三、实验材料1. 试剂:硫酸铁、硫酸钴、硫酸镍、氢氧化钠、盐酸、硫酸铜、氯水、溴水等。
2. 仪器:试管、烧杯、滴管、酒精灯、铁架台、石棉网等。
四、实验步骤1. 铁的化学性质研究(1)铁与硫酸铜反应取一定量的硫酸铁溶液于试管中,加入少量硫酸铜溶液,观察反应现象。
(2)铁与盐酸反应取一定量的硫酸铁溶液于试管中,加入少量盐酸,观察反应现象。
2. 钴的化学性质研究(1)钴与硫酸铜反应取一定量的硫酸钴溶液于试管中,加入少量硫酸铜溶液,观察反应现象。
(2)钴与氯水反应取一定量的硫酸钴溶液于试管中,加入少量氯水,观察反应现象。
3. 镍的化学性质研究(1)镍与硫酸铜反应取一定量的硫酸镍溶液于试管中,加入少量硫酸铜溶液,观察反应现象。
(2)镍与溴水反应取一定量的硫酸镍溶液于试管中,加入少量溴水,观察反应现象。
五、实验现象1. 铁与硫酸铜反应:生成红色沉淀,溶液由蓝色变为浅绿色。
2. 铁与盐酸反应:生成气泡,溶液由黄色变为无色。
3. 钴与硫酸铜反应:生成蓝色沉淀,溶液由蓝色变为浅绿色。
4. 钴与氯水反应:无明显现象。
5. 镍与硫酸铜反应:无明显现象。
6. 镍与溴水反应:无明显现象。
六、实验结论1. 铁与硫酸铜反应生成红色沉淀,说明铁可以置换出铜。
2. 铁与盐酸反应生成气泡,说明铁可以与盐酸反应生成氢气。
3. 钴与硫酸铜反应生成蓝色沉淀,说明钴可以置换出铜。
4. 钴与氯水反应无明显现象,说明钴不易被氯水氧化。
5. 镍与硫酸铜反应无明显现象,说明镍不易被硫酸铜氧化。
6. 镍与溴水反应无明显现象,说明镍不易被溴水氧化。
七、实验讨论1. 本实验中,铁、钴、镍的化学性质具有一定的相似性,如都能与硫酸铜反应生成相应的金属沉淀。
铁、钴、镍实验报告

Co(Ⅲ)的氢氧化物
CoCl2+NaOH
Co2++2OH-=Co(OH)2↓
上述溶液+H2O2
2Co(OH)2+H2O2=2Co(OH)3↓
沉淀+浓HCl,用KI-淀粉试纸检验气体
2Co(OH)3+6HCl=2CoCl2+Cl2↑+6H2O
Cl2+2I-=I2+2Cl-
一试管加H2O2
2Fe(OH)2+H2O2=2Fe(OH)3↓
一试管加Br2水
2Fe(OH)2+Br2+2OH-=2Fe(OH)3↓+2Br-
Co(Ⅱ)的氢氧化物
三试管各+CoCl2+NaOH
Co2++2OH-=Co(OH)2↓
一试管振荡,空气中放置
4Co(OH)2+O2+2H2O=4Co(OH)3↓
结论
Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)的氢氧化物都有还原性,其还原能力依Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)的顺序减弱。
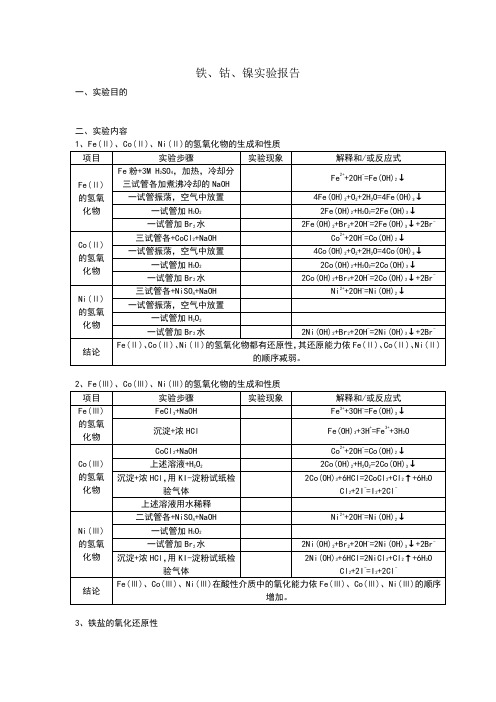
2、Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)的氢氧化物的生成和性质
项目
实验步骤
实验现象
解释和/或反应式
Fe(Ⅲ)的氢氧化物
FeCl3+NaOH
Fe3++3OH-=Fe(OH)3↓
沉淀+浓HCl
Ni2(OH)2SO4+12NH3=2[Ni(NH3)6]2++2OH-+SO42↓
与SCN-形成的配合物
FeCl3+KSCN
整理铁、钴、镍的性质

整理铁、钴、镍的性质-CAL-FENGHAI-(2020YEAR-YICAI)_JINGBIAN实验六 铁、钴、镍的性质一、实验目的1、 试验并掌握铁、钴、镍氢氧化物的生成和氧化还原性质;2、试验并掌握铁、钴、镍配合物的生成及在离子鉴定中的作用。
二、实验原理铁、钴、镍常见氧化值:+2和+3 另外 Fe 还有+6 1、Fe 2+、Co 2+、Ni 2+的还原性 (1)酸性介质Cl 2 + 2Fe 2+(浅绿)=2Fe 3+(浅黄)+2Cl -(2)碱性介质铁(II )、钴(II )、镍(II )的盐溶液中加入碱,均能得到相应的氢氧化物。
Fe(OH)2易被空气中的氧气氧化,往往得不到白色的氢氧化亚铁,而是变成灰绿色,最后成为红棕色的氢氧化铁。
Co (OH )2也能被空气中的氧气慢慢氧化。
2、Fe 3+、Co 3+、Ni 3+的氧化性由于Co 3+和Ni 3+都具有强氧化性,Co(OH)3,NiO(OH)与浓盐酸反应分别生成Co(II)和Ni(II),并放出氯气。
CoO(OH)和NiO(OH )通常由Co (II )和Ni(II)的盐在碱性条件下用强氧化剂(Cl 2、Br 2)氧化得到。
Fe 3+易发生水解反应。
Fe 3+具有一定的氧化性,能与强还原剂反应生成Fe 2+。
白色粉红绿色黑色Co(OH)2Co(OH)3Fe(OH)2Fe(OH)3还原性增强氧化性增强Ni (OH )2Ni (OH )33、配合物的生成和Fe 2+、Fe 3+、Co 2+、Ni 2+的鉴定方法 (1)氨配合物Fe 2+和Fe 3+难以形成稳定的氨配合物。
在水溶液中加入氨时形成Fe(OH)2和Fe(OH)3沉淀。
将过量的氨水加入Co 2+或Ni 2+离子的水溶液中,即生成可溶性的氨合配离子[Co(NH 3)6]2+或[Ni(NH 3)6]2+。
不过[Co(NH 3)6]2+ 不稳定,易氧化成[Co(NH 3)6]3+。
(2)氰配合物Fe 3+,Co 3+,Fe 2+,Co 2+,Ni 2+都能与CN -形成配合物。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2Co(OH)2+H2O2=2Co(OH)3↓
一试管加Br2水
2Co(OH)2+Br2+2OH-=2Co(OH)3↓+2Br-
Ni(Ⅱ)的氢氧化物
三试管各+NiSO4+NaOH
Ni2++2OH-=Ni(OH)2↓
一试管振荡,空气中放置
一试管加H2O2
一试管加Br2水
2Ni(OH)2+Br2+2OH-=2Ni(OH)3↓+2Br-
Ni2(OH)2SO4+12NH3=2[Ni(NH3)6]2++2OH-+SO42↓
与SCN-形成的配合物
FeCl3+KSCN
Fe3++n SCN-=[Fe(SCN)n]3-n(n=1~6)
FeSO4+KSCN
CoCl2+KSCN+丙酮
Co2++4SCN-=[Co(SCN)4]2-
NiSO4+KSCN
结论
Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)在酸性介质中的氧化能力依Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)的顺序增加。
3、铁盐的氧化还原性
项目
实验步骤
实验现象
解释和/或反应式
Fe(Ⅱ)还原性
FeSO4+H2SO4+KMnO4
MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
FeSO4+H2SO4+K2Cr2O7
Fe3++K4Fe(CN)6=KFe[Fe(CN)6]↓+3K+
FeSO4+K3Fe(CN)6
Fe2++K3Fe(CN)6=KFe[Fe(CN)6]↓+2K+
NiSO4+DMG+NH3水
CoCl2+OH-=Co(OH)Cl↓+Cl-
上述溶液+过量NH3水
Co(OH)Cl+6NH3=[Co(NH3)6]2++OH-+Cl-
4[Co(NH3)6]2++O2+2H2O=4[Co(NH3)6]3++4OH-
NiSO4+适量NH3水
2Ni2++2OH-+SO42-=Ni2(OH)2SO4↓
上述溶液+过量NH3水
一试管加H2O2
2Fe(OH)2+H2O2=2Fe(OH)3↓
一试管加Br2水
2Fe(OH)2+Br2+2OH-=2Fe(OH)3↓+2Br-
Co(Ⅱ)的氢氧化物
三试管各+CoCl2+NaOH
Co2++2OH-=Co(OH)2↓
一试管振荡,空气中放置
4Co(OH)2+O2+2H2O=4Co(OH)3↓
上述溶液用水稀释
Ni(Ⅲ)的氢氧化物
二试管各+NiSO4+NaOH
Ni2++2OH-=Ni(OH)2↓
一试管加H2O2
一试管加Br2水
2Ni(OH)2+Br2+2OH-=2Ni(OH)3↓+2Br-
沉淀+浓HCl,用KI-淀粉试纸检验气体
2Ni(OH)3+6HCl=2NiCl2+Cl2↑+6H2O
Cl2+2I-=I2+2Cl-
结论
Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)的氢氧化物都有还原性,其还原能力依Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)的顺序减弱。
2、Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)的氢氧化物的生成和性质
项目
实验步骤
实验现象
解释和/或反应式
Fe(Ⅲ)的氢氧化物
FeCl3+NaOH
Fe3++3OH-=Fe(OH)3↓
沉淀+浓HCl
4、Fe、Co、Ni的配合物
项目
实Байду номын сангаас步骤
实验现象
解释和/或反应式
氨的配合物
FeCl3+适量NH3水
Fe3++3OH-=Fe(OH)3↓
上述溶液+过量NH3水
FeSO4+适量NH3水
Fe2++2OH-=Fe(OH)2↓
4Fe(OH)2+O2+2H2O=4Fe(OH)3↓
上述溶液+过量NH3水
CoCl2+适量NH3水
Cr2O72-+6Fe2++14H+=6Fe3++2Cr3++7H2O
Fe(Ⅲ)的氧化性
FeCl3+TAA,加热
2Fe3++H2S=2Fe2++S↓+2H+
FeCl3+KI+CCl4
2Fe3++2I-=2Fe2++I2
I2在CCl4中显 色
结论
在酸性介质中Fe(Ⅲ)有一定的氧化能力,Fe(Ⅱ)还原性较弱需较强氧化剂将其氧化。
结论
铁盐生成氢氧化物不溶于过量的氨水,钴盐和镍盐生成碱式盐溶于过量的氨水生成氨配合物,Co(Ⅱ)氨配合物易氧化转化成 Co(Ⅲ)氨配合物。Fe(Ⅲ)、Co(Ⅱ)与SCN-生成配合物,Fe(Ⅱ)、Ni(Ⅱ)与SCN-不生成配合物,
5、离子的鉴定
实验步骤
实验现象
解释和/或反应式
FeCl3+K4Fe(CN)6
铁、钴、镍实验报告
一、实验目的
二、实验内容
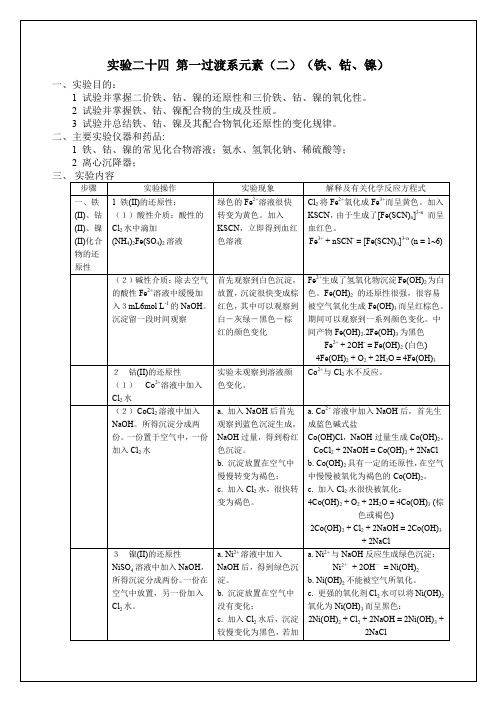
1、Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)的氢氧化物的生成和性质
项目
实验步骤
实验现象
解释和/或反应式
Fe(Ⅱ)的氢氧化物
Fe粉+3MH2SO4,加热,冷却分三试管各加煮沸冷却的NaOH
Fe2++2OH-=Fe(OH)2↓
一试管振荡,空气中放置
4Fe(OH)2+O2+2H2O=4Fe(OH)3↓
Fe(OH)3+3H+=Fe3++3H2O
Co(Ⅲ)的氢氧化物
CoCl2+NaOH
Co2++2OH-=Co(OH)2↓
上述溶液+H2O2
2Co(OH)2+H2O2=2Co(OH)3↓
沉淀+浓HCl,用KI-淀粉试纸检验气体
2Co(OH)3+6HCl=2CoCl2+Cl2↑+6H2O
Cl2+2I-=I2+2Cl-
