固体制剂批生产记录
固体制剂生产记录表单大全

PA-04-009-00PF-04-029-00整粒生产记录在产物品标签在产物品标签PF-04-022-00一般生产区清场记录年月试产品销毁记录试产品销毁记录试产品销毁记录TF-00-007-00片剂工艺查证记录PF-04-025-00批物料平衡表PF-03-01-00批生产计划指令单批包装记录附件1、印有批号的标签样张;2、印有批号的小盒、中盒样张;3、使用说明书样张;4、产品合格证样张。
粘贴处:批包装记录附件5、印有批号的标签样张;6、印有批号的小盒、中盒样张;7、使用说明书样张;8、产品合格证样张。
粘贴处:批包装记录附件9、印有批号的标签样张;10、印有批号的小盒、中盒样张;11、使用说明书样张;12、产品合格证样张。
粘贴处:PF-04-028-00 模具筛网使用记录表颗粒剂工艺查证记录日期:年月胶囊剂工艺查证记录工艺指令(一)日期:工艺指令(二)日期:工艺指令(三)日期:PA-04-008-00 工衣清洁记录PF-04-009-00 高效包衣生产记录PA-04-010-00 车间包装材料退库记录咖啡店创业计划书第一部分:背景在中国,人们越来越爱喝咖啡。
随之而来的咖啡文化充满生活的每个时刻。
无论在家里、还是在办公室或各种社交场合,人们都在品着咖啡。
咖啡逐渐与时尚、现代生活联系在一齐。
遍布各地的咖啡屋成为人们交谈、听音乐、休息的好地方,咖啡丰富着我们的生活,也缩短了你我之间的距离,咖啡逐渐发展为一种文化。
随着咖啡这一有着悠久历史饮品的广为人知,咖啡正在被越来越多的中国人所理解。
第二部分:项目介绍第三部分:创业优势目前大学校园的这片市场还是空白,竞争压力小。
而且前期投资也不是很高,此刻国家鼓励大学生毕业后自主创业,有一系列的优惠政策以及贷款支持。
再者大学生往往对未来充满期望,他们有着年轻的血液、蓬勃的朝气,以及初生牛犊不怕虎的精神,而这些都是一个创业者就应具备的素质。
大学生在学校里学到了很多理论性的东西,有着较高层次的技术优势,现代大学生有创新精神,有对传统观念和传统行业挑战的信心和欲望,而这种创新精神也往往造就了大学生创业的动力源泉,成为成功创业的精神基础。
0913-2胶囊批生产记录
□按要求操作□未按要求操作
墙壁无粉尘,污渍,地面无积水、无物料残渍。
□ 合格□不合格
地漏清洁无污渍,并灌有消毒液进行水封
□ 合格□不合格
4.清洁洁具
执行《生产辅助器具清洁程序》(SOP-CLP 116)清洁洁具,
□按要求操作□未按要求操作
发放日期
批准人
批准日期
原辅料领料单
名称
物料编号
批号
上批留用
实发数量
检验报告号
发料人
领料人
领料日期
诺氟沙星
kg
kg
淀粉
kg
kg
硬脂酸镁
kg
kg
空心胶囊
万粒
万粒
称量记录
操作步骤
规定工艺要求
实际操作
1.称量前检查
房间号:G414
清场合格,有上批清场合格副本。
□符合要求□不符合要求
操作时间:
操作人:
复核人:
□ 合格□不合格
4.清洁洁具
执行《生产辅助器具清洁程序》(EOP-CLP 127)清洁洁具,
□按要求操作□未按要求操作
洁具放于洁具间
□ 合格□不合格
5.生产记录
本批记录填写符合要求,并将与本批产品有关的记录清理出现场。
□按要求操作□未按要求操作
6.更换房间状态标识
已更换为“清场合格(副本)”状态标识。
□ 合格□不合格
2.清洁容器具
执行容器具清洁标准操作程序(SOP-CLP 121)清洁容器具,
□按要求操作□未按要求操作
容器具内外表面无粉尘,污渍。
□ 合格□不合格
药品批生产记录

批生产记录
药业有限公司
批生产记录
页号:1/2
批生产记录
页号:2/2
称量单
页号:1/1
批生产记录
页号:1/2
批生产记录
页号:2/2
批生产记录
页号:1/2
批生产记录
页号:2/2
批生产记录
页号:1/3
批生产记录
页号:2/3
批生产记录
页号:3/3
批生产记录
页号:1/3
批生产记录
页号:2/3
批生产记录
页号:3/3
充填中间控制记录
页号:1/3
充填中间控制记录
页号:2/3
充填中间控制记录
页号:3/3
批生产记录
页号:1/2
批生产记录
页号:2/2
批生产记录
页号:1/3
批生产记录
页号:2/3
批生产记录
页号:3/3
内包装中间控制记录
页号:1/2
内包装中间控制记录
页号:2/2
批生产记录
页号:1/3
批生产记录
页号:2/3
批生产记录
页号:3/3
外包装中间控制记录
外包装中间控制记录
附页
变更记载。
片剂、胶囊、颗粒剂生产记录

片剂制剂批生产指令制定人:制定日期:审核人:审核日期:批准人:批准日期:颁发部门:生效日期:分发部门:生产部、质控部、物控部、生产车间品名批号批量规格完成时间月日时至月日时生产地点固体制剂车间环境要求30万级洁净区物料设备名称代码名称单位数量□槽型混合机□摇摆制粒机□热风循环干燥箱□V型混合机□ZP-33冲压片机质量要求工时定额相关文件编号文件名()工艺规程片剂剂制剂批生产记录生产过程执行情况车间主任:年月日质量情况QA:年月日()颗粒剂制剂批生产指令制定人:制定日期:审核人:审核日期:批准人:批准日期:颁发部门:生效日期:分发部门:生产部、质控部、物控部、生产车间品名批号批量规格完成时间月日时至月日时生产地点固体制剂车间环境要求30万级洁净区物料设备名称代码名称单位数量□槽型混合机□摇摆制粒机□热风循环干燥箱□V型混合机□SB-80颗粒包装机质量要求工时定额相关文件编号文件名()工艺规程()颗粒剂制剂批生产记录生产过程执行情况车间主任:年月日质量情况QA:年月日()胶囊剂制剂批生产指令制定人:制定日期:审核人:审核日期:批准人:批准日期:颁发部门:生效日期:分发部门:生产部、质控部、物控部、生产车间品名批号批量规格完成时间月日时至月日时生产地点固体制剂车间环境要求30万级洁净区物料设备名称代码名称单位数量□槽型混合机□摇摆制粒机□热风循环干燥箱□V型混合机□VH-800型胶囊填充机□JMJ-Ⅱ胶囊抛光机□铝塑泡罩包装机质量要求工时定额相关文件编号文件名()工艺规程()胶囊剂制剂批生产记录生产过程执行情况车间主任:年月日质量情况QA:年月日SC-GJ-01302片剂批生产记录目录目录一.批生产指令 (1)二.物料流转表 (2)三.批生产记录目录 (3)四.批生产记录汇总表·································4五.称量岗位记录 (5)六.称量岗位清场记录 (6)七.混合岗位记录 (7)八.混合岗位清场记录 (8)九.制粒岗位记录 (9)十.制粒岗位清场记录 (10)十一.总混合岗位记录 (11)十二.总混合岗位清场记录 (12)十三.压片岗位记录 (13)十四.压片岗位清场记录 (14)十五.片剂分装岗位记录 (15)十六.片剂分装岗位清场记录 (16)十七.批包装生产记录 (17)批生产记录汇总表工艺员: 车间主任: 生产部:产品名称 产品批号制剂规格生产日期生产批量生 产 过 程称量原辅料名称批号 数量 混合总投料量 kg kg 合格颗粒量 kgkg 得率 % kg 物料平衡 % kg 压片 总投料量 kg kg 片子总重量 kg kg 得率 %kg 物料平衡 % 制粒 干燥总投料量kg 片 剂 分 装 投料量 万片 干颗粒重量 kg 半成品 万片 得率 % 得率 % 物料平衡%物料平衡%制剂总得率 偏差分析生产记录审核标准审核结果填写及时,自己清楚,内容真实、数据完整,并有操作人及复合人签名批生产记录整洁,无任意撕毁和任意涂改现象;更改时在更改处签名,并使原数据仍可辨认。
片剂批生产记录范文

片剂批生产记录范文<<片剂批生产记录>>批号:XXXXX生产日期:XXXX年XX月XX日生产工艺:XXX工艺生产线:XXX生产线1.原辅料准备:1.1配方:按照配方要求准备原辅料,确保原辅料符合《药品质量管理规范》的要求。
1.2填料区:将原辅料按照配方准确称量,记录称量数据,并签名确认。
1.3原料检查:对所使用的原辅料进行外观、标识、纯度等检查,记录检查结果,并签名确认。
1.4净化区:将准备好的原料送入净化区进行净化处理,确保原料的纯净度。
1.5粉碎:将净化后的原料送入粉碎设备进行粉碎,确保颗粒的大小符合要求,记录粉碎结果,并签名确认。
2.混合制粒:2.1将粉碎后的原料送入混合料仓,按照配方要求加入辅料,启动混合机,将原料和辅料充分混合均匀,记录混合时间,确保混合效果良好。
2.2将混合好的料送入制粒机进行制粒,确保颗粒的大小符合要求,记录制粒结果,并签名确认。
3.平片:3.1将制粒后的料送入平片机,设置适当的压片参数,启动平片机,将料压制成片,记录压片参数,并签名确认。
3.2检查片剂的外观、尺寸、硬度等指标,记录检查结果,并签名确认。
4.包装:4.1将平片好的片剂送入包装线进行包装,包装材料应符合相关要求。
4.2包装机自动计数、封口,并进行瓶装、包装箱装等操作,确保包装完整、无错漏。
4.3封口质量检查:对包装好的片剂进行封口质量检查,记录检查结果,并签名确认。
4.5包装记录:记录包装时的相关参数,包括包装机号、封口质量检查结果、包装箱数等,并签名确认。
5.清场:5.1包装线清场:清除包装线上的残留物和废品,确保下次生产使用的环境卫生。
5.2清点包装材料:清点包装材料的库存情况,记录库存数量,并签名确认。
以上记录内容属实,记录人员应严格按照相关规定操作,保证记录的准确性和真实性。
记录人:签名。
药品批生产记录

批生产记录产品名称:规格:代号:制定人:拟订日期:年月日审核人:审查日期:年月日审核人:审查日期:年月日批准人:同意日期:年月日文件编号:奏效日期:年月日产品批号:批量:车间审查:QA 审查:药业有限公司页号:1/2品名:胶囊规格:代号:批号:批量:万粒工序:称量文件编号:日期时间操作步骤生产记录操作人复核人称量前准备—对作业场所、环境的检查* 检查操作间温湿度、压差能否切合要求□是□否* 检查工作地区能否有与本批生产没关的物件□无□有* 检查生产地区卫生能否切合要求□切合要求□不切合要求—对电子台秤进行检查* 检查能否完满洁净待用□完满洁净□不完满洁净* 检查能否在其查验有效期内□是□否—检查生产所需物料能否备齐* 批生产指令单中的物料□已备齐□未备齐—洁净准备好的工用具,并用75%的乙醇消毒□已洁净□已消毒□未洁净□未消毒—替代状态标记* 用生产允许证替代清场合格证□已替代称量开始1.检查称量所用物料的品名、代号、批号、性状及查验报告应无□无误差误差* 检查应能过 100 目筛网□切合规定* 检查低代替羟丙基纤维素应能过80 目筛网□切合规定* 检查微晶纤维素应能过80 目筛网□切合规定* 检查淀粉应能过80 目筛网□切合规定* 检查滑石粉应能过80 目筛网□切合规定* 检查碳酸氢钠应能过80 目筛网□切合规定□未替代□有误差(见误差或备注)□不切合规定□不切合规定□不切合规定□不切合规定□不切合规定□不切合规定页号:2/2品名:胶囊规格:代号:批号:批量:万粒工序:称量文件编号:日期时间操作步骤生产记录操作人复核人* 检查硬脂酸镁应能过80 目筛网□切合规定□不切合规定2.按批生产指令单对原辅料进行称量配料见称量单称量结束清场—消除现场与本批生产相关的物件□已消除□未消除—对计量用具进行洁净,并用75%的乙醇消毒*电子台秤—对工作地区进行洁净—对工用具、卫生洁具进行洁净、消毒,并按规定寄存—替代状态标记□已洁净□已消毒□未洁净□未消毒□已洁净□未洁净□已洁净□已消毒□未洁净□未消毒□已定置□不决置* 用清场合格证替代生产允许证□已替代□未替代—检查 BPR 的完好性,相关凭据应已附到BPR 上□完好□不完好备注:称量单页号:1/1品名:胶囊规格:代号:批号:批量:万粒工序:称量文件编号:代号品名处方量分度值批号查考证号称量数目称量人复核人复核数目查对人复核人备注料次:第一料42134237 低代替羟丙基纤维素4241 微晶纤维素4204 淀粉42134237 低代替羟丙基纤维素4241 微晶纤维素4204 淀粉42134237 低代替羟丙基纤维素4241 微晶纤维素4204 淀粉4210 滑石粉4252 碳酸氢钠4207 硬脂酸镁备注:kg kgkg kgkg kgkg kg料次:第二料kg kgkg kgkg kgkg kg料次:第三料kg kgkg kgkg kgkg kg 外加辅料kg kgkg kgkg kgQA :批生产记录页号:1/2品名:胶囊规格:代号:批号:批量:万粒工序:制粒文件编号:日期时间操作步骤生产记录操作人复核人制粒前准备—对作业场所、环境的检查* 检查操作间温湿度、压差能否切合要求□切合要求□不切合要求* 检查工作地区能否有与本批生产没关的物件□无□有* 检查生产地区卫生能否切合要求□切合要求□不切合要求—对生产介质进行检查* 纯化水□正常□不正常* 压缩空气□正常□不正常—对计量用具进行检查* 电子台秤能否完满洁净待用,能否在其查验有效期内□完满洁净□是□不完满洁净□否* 检查酒精计能否完满洁净待用□完满洁净□不完满洁净—对湿法混淆颗粒机进行检查设施型号: SHK-220B 编号:* 检查搅拌桨、切碎刀中心部位的进气气流能否正常□正常□不正常* 调理流量计控制进气气流(气压P 应大于0.5MPa )□切合规定□不切合规定* 检查设施能否洁净,并用浸润75%乙醇的干净抹布擦□已擦抹□未擦抹拭与产品接触的部位□洁净□不洁净* 检查搅拌桨、切碎刀能否正常运行□正常□不正常—洁净准备好的工用具,并用75%的乙醇消毒□已洁净□已消毒□未洁净□未消毒—替代状态标记* 用生产允许证替代清场合格证□已替代□未替代* 用正在运行标记替代已洁净标记□已替代□未替代页号:2/2品名:胶囊规格:代号:批号:批量:万粒工序:制粒文件编号:日期时间操作步骤生产记录操作人复核人制粒开始1.按批生产指令单领取称量好的制粒用原辅料,查对品名、代号、批号、数目应无误差2.向 95%的乙醇中加入适当纯化水,制备 50%的乙醇水溶液(量具:酒精计)3.封闭湿法混淆颗粒机出料活塞;待门信号灯亮后,翻开物料锅盖,将、低代替羟丙基纤维素、微晶纤维素、淀粉倒入锅内;封闭物料锅盖,调整时间继电器为 240 秒,开始搅拌混淆4.将制备好的50%乙醇水溶液均匀洒入湿法混淆颗粒机原辅猜中,按下“启动”按钮,混淆搅拌120-240 秒,混合搅拌过程中切碎 60-180 秒制成适合湿颗粒,要求颗粒可以达到“捏之成团,一弹则散”□无误差□有误差见粘合剂配制记录第一锅第二锅第三锅混淆时间秒秒秒第一锅第二锅Ⅰ速Ⅱ速Ⅰ速Ⅱ速搅拌时间秒秒秒秒切碎时间秒秒秒秒粘合剂用量kg kg 搅拌电流A A第三锅Ⅰ速Ⅱ速搅拌时间秒秒粘合剂用量kg 切碎时间秒秒搅拌电流 A 粘合剂实质总用量:kg制粒结束—检查 BPR 的完好性□完好□不完好备注:品名:胶囊规格:代号:日期时间操作步骤干燥整粒前准备—对作业场所、环境的检查*检查操作间温湿度、压差能否切合要求*检查工作地区能否有与本批生产没关的物件*检查生产地区卫生能否切合要求—对生产介质进行检查*蒸汽—对烘房进行检查*检查能否完满洁净待用*接通电源,开启排水阀门,翻开风机,将烘房温度设定切合要求,翻开预警装置,将烘房试运行—对摇晃式颗粒机进行检查批号:批量:万粒工序:干燥整粒生产记录□切合要求□不切合要求□无□有□切合要求□不切合要求□正常□不正常设施型号: CT-C-Ⅱ编号:□完满洁净□不完满洁净□正常□不正常页号: 1/2文件编号:操作人复核人*检查能否完满洁净待用*装上 24 目铁质筛网,接通电源,按下启动按钮,将摇晃式颗粒机试运行—洁净准备好的工用具,并用75%的乙醇消毒—替代状态标记□完满洁净□不完满洁净实质筛网目数:目□正常□不正常□已洁净□已消毒□未洁净□未消毒* 用正在运行标记替代已洁净标记□已替代□未替代干燥整粒开始1.将湿颗粒均匀摊布于烘盘中;将推车推入烘房,翻开风机,并适当调理排水阀门;开启蒸汽阀;开启预警装置;并控制:页号:2/2品名:胶囊规格:代号:批号:批量:万粒工序:干燥整粒文件编号:日期时间操作步骤生产记录操作人复核人*铺盘厚度≤ 2cm* 湿颗粒进烘房前烘房温度应控制在80-90 ℃*干燥温度≤ 95℃* 干燥时间3-4 小时,每隔 1 小时翻盘一次*干燥结束时水分≤ 1.0%2.将干颗粒送整粒岗位,用摇晃式颗粒机进行整粒,整粒时应随时察看筛网有无破坏,若有破坏应实时改换。
药品批生产记录

药品批生产记录
药业有限公司
批生产记录
页号:1/2
批生产记录
页号:2/2
称量单
页号:1/1
批生产记录
页号:1/2
批生产记录
页号:2/2
批生产记录
页号:1/2
批生产记录
页号:2/2
批生产记录
页号:1/3
批生产记录
批生产记录
批生产记录
批生产记录
批生产记录
充填中间控制记录
充填中间控制记录
充填中间控制记录
批生产记录
批生产记录
批生产记录
批生产记录
批生产记录
内包装中间控制记录
内包装中间控制记录
批生产记录
批生产记录
批生产记录
外包装中间控制记录
页号:1/2
外包装中间控制记录
页号:2/2
附页
变更记载。
药品批生产记录
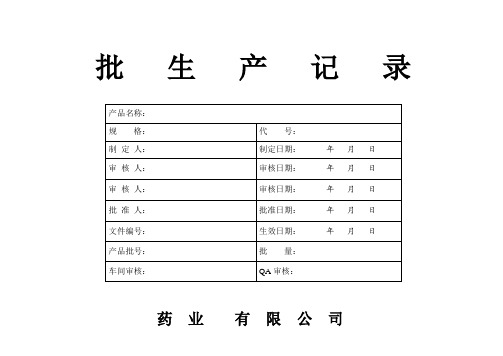
0.02kg
kg
kg
4241
微晶纤维素
16.68kg
0.02kg
kg
kg
4204
淀粉
10.68kg
0.02kg
kg
kg
外加辅料
4210
滑石粉
1.92kg
0.02kg
kg
kg
4252
碳酸氢钠
2.88kg
0.02kg
kg
kg
4207
硬脂酸镁
0.20kg
0.02kg
kg
kg
QA:
备注:
批生产记录
批号:
批量:万粒
工序:干燥整粒
文件编号:
日期
时间
操作步骤
生产记录
操作人
复核人
*铺盘厚度≤2cm
□符合要求□不符合要求
*湿颗粒进烘房前烘房温度应控制在80-90℃
进烘房时的实际温度:℃
*干燥温度≤95℃
干燥时间
1小时
2小时
3小时
4小时
*干燥时间3-4小时,每隔1小时翻盘一次
烘干温度
℃
℃
℃
℃
干燥开始时间:
*检查是否完好清洁待用
□完好清洁□不完好清洁
*接通电源,开启排水阀门,打开风机,将烘房温度设定符合要求,打开预警装置,将烘房试运行
□正常□不正常
—对摇摆式颗粒机进行检查
*检查是否完好清洁待用
□完好清洁□不完好清洁
*装上24目铁质筛网,接通电源,按下启动按钮,将摇摆式颗粒机试运行
实际筛网目数:目
□正常□不正常
页号:1/2
品名:胶囊
规格:
代号:
