烷烃及其同分异构体共19页
烷烃的同系列及同分异构现象

CH3CH2CH2CH
CHCH 56
2CH2CH2CH2CH2CH3 7 8 9 10 11
CH3CH2CH2CHCHCH 3 1 2 3 4 CH3
1 确定主链:有两根等长的长链。两根长链均有两个侧链。侧链位次
均为4,5。侧链的碳原子数均为3,7。
黑字长链4位无侧分支,5位有侧分支。绿字长链4,5位
侧链均有侧 分支。侧分支少优先。
2 编 号:黑字编号,取代基位置4,5。蓝字编号取代基位置7,8。取黑字编号。
3 命 名: 中文命名 4-丙基-5-(1-异丙基丁基)十一烷
英文命名 5-(1-isopropylbutyl)-4-propylundecane
20
第三节 烷烃的构型及分子模型
一、碳原子的四面体概念及分子模型 构型:
由于C的四个sp3轨道的几何构型为正四面体,轨道对称夹角为 109028`,这就决定的烷烃分子中碳原子的排列不是直线形的。 甲烷的正四面体构型可用契性透视式表示:
实线表示处在纸平面上的价键,虚契性线表示处在纸面的价键, 实契性线表示处在纸面前的价键。
23
有机化学中的同分异构现象
碳架异构体
位置异构体
或 CH3(CH2)4CH3
6
有机化合物构造式的表达方式 :
蛛网式
H HH HH HC C C C C H
HH HHH
结构简式
H3C CH CH2 CH2 CH3 CH3
CH3CHCH2CH2CH2CH3 CH3
键线式
OH
7
碳、氢原子的级
CH3
CH3
1oH 2oH 3oH
H3C C CH2 CH CH3 1oC 2oC 3oC 4oC
烷烃(同系物和同分异构体)
烷烃复 习一: 什么叫烷烃? 链状、单键、饱和
烷烃的通式是?其完全燃烧生成的水和二氧化碳 之比为多少? C2H2n+2 (n≥1) 已知10ml的某气态烷烃在50mlO2中充分燃烧,得到 液态水和体积为35ml的混合气体(所有气体都在同温同 压下测定),则该烃可能是什么?
烷烃的表示方法
有机物的几种表示方法
烷烃的化学性质
(1)烷烃的氧化反应 烷烃完全燃烧的通式: CnH2n+2+(3n+1)/2O2 → nCO2+(n+1)H2O
通常情况下,烷烃与高锰酸钾等强氧化剂不发 生反应,不能与强酸和强碱溶液反应。
(2)烷烃的取代反应
其它烷烃与甲烷一样,一定条件下能发生取
代反应。因为可以被取代的氢原子多,所以
H
C
H
C H
H
对称氢原子的概念
我们先看看最简单的甲烷分子… 我们知道甲烷的四个氢原 子是对称的。 如果将甲烷的四个氢原子 用甲基取代,结果会…?
由此可以得到两个规律…
对称氢原子确定的规律
同一碳原子上的氢原子完全对称 。 与同一碳原子相连的甲基上的氢原
子完全对称。
与同一碳原子相连的相同基团对应位置上的
烷烃组成和结构的表示方法
结构简式怎么写?------p23(有机化学)
1.将结构式中的C—H省略,其他的共价键一律不省略.C—C 可省也可不省.但其它如双键,叁键一律不能省. 实际上写结构简式的最简单处理方法就是省略C—H,
其它一概不变!
2.连在同一个C上的相同基团有时也可以合并,并带上括号. 3.同一条链上连续的相同的基团也可以合并,并带上括号
4、主链少三个碳原子
C C ∣ ∣ C -C - C - C ∣ ∣ C C
化学人教版(2019)必修第二册7.1.2同系物 同分异构体(共20张ppt)

课堂学习
同分异构体
在进行同分异构体的命名时,我们习惯的把不带支链的化合物称为正某烷,一条支链的化 合物称为异某烷,两条支链的化合物称为新某烷。
正丁烷
异丁烷
正戊烷
异戊烷
新戊烷
课堂学习
同分异构体
同分异构体具有“三同两不同”的特点:
同分异 构体
三同 两不同
分子式 分相子同组 成分相子同量 结相构同不 性同质不
同
例如正丁烷和异丁烷的物理性质有如下差异:
名称 正丁烷 异丁烷
熔点/℃ -138.4 -159.6
沸点/℃ -0.5 -11.7
相对密度 0.5788 0.557
能够发现对于同分异构体来说,物理性质有一 定差异,支链越多,熔沸点越低,密度越小; 化学性质上也不一定相似。
上面一组物质分子式相同,不可能为 同系物,下面一组物质虽然分子式相 差一个CH2,但是结构不相似,也不 属于同系物。
课堂学习
同分异构体
在刚才的判断中,我们发现同样分子式的物 质也可以具有不同的结构,这种现象是偶然 还是另有蹊跷,请你书写戊烷的结构式、结 构简式和键线式,检测能够写出几种结果?
某些化合物具有相同的分子式,但具有不同 结构的现象,叫做同分异构体现象。 具有同分异构体现象的化合物互称为同分异 构体。
同分异构体的书写
第一步:排主链,主链由长到短,因此将分子中的 全部碳原子连成直链作为主链。
碳链:
C—C—C—C—C—C
物质:
CH3—CH2—CH2—CH2—CH2—CH3
主链由长到短 支链由整到散 位置由心到边
排列对邻到间
课堂学习
烷烃同分异构体:碳原子数为10以内的所有烷烃(共150种)

碳原子数为10以内的所有烷烃同分异体(共150种)1种)一、CH4同分异构体(共1、甲烷二、C同分异构体(共1种)2H61、乙烷同分异构体(共1种)三、C3H81、丙烷四、C同分异构体(共2种)4H101、丁烷2、2—甲基丙烷五、C同分异构体(共3种)5H121、戊烷2、2—甲基丁烷3、2 , 2—二甲基丙烷六、C同分异构体(共5种)6H141、己烷2、2—甲基戊烷3、3—甲基戊烷4、2 , 2—二甲基丁烷5、2 , 3—二甲基丁烷同分异构体(共9种)七、C7H161、庚烷2、2—甲基己烷3、3—甲基己烷4、3—乙基戊烷5、2 , 2—二甲基戊烷6、2 , 3—二甲基戊烷7、2 , 4—二甲基戊烷8、3 , 3—二甲基戊烷9、2 , 2 , 3—三甲基丁烷同分异构体(共18种)八、C8H181、辛烷2、2—甲基庚烷3、3—甲基庚烷4、4—甲基庚烷5、3—乙基己烷6、2 , 2—二甲基己烷7、2 , 3—二甲基己烷8、2 , 4—二甲基己烷9、2 , 5—二甲基己烷10、3 , 3—二甲基己烷11、3 , 4—二甲基己烷12、2—甲基—3—乙基戊烷13、3—甲基—3—乙基戊烷14、2 , 2 , 3—三甲基戊烷15、2 , 2 , 4—三甲基戊烷16、2 , 3 , 3—三甲基戊烷17、2 , 3 , 4—三甲基戊烷18、2 , 2 , 3 , 3—四甲基丁烷九、C同分异构体(共35种)9H201、壬烷2、2—甲基辛烷3、3—甲基辛烷4、4—甲基辛烷5、3—乙基庚烷6、4—乙基庚烷7、2 , 2—二甲基庚烷8、2 , 3—二甲基庚烷9、2 , 4—二甲基庚烷10、2 , 5—二甲基庚烷11、2 , 6—二甲基庚烷12、3 , 3—二甲基庚烷13、3 , 4—二甲基庚烷14、3 , 5—二甲基庚烷15、4 , 4—二甲基庚烷16、2—甲基—3—乙基己烷17、2—甲基—4—乙基己烷18、3—甲基—3—乙基己烷19、3—甲基—4—乙基己烷20、2 , 2 , 3—三甲基己烷21、2 , 2 , 4—三甲基己烷22、2 , 2 , 5—三甲基己烷23、2 , 3 , 3—三甲基己烷24、2 , 3 , 4—三甲基己烷25、2 , 3 , 5—三甲基己烷27、3 , 3 , 4—三甲基己烷28、3 , 3—二乙基戊烷29、2 , 2—二甲基—3—乙基戊烷30、2 , 3—二甲基—3—乙基戊烷31、2 , 4—二甲基—3—乙基戊烷32、2 , 2 , 3 , 3—四甲基戊烷33、2 , 2 , 3 , 4—四甲基戊烷34、2 , 2 , 4 , 4—四甲基戊烷35、2 , 3 , 3 , 4—四甲基戊烷同分异构体(共75种)十、C10H221、癸烷2、2—甲基壬烷3、3—甲基壬烷4、4—甲基壬烷5、5—甲基壬烷6、3—乙基辛烷7、4—乙基辛烷8、2 , 2—二甲基辛烷9、2 , 3—二甲基辛烷10、2 , 4—二甲基辛烷11、2 , 5—二甲基辛烷12、2 , 6—二甲基辛烷13、2 , 7—二甲基辛烷14、3 , 3—二甲基辛烷15、3 , 4—二甲基辛烷16、3 , 5—二甲基辛烷17、3 , 6—二甲基辛烷18、4 , 4—二甲基辛烷19、4 , 5—二甲基辛烷20、4—正丙基庚烷21、4—异丙基庚烷22、2—甲基—3—乙基庚烷23、3—甲基—3—乙基庚烷24、4—甲基—3—乙基庚烷25、2—甲基—4—乙基庚烷26、3—甲基—4—乙基庚烷27、4—甲基—4—乙基庚烷28、2—甲基—5—乙基庚烷29、3—甲基—5—乙基庚烷30、2 , 2 , 3—三甲基庚烷31、2 , 2 , 4—三甲基庚烷32、2 , 2 , 5—三甲基庚烷34、2 , 3 , 3—三甲基庚烷35、2 , 3 , 4—三甲基庚烷36、2 , 3 , 5—三甲基庚烷37、2 , 3 , 6—三甲基庚烷38、2 , 4 , 4—三甲基庚烷39、2 , 4 , 5—三甲基庚烷40、2 , 4 , 6—三甲基庚烷41、2 , 5 , 5—三甲基庚烷42、3 , 3 , 4—三甲基庚烷43、3 , 3 , 5—三甲基庚烷44、3 , 4 , 4—三甲基庚烷45、3 , 4 , 5—三甲基庚烷46、2—甲基—3—异丙基己烷47、3 , 3—二乙基己烷48、3 , 4—二乙基己烷49、2 , 2—二甲基—3—乙基己烷50、2 , 3—二甲基—3—乙基己烷51、2 , 4—二甲基—3—乙基己烷52、2 , 5—二甲基—3—乙基己烷53、3 , 4—二甲基—3—乙基己烷54、2 , 2—二甲基—4—乙基己烷55、2 , 3—二甲基—4—乙基己烷56、2 , 4—二甲基—4—乙基己烷57、3 , 3—二甲基—4—乙基己烷58、2 , 2 , 3 , 3—四甲基己烷59、2 , 2 , 3 , 4—四甲基己烷60、2 , 2 , 3 , 5—四甲基己烷61、2 , 2 , 4 , 4—四甲基己烷62、2 , 2 , 4 , 5—四甲基己烷63、2 , 2 , 5 , 5—四甲基己烷64、2 , 3 , 3 , 4—四甲基己烷65、2 , 3 , 3 , 5—四甲基己烷66、2 , 3 , 4 , 4—四甲基己烷67、2 , 3 , 4 , 5—四甲基己烷68、3 , 3 , 4 , 4—四甲基己烷69、2 , 4—二甲基—3—异丙基戊烷70、2—甲基—3 , 3—二乙基戊烷71、2 , 2 , 3—三甲基—3—乙基戊烷72、2 , 2 , 4—三甲基—3—乙基戊烷73、2 , 3 , 4—三甲基—3—乙基戊烷74、2 , 2 , 3 , 3 , 4—五甲基戊烷75、2 , 2 , 3 , 4 , 4—五甲基戊烷。
烷烃的同系物和同分异构体-高一化学同步精品课件(人教版2019必修第二册)

结构相似,组成上差一个或n个CH2
有机物
C2H6、C4H10
相同分子式,不同结构的化合物
化合物
CH3(CH2)3CH3、C(CH3)4
同位素、同素异形体、同系物、同分异构体的比较
①O2和O3②CH3CH3和CH3CH2CH2CH3 和 ④金刚石和石墨 ⑤氕、氘和氚 ⑥CH3CH2C(CH3)2CH2CH3和 CH3CH2CH(CH3)CH(CH3)CH3
② CH2=CH2和
③ CH4 和 CH3CH3
④ CH3CH2CH3 和
否
否
是
是
⑤
否
分子组成上不是相差“—CH2—”
结构不相似
分子式相同,分子组成上没有相差“—CH2—”
②和④
3、同系物判断的三个关键点①“同”——必须属于同一类物质,通式也相同②“似”——结构相似,是指化学键类型相似,分子中各原子的结合方式相似。(即两种物质属于同一类物质)③“差”——组成上相差n个CH2原子团(n≥1)。同系物一定具有不同的碳原子数(或分子式)
4
2 3
——找准称轴、点、面
CH3CH2CH2CH2CH3
对称轴
③ ② ① ② ③
对称点
①
②
②
②
③
③
③
③
对称点
对称面
①
②
①
①
等效氢法
化学性质相似的物质不一定是同系物
相对分子质量
同系物的相对分子质量一定不相同,相差14n
思考与讨论
正丁烷和异丁烷的分子式的分子式都是C4H10。它们是否为同一种物质?
CH3CH2CH2 CH3
正丁烷
异丁烷
甲烷,乙烷和丙烷的结构只有一种,丁烷却有两种不同的结构(如上图),一种是碳原子形成直链的正丁烷,另一种是带有支链的异丁烷。二者的组成虽然相同,但分子中原子的结合顺序不同,即分子结构不同,因此性质就存在一定差异,是两种不同的化合物。
《烷烃》 讲义

《烷烃》讲义一、烷烃的定义与分类烷烃是一类有机化合物,它们是只含有碳(C)和氢(H)两种元素,且碳与碳之间都以单键相连,其余的价键都与氢原子结合的烃类化合物。
根据碳原子数的不同,烷烃可以分为以下几类:1、甲烷(CH₄):这是最简单的烷烃,只有一个碳原子。
2、乙烷(C₂H₆):有两个碳原子。
3、丙烷(C₃H₈):包含三个碳原子。
4、丁烷(C₄H₁₀):由四个碳原子组成。
随着碳原子数的增加,烷烃的种类越来越多。
一般来说,当碳原子数在 1 到 4 时,烷烃在常温常压下通常是气态;当碳原子数在 5 到 16 时,多为液态;而碳原子数大于 17 时,则往往是固态。
二、烷烃的通式烷烃的通式可以表示为 CₙH₂ₙ₊₂,其中 n 表示碳原子的个数。
通过这个通式,我们可以方便地计算出任何一种烷烃分子中碳和氢原子的数目。
例如,当 n = 5 时,这种烷烃就是戊烷(C₅H₁₂);当 n = 10 时,就是癸烷(C₁₀H₂₂)。
三、烷烃的命名烷烃的命名有一套系统的规则。
1、对于直链烷烃,根据碳原子的数目,依次称为“甲烷”、“乙烷”、“丙烷”等。
2、对于含有支链的烷烃,命名时要遵循以下原则:选择最长的碳链作为主链。
从距离支链最近的一端开始给主链上的碳原子编号。
将支链的位置和名称写在前面,主链的名称写在后面。
例如,对于结构为 CH₃CH(CH₃)CH₂CH₃的烷烃,其名称为 2-甲基丁烷。
其中,“2-”表示甲基在主链的第 2 个碳原子上。
四、烷烃的物理性质1、状态如前面提到的,烷烃的状态与碳原子数密切相关。
气态烷烃分子间的距离较大,相互作用力较弱;液态烷烃分子间的距离较小,相互作用力较强;固态烷烃分子排列紧密,相互作用力很强。
2、溶解性烷烃一般不溶于水,而易溶于有机溶剂,这是因为相似相溶原理,烷烃是非极性分子,水是极性分子。
3、密度烷烃的密度通常小于水的密度,且随着碳原子数的增加,密度逐渐增大。
五、烷烃的化学性质1、稳定性在常温下,烷烃一般不与强酸、强碱、强氧化剂等发生反应,表现出较高的化学稳定性。
烷烃的同分异构体
烷烃是一类碳氢化合物,由碳和氢原子构成。
它们的分子结构由碳原子形成链状,氢原子附着在碳链上。
烷烃的同分异构体是指具有相同分子式(相同的碳氢比)但结构不同的化合物。
烷烃的同分异构体主要是由于碳原子在空间中的不同排列方式导致分子结构的差异。
以下是烷烃的同分异构体示例:
1.丙烷(C3H8)和异丙烷(C3H8):它们的分子式相同,都由三个碳原子和八
个氢原子组成,但结构不同。
丙烷的三个碳原子排列成直链,而异丙烷的三个碳原子中间的碳原子与两个其他碳原子形成支链结构。
2.正丁烷(C4H10)和异丁烷(C4H10):它们的分子式相同,都由四个碳原子
和十个氢原子组成,但结构不同。
正丁烷的四个碳原子排列成直链,而异丁烷的四个碳原子中间的两个碳原子形成支链结构。
3.戊烷(C5H12)和异戊烷(C5H12):它们的分子式相同,都由五个碳原子和
十二个氢原子组成,但结构不同。
戊烷的五个碳原子排列成直链,而异戊烷的五个碳原子中间的一个碳原子形成支链结构。
烷烃的同分异构体是有机化学中的常见现象,同分异构体的存在使得有机化合物的种类变得更加丰富多样。
在有机合成和化学工业中,对同分异构体的识别和区分是十分重要的。
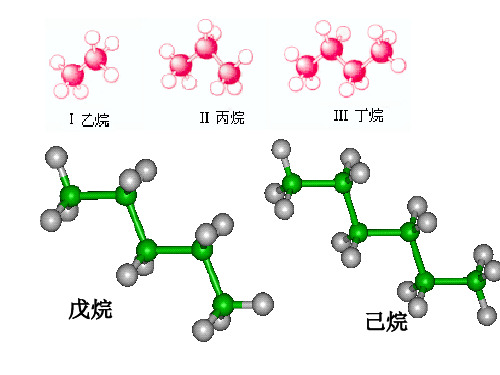
烷烃的同系列及同分异构现象
2-1第2章 烷 烃一、 烷烃的同系列及同分异构现象(一) 烷烃的同系列最简单的烷烃是甲烷,依次为乙烷、丙烷 、丁烷、戊烷等,它们的分子式、构造式为:分子式 构造式 构造简式 甲烷 CH 4 CH 4乙烷 C 2H 6 CH 3CH 3 丙烷 C 3H 8 CH 3CH 2CH 3丁烷 C 4H 10 CH 3CH 2CH 2CH 3从上述结构式可以看出,链烷烃的组成都是相差一个或几个CH 2(亚甲基)而连成碳链,碳链的两端各连一个氢原子。
故:通式烷烃的为 或 C n H 2n+2 。
具有同一通式,结构和化学性质相似,组成上相差一个或多个CH 2的一系列化合物称为同系列。
同系列中的化合物互称为同系物。
由于同系列中同系物的结构和性质相似,其物理性质也随着分子中碳原子数目的增加而呈规律性变化,所以掌握了同系列中几个典型的有代表性的成员的化学性质,就可推知同系列中其他成员的一般化学性质,为研究庞大的有机物提供了方便。
在应用同系列概念时,除了注意同系物的共性外,还要注意它们的个性(因共性易见,个性则比较特殊),要根据分子结构上的差异来理解性质上的异同,这是我们学习有机化学的基本方法之一。
(二) 烷烃的同分异构现象H CH H C H H H H C H H C H H C H HH H C H H C H H C H H C H HH H CH 2H()H C H H H2-2 1. 异构现象甲、乙、丙烷只有一种结合方式,无异构现象,从丁烷开始有同分异构现象,可由下面方式导出,正丁烷(沸点-0.5℃)异丁烷 (沸点-10.2)由两种丁烷可异构出三种戊烷上述这种分子式相同而构造式不同的化合物称为同分异构体,这种现象称为构造异构现象。
构造异构现象是有机化学中普遍存在的异构现象的一种,这种异构是由于碳链的构造不同而形成的,故又称为碳链异构。
随着碳原子数目的增多,异构体的数目也增多。
2. 异构体的导出步骤(三) 伯、仲、叔、季碳原子在烃分子中仅与一个碳相连的碳原子叫做伯碳原子(或一级碳原子,用1°表示) 在烃分子中与两个碳相连的碳原子叫做仲碳原子(或二级碳原子,用2°表示) 在烃分子中与三个碳相连的碳原子叫做叔碳原子(或三级碳原子,用3°表示) 在烃分子中与四个碳相连的碳原子叫做季碳原子(或四级碳原子,用4°表示) 例如:H C H H C C H H H H H H C C C C H H H H H H H HH H C C C H H H CHH HH H H CH 3-CH 2-CH 2-CH 3CH 3CH 2CH 2CH 2CH 3CH 3-CH 2-CH-CH 3正戊烷 b.p 36.1℃异戊烷 b.p 28℃CH 3-CH 2-CH-CH 3CH 3C CH 3CH 3CH 3新戊烷 b.p 9.5℃CH 3CH 3CH 3 C CH 2 CH CH 3CH3CH 31234CH 31°°°°°2-3与伯、仲、叔碳原子相连的氢原子,分别称为伯、仲、叔氢原子。
(完整版)专题13烷烃的命名及同分异构体书写
专题十三烷烃的命名及同分异构体书写第一部分:烷烃的命名一、习惯命名法:1、通常把烷烃泛称某烷”某是指烷烃中碳原子总数(系统命名法为主链碳数)。
由一到十用甲、乙、丙、丁、戊、己、庚、辛、壬、癸表示,自十一起用汉字数字表示。
例如:CH4叫甲烷,CH3CH3叫乙烷,CH3CH2CH3叫丙烷;C15H32叫十五烷。
2、为了区别同分异构体,用正”、异”和新”来表示。
(1)CH3—CH2 —CH2 —CH3 正丁烷(2)CH3 —CH —CH3 异丁烷ICH3习惯命名法只能使用于结构比较简单的烷烃。
对于结构比较复杂的烷烃必须用系统命名法。
—、系统命名法:在系统命名法中,对于支链烷烃,把它看作直链烷烃的烷基取代基衍生物。
烃分子失去一个氢原子所剩余的部分叫做烃基;烷烃分子失去一个氢原子所剩余的部分叫做烷基。
通式:C n H2n+1 (n》1 ),通常用“ R—"表示。
常见的烷基:CH 3 —甲基CH 3 —CH 2 —乙基CH3 —CH2—CH2—正丙基CH3 —CH —异丙基(注意:碳原子处于上下位置时中间短线不能省)ICH3对于支链烷烃的命名法可按照下列步骤进行:1、选主链,称“某烷”。
(最长最多为主链)选定分子里最长碳链为主链,并按主链上碳原子的数目称为“某烷”。
(碳原子数在1~10的用甲、乙、丙、丁、戊、己、庚、辛、壬、癸命名。
)CFRIClk —C II —CII—€ II —Clk —< —CIEJ 1 r 1 1例:-H H - .ii- ■ H主链含八个碳原子故叫辛烷。
侧链则当作取代基。
2、编碳号,定基位。
在选定主链以后,就要进行主链的位次编号,也就是确定取代基的位次,主链从一端向另一端连续编号,号数用1, 2, 3-…等表示,读成1号位,2号位,3号位等。
①主链中离支链最近的一端作为起点,用阿拉伯数字给主链的各个碳原子依次编号定位,以确定支链的位置②若有两个不同支链,且分别处于距主链两端同近的位置,从较简单的支链一端开始编号③若两个相同支链分别处在距主链两端同近位置,中间还有其他支链,从主链两个方向编号,可得到两种标号,将支链位置相加求和,和小者为正确编号。
烷烃 同分异构
结束
设问: 设问: 戊烷有几种同分异构体, 戊烷有几种同分异构体,能写出 它们的结构式吗? 它们的结构式吗?
结束
结束
随着碳原子数目的增多,异构体的数目 随着碳原子数目的增多, 也增多,异构体的推导方法: 也增多,异构体的推导方法: 1.写出该烃的最长碳链。 写出该烃的最长碳链。 2.少写一个作为取代基,依次取代于主 少写一个作为取代基, 链上。 链上。 3.再少写二个,分别取代于主链上 再少写二个, ……
第二章
烷 烃
结束
教学目标
1、烷烃的概念、通式。 、烷烃的概念、通式。 2、烷烃的结构。 、烷烃的结构。 3、烷烃的物理性质。 、烷烃的物理性质。 4、烷烃的化学性质。 、烷烃的化学性质。 5、同系物、同分异构现象。 、同系物、同分异构现象。 6、同分异构体的书写方法。 、同分异构体的书写方法。 7、烷烃的系统命名方法。 、烷烃的系统命名方法。
结束
动手实践一下,看看丁烷有且只有一种结构吗? 动手实践一下,看看丁烷有且只有一种结构吗?
正丁烷和异丁烷是同一种物质吗? 正丁烷和异丁烷是同一种物质吗?
结束
三、同分异构现象和同分异构体
具有相同的分子式,但具有不 具有相同的分子式, 同分异构现象。 同结构现象成为同分异构现象 同结构现象成为同分异构现象。 具有同分异构现象的化合物互 称为同分异构体 同分异构体。 称为同分异构体。
结束
甲烷
C2H6
C3H8
C4H10
结束
2、命名
根据分子中碳原子数目称为“某烷” 根据分子中碳原子数目称为“某烷”,碳 原子数十个以内的依次用“天干” 原子数十个以内的依次用“天干” 即:甲、乙、丙、丁、戊、己、庚、辛、壬、 表示, 癸表示, 十以上的用汉字数字表示碳原子数,用正、 十以上的用汉字数字表示碳原子数,用正、 新表示同分异构体。 异、新表示同分异构体。
