酸的通性练习题
常见的酸酸的通性

常见的酸酸的通性第一篇:常见的酸酸的通性常见的酸酸的通性(1)一、选择题1.下列能导电且是电解质的是()A铅笔芯B酒精C氯化钠晶体D熔化的硝酸钾2.下列叙述正确的是()A氯酸钾在水溶液中能电离出自由移动的氯离子B浓盐酸有有刺激性气味和腐蚀性C液态氯化氢就是浓度最大的盐酸D盐酸遇石蕊试液变红色3.下列属于酸的是()—++、+2-+-+-A.NH4、ClB.Na、H、CO3C.H、NO3D.K、OH4.浓盐酸和浓硫酸敞口放置在空气中一段时间后,它们的质量分数变化分别是()A.前者变大,后者变小B.前者变小,后者变大C.二者都变大D.二者都变小5.下列化学实验操作正确的是()A.将浓硫酸慢慢注入盛有水的量筒中进行稀释B.制作过滤器时,滤纸的边缘应比漏斗口稍低C.氢气还原氧化铜实验结束时,先停止通氢气再熄灭酒精灯D.实验室制备气体时,先装药品再检验装置的气密性6.下列叙述中,错误的是()A.打开浓盐酸的瓶盖,瓶口出现白雾B.酚酞滴入稀盐酸中,显无色C.纯净的盐酸是混合物D.工业盐酸和试剂纯的盐酸都是无色透明液体7.在下列溶液中,有一种无色溶液可使紫色石蕊试液变红色,还能和BaCl2反应生成白色沉淀,这种溶液是()A盐酸B稀硫酸C 硫酸钠D澄清的石灰水8.下列物质能由金属和酸直接反应制得的是()A. FeCl3B.CuCl2C. HgCl2D.FeCl29.要除去盐酸中的少量硫酸,可加入适量的()ANaOH溶液BAgNO3溶液CBaCl2溶液DBa(OH)2溶液10.试管内壁俯有下列物质,不能用稀盐酸除去的是()A盛石灰水后留下的白色固体B用足量的H2还原CuO后留下的红色固体C硫酸铜溶液和氢氧化钠溶液反应后留下的蓝色絮状沉淀D用足量的CO还原Fe2O3后留下的黑色固体11.下列能与盐酸反应,但不生成沉淀或气体的是()A.Na2CO3B.FeC.AgNO3溶液D.CuO12.稀硫酸与盐酸常用作金属表面的清洗剂,是利用了它们化学性质中的()A.能与碱反应B.能与金属反应C.能与金属氧化物反应D.能与石蕊试液反应13.要把盐酸与稀硫酸两种无色溶液区分开来,应选用的试剂是()A.石蕊试液B.锌粒C.AgNO3溶液D. Ba(NO3)2溶液14.足量的Zn、ZnO、Zn(OH)2、ZnCO3分别与等质量的相同质量分数的稀硫酸反应,所得溶液中硫酸锌的质量分数最大的是()A.ZnCO3B.Zn(OH)2C. ZnOD.Zn15.现有等质量的①铁粉、②镁粉、③锌粉,分别跟足量的同温度同浓度的稀硫酸反应。
九年级化学下册《酸的通性》练习题1_

九年级化学下册《酸的通性》练习题1_
第八章酸碱盐(三)
酸的通性pH
基础应用
一、选择题每小题只有一个选项符合题意。
1.酸具有通性的原因是
A酸都能与碱发生中和反应B酸都能与活泼金属反应放出氢气
C酸中都含有氢元素D酸电离时,生成的阳离子都是氢离子
2.下列描述属于物质化学性质的是
A盐酸具有挥发性B浓硫酸的吸水性
C HNO3的强氧化性D溶液的导电性
3.下列几种酸的命名错误的是
A HCl盐酸
B HNO3硝酸
C H2SO4氢硫酸
D H2SiO3硅酸4.下列各酸中,既属于二元酸,又属于无氧酸的是A HNO3 B H2S C HCl D H2CO3 5.下列属于碱性氧化物的是
A氧化钠B二氧化硫C水D氯酸钾6.下列属于中和反应的是
A氧化铜和盐酸反应B纯碱和硫酸反应
C氢氧化钡和硝酸反应D二氧化碳和石灰水反应
7.pH等于零的溶液为
A酸性溶液B碱性溶液C中性溶液D无此溶液8.将浓H2SO4滴在干燥的石蕊试纸上,可观察到试纸
A只变红B先变红后变黑C只变黑D先变黑后变红9.下列金属中能与相同的酸反应放出氢气,且反应最快的是
A Na
B Al
C Ag
D Cu
10.往某溶液中滴入酚酞试液,溶液变为红色说明
A该溶液pH=7 B该溶液pH<7
C该溶液pH>7 D该溶液一定是酸
11.酸都具有一些相似的化学性质是因为
A酸的pH都小于7 B酸溶液中都有酸根离子
C酸溶液中阳离子都是氢离子D酸溶液中都含有氢气12.日常生活中接触到的下列物质中,不含酸的是
A汽水B食醋C食盐D发酵后的面粉
感谢您的阅读!。
专题训练(一) 酸的通性(2021年初中科学浙教版)
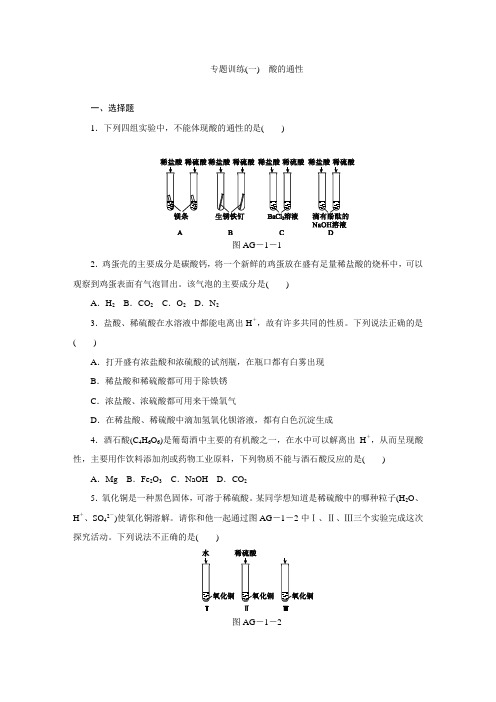
专题训练(一)酸的通性一、选择题1.下列四组实验中,不能体现酸的通性的是()图AG-1-12.鸡蛋壳的主要成分是碳酸钙,将一个新鲜的鸡蛋放在盛有足量稀盐酸的烧杯中,可以观察到鸡蛋表面有气泡冒出。
该气泡的主要成分是()A.H2B.CO2C.O2D.N23.盐酸、稀硫酸在水溶液中都能电离出H+,故有许多共同的性质。
下列说法正确的是()A.打开盛有浓盐酸和浓硫酸的试剂瓶,在瓶口都有白雾出现B.稀盐酸和稀硫酸都可用于除铁锈C.浓盐酸、浓硫酸都可用来干燥氧气D.在稀盐酸、稀硫酸中滴加氢氧化钡溶液,都有白色沉淀生成4.酒石酸(C4H6O6)是葡萄酒中主要的有机酸之一,在水中可以解离出H+,从而呈现酸性,主要用作饮料添加剂或药物工业原料,下列物质不能与酒石酸反应的是() A.Mg B.Fe2O3C.NaOH D.CO25.氧化铜是一种黑色固体,可溶于稀硫酸。
某同学想知道是稀硫酸中的哪种粒子(H2O、H+、SO42-)使氧化铜溶解。
请你和他一起通过图AG-1-2中Ⅰ、Ⅱ、Ⅲ三个实验完成这次探究活动。
下列说法不正确的是()图AG-1-2A.实验Ⅰ能说明H2O不能使CuO溶解B.在Ⅲ中应该加入盐酸C.此实验说明稀硝酸也能溶解CuOD.可以提出的假设:溶液中的H+使CuO溶解6. 2018·上城区一模室温下,将稀盐酸滴入装有氢氧化钠溶液的烧杯中(滴有酚酞),用温度计测出烧杯中溶液的温度(中和反应放热),变化情况如图AG-1-3所示,下列叙述不正确的是()图AG-1-3A.从A到C过程中,烧杯中溶液的pH逐渐减小B.从A到C过程中,反应放出的热量由少变多再变少C.C处溶液的溶质有两种(不考虑酚酞)D.B点溶液颜色刚好从红色变为无色二、填空题7.2018·江干区模拟从微观角度看物质的变化是科学特有的思维方式。
图AG-1-4中三幅示意图分别表示生成氯化钠的不同化学反应。
根据图示回答相关问题。
图AG-1-4(1)从甲图中可以看出钠在氯气中燃烧生成的氯化钠由______________构成。
高中化学复习知识点:酸的通性

10.CD
【解析】
【详解】
A.浓硫酸使其他物质脱水生成新的物质,属于化学反应,是化学性质,故A正确;
B.浓硫酸具有强的氧化性,常温下能够使铁、铝发生钝化,故B正确;
C.制备乙酸乙酯的反应中起催化剂和吸水剂作用,故C错误;
D.浓硫酸与氯化钠固体共热制氯化氢气体时,表现难挥发性,故D错误;
3.D
【解析】
【分析】
【详解】
A、该反应没有化合价的变化,不属于氧化还原反应,H2SO4只表现了酸性,故A不符合题意;
B、该反应没有化合价变化,不属于氧化还原反应,H2SO4只表现了酸性,故B不符合题意;
C、H2SO4中S的价态由+6价→+4价,化合价降低,硫酸在此反应中只体现氧化性,故C不符合题意;
答案选A。
【点睛】
酸性需要通过酸碱指示剂,或者是化学反应中体现出来的,蔗糖遇到浓硫酸的实验中没有体现出酸性。
6.D
【解析】
【分析】
浓硫酸和稀硫酸都具有酸性,但浓硫酸还具有吸水性、脱水性和强氧化性;不能区分浓硫酸和稀硫酸,说明其反应现象相同,据此分析解答。
【详解】
A.稀硫酸和铁反应生成氢气,浓硫酸和铁发生钝化现象,所以现象不同,可以区分,故A不选;
②C+2H2SO4(浓) CO2↑+2SO2↑+2H2O
③Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
④2FeO+4H2SO4(浓)===Fe2(SO4)3+SO2↑+4H2O
A.①②B.③④C.①③D.②④
3.下列反应中,浓硫酸既表现出强氧化性又表现出酸性的是()
A.2NaCl+H2SO4(浓) Na2SO4+2HCl↑
2019-2020学年九年级化学全册酸的通性练习1鲁教版.docx

2019-2020 学年九年级化学全册酸的通性练习 1 鲁教版1、熟记溶液颜色:大多数溶液是无色24CuCl 、 CuSO的水溶液因为含为色FeCl 3、 Fe2(SO4) 3的水溶液因为含为色FeCl 2、 FeSO4的水溶液因为含为色2、由于酸在溶液里电离出的阳离子都是相同的,所以酸类物质有以下明显的“通性”:(写出有关化学方程式举例)(1)酸跟指示剂作用:酸溶液使紫色石蕊试液,无色酚酞(2)酸+→+举例:(3)酸+→+举例:(4)酸+→+(中和反应)举例:3、重要知识点:金属活动性顺序表K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au金属活动性逐渐减弱(1.)在金属活动性顺序里:金属的位置越______ ,它的活动性就越强。
越容易失去电子.(2.)在金属活动性顺序里:位于____前面的金属能与酸反应放出_____。
(其中对于酸来说、除外)3.单质铁参加置换反应时,生成+2 价铁的化合物。
练习:1、分别写出镁与稀盐酸、镁与稀硫酸反应的化学方程式(反应)(反应)现象2、分别写出锌与稀盐酸、锌与稀硫酸反应的化学方程式(反应)(反应)现象3分别写出铁与稀盐酸、铁与稀硫酸反应的化学方程式(反应)(反应)现象 : ( 1)(2)4、铝与稀盐酸反应化学方程式、现象小结:酸+活泼的金属单质→ 盐+氢气。
反应类型:置换反应定义:一种单质与一种化合物反应生成另一种单质与另一种化合物,这种反应叫做置换反应。
4、生锈铁钉中铁锈主要成分是,颜色是色。
将一枚生锈的铁钉放入盐酸中,首先观察到铁锈,溶液由色变为色,该反应化学方程式(反应);过一会儿,还能观察到的现象是,该反应的化学方程式(反应)。
根据上述反应特征,盐酸在工业上可以用来。
工业上能否将生锈的铁制品长时间浸泡在盐酸中?为什么?5、氧化铜与稀硫酸反应的化学方程式(反应)现象:( 1)( 2)小结:酸+金属氧化物→ 盐+水。
常见的酸

常见的酸盐酸硫酸硝酸磷酸1、酸的通性(1)酸溶液能跟酸碱指示剂起反应。
紫色石蕊试液遇酸变红,无色酚酞试液遇酸不变色。
注意显色的物质是指示剂。
(2)酸能跟多种活泼金属起反应,通常生成盐和氢气。
只有位于金属活动性顺序表中氢前面的金属才能与稀酸(HCl、H2SO4)反应,产生氢气。
位于氢后的金属不能与稀酸(HCl、H2SO4)反应,但能与浓硫酸和浓硝酸反应。
例如:①Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O②3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O可见,金属和浓硫酸、硝酸反应都没有氢气产生,这就是实验室不能用浓硫酸和硝酸与锌反应制氢气的原因。
(3)酸能跟碱性氧化物反应生成盐和水:H2SO4 + CaO == CaSO4 + H2O(4)酸能跟某些盐反应生成新酸和新盐:H2SO4 + BaCl2 === BaSO4↓+ 2HCl(5)酸跟碱起中和反应生成盐和水:H2SO4+Ba(OH)2 === BaSO4↓(白色沉淀)+2H2O常见的酸有盐酸、硫酸和硝酸,它们虽然具有上述五点通性(因为电离出的阳离子都是H+)。
但又各具不同的物理化学性质。
①盐酸是氯化氢的水溶液,是一种混合物。
纯净的盐酸是无色的液体,有刺激性气味。
工业品浓盐酸因含有杂质(Fe3+)带有黄色。
浓盐酸具有挥发性,打开浓盐酸的瓶盖在瓶口立即产生白色酸雾。
这是因为从浓盐酸中挥发出来的氯化氢气体跟空气中水蒸汽接触,形成盐酸小液滴分散在空气中形成酸雾。
②硫酸是一种含氧酸,对应的酸酐是SO3(SO3+H2O==H2SO4)。
纯净的硫酸是没有颜色、粘稠、油状的液体,不易挥发。
常用的浓硫酸中的H2SO4的质量分数为98%,密度为1.84克/厘米3。
稀H2SO4具有酸的通性。
浓硫酸除去具有酸的通性外,还具有三大特性:a、吸水性:浓H2SO4吸收水形成水合硫酸分子(H2SO4•nH2O),并放出大量热,所以浓硫酸通常用作干燥剂。
酸的通性练习题
填空:
1、与指示剂作用(除H2SiO3)。
盐酸能使紫色石蕊试液变成色,使无色酚酞不变色。
2、酸+=盐+氢气
氢前的金属。
酸指稀盐酸和稀硫酸。
(稀、浓硝酸和浓硫酸有氧化性,不包括弱酸。
)Zn+2HCl= +H2↑
Zn+H2SO4= +H2↑
3、酸+=盐+水
①凡是跟酸起反应,生成盐和水的氧化物,叫做氧化物。
如:CuO、CaO、MgO等。
②金属氧化物大多数是碱性氧化物。
③K2O、CaO、Na2O可溶于水。
(MgO需加热)
Fe2O3+6HCl=2 +3H2O
CuO+2HCl= +H2O
Fe2O3+ 3H2SO4= +3H2O
+ H2SO4=Cu SO4+H2O
4、酸+=盐+水
①酸跟碱作用生成盐和水的反应叫做反应。
②改良酸性土壤。
Ca(OH)2
+2HCl=CuCl2+2H2O
+ H2SO4=Cu SO4+2H2O
5、酸+=新盐+新酸
+2HCl=CaCl2+CO2↑+H2O (检验CO32-)
+HCl=AgCl↓+HNO3(检验Cl-)
+H2SO4=BaSO4↓+2HCl (检验SO42-)
酸溶液中都有H+存在,决定了酸具有相似的化学性质(通性)。
鲁教版九年级化学下册第七单元《酸的通性》同步练习(含答案)
鲁教版九年级化学下册第七单元《酸的通性》同步练习(含答案)01知识管酸的化学性质具有通性原因:酸的水溶液中都含有相同的阳离子——________,所以酸的水溶液都具有相似的________性质,即酸溶液具有通性。
与指示剂反应:酸溶液能使紫色石蕊溶液变________,不能使无色酚酞溶液变色。
与金属反应:酸能与多种________发生置换反应并产生________,如:铁与稀盐酸的反应________________;锌与稀硫酸的反应________________。
与金属氧化物反应:酸能与某些________反应生成________,如:稀盐酸和稀硫酸可分别与铁锈反应,其化学方程式分别为____________________、__________________________。
注意:(1)铁与稀盐酸、稀硫酸的反应生成物为FeCl2、FeSO4,其中铁元素的化合价为+2价,溶液为浅绿色;而在Fe2O3中,铁元素的化合价为+3价,与稀盐酸、稀硫酸的反应生成物为FeCl3、Fe2(SO4)3,溶液为黄色。
(2)用酸除铁锈时,不能将铁器长时间放在酸溶液里浸泡,因为铁锈除去后,铁也能跟酸反应,消耗金属。
02基础题1.(泸州中考)化学上常对物质进行分类和研究,以下物质中属于酸的是( )A.HNO3 B.MgO C.O2 D.NaCl2.(上海中考)除铁锈的试剂是( )A.氯化钠溶液 B.稀盐酸C.氢氧化钠溶液 D.水3.大理石雕像很容易被酸雨腐蚀,下列材料代替大理石做雕像比较耐腐蚀的是( ) A.铁 B.铝C.铜 D.表面镀锌的金属4.(淄博中考)用稀盐酸除去铁锈主要成分的原理是( )A.FeO+2HCl===FeCl2+H2OB.FeO+2HCl===FeCl3+H2OC.Fe2O3+6HCl===2FeCl2+3H2OD.Fe2O3+6HCl===2FeCl3+3H2O5.将表面生锈的铁钉投入到稀硫酸中,开始时观察到的现象是_____________________,化学方程式为______________________;较长时间后观察到的现象是————————__________________________,化学方程式为______________。
第3讲酸的通性(原卷版+解析)
第3讲酸的通性[知识目录]模块一:酸的通性 (1)模块二:检验硫酸根离子与氯离子 (4)【巩固训练】 (6)[知识掌握]模块一:酸的通性1.能使紫色石蕊试液,无色酚酞。
2.金属+ 酸= 盐+氢气将锌、铁等金属放入酸中,有气泡产生。
经检验,该气体能燃烧,并发出的火焰,气体是。
这说明酸能和某些金属反应生成氢气。
写出锌与硫酸,镁和盐酸反应的化学方程式:、。
3.金属氧化物+ 酸= 盐+水将生锈的铁钉放入硫酸中,铁锈会消失,并生成色溶液,一段时间后会有气泡产生。
这说明酸能和金属氧化物反应生成盐和水。
请写出生锈的铁钉与硫酸反应的化学方程式:、。
4.碱+酸= 盐+水在蓝色的氢氧化铜沉淀中加入盐酸,沉淀会溶解,变为蓝色溶液。
这说明酸能和碱反应产生盐和水。
请写出氢氧化铜和盐酸,氢氧化铁和硫酸反应的方程式:、。
5.盐+酸= 新盐+新酸在石灰石、大理石上滴加盐酸,有气泡产生,该气体能使燃烧的木条熄灭,该气体是。
说明酸能和某些盐反应。
石灰石和盐酸反应的方程[例题1](2022秋•杭州期末)在①氧化铜②金属镁③氢氧化钠溶液④硝酸钡溶液这四种物质中,跟稀硫酸能发生反应且反应中表现了“酸的通性”的组合是()A.①②③B.②③④C.①③④D.①②③④[例题2](2022秋•萧山区期中)现有①K2CO3、②Fe、③BaCO3、④CuO、⑤CO2五种物质,其中不能溶于水,但能与稀硫酸反应放出无色气体的是()A.①②B.②③C.②⑤D.②④[例题3](2022秋•椒江区校级期中)某化学小组在课外活动时做了一个实验,在甲试管中装入固体物质,乙试管装入某溶液,按如图所示组装好仪器(图中铁架台等仪器已略去)。
通过分液漏斗加入足量稀盐酸,同时打开止水夹,乙试管溶液中只看到有气泡冒出;再关闭止水夹,发现一段时间后乙中溶液变浑浊。
则甲、乙试管内所盛试剂符合此实验现象的一组是()A.Zn、AgNO3溶液B.Na2CO3、NaOH溶液C.KOH、BaCl2溶液D.CaCO3、Ca(OH)2溶液[例题4](2022秋•临海市期末)为验证“酸的通性”,小科进行了如图实验。
酸的通性练习题
}酸的通性练习1 下列关于浓硫酸的描述错误的是()A.溶于水时放出大量的热 B.有强烈的腐蚀性C.稀释时切不可将水倒进浓硫酸中 D.可在量筒中用浓硫酸配制稀硫酸3.(张家界中考)制作馒头时,需加入面碱(主要含碳酸钠),如果面碱放多了,蒸出的馒头会发黄,且口感不好。
为除去过多的面碱,做馒头时可加入适量的()A、食醋B、食盐C、料酒D、味精4.(桂林中考)下列对实验意外事故的处理错误的是()A.硫酸洒在实验台上,立即用氢氧化钠溶液冲洗&B.实验药液溅入眼睛,立即用水冲洗,切不可用手揉搓C.酒精灯洒出的酒精在桌上燃烧,立即用湿布或沙子扑灭D.浓硫酸沾到皮肤上,立即用大量的水冲洗,再涂上3%~5%的碳酸氢钠溶液5.(莱芜中考)从物质的组成角度解释酸具有酸的通性的原因是()A.酸溶于水都能电离出H+ B.酸都含有酸根C.酸中都含有氢元素 D.酸中都含有氧元素6.下列物质露置在空气中质量增加且溶质质量分数减少的是()A.氯化钠 B.浓盐酸`C.浓硫酸 D.硝酸钾7.下列物质,能由金属跟盐酸直接作用而制得的是( )A.MgCl2B.FeCl3C.CuCl2D.AgCl1.下列反应的化学方程式,书写正确的是()A.B.C.D.》2.下列关于盐酸的性质中,属于物理性质的是()A.盐酸可以使紫色石蕊试液变为红色B.浓盐酸在空气中易挥发形成白雾C.盐酸可以除去铁表面生成的铁锈D.盐酸可以跟硝酸银溶液反应生成白色沉淀5.(2010•莱芜中考)从物质的组成角度解释酸具有酸的通性的原因是() A.酸溶于水都能电离出H+ B.酸都含有酸根C.酸中都含有氢元素 D.酸中都含有氧元素%3.下列物质中能跟盐酸反应,既不生成沉淀,又无气体放出且溶液呈无色的是()A.B.C.D.4.下列物质都能电离出氢离子,其中不属于酸的是()A.B.C.D.5.下列物质敞口放置在空气中,一段时间后物质质量增加的是()A.浓 B.浓 C.食盐水 D.水6.硫酸可用于金属表面除锈,这是因为硫酸()A.具有吸水性 B.能跟金属反应,C.能跟碱反应 D.能跟金属氧化物反应7.下列各组中的两种物质分别跟稀反应,能生成相同的盐的是()A.和 B.和C.和 D.和8.检验硫酸应使用下列试剂中的()A.紫色石蕊试液 B.无色酚酞试液C.硝酸银溶液 D.紫色石蕊试液和氯化钡溶液8.(2010·上海中考)能反映相关实验过程中量的变化的图像是( )、10.相同质量的锌和镁,分别和足量的稀硫酸反应,生成氢气的质量()A.一样多B.锌与硫酸反应生成的多C.镁与硫酸反应生成的多D.无法比较12.下列各物质敞口放置在空气中一段时间后,质量会减少的是()A.浓硫酸B.食盐溶液C.澄清的石灰水D.浓盐酸、13.下列物质发生反应,能产生氢气的是()A.氧化铁和稀硫酸 B.锌和浓硫酸C.铁和稀盐酸 D.氧化锌和硝酸14.有一瓶无色液体,可能是和,选用下列哪种试剂可以鉴别()A. B.石蕊试液 C.酚酞试液 D.溶液15.下列反应中,反应前后元素的化合价保持不变的是()A. B.C. D.|16.质量相同的下列金属与足量稀反应,放出最少的是()A.Zn B.Al C.Mg D.Na17.下列对盐酸的性质叙述正确的是()A.浓盐酸是一种无色无味的液体B.浓盐酸有挥发性C.浓盐酸挥发在空气中会产生白烟D.浓盐酸有强氧化性18.把盛浓硫酸的试剂瓶敞口放置一段时间后,它的变化情况是()A.溶液变浓了 B.质量变小了C.溶液中溶质质量分数变小 D.不变!11.(2012.鸡西市)除去下列物质中所含的少量杂质,下表中除杂方法正确的是()选项物质所含杂质除杂质的方法A氧化铜氯化钠加水溶解、过滤、蒸发B氧气;水蒸气通过盛有浓硫酸的洗气瓶C硫酸钠溶液稀硫酸加入过量碳酸钠溶液,过滤D二氧化碳一氧化碳点燃15.要使右图装置中的小气球鼓起来,则使用的固体和液体可以是:()①锌和稀硫酸②石灰石和盐酸③氯化钠和水④铁锈和盐酸—⑤二氧化锰和双氧水⑥氧化钙和水.A.①②③⑤B.①②④⑤C.①②⑤⑥D.①②③④⑤⑥%24.下列属于硫酸的性质的是()①具有挥发性②具有吸水性③有腐蚀性④有脱水性⑤有刺激性气味⑥使紫色的石蕊试液变蓝⑦有酸味A.①②④⑤B.②③④C.③④⑤⑦D.②⑤④⑦二、填空题1.浓硫酸是______色______状液体,______挥发。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
酸的通性练习
1 下列关于浓硫酸的描述错误的是()
A.溶于水时放出大量的热 B.有强烈的腐蚀性
C.稀释时切不可将水倒进浓硫酸中 D.可在量筒中用浓硫酸配制稀硫酸
3.(张家界中考)制作馒头时,需加入面碱(主要含碳酸钠),如果面碱放多了,蒸出的馒头会发黄,且口感不好。
为除去过多的面碱,做馒头时可加入适量的()
A、食醋
B、食盐
C、料酒
D、味精
4.(桂林中考)下列对实验意外事故的处理错误的是()
A.硫酸洒在实验台上,立即用氢氧化钠溶液冲洗
B.实验药液溅入眼睛,立即用水冲洗,切不可用手揉搓
C.酒精灯洒出的酒精在桌上燃烧,立即用湿布或沙子扑灭
D.浓硫酸沾到皮肤上,立即用大量的水冲洗,再涂上3%~5%的碳酸氢钠溶液
5.(莱芜中考)从物质的组成角度解释酸具有酸的通性的原因是()
A.酸溶于水都能电离出H+ B.酸都含有酸根
C.酸中都含有氢元素 D.酸中都含有氧元素
6.下列物质露置在空气中质量增加且溶质质量分数减少的是()
A.氯化钠 B.浓盐酸
C.浓硫酸 D.硝酸钾
7.下列物质,能由金属跟盐酸直接作用而制得的是( )
A.MgCl
2B.FeCl
3
C.CuCl
2
D.AgCl
1.下列反应的化学方程式,书写正确的是()
A.
B.
C.
D.
2.下列关于盐酸的性质中,属于物理性质的是()A.盐酸可以使紫色石蕊试液变为红色
B.浓盐酸在空气中易挥发形成白雾
C.盐酸可以除去铁表面生成的铁锈
D.盐酸可以跟硝酸银溶液反应生成白色沉淀
5.(2010•莱芜中考)从物质的组成角度解释酸具有酸的通性的原因是() A.酸溶于水都能电离出H+ B.酸都含有酸根
C.酸中都含有氢元素 D.酸中都含有氧元素
3.下列物质中能跟盐酸反应,既不生成沉淀,又无气体放出且溶液呈无色的是()
A.B.C.D.
4.下列物质都能电离出氢离子,其中不属于酸的是()
A.B.C.D.
5.下列物质敞口放置在空气中,一段时间后物质质量增加的是()
A.浓 B.浓 C.食盐水 D.水6.硫酸可用于金属表面除锈,这是因为硫酸()
A.具有吸水性 B.能跟金属反应
C.能跟碱反应 D.能跟金属氧化物反应
7.下列各组中的两种物质分别跟稀反应,能生成相同的盐的是()A.和 B.和
C.和 D.和
8.检验硫酸应使用下列试剂中的()
A.紫色石蕊试液 B.无色酚酞试液
C.硝酸银溶液 D.紫色石蕊试液和氯化钡溶液
8.(2010·上海中考)能反映相关实验过程中量的变化的图像是( )
10.相同质量的锌和镁,分别和足量的稀硫酸反应,生成氢气的质量()A.一样多B.锌与硫酸反应生成的多
C.镁与硫酸反应生成的多D.无法比较
12.下列各物质敞口放置在空气中一段时间后,质量会减少的是()A.浓硫酸B.食盐溶液C.澄清的石灰水D.浓盐酸
13.下列物质发生反应,能产生氢气的是()
A.氧化铁和稀硫酸 B.锌和浓硫酸
C.铁和稀盐酸 D.氧化锌和硝酸
14.有一瓶无色液体,可能是和,选用下列哪种试剂可以鉴别()
A. B.石蕊试液 C.酚酞试液 D.溶液
15.下列反应中,反应前后元素的化合价保持不变的是()
A. B.
C. D.
16.质量相同的下列金属与足量稀反应,放出最少的是()A.Zn B.Al C.Mg D.Na
17.下列对盐酸的性质叙述正确的是()
A.浓盐酸是一种无色无味的液体B.浓盐酸有挥发性
C.浓盐酸挥发在空气中会产生白烟D.浓盐酸有强氧化性
18.把盛浓硫酸的试剂瓶敞口放置一段时间后,它的变化情况是()A.溶液变浓了 B.质量变小了
C.溶液中溶质质量分数变小 D.不变
11.(2012.鸡西市)除去下列物质中所含的少量杂质,下表中除杂方法正确的是()
选项物质所含杂质除杂质的方法
A 氧化铜氯化钠加水溶解、过滤、蒸发
B 氧气水蒸气通过盛有浓硫酸的洗气瓶
C 硫酸钠溶液稀硫酸加入过量碳酸钠溶液,过
滤
D 二氧化碳一氧化碳点燃
①锌和稀硫酸②石灰石和盐酸
③氯化钠和水④铁锈和盐酸
⑤二氧化锰和双氧水⑥氧化钙和水.
A.①②③⑤B.①②④⑤C.①②⑤⑥D.①②③④⑤⑥
24.下列属于硫酸的性质的是()
①具有挥发性②具有吸水性③有腐蚀性④有脱水性
⑤有刺激性气味⑥使紫色的石蕊试液变蓝⑦有酸味
A.①②④⑤B.②③④C.③④⑤⑦D.②⑤④⑦
二、填空题
1.浓硫酸是______色______状液体,______挥发。
在稀释浓硫酸时,一定要把______沿着烧杯壁或玻璃棒缓缓注入______里,边注入边______使产生
______迅速地扩散。
2.除去铁器的锈(主要成分:),通常可用______和______。
3.将浓硫酸长时间放在敞口容器中,质量分数会变______。
这是因为浓硫酸有______性;浓硫酸滴在纸上或布上时,纸和布的颜色会变______,这是浓硫酸使它们______的缘故,因为浓硫酸还有______性。
4.在下表中,A组的______能跟B组中所有物质发生反应。
A组盐酸硫酸
B组硝酸钡溶液氧化铜氢氧化钠溶液
写出能反应的化学方程式:_______________________________
_______________________________
_______________________________
5.硫酸_______水(填“易溶于”、“难溶于”、“溶于”)溶解时需_______。
6.在稀释浓硫酸时,一定要把_______沿着器壁慢慢注入_______里并不断_______,使产生热量迅速扩散。
7.由两种_______互相交换成分,生成另外两种_______的反应叫做复分解反应,例如_______。
8.把盛有氧化铜的试管里,加入适量的稀硫酸,观察到的现象是_______,反应的化学方程式是_______,此反应属于_______。
(填反应类型)
9.纯净的浓盐酸是_______的液体,工业品浓盐酸是黄色是因为_______。
10.酸可用于金属表面的除锈,是因为_______。
17.向放有表面生锈的铁钉的试管中加入过量盐酸,刚开始时的现象______________________________反应的化学方程式是______________________________,充分反应后的现象是______________________________,反应的化学方程式:______________________________。
18.将浓硫酸、浓盐酸敞口放置在空气中,能形成白雾的是,质量变大的是,质量变小的是,它们的质量分数。
