乙苯
乙苯的制备原理

乙苯的制备原理乙苯是一种有机化合物,也被称为苯乙烷,化学式为C8H10。
它是一种无色液体,具有特殊的香味,常用作溶剂和作为化学反应的起始物质。
乙苯的制备原理有多种方法,最常用的方法是通过重整合成反应来制备乙苯。
以下将详细介绍其中两种常见的制备方法。
1. 乙苯烷烃化乙苯烷烃化是最常用的制备乙苯的方法之一。
这种方法使用乙烯(C2H4)和苯(C6H6)作为原料,在适宜的反应条件下进行反应,制备乙苯。
反应方程式如下:C2H4 + C6H6 →C6H5CH3反应条件是在催化剂存在的条件下进行,通常选择过渡金属催化剂,例如铝的氯化物作为催化剂。
反应温度一般在180-220C之间,压力为1-10大气压。
在反应过程中,乙烯和苯被加热,并吹入高压环境下的催化剂床,通过化学反应生成乙苯。
该方法的优点是反应具有较高的收率,并且催化剂可以循环使用,有效降低制备成本。
然而,这种方法需要对废气进行处理,以减少对环境的污染。
2. 甲苯甲基化乙苯也可以通过甲苯甲基化的方法制备。
甲苯(C7H8)是一个含有甲基基团的化合物,因此通过将甲苯和甲烷(CH4)反应,可以得到乙苯。
反应方程式如下:CH3CH3 + C7H8 →C6H5CH3 + H2此方法的反应条件与乙苯烷烃化方法类似。
反应温度一般在500-600C之间,压力为10-30大气压。
反应产物乙苯直接升华,并通过冷凝回收,同时也可以回收未反应的甲烷。
这种方法的优点是原材料的选择相对较宽,不仅可以使用乙烯,还可以使用甲烯、乙炔等作为甲基化试剂。
此外,反应产物乙苯的纯度较高,并且不需要额外的废弃物处理。
除了以上两种方法,还有其他一些制备乙苯的方法,例如:煤炭气化法、氢化苯法等。
这些方法主要适用于特殊条件下的制备,其原理和反应条件与前述方法有所不同。
综上所述,乙苯的制备原理主要通过烃烃化或甲基化的方法进行。
不同的方法适用于不同的条件和要求,但它们都需要催化剂的参与,通过适当的反应条件和原料选择,可以高效地制备乙苯。
MSDS-乙苯

救
措
施
皮肤接触:脱去被污染的衣着,用肥皂水和清水彻底冲洗皮肤。
眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。就医。
吸入:迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,给输氧。如呼吸停止,立即进行人工呼吸。就医。
食入:饮足量温水,催吐,就医。
食入:饮足量温水,催吐,用2%~5%硫酸钠溶液洗胃,导泻。就医。
标
识
中文名:乙苯
英文名:ethylbenzene
分子式:C8H10;C6H5CH2CH3
分子量:106.16
CAS号:100-41-4
危险性类别:第3.2 类中闪点易燃液体
化学类别:无资料
主
要
组
成
与
性
状
主要成分:纯品
主要用途: 用于有机合成和用作溶剂
外观与性状:无色液体,有芳香气味
健
康
危
害
侵入途径:吸入、食入、经皮吸收。
健康危害:健康危害:本品对皮肤、粘膜有较强刺激性,高浓度有麻醉作用。
急性中毒:轻度中毒有头晕、头痛、恶心、呕吐、步态蹒跚、轻度意识障碍及眼和上呼吸道刺激症状。重者发生昏迷、抽搐、血压下降及呼吸循环衰竭。可有肝损害。直接吸入本品液体可致化学性肺炎和肺水肿。
慢性中毒:眼及上呼吸道刺激症状、神经衰弱综合征。皮肤出现粘糙、皲裂、脱皮。
理
化
性
质
熔点(℃):-94.9
沸点(℃):136.2
相对密度(水=1):0.87
相对密度(空气=1):3.66
饱和蒸气压(Kpa):1.33/25.9℃
辛醇/水分配系数的对数值 :3.15
燃烧热(KJ/mol):无资料
临界温度(℃):343.1
乙苯
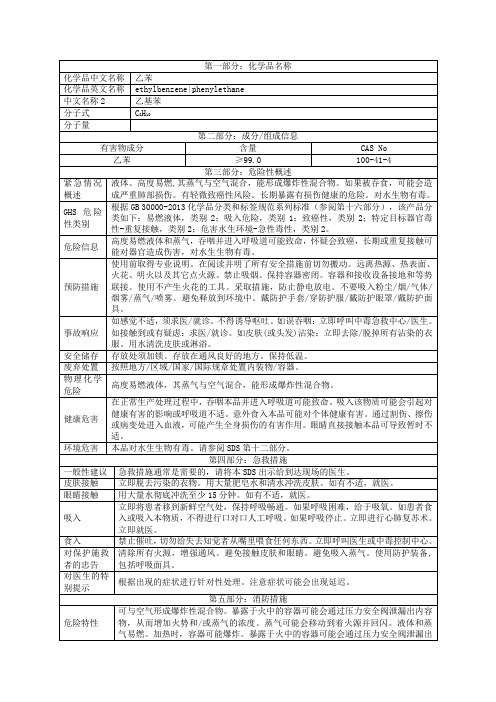
爆炸上限%(V/V)
6.7
爆炸下限%(V/V)
1
溶解性
不溶于水
易燃性
不适用
第十部分:稳定性和反应活性
稳定性
在正确的使用和存储条件下是稳定的。
不相容的物质
卤化物、氧化剂和卤素。
应避免的条件
不相容物质,热、火焰和火花。
危险反应
可与卤化物发生活性反应。
分解产物
在正常的储存和使用条件下,不会产生危险的分解产物。
第十五部分:法规信息
中国化学品管理名录
A
B
C
D
E
F
G
H
[A]《危险化学品目录(2015年版)》,安监总局2015年第5号公告;
[B]《重点环境管理危险化学品目录》,环保部办公厅2014年第33号文;
[C]《中国严格限制进出口的有毒化学品目录》,环保部2013年第85号公告
[D]《麻醉药品和精神药品品种目录(2013年版)》,食药总局2013年第230号通知;
第一部分:化学品名称
化学品中文名称
乙苯
化学品英文名称
ethylbenzene|phenylethane
中文名称2
乙基苯
分子式
C8H10
分子量
第二部分:成分/组成信息
有害物成分
含量
CAS No
乙苯
≥99.0
100-41-4
第三部分:危险性概述
紧急情况概述
液体。高度易燃,其蒸气与空气混合,能形成爆炸性混合物。如果被吞食,可能会造成严重肺部损伤。有轻微致癌性风险。长期暴露有损伤健康的危险。对水生物有毒。
皮肤和身体防护
穿阻燃防静电防护服和抗静电的防护靴。
乙苯

乙苯(1)化学品及企业标识化学品中文名乙苯;乙基苯化学品英文名 ethylbenzene;phenylethane分子式 C8H10 相对分子质量 106.18(2)成分/组成信息√纯品混合物有害物成分浓度 CAS No.乙苯 100—4l—4(3)危险性概述危险性类别第3.2类中闪点液体侵入途径吸入、食入健康危害本品对皮肤、黏膜有较强刺激性,高浓度有麻醉作用。
急性中毒:轻度中毒有头晕、头痛、恶心、呕吐、步态蹒跚、轻度意识障碍及眼和上呼吸道刺激症状。
重者发生昏迷、抽搐、血压下降及呼吸循环衰竭。
可有肝损害。
直接吸人本品液体可致化学性肺炎和肺水肿。
慢性影响:眼及上呼吸道刺激症状、神经衰弱综合征。
皮肤出现粘糙、皲裂、脱皮。
环境危害对水体、土壤和大气可造成污染。
燃爆危险易燃,其蒸气与空气混合,能形成爆炸性混合物。
(4)急救措施皮肤接触脱去污染的衣着,用肥皂水和清水彻底冲洗皮肤。
如有不适感,就医。
眼睛接触提起眼睑,用流动清水或生理盐水冲洗。
如有不适感,就医。
吸入迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
呼吸、心跳停止,立即进行心肺复苏术。
就医。
食入饮水,禁止催吐。
给服活性炭悬液。
就医。
(5)消防措施危险特性易燃,其蒸气与空气可形成爆炸性混合物,遇明火、高热或与氧化剂接触,有引起燃烧爆炸的危险。
与氧化剂接触发生猛烈反应。
流速过快,容易产生和积聚静电。
蒸气比空气重,沿地面扩散并易积存于低洼处,遇火源会着火回燃。
有害燃烧产物一氧化碳灭火方法用泡沫、干粉、二氧化碳、砂土灭火灭火注意事项及措施消防人员必须佩戴空气呼吸器、穿全身防火防毒服,在上风向灭火。
喷水冷却容器,可能的话将容器从火场移至空旷处。
容器突然发出异常声音或出现异常现象,应立即撤离。
(6)泄漏应急处理应急行动消除所有点火源。
根据液体流动和蒸气扩散的影响区域划定警戒区,无关人员从侧风、上风向撤离至安全区。
建议应急处理人员戴正压自给式呼吸器,穿防静电服,戴橡胶耐油手套。
制取乙苯的反应方程式

制取乙苯的反应方程式介绍乙苯是一种重要的有机化合物,广泛用于化工和医药等领域。
本文将探讨制取乙苯的反应方程式及其相关知识。
乙苯的性质乙苯的分子式为C6H6,是一种无色透明的液体,具有芳香气味,密度较小,熔点为5.5℃,沸点为80.1℃。
乙苯可与其他化合物发生取代反应,也可通过加氢反应制得环已烷。
制取乙苯的反应方程式要制取乙苯,一种常用的方法是通过苯甲酸和甲酸钠的缩合反应得到。
具体的反应方程式如下:苯甲酸 + 甲酸钠→ 乙苯 + CO2 + H2O该反应是一种酯化反应,通过甲酸根离子和苯甲酸的缩合得到乙苯,并产生二氧化碳和水。
这个反应通常在酸性条件下进行,常用的催化剂是稀硫酸或磷酸。
反应机理在酸性催化下,甲酸钠先与酸发生反应生成甲酸根离子,然后甲酸根离子攻击苯甲酸的羰基碳,形成中间体,再经脱羧得到乙苯。
该反应的机理如下:1.CH3COONa + H+ → CH3COOH + Na+2.CH3COOH + H+ → CH3COOH2+3.CH3COOH2+ + C6H5COOH → C6H5COOCH3 + H2O4.C6H5COOCH3 → C6H6 + CO2实验操作制取乙苯的反应需要以下实验操作:材料准备1.苯甲酸(化学纯)2.甲酸钠(好氧纯)3.稀硫酸或磷酸(催化剂)4.无水乙醇5.反应釜6.温控设备步骤1.在反应釜中加入苯甲酸和甲酸钠,按一定的摩尔比例(通常是1比1)。
2.加入稀硫酸或磷酸作为催化剂。
3.将反应釜加热至适当温度,保持一定的反应时间。
4.反应结束后,从反应釜中分离乙苯。
5.对乙苯进行精馏和纯化。
实验条件的选择与优化制取乙苯的反应条件可以根据需要进行选择与优化。
以下几个因素需要考虑:1.反应温度:反应温度的选择与催化剂相关,通常在120℃至180℃之间。
2.催化剂选择:常用的催化剂有稀硫酸和磷酸,选择合适的催化剂可以提高反应速率和产率。
3.摩尔比例:苯甲酸和甲酸钠的摩尔比例直接影响乙苯产率。
乙苯资料

乙苯相关图片编辑词条参与讨论所属分类:各种化学名称C6H5C2H5 。
存在于煤焦油和某些柴油中。
无色液体。
熔点-95℃,沸点136.2℃,相对密度0.8670(20/4℃)。
不溶于水,易溶于乙醇和乙醚。
乙苯在催化剂存在下去氢,生成苯乙烯。
工业上由苯与乙烯在催化剂,如铁的氧化物存在下反应生成,也可从石脑油重整产物的C8馏分中分离。
乙苯可用作溶剂,或加在汽油中以提高其抗爆性能。
由乙苯生成的苯乙烯是生产塑料和橡胶的重要原料。
∙•基本资料∙•理化特性∙•主要用途∙•应急处置∙•管理信息[显示全部]乙苯-基本资料英文名称:ethylbenzene别名:乙基苯。
CAS No.:100-41-4分子式:C8H10;C6H5CH2CH3。
分子量:106.16危险标记:7(易燃液体)。
包装方法:小开口钢桶;安瓿瓶外普通木箱;螺纹口玻璃瓶、铁盖压口玻璃瓶、塑料瓶或金属桶(罐)外普通木箱。
乙苯-理化特性主要成分:纯品外观与性状:无色液体,有芳香气味。
熔点(℃):-94.9沸点(℃):136.2相对密度(水=1):0.87相对蒸气密度(空气=1):3.66饱和蒸气压(kPa):1.33(25.9℃)临界温度(℃):343.1临界压力(MPa):3.70辛醇/水分配系数的对数值:3.15闪点(℃):15引燃温度(℃):432爆炸上限%(V/V):6.7爆炸下限%(V/V):1.0稳定性和反应活性:稳定。
危险特性:易燃,其蒸气与空气可形成爆炸性混合物。
遇明火、高热或与氧化剂接触,有引起燃烧爆炸的危险。
与氧化剂接触会猛烈反应。
流速过快,容易产生和积聚静电。
其蒸气比空气重,能在较低处扩散到相当远的地方,遇明火会引着回燃。
溶解性:不溶于水,可混溶于乙醇、醚等多数有机溶剂。
乙苯-主要用途用于有机合成和用作溶剂。
乙苯的摩尔质量

乙苯的摩尔质量一、引言乙苯(C8H10)是一种有机化合物,由苯环上相邻的两个氢原子被甲基基团所取代而得到。
乙苯是一种无色液体,具有独特的芳香味道,在工业上被广泛用作溶剂和原料。
乙苯的摩尔质量是指单个乙苯分子的质量,它对于化学计算和实验分析非常重要。
本文将深入探讨乙苯的摩尔质量及其相关内容。
二、乙苯的化学结构乙苯的化学式为C8H10,其分子结构由苯环和一个甲基基团组成。
苯环是由六个碳原子和六个氢原子组成的六元环,每个碳原子上还连接有一个氢原子。
甲基基团是由一个碳原子和三个氢原子组成的。
三、乙苯的分子质量计算乙苯的摩尔质量可以通过计算其分子的质量之和来得到。
根据元素周期表,碳的相对原子质量为12.01,氢的相对原子质量为1.01,因此乙苯分子的摩尔质量可以计算如下:摩尔质量= 8 × 12.01 + 10 × 1.01 = 106.17 g/mol所以乙苯的摩尔质量为106.17 g/mol。
四、乙苯的物理性质乙苯是一种无色液体,具有特殊的芳香气味。
以下是乙苯的一些物理性质:1.密度:0.88 g/mL2.沸点:136.2 °C3.熔点:-95 °C4.折射率:1.505.可溶性:乙苯可以溶于许多有机溶剂,如乙醇和乙醚。
五、乙苯的化学性质乙苯也具有一些重要的化学性质,包括以下几个方面:1.燃烧性:乙苯可以燃烧,产生二氧化碳和水。
燃烧乙苯的化学方程式为:2C8H10 + 17O2 -> 16CO2 + 10H2O。
2.亲电性:乙苯是一种亲电性较弱的化合物,通常需要通过催化剂的作用才能进行反应。
3.反应性:乙苯可以发生取代反应,其中一个或多个氢原子被其他官能团取代。
例如,乙苯可以与溴反应形成溴乙苯。
4.溶解性:乙苯是一种良好的溶剂,可以溶解许多有机化合物,如脂肪烃和芳香烃等。
六、乙苯的应用由于乙苯具有良好的溶剂性和化学稳定性,它在工业上有广泛的应用。
以下是乙苯的一些主要应用:1.溶剂:乙苯是一种常用的溶剂,特别是在涂料、油墨、胶水、塑料等行业中广泛使用。
乙苯 简介
介绍化学加工业主要涉及制造范围广泛的产品,以提高人类的生活质量。
乙苯又称苯乙烷、乙基苯,C6H5CH2CH3,是单环烷基芳香族化合物。
它几乎完全(> 90%)用作制造苯乙烯单体的中间体,C6H5CH=CH2。
苯乙烯是制造聚苯乙烯的基础材料,用于生产一次性塑料餐具和餐具、CD“珠宝”盒、烟雾探测器外壳等。
工业上使用的方法是苯与乙烯在氯化铝(AlCl3)为催化剂上的液相烷基化。
该工艺中应用的催化剂AlCl3具有很强的腐蚀性,因此需要昂贵的耐酸设备。
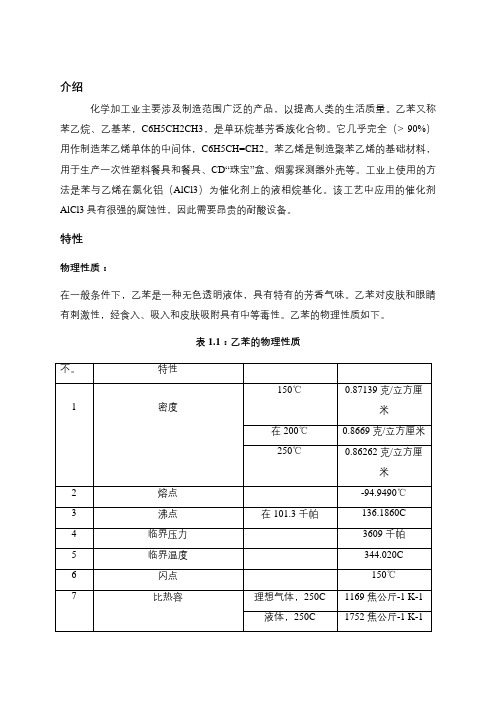
特性物理性质:在一般条件下,乙苯是一种无色透明液体,具有特有的芳香气味。
乙苯对皮肤和眼睛有刺激性,经食入、吸入和皮肤吸附具有中等毒性。
乙苯的物理性质如下。
表 1.1:乙苯的物理性质化学性质:乙苯最重要的商业反应是其脱氢生成苯乙烯。
反应在高温(600-6600℃)下进行。
通常在氧化铁催化剂上。
蒸汽用作稀释剂。
商业上,对苯乙烯的选择性范围为89% 至96%,单程转化率为 65% 至 70%。
副反应主要涉及乙苯脱烷基为苯和甲苯。
另一个具有商业重要性的反应是乙苯被空气氧化成过氧化氢,C6H5CH(OOH)CH3。
该反应在液相中进行,不需要催化剂。
然而,由于过氧化氢是不稳定的化合物,因此必须尽量减少暴露在高温下以降低分解速度。
如果在反应过程中逐渐降低温度,则副产物的产生会减少。
随后过氧化氢与丙烯在产生苯乙烯和环氧丙烷作为副产物的过程中反应。
使用合适的催化剂,乙苯可以转化为二甲苯。
异构化二甲苯的商业方法通常涉及乙苯的催化异构化或脱烷基烷基化。
与甲苯一样,乙苯可以催化或热脱烷基化为苯。
乙基苯还经历其他典型的烷基芳族化合物反应。
乙苯可以催化或热脱烷基化为苯。
乙基苯还经历其他典型的烷基芳族化合物反应。
乙苯可以催化或热脱烷基化为苯。
乙基苯还经历其他典型的烷基芳族化合物反应。
用途基本上所有商业乙苯生产都被用于制造苯乙烯单体。
苯乙烯用于生产聚苯乙烯和多种其他塑料(苯乙烯)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
乙苯
乙苯(ethylbenzene)一种芳烃。
分子式C6H5C2H5 。
存在于煤焦油和某些柴油中。
易燃,其蒸气与空气可形成爆炸性混合物。
遇明火、高热或与氧化剂接触,有引起燃烧爆炸的危险。
简介
乙苯
乙苯是一个芳香族的有机化合物,主要用途是在石油化学工业作为生产苯乙烯的中间体,所制成的苯乙烯一般被用来制备常用的塑料制品——聚苯乙烯。
尽管在原油里存在少量的乙苯,但大批量生产仍然是靠在酸催化下苯与乙烯反应。
乙苯经过催化脱氢,生成氢气和聚苯乙烯。
乙苯也存在与某些颜料中。
基本信息
中文名称:乙苯
分子式: C8H10
结构简式: C6H5-CH2-CH3
分子量: 106.16
理化特性
主要成分:纯品
外观与性状:无色液体,有芳香气味。
熔点(℃): -94.9
沸点(℃): 136.2
相对密度(水=1): 0.87
相对蒸气密度(空气=1): 3.66
饱和蒸气压(kPa): 1.33(25.9℃)
临界温度(℃): 343.1
临界压力(MPa): 3.70
辛醇/水分配系数的对数值: 3.15
闪点(℃): 15
引燃温度(℃): 432
爆炸上限%(V/V): 6.7
爆炸下限%(V/V): 1.0
溶解性:不溶于水,可混溶于乙醇、醚等多数有机溶剂。
作用
用于有机合成和用作溶剂。
应急处置
皮肤接触:脱去被污染的衣着,用肥皂水和清水彻底冲洗皮肤。
眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。
就医。
吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给予输氧。
如呼吸停止,立即进行人工呼吸。
就医。
食入:饮足量温水,催吐,就医。
呼吸系统防护:空气中浓度超标时,应该佩戴自吸过滤式防毒面罩(半面罩)。
紧急事态抢救或撤离时,应该佩戴空气呼吸器或氧气呼吸器。
眼睛防护:戴化学安全防护眼镜。
身体防护:穿防毒渗透工作服。
手防护:戴乳胶手套。
其他防护:工作现场禁止吸烟、进食和饮水。
工作毕,淋浴更衣。
保持良好的卫生习惯。
泄漏应急处理:迅速撤离泄漏污染区人员至安全区,并进行隔离,严格限制出入。
切断火源。
迅速用砂土、泥块阻断洒在地上的乙苯向四周扩散。
筑坝切断被污染的水体的流动,或用围栏限制水面乙苯的蔓延。
配戴防毒面具、手套,将漏液收集在适当容器内封存,并用砂土或其他惰性材料吸附漏液,转移到安全地带。
当乙苯洒到土壤中时,立即将被污染土壤收集起来,转移到安全地带。
对污染地带加强通风,蒸发残液,排除乙苯蒸气。
有害燃烧产物:一氧化碳、二氧化碳。
灭火方法:喷水保持火场容器冷却。
尽可能将容器从火场移至空旷处。
处在火场中的容器若已变色或从安全泄压装置中产生声音,必须马上撤离。
灭火剂:泡沫、干粉、二氧化碳、砂土;用水灭火无效。
管理信息
操作的管理:密闭操作,加强通风。
操作人员必须经过专门培训,严格遵守操作规程。
建议操作人员佩戴自吸过滤式防毒面具(半面罩),戴化学安全防护眼镜,穿防毒物渗透工作服,戴橡胶耐油手套。
远离火种、热源,工作场所严禁吸烟。
使用防爆型的通风系统和设备。
防止蒸气泄漏到工作场所空气中。
避免与氧化剂接触。
灌装时应控制流速,且有接地装置,防止静电积聚。
搬运时要轻装轻卸,防止包装及容器损坏。
配备相应品种和数量的消防器材及泄漏应急处理设备。
倒空的容器可能残留有害物。
储存的管理:储存于阴凉、通风的库房。
远离火种、热源。
库温不宜超过30℃。
保持容器密封。
应与氧化剂分开存放,切忌混储。
采用防爆型照明、通风设施。
禁止使用易产生火花的机械设备和工具。
储区应备有泄漏应急处理设备和合适的收容材料。
运输的管理:本品铁路运输时限使用钢制企业自备罐车装运,装运前需报有关部门批准。
铁路非罐装运输时应严格按照铁道部《危险货物运输规则》中的危险货物配装表进行配装。
运输时运输车辆应配备相应品种和数量的消防器材及泄漏应急处理设备。
夏季最好早晚运输。
运输时所用的槽(罐)车应有接地链,槽内可设孔隔板以减少震荡产生静电。
严禁与氧化剂、食用化学品等混装、混运。
运输途中应防曝晒、雨淋,防高温。
中途停留时应远离火种、热源、高温区。
装运该物品的车辆排气管必须配备阻火装置,禁止使用易产生火花的机械设备和工具装卸。
公路运输时要按规定路线行驶,勿在居民区和人口稠密区停留。
铁路运输时要禁止溜放。
严禁用木船、水泥船散装运输。
废弃的管理:用焚烧法处置。
毒理学资料
急性毒性:LD50:3500 mg/kg(大鼠经口);5 g/kg(兔经皮)。
亚急性和慢性毒性:动物慢性毒性表现为肝肾及睾丸轻度损害。
代谢:乙苯可经消化道、呼吸道及皮肤吸收,皮肤可吸收少量,经肠胃道虽可完成完全吸收,但实际意义不大。
吸入人体内的乙苯,有40%~60%未经转化即由呼气排出体外,经肾排出的不到2%;约40%在体内被氧化,首先转化为苯乙醇,第二步转化为酚(主要是对乙基苯酚,小量邻乙基苯酚)。
所形成的乙基苯酚与硫酸根和葡萄糖醛酸结合后排出体外,小部分乙苯直接与谷胱甘肽结合生成苯基硫醚氨酸亦由尿排出,另一小部分被积蓄在体内含脂肪较多的组织内,以缓慢的速度同样转化为上述代谢物而排出。
所以一次性吸入或接触乙苯后,大部分代谢物在2 h内被排出,少部分代谢物约在48 h后排出,在体内残留和蓄积较少;反复多次吸入时,则随蓄积量的增加,排出的时间也就更长。
乙苯在人体组织内的分布情况是:若
以血液中含量为1,则骨髓为18,腹腔脂肪中为10,心脏为15,脑组织内2.5,红细胞中的乙苯浓度比血浆中的含量大2倍。
刺激性:家兔经眼:500 mg,重度刺激。
家兔经皮开放性刺激试验:15 mg/24 h,轻度刺激。
致突变性:姊妹染色单体交换:人淋巴细胞10 mmol/L。
哺乳动物体细胞突变:小鼠淋巴细胞80 mg/L。
生殖毒性:大鼠吸入最低中毒浓度(TCL0):985 ppm(7 h,孕1~19 d),致胚胎毒性(如胚胎发育迟缓)。
家兔吸入最低中毒浓度(TCL0):99 ppm(7 h,孕1~18 d),影响每窝胎数。
环境危害:该物质对环境有危害,由于其挥发性比较大,在地表水体中的乙苯主要迁移过程是挥发和在空气中的光解,故生物富集量不多。
非生物降解性:乙苯主要通过工业废水和废气进入环境,在地表水体中的乙苯主要迁移过程是挥发和在空气中的光解。
也有可能包括生物降解和化学降解和迁移转化过程。
由于乙苯在水溶液中挥发趋势大,废水中的乙苯很快挥发至大气中,在水体中的残留也很少。
乙苯是一种易燃易爆有机物,与空气混合形成爆炸性混和物。
由于其蒸气比空气重,可沿地面扩散到相当距离外的火源点燃,并将火焰引回来。
大量乙苯泄漏进入水中时,由于比水轻,漂浮在水面,可造成鱼类和水生生物死亡,被污染水体散发出异味。
健康危害
本品对皮肤、粘膜有较强刺激性,高浓度有麻醉作用。
急性中毒:轻度中毒有头晕、头痛、恶心、呕吐、步态蹒跚、轻度意识障碍及眼和上呼吸道刺激症状。
重者发生昏迷、抽搐、血压下降及呼吸循环衰竭。
可有肝损害。
直接吸入本品液体可致化学性肺炎和肺水肿。
慢性影响:眼及上呼吸道刺激症状、神经衰弱综合征。
皮肤出现粘糙、皲裂、脱皮。
应急医疗
诊断要点:
(1)接触高浓度乙苯,首先对眼产生严重的刺激反应,如流泪、灼痛、结膜充血及水肿、角膜损伤。
(2)轻者表现头疼、眩晕、恶心、呕吐、胸闷、步态蹒跚、共济失调,重者出现昏迷、抽搐等脑水肿表现。
(3)可伴有中毒性肝病。
(4)经呼吸道吸入,可致化学性气管炎、肺炎、肺出血、肺水肿。
(5)尿中苯酰甲酸和苦杏仁酸的测定,可作为接触指标帮助诊断或鉴别诊断。
危险特性
本品易燃,具强刺激性。
易燃,其蒸气与空气可形成爆炸性混合物,遇明火、高热或与氧化剂接触,有引起燃烧爆炸的危险。
与氧化剂接触猛烈反应。
流速过快,容易产生和积聚静电。
其蒸气比空气重,能在较低处扩散到相当远的地方,遇火源会着火回燃。
制取
1.以苯和氯乙烷为原料,以三氯化铝为催化剂[1];直接反应得到乙苯。
2.以用苯和乙酰氯为原料,以三氯化铝为催化剂反应得到苯乙酮,在用Zn+浓盐酸将苯乙酮还原成乙苯,可以回避FC烷基化的低产率、分离难。
