第三章 第三节
第三章第3节光的反射知识点
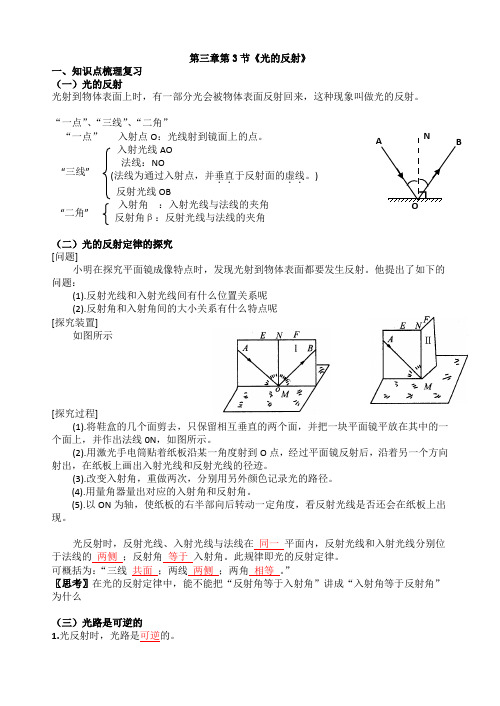
第三章第3节《光的反射》一、知识点梳理复习(一)光的反射光射到物体表面上时,有一部分光会被物体表面反射回来,这种现象叫做光的反射。
“一点”、“三线”、“二角”“一点” 入射点O :光线射到镜面上的点。
入射光线AO法线:NO (法线为通过入射点,并垂直..于反射面的虚线..。
) 反射光线OB 入射角:入射光线与法线的夹角反射角β:反射光线与法线的夹角(二)光的反射定律的探究[问题]小明在探究平面镜成像特点时,发现光射到物体表面都要发生反射。
他提出了如下的问题:(1).反射光线和入射光线间有什么位置关系呢(2).反射角和入射角间的大小关系有什么特点呢[探究装置]如图所示[探究过程](1).将鞋盒的几个面剪去,只保留相互垂直的两个面,并把一块平面镜平放在其中的一个面上,并作出法线0N ,如图所示。
(2).用激光手电筒贴着纸板沿某一角度射到O 点,经过平面镜反射后,沿着另一个方向射出,在纸板上画出入射光线和反射光线的径迹。
(3).改变入射角,重做两次,分别用另外颜色记录光的路径。
(4).用量角器量出对应的入射角和反射角。
(5).以ON 为轴,使纸板的右半部向后转动一定角度,看反射光线是否还会在纸板上出现。
光反射时,反射光线、入射光线与法线在 同一 平面内,反射光线和入射光线分别位于法线的 两侧 ;反射角 等于 入射角。
此规律即光的反射定律。
可概括为:“三线 共面 ;两线 两侧 ;两角 相等 。
”〖思考〗在光的反射定律中,能不能把“反射角等于入射角”讲成“入射角等于反射角”为什么(三)光路是可逆的1.光反射时,光路是可逆的。
“三线” “二角” AN O2.甲同学通过平面镜看到乙同学;那么,乙同学能通过平面镜看到甲同学。
(填:“能”、“不能”)(四)镜面反射与漫反射1.分类:人们根据反射面...的不同,将光的反射分为镜面反射和漫反射两类。
2.定义:平滑的表面能将平行的入射光线都沿某一相同方向反射出去,其反射光线也是平行的。
世界史上第三章第三节马克思主义的诞生和社会主义的发展

①有了科学的革命理论作指导,斗争目标更明确;
②组织程度更高、规模更大; ③日益走向国际化,从孤立分散走向国际联合,第一国际的成 返回 立即是证明。
马义的三大思想来源和三大组成部分 思想来源 来源 内容 德意志的 黑格尔辩证法 古典哲学 费尔巴哈的唯物 主义 英古典政 亚当· 斯密 治经济学 大卫· 李嘉图 劳动价值论 英法空想 社会主义 三大组成部分 马克思主义哲学 建立了辩证唯物 主义和历史唯物 主义 建立了马义政治 经济学(剩余价 值论)
A,巴黎公社起义的爆发是由于生产关 系阻碍了生产力的发展
√
B,无产阶级夺取政权的时机只在巴黎 一个城市成熟 C,巴黎公社革命具有自发性和偶然性
D,巴黎公社是建立无产阶级专政的第 一次伟大尝试
再见!
思考:
工业革命影响下,资本主义暴露了哪些弊 端?引起了哪些后果?
基本矛盾 生产资料私人占有制和
社会化大生产的矛盾 经济危机
主要矛盾
资阶和无阶矛盾
工人运动
需要注意的是,工人运动和社会主义运动是有区别的。社会 主义运动的主力虽然是工人阶级,但是社会主义运动是在马 克思主义诞生以后才产生的。
返回
国际工人运动的阶段特征:1、19世纪30、40年代以前的工人 运动主要特点:①自发性(表现为暴力斗争); ② 从破坏机 器开始; ③主要是经济斗争。 2、19世纪30、40年代的工人运动(欧洲三大工人运动): ① 工人阶级开始独自进行政治经济斗争,矛头指向资本主义制度; ②没有科学的理论作指导; ③标志着工人阶级作为一支独立的 政治力量登上历史舞台。(独立指工人阶级不再根据资产阶级 提出的纲领口号进行斗争而是提出来了本阶级独立的要求,说 明无产阶级开始了公开地反对资本主义剥削和资产阶级统治的 政治斗争。) 3、19世纪50、60年代工人运动主要特点:
第三章第三节

比苯环
对—OH 影响更大。
自 主 探 究
精 要 解 读
实 验 探 究
活页规范训练
【体验 1】下列物质既能与 NaOH 溶液反应,又能使溴水褪色 的是( )。
解析
B、C、D 均可与 NaOH 溶液反应,D 中的
可
使溴水褪色。 答案 D
自 主 探 究
精 要 解 读
实 验 探 究
活页规范训练
酯化反应的原理及基本类型
实 验 探 究
活页规范训练
醇、酚、酸分子中羟基的活性比较
醇、酚、羧酸的结构中均有—OH,由于这些—OH 所连的基团 不同,—OH 受相连基团的影响就不同。故羟基上的氢原子的 活性也就不同,表现在性质上也相差较大,其比较如下: 含羟基的物质 比较项目 羟基上氢原子 活泼性
自 主 探 究
醇
酚
羧酸
逐渐增强 ―――→ ―――
自 主 探 究 精 要 解 读 实 验 探 究 活页规范训练
【慎思 4】 甲酸是最简单的羧酸,根据甲酸的结构分析,它除 具有羧酸的通性外还应具有什么性质?
提示甲酸的结构简式为:
,它既含有羧基,又含有醛
基,因此它还应具有醛的性质,能被氧化;如发生银镜反应, 与新制 Cu(OH)2 悬浊液反应;更容易被强氧化剂氧化。
精 要 解 读
实 验 探 究
活页规范训练
在水溶液中电离
酸碱性 与Na反应 与NaOH反应 与NaHCO3反应 能否由酯水解生成
极难电离
中性 反应放出H2 不反应 不反应 能
微弱电离
很弱的酸性 反应放出H2 反应 不反应 能
部分电离
弱酸性 反应放 出H2 反应 反应放 出CO2 能
自 主 探 究
第三章第三节河流水情

二、年径流的有关概念
•
年径流量:一个年度内通过河流某断面的水量,
称为该断面以上流域的年径流量。
•
多年平均径流量:实测各年径流量的平均值,称为多年
t2
W t1 Q(t)dt Q(t2 t1)
Q W W t2 t1 t
流量历时曲线:绘制方法与水位历史曲线类似
(3)、水位-流量关系曲线
①水位与流量的关系:
河流水位的变化,从本质上看是河流流量的变化,流量增大, 水位升高;流量减小,水位降低。因此,水位变化实质上是流量 变化的外部反映和表现;另一方面,流量大小可以通过水位高低 反映出来,即二者呈某种函数关系Q=F(H),水位升高,流量增大。 即Q=F(H)呈单调递增函数。
水位面积关系曲线F=f2(H),由于面积A是随水位H的增高而增 大,H越高,A增加越快(即A相对于H的变化率越大),故曲线是 上凸下凹的。
流速曲线V=f3(H),随着水位增高,起初流速V随水位增高而 增加很快,后来流速随水位增高而增加缓慢,即流速曲线 V=f3(H)呈向上凹形。
(3)水位流量关系曲线的用途
总之,影响水位变化的因素众多复杂,水位变化 是各种影响因素综合作用的结果,因此河流水位 情势是非常复杂的。
(3)、水位变化及水位过程线
• 河流水位有年内变化和年际变化,山区冰雪融水 补给河流和感潮河段,水位日变化明显。
• 河流水位随气候的季节变化和年际变化而变化。 例如由雨水补给的河流,其水位随降雨的变化而 变化,雨季水位高,旱季水位低。由冰雪融水补 给的河流,其水位随气温的变化而变化,气温高, 冰雪融水量多,则河流水位高;气温低,冰雪融 水量少,则河流水位下降。
第三章 第三节 让改革创新成为青春远航的动力

第三章第三节让改革创新成为青春远航的动力
一、改革开放是当代中国的显著特征
改革开放是党在新的历史条件下领导人民进行新的伟大革命,是决定当代中国命运的关键抉择。
实践证明,改革开放是当代中国发展进步的活力之源
以数千年大历史观之,变革和开放总体上是中国的历史常态
商鞅变法王安石变法戊戌变法……
改革开放是当代中国最鲜明的特色
中国特色社会主义之所以具有蓬勃的生命力,就在于实行的是改革开放的社会主义创新是改革开放的生命
二、改革创新是新时代的迫切要求
创新决定未来,改革关乎国运。
创新是推动人类社会发展的第一动力
创新决定着世界政治经济力量对比的变化,也决定着各国各民族的前途命运。
创新能力是当今国际竞争新优势的集中体现
改革创新是赢得未来的必然要求
如何做?
必须把创新作为引领发展的第一动力,把人才作为支撑发展的第一资源,把创新
摆在国家发展全局的核心位置,把创新驱动发展战略作为国家重大战略,让创新
贯穿党和国家一切工作,让创新在全社会蔚然成风。
实施创新驱动发展战略,最根本的是要增强自主创新能力,最紧迫的是要破除体
制机制障碍,让改革释放创新活力,让一切创新源泉充分涌流。
三、做改革创新生力军
青年人如何做改革创新的实践者?
(一)树立改革创新的自觉意识
增强改革创新的责任感
树立敢于突破陈规的意识
树立大胆探索未知领域的信心
(二)增强改革创新的能力本领
夯实创新基础
培养创新思维
投身改革创新实践。
《高等数学》第三章第三节

(设 x 0)
x ex e Rn ( x ) x n 1 x n1 (0 1). ( n 1)! ( n 1)!
1 1 取x 1, e 1 1 2! n!
其误差
e 3 Rn . ( n 1)! ( n 1)!
思考:e –x=?
误差 Rn ( x ) f ( x ) Pn ( x )
首页 上页 返回 下页 结束
二、 Pn 和 Rn 的确定
分析:
近 似 程 度 越 来 越 好
1.若在 x0 点相交
y
y f ( x)
Pn ( x0 ) f ( x0 )
2.若有相同的切线
Pn( x0 ) f ( x0 )
(如下图)
首页 上页 返回 下页 结束
例如 取 x0=0, 当 x 很小时, e x 1 x , ln(1 x ) x
ye
y ex
x
y x
y ln(1 x )
y 1 x
o
首页 上页 返回
o
下页 结束
不足: 1、精确度不高; 2、误差不能估计.
问题: 寻找函数 P ( x ) ,使得 f ( x ) P ( x )
( n 1 )
( x)
f ( n1) ( ) Rn ( x ) ( x x0 )n1 (在x0与x之间) n 1!
f ( k ) ( x0 ) Pn ( x ) ( x x0 ) k k 0 k! 称为 按 的幂展开的 n 次近似多项式
n
f ( k ) ( x0 ) f ( x) ( x x 0 ) k Rn ( x ) k 0 k! 称为 按 的幂展开的 n 阶泰勒公式
第三章 第3节 酸碱滴定基本原理

很显然,指示剂的颜色转变依赖于比值: [In-] / [HIn]
[HIn]代表酸色的深度;
酸碱指示剂的讨论:
K HIn [In ] [H ] [HIn]
(1)KHIn / [H+] = [In-] / [HIn] [In-] / [HIn] = 1 时: 中间颜色 ≤ 1/10 时: 酸色, ≥ 10/1 时: 碱色, KHIn一定,指示剂颜色随溶液[H+] 改变而变。 指示剂变色范围:pH= pKHIn ± 1
滴定开始点pH抬高,滴定突跃范围变小。
弱酸滴定曲线的讨论:(69页图2~10)
( 1 )滴定前,弱酸在溶液中部分电离,与强酸 相比,曲线开始点提高; (2)滴定开始时,溶液pH升高较快,这是由于 中和反应生成的酸根离子(Ac-)产生同离子效应, 使弱酸(HAc)更难离 解,[H+]降低较快; (3)继续滴加NaOH, 溶液形成缓冲体系,曲 线变化平缓; (4)接近化学计量点 时,溶液中剩余的HAc已 很少,pH变化加快。
1.酸碱滴定曲线的计算
(1) 强碱滴定强酸
例:0.1000 mol/L NaOH 溶液滴定 20.00 ml 0.1000 mol/L HCl溶液。
a. 滴定前
加入滴定剂(NaOH)体积为 0.00 ml时: 0.1000 mol/L 盐酸溶液的pH=1
(1) 强碱滴定强酸
b.滴定中 加入滴定剂体积为 18.00 ml时:
pKb= 14- pKa = 14-4.74 = 9.26 [OH-] = (cb Kb )1/2 = (5.0010-2 10-9.26 )1/2 = 5.2410-6 mol/L 溶液 pOH = 5.28 pH = 14-5.28 = 8.72
第三章第三节存货的核算

优点:有利于企业加强对存货的管理;有利于成本计算的真实 性
(二)永续盘存制
期末实地盘点的结果
本
本
核
期
期
期
期
对
末
初
购
发
= + - 存
存
入
出
货
货
存
存
数
数
货
货
量
量
数
数
量
量
平时在账面记录中反映
(二) 存货清查的核算
1.存货清查的概念及原因 (1)存货清查的概念
公司2019年3月5日出售商品一批,该批 商品售价50 000元,相应的增值税销项 税额8 500元,购货方尚未支付货款。该 批商品的成本为40 000元。
借:应收账款
58 500
贷:主营业务收入
50 000
应交税费——应交增值税(销项税额) 8 500
借:主营业务成本
40 000
贷:库存商品
40 000
A.财务费用
B.营业外支出
C.资产减值损失
1
2
3
4
材料入库和付款时间不一致的情况
货款已付 材料同时 验收入库
货款已付 货款未付
材料尚未 材料已经 验收入库 验收入库
预付款项 购货
例1.正保大酒店3月发生以下业务:
① 从市第一粮店购进大米500斤,单价 1.80元,金额900元,货款尚未支付,大米
已验收入库。
借:原材料
900
贷:应付账款——市第一粮店 900
小规模纳税人实行简易办法计算并缴纳增值税。小 规模纳税人征收率为3%。购进货物所含的税金不得抵扣, 应当按照规定计入相关成本。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第三节用途广泛的金属材料学习目标核心素养建构1.了解合金的含义及特性。
2.认识常见合金的重要应用。
3.认识如何正确选用合金材料及合理使用金属材料的意义。
[知识梳理]一、常见合金的重要应用1.合金(1)定义:由两种或两种以上的金属与金属(或非金属)熔合而成的具有金属特性的物质。
(2)性质:合金具有许多优良的物理、化学或机械性能,在许多方面不同于各成分金属。
①硬度:合金的硬度一般大于成分金属。
②熔点:合金的熔点多数低于成分金属。
2.常见的合金(1)铜合金(2)钢【自主思考】1.合金一定是多种金属的混合物吗?碳素钢和纯铁,哪种物质的熔点高?提示不一定。
①合金也可能含有非金属。
②合金不是多种金属的简单混合,它是由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质。
碳素钢属于合金,其熔点低于纯铁,故纯铁熔点高。
二、正确选用金属材料1.分类金属材料⎩⎪⎨⎪⎧按组成分⎩⎨⎧①纯金属②合金按性能特点分⎩⎨⎧①黑色金属:包括铁、铬、锰以及它们的合金②有色金属:除黑色金属以外的其他金属及 合金2.金属材料的正确选用 选择金属材料时,一般考虑的主要因素是:①主要用途;②外观;③物理性质;④化学性质;⑤价格;⑥加工难度;⑦日常维护;⑧对环境的影响等等。
【自主思考】2.列举生活中的合金材料,并简述选择该材料时利用了该合金的哪些优异性能?而金属制品在使用的过程中会被腐蚀或损坏,对于废旧金属,我们应如何处理才好呢?提示 ①铝合金门窗:质轻、耐腐蚀;②黄金首饰:贵重、色泽艳丽;③易拉罐:质轻、易回收利用。
废旧金属虽是一种固体废弃物,处理不当,会污染环境,对于我们来说,应把废旧金属作为一种资源加以回收利用,变废为宝,既可以防止污染,又可以缓解资源短缺的矛盾。
[效 果 自 测]1.判断正误,正确的打“√”,错误的打“×”。
(1)合金一定是不同金属熔合而成的具有金属特性的化合物。
( )(2)生铁的熔点比铁低,但机械强度和硬度比铁高。
( )(3)青铜比纯铜的硬度低。
( )(4)生铁中的铁与纯铁的化学性质不同。
( )(5)金与黄铜的颜色很相近,可以用稀H 2SO 4鉴别。
( )(6)对于废旧金属,我们应该加以回收利用。
( )答案 (1)× (2)√ (3)× (4)× (5)√ (6)√2.联合国卫生组织认为我国的铁锅是一种理想的炊具而向世界推广。
其主要原因是()A.升热慢,退热也慢,保温效果好B.烹饪的食物中含有丰富的“铁质”C.生产过程简单,价格便宜D.生铁中含有碳元素,因而含有对人体有益的有机物答案 B3.下列关于合金的叙述中正确的是()A.合金是由两种或多种金属熔合而成的B.日常生活中用到的五角硬币属于铜合金C.合金在任何情况下都比单一金属性能优良D.钢不属于合金解析合金是金属与金属或金属与非金属熔合而成的,A项错误;在机械加工时,合金的性能一般较单一金属优良,但并不是任何情况下都是,如纯铝导电性比铝合金要强,C项错误;钢是铁碳合金,D项错误。
答案 B4.请用连线把Ⅰ、Ⅱ中对应的两项连在一起:Ⅰ项Ⅱ项质量组成75% Au,12.5% Ag,12.5% Cu 黄铜装饰用的“金粉”、“金箔”18K白金司母戊方鼎合金钢人造骨18K黄金质量组成75% Au,3.5% Cu,16.5% Ni,5% Zn 青铜家用不锈钢餐具钛合金答案探究一、合金的组成、性质及作用【探究讨论】1.合金的性质是各成分金属的性质之和吗?提示合金具有许多优良的物理、化学性质和机械性能,在物理性质、机械性能方面优于各成分金属,不是简单地加合;但一般认为在化学性质上,合金体现的是各成分金属的化学性质。
2.已知铜的熔点为1 083 ℃,钠的沸点为883 ℃,试问铜与钠能否形成合金?提示不能。
当铜开始熔化时,钠已经气化,所以二者不能形成合金。
【点拨提升】1.合金的组成及性质(1)合金中一定含有金属元素,可能含有非金属元素。
(2)合金是混合物,没有固定的熔点。
(3)合金具有金属特性,如导电、传热等。
(4)合金形成后会影响各成分金属的物理性质,如合金的熔点一般比成分金属低,而硬度、机械强度一般比成分金属高;但一般来说各成分金属均保持了其原有的化学性质。
2.合金的形成条件(1)金属与金属形成合金时:合金是金属在熔化状态时相互混合形成的,熔化时的温度需达到成分金属中熔点最高的金属的熔点,但又不能超出成分金属中沸点最低的金属的沸点。
一种金属的熔点高于另一种金属的沸点时则不能形成合金。
(2)金属与非金属形成合金时:部分不活泼非金属与金属可形成合金,活泼非金属与活泼金属则不能形成合金。
【典题例证1】下列关于合金的说法错误的是()A.合金是由两种或两种以上的金属或金属与非金属熔合而成的具有金属特性的物质B.镁铝合金的熔点比镁和铝都高C.在合金中加入适量的稀土金属能大大改善合金的性能D.青铜、硬铝、钢都是合金解析合金是由两种或两种以上的金属或金属与非金属熔合而成的具有金属特性的物质,故A正确;镁铝合金的熔点比镁和铝都低,故B错误;在合金中加入适量稀土金属或稀土金属的化合物,就能大大改善合金的性能,故C正确;青铜、硬铝、钢都是由两种或两种以上的金属(或金属与非金属)熔合在一起形成的具有金属特性的物质,属于合金,故D正确。
答案 B【学以致用1】合金相对于纯金属制成的金属材料来说优点是()①合金的硬度一般比它的各成分金属的大②一般合金的熔点比它的各成分金属的更低③改变原料的配比,改变生成合金的条件,可得到具有不同性能的合金④合金比纯金属的导电性更强⑤合金比纯金属的应用范围更广泛A.①②③⑤B.②③④C.①②④D.①②④⑤解析合金具有许多优良的物理、化学或机械性能,在许多方面优于各成分金属。
例如,合金的硬度一般比其各成分金属的硬度大,多数合金的熔点比其各成分金属的熔点低,但合金的导电性比纯金属弱。
答案 A探究二、正确使用金属材料【探究讨论】1.为什么航空业上铝合金比铁合金用途更广泛?提示①铝合金比铁合金要轻,易于用于航空业;②铝合金表面易形成致密的氧化膜,此氧化膜耐高温、防腐蚀,而铁合金的氧化膜易脱落,起不到防腐蚀的作用。
2.钛被称为“21世纪金属”,其合金大规模应用于航天航空,利用的是合金的哪些优点?提示钛合金耐高温、耐腐蚀、高强度、密度小。
【点拨提升】1.选择材料应注意的问题某种金属能不能成为一种应用广泛的材料主要取决于该金属的储量、冶炼成本、市场价格以及所具有的性能和是否易于加工等。
选择金属材料时,除了要考虑金属的用途、外观和价格外,还要考虑金属的物理性质和化学性质。
(1)物理性质:密度、硬度、强度、导电性和导热性等,这些性质决定金属材料的加工难易程度。
(2)化学性质:对水的作用、耐腐蚀性等,这些性质决定金属材料的日常维护和环境对其的影响。
2.金属的回收和资源保护(1)废旧金属的最好处理方法是回收利用。
(2)回收利用废旧金属的意义是减少垃圾量,防止污染环境且缓解资源短缺的矛盾。
【典题例证2】钛和钛的合金被誉为“21世纪最有发展前景的金属材料”,它们具有很多优良的性能,如熔点高、密度小、可塑性好、易于加工,尤其是钛合金与人体器官具有很好的“生物相容性”。
根据它们的主要性能,下列用途不切合实际的是()A.用来作保险丝B.用于制造航天飞机C.用来制造人造骨D.用于家庭装修,作钛合金装饰门解析钛和钛的合金密度小,可塑性好,因此可用于航天领域,B正确;由于钛和钛合金与人体器官具有很好的“生物相容性”,可与人体的组织相容,不引起排异反应,因此可以用来制造人造骨,C正确;由于其密度小、可塑性好、易于加工,因此可用于家庭装修,作钛合金装饰门,D正确;由于其熔点高,不适合作保险丝,A错误。
答案 A【学以致用2】钢材可以用作桥梁的结构材料,是因为它()A.有良好的导热性B.有一定的机械强度C.不易受空气和水的作用D.有良好的导电性解析钢材被大量应用于桥梁的结构材料说明它具有很强的机械强度而不是利用其导电、导热性。
答案 B1.我国人民早在商代就已掌握青铜(铜、锡、铅合金)冶铸技术。
在商代首都——河南安阳,曾经发现多处炼铜遗址和大量青铜器件,其中有一件司母戊鼎,高133 cm、长110 cm、宽78 cm、重875 kg,是迄今被发现的我国古代青铜器中最壮观的一件珍品。
下列有关说法不正确的是()A.铜是人类历史上使用最早的金属材料B.青铜合金具有比铜单质更好的机械性能C.青铜不易生锈是因为铜的性质不活泼D.铜被最早使用是因为铜的性质不活泼,易冶炼解析铜的化学性质不活泼,易冶炼,是最早被使用的金属,故A、D项正确;合金比纯金属具有更优良的物理、化学和机械性能,青铜比铜单质的机械性能好,且提高了其耐腐蚀性能,故B项正确、C项错误。
答案 C2.只含有下列成分的物质一定不是合金的是()A.Fe、C B.Cu、ZnC.Al、Cu D.C、Si解析合金必须要含有金属,是两种或两种以上的金属(或金属跟非金属)熔合在一起所形成的具有金属特性的物质。
答案 D3.选用金属材料时,以下方面需要考虑的是()①主要用途②物理性质、化学性质③价格④加工难度⑤日常维护⑥对环境的影响A.①②③B.③④⑤C.①⑤⑥D.①②③④⑤⑥解析在选用材料时要综合考虑所选材料的性能、价格、加工难度、日常维护、对环境的影响等因素,从众多材料中选取合适者。
答案 D4.历史上金、银、铜主要是作为货币金属或装饰品被应用。
(1)金、银、铜常被作为钱币流通,从化学角度来看,主要是利用它们的________。
A.硬度适中B.密度适中C.在自然界里都可得到纯净的单质D.不活泼性(2)一位收藏者有一枚表面是黑色,且有少量绿色锈状物的铜币,黑色物质是________,绿色物质是________,这枚金属币的真面目为________色。
解析(1)金、银、铜都属于不活泼金属,易加工,因此,在历史上都曾经用作货币。
(2)铜稳定性略微差一些,容易与氧气等物质反应而“生锈”。
答案(1)D(2)CuO Cu2(OH)2CO3红课时作业基础巩固1.目前世界上用量最大、用途最广的合金是()A.铝合金B.青铜C.钢铁D.塑钢解析目前世界上用量最大、用途最广的合金是铁合金,即钢铁。
答案 C2.下列关于合金的叙述正确的是()A.大多数合金的熔点比它的各成分金属的高B.生铁和钢都是铁的合金,生铁的含碳量低于钢C.日常生活中使用更多的是纯金属而不是合金D.青铜是我国使用最早的合金解析合金的熔点比它的各成分金属的熔点低,A项错误;生铁的含碳量高于钢,B项错误;日常生活中使用更多的是合金,C项错误;铜的化学性质不活泼,易冶炼,青铜是我国最早使用的合金,D项正确。
答案 D3.铝硅合金(Si的质量分数为13.5%)在凝固时收缩率很小,因而这种合金适合铸造。
