11第十一章醛、酮和醌10
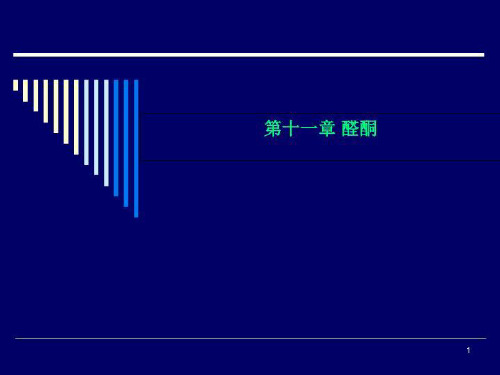
第十一章 醛酮
O CH3 C CH2CHCH3
CH3
4 _ 甲 基 _ 2 _ 戊 酮
CH3COCHCO3CH
CH2CH=CH2
3_烯丙基_2,4 _戊二酮
O
= CH3 C CH C CH3
CH3
4 _ 甲 基 _ 3 _ 戊 烯 _ 2 _ 酮
O C CH CH3
CH3
2 _ 甲 基 _ 1 _ 环 己 基 _ 1 _ 丙 酮
8
O
CH3
C CH=C CH3
CH3
CH3
3 _ 甲 基 _ 1 _ 2 ' , 4 ' _ 二 甲 基 苯 基 _ 2 _ 丁 烯 _ 1 _ 酮
练习: 写出下列化合物的名称或结构式:
(1). H= C CCH 2CC = H CH HCH (2)O . C3HCC2HCC3H
C3H
OO
=
=
= =
R C OH M 3 O +R C g O X 3 ° 醇 H
R
RR ' '
RR ' '
例:选择适当的原料合成2-甲基-2-戊醇。
24
4、与醇的加成反应
R H CO+
( R' )
无水HCR l OH
R''OH
C
H OR''
( R' )
R''OH R C OR''+H2O 干HCH l OR''
( R' )
OH
(C3H)2CC2H NH 2
OH
20
2、与饱和亚硫酸氢钠的加成反应
醇 钠 O C O+NaO-S-OH C ONa
有机化学醛酮和醌H

甲基环戊基甲酮
乙酸环戊酯
酮分子中α-碳碳键断键的优先顺序:
R3C- > R2CH-,C5-6环烷基 > Ph- > PhCH2- > RCH2- > CH3-
2.2 还原反应 2.2.1 催化氢化
CH3CH=CHCH2CHO H2/Ni T,P CH3(CH2)3CH2OH
3-戊烯醛
1-戊醇
反应物分子中的C=C、C=O双键均被还原。
无α-H的醛
甲醛
甲酸钠
苄醇
3、α-H的反应
醛、酮分子中α -H原子具有酸性,原因是羰基的
极化作用,使生成的共轭碱变得相对稳定(负电荷被
离域化)。事实上,这种转化是以烯醇负离子的形式 为纽带的。
O RCH
-H+
C H( or CH3)
H+ -H+
烯醇负离子
H+
α
RCH2
O C H( or CH3)
水会分解,故需在干醚或四氢呋喃中使用。
2.2.3 异丙醇铝-异丙醇还原法
异丙醇铝
CH3CH=CHCH2CHO + i-PrOH Al(PrO-i)3 CH3CH=CHCH2CH2OH + (CH3)2CO
3-戊烯醛
异丙醇
3-戊烯-1-醇
丙酮
反应物分子中的C=O双键被还原。 该反应又称为麦尔外因-庞道夫-维尔莱 (Meerwain-Ponudorf-Verley)还原法。其逆反应 称为欧芬脑尔(Oppenauer)反应。
使用挥发性的剧毒物HCN。例如:
PhCHO NaHSO3 PhCHSO3Na OH NaCN H2O PhCHCN OH HCl
回流
CH11醛酮和醌
δ δ +
δ + δ
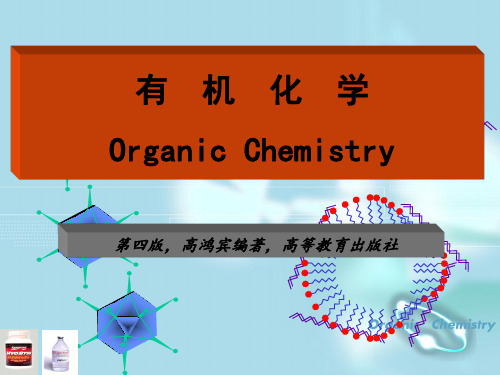
R M g X + CO
RCO M g X H 2ORCO H
与甲醛加成形成伯醇; 与其他醛加成形成仲醇; 与酮加 成形成叔醇。
RMgX
H H CO
H R CH OMgX H2O RCH2OH
R1MgX
H R2 C O
R2
R2
R1 CH OMgX H2O R1 CH OH
R1MgX
R3 R2 C O
R3
R3
R1 C OMgX H2O R1 C OH
R2
R2
b. 与铜锂试剂反应:制备空间位阻大的叔醇。
O
( CH3 )3C C C(CH 3 )3 + (CH 3)3CLi
ROR -70oC
((CH 3) 3C) 3COH
c. 与炔钠反应:
O
① H CC N -a + ② H 2 O ; H+
出版社, 1993.
3. F A Carey. Organic Chemistry, 4th ed. New York:
McGraw – Hill Companies Inc, 2000.
4. T W G Solomons, C B Fryhle. Organic Chemistry, 7th ed.
C H C 3 H C 2 H C 2 H C 2 H O 正戊醛
C H3(C H2)10 C H O 正十二醛(月桂醛)
C H C 3 H C H C 2 H O C H 3 异戊醛
单酮:二“某基”酮 脂肪混酮:小基团在前,大基团在后,“某基某基酮”
C H C H 3 C O 2 C H C H 2 3C H C O 3 C H C H 2 3C H C O 3 C H C H 2 C H 2 3
醛、酮、醌
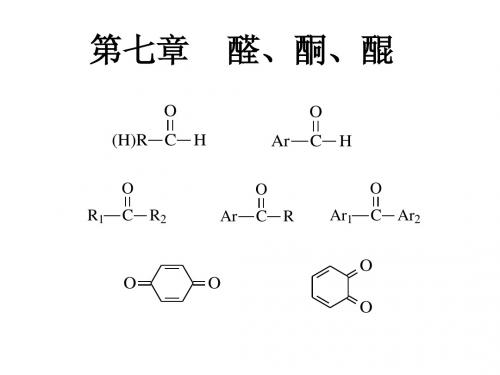
无水HCl
R C
OH OR'
R'OH
无水HCl
R C H
OR' OR'
半缩醛
缩醛
醛与醇生成半缩醛、缩醛的反应是按下列历程进行的:
R H C O H
+
R H
R C O H
Ⅰ
+ +
H
C OH
+
.. R'OH
R C H
OH
+ .OR' .
H
Ⅱ
-H
+
R C H
OH OR'
H O C CHOH CHOH CHOH .. CH2 OH
分子内的六员环状半缩醛
H
OH C CHOH CHOH O CHOH CH2
4. 与格氏试剂的加成反应
格氏试剂是较强的亲核试剂,非常容易与醛、酮 进行加成反应,加成的产物不必分离便可直接水解生 成相应的醇,是制备醇的最重要的方法之一。
无水 乙 醚 R C O MgX H2O H
+
C O + RMgX
R C
OH
+ Mg(OH)X
甲醛与格氏试剂加成产物水解后可以得到比格氏试剂 分子中的烃基多一个碳原子的伯醇;其它醛与格氏试剂 加成后,水解的最终产物是仲醇;酮与格氏试剂加成后, 水解的最终产物是叔醇。
H C O + R MgX H
无水乙醚
H R C OMgX H H2O H
+
HCl OH R C SO3Na R Na2CO3 (CH3)H C O + Na2SO3 + NaHCO3 H(CH3) R C O (CH3)H + NaCl + SO2 + H2O
有机化学(第四版)习题解答

高鸿宾(主编)有机化学(第四版)习题解答化学科学学院罗尧晶编写高鸿宾主编《有机化学》(第四版)作业与练习第二章饱和烃:烷烃和环烷烃练习(P60—62):(一的1,3,5,7,9,11小题)、(五)、(六)、(十三)第三章不饱和烃:烯烃和炔烃作业:(P112—117):(二)、(四)、(七)、(十一)、(十五的2,3小题)、(十六的2~5小题)、(二十一)第四章二烯烃共轭体系练习:(P147—149):(三)、(十)、(十一)、(十三)第五章芳烃芳香性作业:(P198—202):(二)、(三)、(九)、(十)、(十六)、(十七)、(十八的2、5~10小题)、(二十四)第六章立体化学练习:(P229—230):(五)、(六)、(七)、(十二)第七章卤代烃作业:(P263);(P290-295):(P263):(习题7.17)、(习题7.18)、(习题7.19)。
(P290-295):(六)、(七)、(八)、(十的1、2、5小题)、(十三的1、2小题)、(十四的1、2小题)第九章醇和酚作业:(P360—362):(二)、(三的2、4小题)、(五)、(九的1、3小题)第十一章醛、酮和醌作业:(P419—421):(一)、(三)、(七题的1—9小题)、(十三)、(十四)第十二章羧酸练习:(P443—444):(一)、(三)、(五)、(七)第十三章羧酸衍生物练习:(P461—464):(一)、(四)、(六)、(七)(八题的1、3小题)、第十四章β-二羰基化合物作业:(P478—480):(一)、(五)、(七)第十五章有机含氮化合物作业:(P526—530):(三)、(四)、(八)、(十一)第二章 烷烃和环烷烃 习题解答(一)题答案:(1) 3-甲基-3-乙基庚烷 (2)2,3 -二甲基-3-乙基戊烷 (3)2,5-二甲基-3,4 -二乙基己烷 (4)1,1-二甲基-4-异丙基环癸烷 (5)乙基环丙烷 (6)2-环丙基丁烷 (7)1,5-二甲基-8-异丙基二环[4.4.0]癸烷(8)2-甲基螺[3.5]壬烷 (9)5-异丁基螺[2.4]庚烷 (10)新戊基 (11)2′-甲基环丙基 (12)1′-甲基正戊基(四)题答案:(1)的透视式: (2)的透视式: (3)的透视式:Cl HCH 3H 3C ClHCH 3CH 3ClHHCH 3Cl ClCH 3H H(4)的投影式: (5)的投影式:BrBr CH 3HH H 3CBrBr CH 3CH 3HH(五)题解答:都是CH 3-CFCl 2的三种不同构象式; 对应的投影式依次分别如下:ClClClClClClFFFHH H H H H H H ( )( )( )123验证如下:把投影式(1)的甲基固定原有构象位置不变,将C-C 键按顺时针方向分别旋转前面第一碳0°、60°、120°、180°、240°得相应投影式如下:ClCl ClClClClClCl ClFF FF F H HH H H HHH H H H H HH H ( )( )( )( )( )ab c de各投影式对应的能量曲线位置如下:由于(a )、(c )、(e )则为(1)、(2)、(3)的构象,而从能量曲线上,其对应能量位置是一样的,所以前面三个透视式只是CH 3-CFCl 2的三种不同构象式。
大学有机化学第11章__醛和酮

O C CH3
苯乙酮
(乙酰苯)
共九十一页
2)系统(xìtǒng)命名 法
O
5
CH3
CH3CH2-C-CH2-CH-CH2CH3
CH3-CH-CH2CH2CHO
HO-CH-CH3
6
4-甲基戊醛
5-乙基-6-羟基 3-庚酮
- (qiǎngjī)
共九十一页
C H 3
C H O
C H 2 C H 2 C H C H O O H C C H 2 C H C H 2 C H O
共九十一页
加成-消除(xiāochú)历程
R’
R—C=O + H2N—G
H+
R’ R-C — N—G
H+ -H2O
R’ R-C=N—G
OH H
(N-取代(qǔdài)亚胺)
这种加成-消除实际上可以看成由分子间脱去一分子水:
R’
R—C=O + H2 N—G
R’ R-C=N—G + H2O
共九十一页
加成-缩合产物(chǎnwù)的结构及名称:
加成-缩合产物的结构(jiégòu)及名称:
R’ R—C=O +
R’
H2N—R H2N—OH
R—C = N-R Schiff base R’
R—C = N-OH 肟(oxime)
H2N—NH2 H2N—NH-
O
R’
R—C=N-NH2 腙(hydrazone) R’
R-C=N-NH-C6H5 苯腙
H2N—NH-C-NH2
R’
R-C=N-NH-CO-NH2 缩氨脲
共九十一页
6) 与格氏试剂加成
有机化学第十一章
羰基化合物的活性次序(电子效应和空间效应): 羰基化合物的活性次序(电子效应和空间效应):
HCHO > CH3CHO > ArCHO > CH3COCH3 > CH3COR> CH3COAr > RCOR' > ArCOAr'
O 2N CHO > CHO
>
H 3C
CHO
1、与HCN的加成 、 的加成
维纶
4、与金属有机试剂的加成 、
(1)格氏试剂 )格氏试剂: H2CO +
MgCl 无水 乙醚
CH2OH 64-96%
H2O CH2OMgCl H SO 2 4
CH3 无水 乙醚 CH3COPh + PhCH2MgCl PhCH2 C OMgCl Ph CH3 H2O PhCH2 C OH NH4Cl Ph 92% Grignard: 1912 Nobel Prize
异 丙 醇 铝 ,丙 酮 丙 苯,回流
80%
CHCH CCH CH2 CH3
CH3 C CH CHCH CCH CH2 CH3 O
Oppenauer氧化: 异丙醇铝是催化剂 反应中双键不受影响。 氧化: 异丙醇铝是催化剂, 反应中双键不受影响。 氧化
脱氢:醇在适当的催化剂条件下脱去一分子氢 生成醛酮。 脱氢:醇在适当的催化剂条件下脱去一分子氢,生成醛酮。
CH3OH 浓H2SO4
COOCH3
CH2 C COOCH3 CH3 90%
过氧化苯甲酰
CH2 C CH3
n
甲基丙烯酸甲酯
聚甲基丙烯酸甲酯 (有机玻璃) 有机玻璃)
2、与NaHSO3的加成 、
加成生成a-羟基磺酸钠 羟基磺酸钠: 醛和甲基酮与饱和的NaHSO3加成生成 羟基磺酸钠: 醛和甲基酮与饱和的
有机化学作业答案10-10
第2章 烷烃1.解:(1)2,3,5,5-四甲基庚烷;(3)2,6-二甲基-4-乙基庚烷;(5)3-甲基-4-乙基庚烷2.解:(1)CH 3CCH 3 ; (3) CH 3CH 2CH 2CHCH 2CH 2CH 3; (5) CH 3CCH 2CHCH 3CH 333)3CH 3CH 3CH 33.解:最稳定构象 最不稳定构象 5.解:(2)(b)>(d)>(e)>(a)>(c)6.解:按稳定性由大到小排列有:(3)>(2)> (1)。
第3章 烯烃和二烯烃1.解:(2) (E)-2-溴-2-戊烯; (4) 4-甲基-3-乙基-1-戊烯;(6) (Z)-3,6,6-三甲基-4-异丙基-3-庚烯 2.解:(1) CH 3C=CH 2;(4) C=CCH 3CH 3CH 3CH 2HCH 2CH 2CH 34.解:(1) CH 3CCH 3;CH 3CHCH 2Br; (2) CH 2CH 2CHCH 2Cl; (3) CH 3CH 2CH 2CH 2OH; (4) CCl 3CH 2CH 2I (反马氏规则产物)CH 3Br CH 3OH(5) CH 3CH 2COOH; (6)CH 3CHCH=CH 2; CH 3CH CH CH 2Cl Cl5.解:(1) ; (2) H 2/Lindlar 催化剂;H 2/Ni; (3)BrBr +BrBr(4)由于中间体,有4种形式:CH 3CCH=CH 2 CH 2=CCHCH 3 CH 3C=CHCH 2 CH 2C=CHCH 3CH 3CH 3++CH 3+CH 3+(A) (B) (C) (D)稳定性,不好评价。
故此有4种产物。
CH 3CCH=CH 2 CH 2=CCHCH 3 CH 3C=CHCH 2 CH 2C=CHCH 3CH 3CH 3CH 3CH 3(A) (B) (C) (D)Br Br Br Br(5)由于中间体,有2种形式:CH 3CH=CHCHCH 2CH 3 CH 2CHCH=CHCH 2CH 3++稳定性,不好评价。
醛、酮
C6H5 । H2C=CH–CHCHCHCHO । । OH Br 3-苯基-4-羟基-2-溴-5-己烯醛
第二节 醛、酮的物理性质
一.物态:C1 g ; C2 ~ C12 脂肪醛、酮 l ; 高级脂肪醛、酮和芳香醛、酮 s 。
二.水溶性:1.C4 ↙的脂肪醛、酮易溶于水。 2.C ↗,水溶性 ↙。易溶于极性溶剂中。
R R O –CH2 \ HO–CH2 H⁺ \ / C=O + ׀ C → / HO–CH2 / \ R R O –CH2
(缩酮)
缩醛具有双醚结构,对碱和氧化剂稳定,但 遇酸迅速水解为原来的醛和醇 O OR' H2O/H+ R-C-H + 2R'OH R-CH-OR'
ÀÀ ÀÀÀÀÀÀÀÀ ¨
4 3 2 1
O CH3 CH3 C CH2 CH CH3
1
2 3 4
5
3-甲基丁醛(b-甲基丁醛)
4-甲基-2-戊酮
CH3CH=CH-CHO
4 3 2 1
CH=CH-CHO
3 2 1
2-丁烯醛
3-苯基丙烯醛 3-甲基-2,5-己二酮
O O CH3 –C-CH-CH2-C-CH3 1 4 5 6 2 3 CH3
² ÀÀÀ
N-OH + H2O
² ÀÀÀÀ
O2N CH3CHO + NH2 -NH-
NO2
O2N CH3CH=NH -NHÀÀ-2,4-ÀÀÀ±À À ù Àê
NO2 + H2O
O CHO + H2N-NH-C-NH2
À³ ±ÀÀ
O CH=N -NH-C-NH2 + H2O
À³ ±ÀÀÀ°À ±
有机化学 第十一章 醛酮
王鹏
山东科技大学 化学与环境工程学院
• d). 制备β-羟基酸酯的Reformatsky反应:
C O + X C H2COO C2H5
Zn
OZn X C C H2COO C2H5
+
OH C C H2COO C2H5
H
• 反应先是a-卤代酸酯和锌反应生成中间体有机锌试 剂,随后的反应与格氏试剂反应相似
δ R δ+ M gX
+
δ+ C
δ O
R
C
O M gX
H 2O
R
C
OH
• 反应的实质是负电性部分与羰基碳连接,正电性部 分与氧原子结合并被氢取代
王鹏
山东科技大学 化学与环境工程学院
11.6.1 醛和酮的亲核加成
• b). 与有机锂试剂反应:制备空间位阻大的叔醇
O ( C H 3) 3 C C C ( C H 3) 3 + ( C H 3) 3 C L i
硬脂酸钴 ~130℃
C
CH3
• 该类反应的关键在于控制氧化剂的氧化强度,使其 停留在醛酮阶段
王鹏
山东科技大学 化学与环境工程学院
11.3 醛酮的制备
二、伯醇和仲醇的氧化
醇的氧化是制备醛酮的常用方法
(C H 3 ) 3 C C H 2 O H
K 2C r2O 7 H 2S O 4
△
(C H 3 ) 3 C C H O(80%)
δ
C
H Nu
O
H
反应是负电性的Nu-首先进攻羰基碳中心,得 到加成后的氧负离子之后与正电性的氢结合
王鹏
山东科技大学 化学与环境工程学院
11.6.1 醛和酮的亲核加成
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
C u
C H 3 C H 2 O H ~ 2 8 0 ℃ C H 3 C H O +H 2
OH
Cu,3。 00 C
O
CH3-CH-3CH(or ZnO,。 38)0 CCH3-C-3C
产品纯度高,吸热反应。通入一定量
的空气,生成的氢气和空气中的氧气结合 成水,生成热直接供给脱氢反应,称氧化 脱氢法。
O H
Oppenauer氧化
CH3CHCH=CHCH=2CC丙 苯 H=酮 , C, H回异 流丙 ,醇 80C铝 %H3C-CH=CHCH=2CC
OH
CH3
O
CH3
特点:C = C不被氧化
RC1。 H醇 2OH
[O] RCHO [O]
醛
RCOOH
酸
OHБайду номын сангаасR-2。 C醇H-R'¡ [O]
及时蒸出
O R-C-R'¡
(2) 羰基合成
烯烃与一氧化碳和氢气在催化剂作用下, 生成比原烯烃多一个碳原子的醛。
C H 3 C H C H 2 + C O + H 2 C o 1 ( C 6 0 O ℃ ) 6 , [ P ~ ( n 6 – C M 4 H P a 9 ) 3 ] 2
C H 3C H 2C H 2C H O+C H 3C H C H O
(2)亲电和亲核反应活性:
δ
δ
CO
取代基。
O
H3C
CHO
CH3
4–甲基环己酮
3–甲基环己基甲醛
•醛酮化合物:醛为母体,酮的羰基氧原 字作取代基,用词头“氧代”表示。
C H3 C H2 C O C H2 C H O 3-氧代戊醛 O C H O 2-氧代环己基甲醛
•碳原子位次有时也用希腊字母表示。与 羰基碳原子直接相连的碳原子为α-碳原 子,其次为β -碳原子,γ -碳原子等。
O
CH3CH2CH2CHCH2CHCH2CH CH3 C2H5
5–甲基–3–乙基辛醛
(3-ethyl-5-methyloctanal)
O
CH3CH2CCHCH2CH3
CH3
4–甲基–3–己酮
(4-methyl-3-hexanone)
O CH3CH CHCH
2–丁烯醛 (巴豆醛)
CH2 CHCH CHCHO
CH3COO。H
b.p 118 C
所以,生成的乙醛很容易脱离体系。
CH3(CH2)5CHCH3 OH
2-辛醇
KH22COr,2O71+0H02。SCO4
CH3(CH2)5CCH3 O
2-辛酮
11.3.3 羧酸衍生物的还原(不讲)
11.3.4 芳环的酰基化
傅—克酰基化
O + CC lA lC l3
合成芳酮的重要方法。
O C + H C l
(82%)
Gattermann–Koch 反应(烷基苯的甲酰化):
芳烃在Lewis酸催化下,与CO + HCl 作用,生成醛。可以看成是傅-克反应的 特殊形式。
C H 3
+ C O + H C lC A u lC C ll 3 C H 3
室 温
C H O
O HC Cl
酮:以甲酮作母体,“甲”字可省略。
O
甲基乙基(甲)酮
CH3 C CH2CH3
甲乙酮
C
二苯甲酮
O
(benzophenone)
11.1.2 系统命名法
• 选择含有羰基的最长的碳链作为主链。 • 从醛基或靠近羰基一端编号。醛基的位 次为1,可不标,酮中的羰基位次要标明。
• 不饱和醛和酮的命名是从靠近羰基一 端编号。 • 英文命名 醛:烷烃名称的词尾 “e” “al”; 酮: “e” “one”
酮
[O]:KMnO4、K2Cr2O7+H2SO4 、CrO3+吡啶、CrO3+醋酐、丙酮-异丙醇铝等
通用,氧化性强,
氧化到醛、酮
氧化到醛、酮, 不破坏双键
须将生成的醛及时蒸出
CH3CH2。OH
b.p 78 C
K2Cr2O7+H2SO4
50。C
CH3CH。O K2Cr2O7+H2SO4
b.p 21 C
C H3 C H2 C O C H2 C H O 3-氧代戊醛 β-氧代戊醛
不饱和醛酮练习:
O CH 3CH 2CCH 2C=CH 2
CH 3
5-甲基-5-己烯-3-酮
CH2=CCH2CHO CH3
CH=CHCHO
3-甲基-3-丁烯醛 3-苯基丙烯醛
C=CHCHO CH3
3-苯基-2-丁烯醛
11.2 醛和酮的结构
(C H 3)3C C H 2O HK H 2C 2S rO 2O 47 (C H 3)3C C H O
△
(80%)
Oppenauer (欧芬脑尔)氧化
伯醇或仲醇在碱——异丙醇铝
[(CH3)2CHO]3Al存在下,丙酮 (CH3COCH3)做氧化剂生成醛和酮。O
R C H 2 C HC HC H R '[(C C H H 3 3 C )2 O C C H H O 3 ]3 A l R C H 2 C HC HCR '
相当于甲酰氯
对位取代为主要产物。
11.4 醛和酮的物理性质(不讲) 11.5 醛和酮的波谱性质(不讲)
11.6 醛和酮的化学性质
醛和酮的反应部位:
氧化还原反应
亲核加成反应
O C C R (H) H
α-氢的反应
11.6.1 羰基的反应活性 (1)极性
Cδ Oδ
偶极矩
μ = (7.7 ~9.7)×10–30C.m
CH3 CH3 2,3–二甲基–4–戊烯醛
O CH3CH CH CH CCH3
CH3 3–甲基–4–己烯–2–酮
• 命名芳香族的醛和酮,把芳基看成取代 基。
CHO
苯甲醛
O C CH2CH3
1–苯基–1–丙酮
(1-phenyl1-propanone)
•脂环族醛和酮的命名:羰基在环内的——
“环某酮”;羰基在环外的——环作为
CO
CC
图 11.1 醛分子的结构
•羰基的碳原子是sp2杂化
•σ键的形成
•羰基的几何构型
•π键的形成
•羰基的极性
H
121.7°
116.5° C
O
H
1 2 1 .7 °
甲醛分子的结构
11.3 醛和酮的制法
11.3.1醛和酮的工业合成
(1) 低级伯醇和仲醇的氧化和脱氢
伯醇催化脱氢成醛;仲醇催化脱氢成酮。 催化剂:Cu、Ag、Ni等。
正丁醛
C H 3
异丁醛
5 :1
醛可以进一步还原成伯醇。
(3) 烷基苯的氧化
甲苯
空气 CrO2Cl2 CrO3
苯甲醛
C H 3+ O 2V ~ 3 2 O 6 0 5 ℃ C H O + H 2 O
乙苯 O2 苯乙酮
C H 2 C H 3+O 2硬 ~ 脂 1 3 酸 0 ℃ 钴
O CC H 3
11.3.2 伯醇和仲醇的氧化
