官能团相互转换大全(part1)
有机合成中的官能团互变与官能团保护

有机合成中的官能团互变与官能团保护官能团互变和官能团保护是有机合成中常用的两种策略,用于在合成过程中对官能团进行转化或保护,以达到所需的目的。
本文将具体介绍官能团互变和官能团保护的原理和应用。
一、官能团互变官能团互变是指将一个官能团转化为另一个官能团,通常通过一系列的反应步骤实现。
这种方法在有机合成中广泛应用,可以有效地构建复杂有机分子。
下面以几种常见的官能团互变反应为例进行介绍。
1. 羰基互变反应羰基互变反应是一种常见的官能团互变方法,通常通过氧化、还原或加成等反应来实现。
例如,醛和酮可以通过还原反应互变,常用的还原剂有金属碱金属催化剂或氧化铝。
此外,也可以通过氧化反应将醇氧化为醛或酮。
2. 环化反应环化反应是官能团互变的重要手段之一,可以将直链分子转化为环状分子。
常见的环化反应有氧化环化和还原环化。
例如,氧化还原反应可以将烯烃转化为环烃,通常采用氢化反应或氧化反应。
3. 置换反应置换反应是官能团互变的一种常见方法,通过官能团之间的取代反应来实现。
例如,烷基取代反应可以将一个烷基官能团替换为另一个烷基官能团,常用的取代试剂有碱金属、烷基卤化物等。
二、官能团保护官能团保护是在有机合成中常用的一种策略,用于保护特定的官能团,以防止其在反应过程中发生不需要的反应。
在合成过程中,有时需要对某些官能团进行保护,以确保其他官能团能够正常进行反应。
下面以几种常见的官能团保护反应为例进行介绍。
1. 羟基保护反应羟基保护反应是一种常见的官能团保护方法,通常通过酯化或硅醚化反应来实现。
酯化反应将羟基转化为酯基,以保护羟基。
硅醚化反应则将羟基转化为硅醚基,以保护羟基。
这些保护基在需要时可以通过去保护反应去除。
2. 氨基保护反应氨基保护反应是一种常见的官能团保护方法,通常通过酰化或巯基化反应来实现。
酰化反应将氨基转化为酰基,以保护氨基。
巯基化反应则将氨基转化为巯基,以保护氨基。
这些保护基在需要时可以通过去保护反应去除。
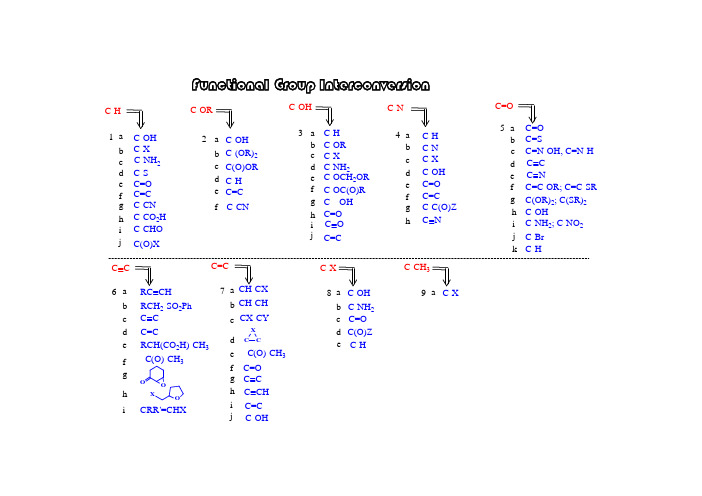
官能团转化
acidic
C6H13
thioketal: inert to LAH; react with RaNi; smell terrible and stay long; discard shoses
neutral basic O Pd-C Ph HCO2NH4 Ph Ph
(3). Wolff-Kishner reduction:
1-a C-OH
(1). for 1', 2' alcohol:
C-H
O CH3 S Cl O
O RCH2 O S O O CH3 tosylate mesylate triflate toluenesulfonyl chloride (s) ~ $ 30 / Kg methanesulfonyy chloride (l) ~ $ 30 / Kg purification textbook dry pyridine: from CaH2 and distilled
C=O 5- a b c d e f g h i j k C=O C=S C=N-OH, C=N-H C C C N C=C-OR; C=C-SR C(OR)2; C(SR)2 C-OH C-NH2; C-NO2 C-Br C-H
2- a C-OH b C-(OR)2 c C(O)OR d C-H e C=C f C-CN
(1). RCH2NH2
C-H
p-TsCl BuLi LiAlH4 RCH2-H
ArSO2Cl RCH2NH2 Hinsberg's test
O
RCH2NH
SO2Ar
BuLi - BuH N SO2Ar
RCH2N SO2Ar
tosylamide RCH2
有机反应中的官能团互换

有机反应中的官能团互换有机反应中的官能团互换是一种常见的有机合成反应,通过官能团的互换,可以合成出各种功能性化合物,为有机化学领域的研究和应用提供了广阔的可能性。
官能团互换反应的研究不仅有助于人们对有机化合物结构和性质的理解,还可以为新药物、高分子材料等领域的研究提供有力支持。
一、醇的官能团互换醇是一类非常重要的官能团,它在有机化合物合成中起着至关重要的作用。
醇的官能团互换反应是有机合成中一种常见的反应类型,通过醇的官能团互换反应,可以合成出不同种类的醇类化合物。
例如,苯酚和溴代烷在氢氧化钠存在下发生互换反应,得到对溴苯醇。
二、醛和酮的官能团互换醛和酮是有机化合物中另一类常见的官能团,它们在生物体内具有重要的生物活性。
醛和酮的官能团互换反应可以通过亚硫酸氢钠等还原剂的作用来实现,产物通常是醇。
例如,苯甲醛和苯酮在硫代氢氨基的还原反应中分别得到苯甲醇和亚苯甲醇。
三、羧酸和酯的官能团互换羧酸和酯是有机化合物中另外两类常见的官能团,它们在药物合成、香料合成等方面有着广泛的应用。
羧酸和酯的官能团互换反应可以通过醇的加成反应或氢化反应来实现。
例如,乙酸和乙酰氯反应得乙酰乙酸乙酯。
四、烃和卤代烃的官能团互换烃和卤代烃是有机化合物中最基本的官能团,它们通过官能团互换反应可以得到不同种类的化合物。
例如,氯代烷和溴乙烷可以在碘乙烷的存在下通过卤代烷的置换反应得到溴代烷。
通过对有机反应中的官能团互换反应的研究,我们可以更深入地了解有机化合物的结构和性质,为有机合成领域的发展提供新的思路和方法。
官能团互换反应的应用不仅可以为很多领域的研究提供帮助,还可以为人类社会的发展和进步做出积极的贡献。
最全官能团转换

1-a C-OH
(1). for 1', 2' alcohol:
C-H
O CH3 S Cl O
O RCH2 O S O O CH3 tosylate mesylate triflate toluenesulfonyl chloride (s) ~ $ 30 / Kg methanesulfonyy chloride (l) ~ $ 30 / Kg purification textbook dry pyridine: from CaH2 and distilled
Functional Group Interconversion
C-H 1- a b c d e f g h i j C C 6- a b c d e f g h i RC CH RCH2-SO2Ph C C C=C RCH(CO2H)-CH3 -C(O)-CH3
O X O O
C-OR C-OH C-X C-NH2 C-S C=O C=C C-CN C-CO2H C-CHO C(O)X C=C 7- a CH-CX b CH-CH c CX-CY
(4). RCH2NH2
RCH2NMe3 X
-
Ag2O
RCH2NMe3 OH-
R=CH2
R-CH3
1-d
C-S
C-H
radical mechanism
EtO2C HN MeO2C S N O
JOC, 1985, 50, 427.
EtO2C CH2Ph
Raney Nickel: Ni - Al alloy, suspension
iii NaBH3CN
NaBH3CN: stable at pH 5-6 JOC, 1976, 41, 3064. Br
有机合成中的新型官能团转化方法

有机合成中的新型官能团转化方法官能团转化是有机合成中的基础步骤之一,它在合成有机化合物时起到至关重要的作用。
传统的官能团转化方法在实践中存在一些限制,例如需要高温、高压条件、使用大量催化剂等。
为了克服这些限制,研究人员一直在不断努力寻找新型官能团转化方法。
本文将介绍一些当前在有机合成领域中广受关注的新型官能团转化方法。
一、C-H键官能团转化传统的官能团转化方法通常需要在分子中存在特定的官能团,才能实现目标反应。
而C-H键官能团转化方法则可以直接将C-H键转化为目标官能团,避免了引入额外的官能团的步骤。
这种方法在有机合成中具有广泛应用潜力。
例如,通过选择性氧化剂可以将烷烃中的C-H键氧化为醇、酮、醛等官能团。
由于烷烃是最常见的有机化合物之一,这种C-H键官能团转化方法为合成化学提供了更为简洁高效的途径。
二、金属催化的官能团转化金属催化的官能团转化方法是有机合成领域中的另一个重要突破。
金属催化剂可以催化反应底物中特定官能团的转化,从而实现特定化学键的形成或断裂。
例如,钯催化的Suzuki偶联反应可以将芳香化合物中的芳基卤素与芳基硼酸酯偶联,生成新的芳基化合物。
这种反应具有高效、可重复性强等优点,在药物合成和材料化学领域得到了广泛应用。
三、可见光催化的官能团转化传统的官能团转化方法中,很多反应需要使用紫外光或高能量光源作为激发源。
然而,这样的条件对于一些化学反应来说并不理想,因为紫外光和高能量光具有一定的危险性,而且也不利于环境保护。
可见光催化的官能团转化方法则可以使用可见光作为激发源,实现特定官能团的转化。
这样的方法具有温和的反应条件、高选择性等优点,在环境友好型合成中具有重要意义。
结论有机合成中的新型官能团转化方法为化学合成领域带来了革命性的变化。
C-H键官能团转化、金属催化的官能团转化和可见光催化的官能团转化等方法都具有独特的优势,为有机化学家提供了更多的选择和可能性。
随着对这些方法的进一步研究和改进,相信官能团转化方法将在有机合成中发挥更加重要的作用,为合成化学的发展做出更大贡献。
重要官能团化合物的典型反应及相互转换的常用方法

重要官能团化合物的典型反应及相互转换的常用方法重要官能团化合物的典型反应及相互转换的常用方法官能团是指分子中具有一定功能性质的特定基团。
在化学中,官能团化合物可以通过化学反应进行自由基聚合、化学加成、脱水、缩合等反应,从而发生相互转化。
以下是重要官能团化合物的典型反应及相互转换的常用方法:1. 羰基化合物的反应及转化羰基化合物是指分子中带有羰基(C=O)的有机化合物。
羰基化合物常见的反应有酸、碱和还原反应。
酸性条件下,羰基化合物可形成酸性羟酮等化合物。
碱性条件下,则会发生羰基的亲核加成反应,生成醇、醛、羧酸等化合物。
还原反应则是将羰基还原成相应的醇。
2. 烯烃化合物的反应及转化烯烃化合物是指分子中具有双键结构的有机化合物。
烯烃化合物可进行加成反应、氧化反应和还原反应等转化。
加成反应是烯烃和亲电试剂发生反应,形成醇、醛、酮、胺等化合物。
氧化反应是将烯烃转化成醛、酮和羧酸等氧化产物。
还原反应是将烯烃还原成相应的饱和烃。
3. 烷基化合物的反应及转化烷基化合物是指分子中只有碳-碳单键的有机化合物。
烷基化合物的反应主要包括取代反应、环化反应、消除反应等。
取代反应是一种置换反应,可以将烷基化合物中的氢原子替换成其他官能团。
环化反应则是通过内部反应,将烷基化合物转化成环化化合物。
消除反应则是通过消除分子中的小分子(如水、氯气等),进行分子结构的改变。
4. 芳香烃化合物的反应及转化芳香烃化合物是指分子中含有至少一个苯环的有机化合物。
芳香烃化合物的反应主要包括芳香亲电取代反应、芳香核磁取代反应、芳香取代加成反应等。
芳香亲电取代反应是通过亲电试剂对苯环上的氢原子进行取代反应,形成新的化合物。
芳香核磁取代反应则是通过用核磁试剂取代苯环上的氢原子,形成新的化合物。
芳香取代加成反应则是将亲电试剂加到苯环中的烯丙基位或芳香环上的碳-碳双键上。
总之,重要官能团化合物的典型反应及相互转换的常用方法是化学中的重要内容。
初学者可以通过学习和掌握这些基本反应类型和相关实验技术,不断提高自己的化学实验技能和知识水平。
有机官能团的转换-127页文档资料

实际上,纯粹SN2与SNl反应仅仅是亲核取代的两种 极限情况。大多数情况下,两种机理并存.并表现为竞
争反应。作用物结构、试剂以及反应条件将对反应产生 很大的影响。
作用物中心碳原子的空间效应对SN2反应影响很大。 中心碳上取代基增多,试剂进攻中心碳受阻,SN2反应
的相对速度便减小。不同结构的作用物进行SN2反应的 活性顺序是:
当取代芳烃再度发生取代时,环上巳存在的基团将
对新基进入芳坏的难易和位置产生很大的影响。这一现 象称为取代基的定位效应。一些基团使取代反应比苯更 易进行,而且将新基主要引入原有取代基的邻、对位, 这类基团称为邻对位定位基;另一类基团使芳环上的取 代比苯难于进行,新基主要进入其间位,称为间位定位 基。一般邻对位定位基对芳环的亲电取代起活化作用, 间位定位基起钝化作用。但卤原子例外,卤原子是吸电 子基因,它们的存在使苯环比较难于取代,但它们所具 有的未共用电于对与苯环组成P—共轭体系,使取代基 的邻、对位电子云密度比间位大一些,因而起邻、对定 位作用。
如果苯环上含有一个以上的取代基时,新基进入的
位置往往受定位效应最强的取代基支配。取代基定位效 应的相对强度同反应类型和反应条件有关,相同的基团
在不同的反应或不同的反应条件下,其相对活性往往有 所不同。根据单取代苯溴代的相对反应速度一些常见邻 对位定位基的定位效应的相对活性顺序为:
根据单取代苯硝化时,问硝基衍生物的产率,一些间位 定位基的相对强度如下顺序:
SN2 机理包括一个由作用物与试剂分子形成的过渡 态,反应按协同方式进行。即试剂从离去基团相反的方 向上进攻中心碳原于,试剂同中心碳之间键的形成,与
离去基团与中心碳之间键的断裂是同时进行的。在过渡 态中,进攻试剂、中心碳原子和离去基团大约处于同一 直线位置。而中心碳上的其余三个原子或基团则位于同 该直线垂直的平面上。这时,进攻试剂与离去基团分别 处于平面的两边。随着新键的逐渐形成,离去基团与中 心碳之间的键逐渐削弱,最后完全脱离中心碳,而完成 反应。
了解有机化合物的官能团转化反应

了解有机化合物的官能团转化反应有机化合物的官能团转化反应是有机化学中的重要内容之一。
它指的是通过一系列化学反应,将有机分子中的一种官能团转变为另一种官能团的过程。
这种转化反应对于有机合成和药物研发等领域具有重要的意义。
本文将介绍一些常见的有机化合物官能团转化反应,并探讨其在实际应用中的意义。
一、醇的官能团转化反应醇是一种常见的有机化合物官能团,通过一系列反应,可以将醇转化为其他官能团,如醛、酮、酯等。
其中,醇的氧化反应是一个重要的官能团转化方法。
一种常用的氧化剂是酸性高锰酸钾溶液,它可以将主链上的一级醇氧化为醛,将主链上的二级醇氧化为酮。
此外,还可以通过醇的酯化反应将醇转化为酯,该反应通常使用酸催化剂,如硫酸。
二、醛和酮的官能团转化反应醛和酮是有机化合物中常见的官能团,它们可以通过多种反应转化为其他官能团。
例如,可以通过还原反应将醛和酮还原为相应的醇。
还原反应通常使用金属氢化物作为还原剂,如氢气和催化剂。
此外,醛和酮还可以通过羟醇化反应将其转化为醇和醚。
羟醇化反应通常使用亲核试剂,如醇和醚等。
三、酸和酸衍生物的官能团转化反应酸和酸衍生物是有机化合物中常见的官能团,它们可以通过多种反应转化为其他官能团。
例如,可以通过酸的酯化反应将酸转化为酯。
酯化反应通常使用醇和酸催化剂。
此外,酸还可以通过酸的羰基化反应或酸的卤代反应转化为醛或酰卤。
四、胺的官能团转化反应胺是有机化合物中重要的官能团,它可以通过一系列反应转化为其他官能团。
例如,可以通过胺的酰胺化反应将胺转化为酰胺。
酰胺化反应通常使用酸催化剂。
此外,胺还可以通过烷基化反应将其转化为胺的烷基衍生物。
五、烯烃的官能团转化反应烯烃是有机化合物中具有双键结构的官能团,它可以通过多种反应转化为其他官能团。
例如,可以通过烯烃的加成反应将烯烃转化为环烷烃。
加成反应通常使用亲电试剂,如酸、醛等。
此外,烯烃还可以通过烯烃的氧化反应或烯烃的卤代反应转化为相应的官能团。
总结起来,有机化合物的官能团转化反应是有机合成中的重要内容,通过这些反应,可以将有机分子中的一种官能团转变为另一种官能团。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
i 5-7-g f e d c b a e d c b a i h g f ed c ba h g f e d cb a h g f e dc b a 6-4-3-1-2-i h g f ed c b a C=C -C(O)-CH 3CH-CH CH-CX F u n c t i o n a l G r o u p I n t e r c o n v e r s i o nC=CC C C=CC C RCH 2-SO 2Ph RC CHC C C-NH 2; C-NO 2C-OHC(OR)2; C(SR)2C=C-OR; C=C-SR C C C NC=N-OH, C=N-H C=SC=O C=O C-C(O)Z C=C C=O C-OH C-X C-N C-H C-N C=O C---OH C-OC(O)R C-X C-OCH 2OR C-NH 2C-OR C-H C-OH C=C C-H C(O)OR C-(OR)2C-OH C-ORC-CHO C-CO 2H C-CN C=C C=O C-S C-X C-OH C-H C=C j C(O)XhC Nj kC-HC-Br 8-C-Xi C-OHC-OH C(O)Z d c b a e d c b a f C-NH 2C-Hj CX-CYC CXC=O h g f iC CH RCH(CO 2H)-CH 3-C(O)-CH 3O OOXCRR'=CHXjC O C-NH 2C-CN9-C-CH 3C-Xa e C=O1-adry pyridine: from CaH 2 and distilledtriflatemesylate tosylate S O O O RCH 2CF 3S OO O RCH 2CH 3CH 3CH 3CH 3OH (2). for 3' alcohol:LiAlH 4(1). for 1', 2' alcohol:1-i h g f e dc b a C-CHO C-CO 2HC-CN C=C C=O C-SC-NH 2C-X C-OH C-H CH 3CH3CH 3H n -Bu SnH C S O PhClRCH 2-HCH 3SOO O RCH 2CH 3S OOCl RCH 2OHpurification textbook~ $ 30 / Kg toluenesulfonyl chloride (s)methanesulfonyy chloride (l)~ $ 30 / Kg jC(O)XPh 2SiHCl / InCl 3PhPhPhPhJOC, 2001, 66, 7741.ii. Ph 2SiHCl / InCl 3i. p -TsCl // LiAlH 4i. ClC(S)OPh // n -Bu 3SnH Cl 2via:a unique Lewis acid catalyst, acceleratedeoxgyenationInCl 3indium trichlorideii. Et 3SiH / Lewis acidJ. Org. Chem. 2000, 65, 6179JOC, 2000, 65, 6179.CHCl 2rt, 3 hr1-bBu 3SnH: (l), easy to remove Ph 3SnH: (s), hard to remove Me 3SnH: too volatile, toxicunstable in acid, form H 2 gas; stable in weak baseNaBH 3CN: stable at pH 5-6hygroscopic, dried self, suggest: buy small amount each time(Grignard reagent)H OJOC, 1969, 34, 3923.HBrNa / NH 3; Li / NH 3; Na / EtOH Zn; Fe; Sn; Mg(3). metal reduction(2). hydride reduction(1). free radical reductionJACS, 1972, 94, 8905.n -Bu 3SnH HBrNaBH 4 / InCl 3 / CH 3CNradical reagentn -Bu 3SnH / AlBN JA CS, 2002, 124, 906.i iii NaBH 3CNi LiAlH 4i ii ii NaBH 4ii THL, 1969, 3095.JOC, 1976, 41, 3064.iv LiBHEt 3 (super hydride)mechanism uncertain, probably radicalburn filter paper if dryRaney Nickel: Ni - Al alloy, suspensionJCS Perkin Trans I, 1973, 654.(3). L iAlH 4 / CuCl 2NaBH 4 / NiCl 2NaBHEt 3 / FeCl 2 (or CoCl 2, VCl 3)(2). Li / NH 3(1). Raney NiBuLi1-d1-c 4RCH 2-HRCH 2NH 2radical mechanismChemistry:R-SH R-S-R R 2SO R 2SO 2R-SS-Rremove: Hg +; Ni(1).(2).Ar-H2Ar-NH 2RCH 2NH 2RCH 2NMe 3R=CH 2R-CH 3(4).X-RCH 2NMe 3OH -2NaH 2(3).Ar-NH 2Ar-H1-e(2). thioketal:(3). Wolff-Kishner reduction:(6). enol derivatives:SHSH/ BFTf2similar:(4). Pd-C / HCO2NH4(7). Et3SiH / CF3COOH1-fb.p. ~ 230 Chighly toxic, cancer suspected agent?= HMPT: h exa m ethyl p hosphoric t riamide (Me 2N)3P=O 1-g (1). K / Al 2O 3 K / HMPA (2). Na / NH 31-h JOC, 1980, 45, 3227HMPA: h exa m ethyl p hosphor a mide (Me 2N)3P=O yes for white mouse, uncertain for humanmodified to: NN O1-i(1). RhCl(PPh 3)3 (Wilkinson's cat)(2). Rh(DPPD)2+ Cl -DPPD = Ph 2P-CH 2CH 2-PPh 21-jHSiEt 3 / B(C 6F 5)3activator / hydride sourceRCH 2OROO RR OROR RCH 2 OCH 2CH 2OH(1). h ν / HSiCl 32-bN NH/ TBDMS-ClTBDPS-ClEt 3N / TMS-Clacid: H 2SO 4H 3PO 4BF 3-Et 2O RC-OCH 2CH=CH2RC-OCPh 3 = RC -OTr RC-O t Bu RC-OCH 3RC-OSiR 3RC-OCH 2Ph = RC-OBZl = RC-OBni. Willianson synthesis OK: Si - Cl bond longii. stability of silyl in acid/base: RC-O-TBDPS > RC-O-TBDMS >> RC-O-TBS iii. abbrev.: TBDMS = tert-butyl-dimethylsilyl = TBS =Silyl group:(RO-Tr)Trityl group: (tirphenylmethyl)i. S N 1 reactionii. abbreviation: triphenylmethyl = trityl = -CPh 3 = -Tr iii. advantage: high MW, easy to handle (small amount become large amount)baseBr Willianson synthesis (base, S N 2) not work: elimination side-product with base t -Butyl group:i. abbreviation: benzyl = PhCH 2 = Bzl = Bn ii. deprotecting: H 2 / Pd-CPhCH 2-ClPhCH 2-Br: reactivity goodPhCH 2-I: reactivity better than PhCH 2Br, generated in situ, PhCH 2Br + NaIPhCH 2-X: Benzyl- group:i. Williamson ether synthesis, S N 2 typeii. not a good protecting group, too stable to convert back to alcohol Me group:CH 3-X: CH 3I; CH 3OSO 2R; (CH 3)3O + BF 4-, (CH 3)2SO 4base: NaH, n -BuLi, Ag 2O(4). t -Bu: acid cat /(3). allyl: base /Br (6). silyl: Et 3N / R 3SiCl (5). trityl: py // Ph 3C-Br(2). PhCH 2-: base / PhCH 2-X e d cb a 2-RC=C RC-H RC(O)ORRC-(OR)2RC-OH RC-OR (1). Me: base / CH 3-X2-a (7). acetal / ketal: (see 3e)fRC-CNgenerate H 2, or butane gasJOC, 1988, 53, 2985.trimethyloxonium tetrafluoroborateJCS, 1930, 2166.(8). ArF / CsFROHradical mechanism: SiCl 3RaNi with C=S2-c2-d (1). hv / HSiCl 3(2). HCl / tBu-OO-t Bu(4). BF 3 / NaBH 42-eC-OH C-H C-OR C-NH 2C-X 3-a b c d3-a(1). [PhI(OAc)-O]2-Mn(TPP)(2). organic electrochemistry(3). X 2 / hv // OH -3-a.13-a.23-a.3(1) Me 3SiCl // MPCBA//H 3O +(2). O 2, LDA, (EtO)3PJA CS, 1975, 97, 6909.i h g f e C=O C---OH C-OC(O)RC-OCH 2OR C=Cj C O(1). Me: application: deprotecting (2). PhCH 2-(5). trityl:(6). silyl: (3). allyl: (4). t-Bu: RC-OCH 2RC-OSiR 3RC-OCH 3RC-OtBuRC-OCPh 3 = RC-OTr RC-OCH 2CH=CH 232Oi. HOAc: weak acid: good leaving groupii. H 2i. F - : HF, Py-H + F -; n -SiMe 3-SiBuMe 2-SiBuPh 2if HOBr: OK for TMDMSJOC, 1987, 52, 4973.OCOCF 3+3-b triphenylmethylorganic base: TMG3-c(1). O H -(2). K O 2 / D M S O 3-d not practically useful: R -O H cheaper than R -XJO C , 1975, 40, 1678.(2). N a 2[F e(C N )5(N O )] / K 2C O 3 / H 2O3-e(1). S ym m etry:ketal: use H 3O +acetal: use H 3O +(2). unsym etry:R O -M O M R O -M E M R O -M T M R O -T H Pi. H 3O +; ii. H C l / M eO H p -T sO H / M eO Hi. H 3O +; ii. Z nB r 2 / C H 2C l 2H gC l 2 / C H 3C N (aq.)actually, a c e t a l e x c h a n g e (3). A g 2O / H 2OT H L , 1975, 3183.JO C , 1986, 51, 3913.R O 2C(C H 2)3H RN H 2R O 2C(C H 2)3H RO H2323-f(1). base: KHCO 3 (or K 2CO 3, NH 3) / MeOH; NaOH (1 %, or 0.5 N)(3). RED: (2). acid: H 3O +PPh 3 / DEAD / RCO 2H // OH -3-gMitsunobu inversionSynthesis, 1981, 1.JOC, 1987, 52, 4235.common esters:formate = HCO 2R ------------------------ KHCO 3 (or K 2CO 3, or NH 3) / MeOH trifluoroacetate = CF 3CO 2R ------------ KHCO 3 (or K 2CO 3, or NH 3) / MeOHacetate = CH 3CO 2R = ROAc --------- KHCO 3 (or K 2CO 3, or NH 3) / MeOH benzoate = PhCO 2R = ROBz -------- NaOH (1 %) / MeOH pivalate = t Bu-CO 2R = ROPv ------ NaOH (0.5 N) / EtOH*HOi LiAlH 4ii. NaAlH 2(OCH 2CH 2OCH 3)CH 3O 2CCO 2CH 3HOOH3)266hydride:electron:Na / NH 3AGIEE, 2002, 41, 3028.。
