APREMILAST(阿普斯特)项目简介
阿普斯特的合成工艺研究

阿普斯特的合成工艺研究阿普斯特(apremilast,商品名Otezla)化学名为(S)-2-[1-(3-乙氧基-4-甲氧基苯基)-2-甲磺酰基乙基]-4-乙酰基氨基异吲哚啉-1,3-二酮。
是由美国新基公司(Celgene)开发的一种首创的口服类的选择性磷酸二酯酶-4抑制剂,2014年和2015分别获得国和欧盟监管机构批准用于活动性银屑病关节炎(PSA)和中度至重度斑块型银屑病适应症的治疗。
该药是过去20年中获批用于银屑病治疗的首个口服药物,也是过去15年中获批用于银屑病关节炎的首个口服药物。
在美国,阿普斯特已被批准用于三种适应症,包括:(1)适合光疗或全身治疗的中度至重度斑块型银屑病患者;(2)患有活动性银屑病关节炎的成年患者;(3)患有与白塞病相关口腔溃疡的成年患者。
该药是第一种也是唯一一种获得监管批准治疗与BD相关口腔溃疡的药物。
目前,Otezla治疗白塞病相关口腔溃疡的新适应症申请也正在接受日本和欧盟的审查。
Otezla在54个国家获得批准,包括主要市场,如德国、法国等欧洲国家和日本。
文献报道阿普斯特的合成路线主要有两条路线,路线一参考美国专利文献报道(US20130217918):以3-乙氧基-4-甲氧基苯腈(7)为起始原料,通过与二甲砜反应后生成化合物1-(3-乙氧基-4-甲氧基苯基)-2-(甲基磺酰基)乙烯(6),6在酸性条件下转化为酮5,5与α-苯乙胺缩合反应生成α-亚胺化合物4,α-亚胺化合物经硼氢化钠还原生成α-胺化合物3,α-胺化合物氢化还原生成2,2与3-乙酰氨基邻苯二甲酸酐酰化反应生成阿普斯特1,工艺路线如下:阿普斯特合成路线一该工艺路线中,选用手性胺α-苯乙胺与酮反应,然后还原为手性S-胺。
工艺存在两个问题:第一,工艺步骤长;第二,工艺需要重金属钯来氢化还原,重金属的残留存在药物安全风险;第三,中间体(S)-1-(3-乙氧基-4-甲氧基苯基)-2-(甲基磺酰基)乙胺(2)的手性纯度不易通过化学反应达到99%以上,不易获得高手性纯度的阿普斯特。
阿普斯特说明书

10 11 12 13 14 16 17
OVERDOSAGE DESCRIPTION CLINICAL PHARMACOLOGY 12.1. Mechanism of action 12.3. Pharmacokinetics NONCLINICAL TOXICOLOGY 13.1. Carcinogenesis, mutagenesis, impairment of fertility CLINICAL STUDIES 14.1 Psoriatic Arthritis HOW SUPPLIED/STORAGE AND HANDLING PATIENT COUNSELING INFORMATION
FULL PRESCRIBING INFORMATION: CONTENTS* 1 INDICATIONS AND USAGE 1.1 Psoriatic Arthritis 2 DOSAGE AND ADMINISTRATION 2.1 Dosage in Psoriatic Arthritis 2.2 Dosage Adjustment in Patients with Severe Renal Impairment 3 DOSAGE FORMS AND STRENGTHS 4 CONTRAINDICATIONS 5 WARNINGS AND PRECAUTIONS 5.1 Depression 5.2 Weight Decrease 5.3 Drug Interactions 6 ADVERSE REACTIONS 6.1 Clinical Trials Experience in Psoriatic Arthritis 7 DRUG INTERACTIONS 7.1 Strong CYP450 Inducers 8 USE IN SPECIFIC POPULATIONS 8.1. Pregnancy 8.3. Nursing mothers 8.4. Pediatric use 8.5. Geriatric use 8.6. Renal Impairment 8.7. Hepatic Impairment
阿普斯特的合成工艺改进

Journal of China Pharmaceutical University2021,52(5):536-540学报阿普斯特的合成工艺改进王栋1*,钟健2,王玲2,周志慧2,蒋海婷1,罗鹏1,王西芝1,王崇益2**(1江苏润安制药有限公司,淮安223299;2江苏正大清江制药有限公司,淮安223001)摘要改进阿普斯特(APST)合成中的氢化还原反应工艺。
以3-硝基邻苯二甲酸酐(4)和(S)-[1-(3-乙氧基-4-甲氧基苯基)-2-(甲磺酰基)乙胺]-N-乙酰基-L-亮氨酸盐(7)为起始原料,经过胺化反应得到(S)-2-[1-(3-乙氧基-4-甲氧基苯基)-2-甲磺酰基乙基]-4-硝基异吲哚啉-1,3-二酮(8),再以甲酸铵作为氢源,氢氧化钯碳为催化剂,将化合物8还原成(S)-2-[1-(3-乙氧基-4-甲氧基苯基)-2-甲磺酰基乙基]-4-氨基异吲哚啉-1,3-二酮(9),最后与醋酐完成乙酰化反应得到APST。
目标产物结构经比旋度、1H NMR、13C NMR、MS和元素分析等确证,胺化、还原和乙酰化3步反应总收率提高至67.0%。
改进后的还原工艺,避开了氢化加压特种反应,降低了安全风险和生产成本,适合工业化生产,具有较高的商业价值。
关键词阿普斯特;磷酸二酯酶-4抑制剂;甲酸铵;合成;工艺改进中图分类号R914文献标志码A文章编号1000-5048(2021)05-0536-05doi:10.11665/j.issn.1000-5048.20210504引用本文王栋,钟健,王玲,等.阿普斯特的合成工艺改进[J].中国药科大学学报,2021,52(5):536–540.Cite this article as:WANG Dong,ZHONG Jian,WANG Ling,et al.Improved synthetic process of apremilast[J].J China Pharm Univ,2021,52(5):536–540.Improved synthetic process of apremilastWANG Dong1*,ZHONG Jian2,WANG Ling2,ZHOU Zhihui2,JIANG Haiting1,LUO Peng1,WANG Xizhi1,WANG Chongyi2**1Jiangsu Runan Pharmaceutical Co.,Ltd.Huai'an223299;2Research Institute,Jiangsu Chiatai Qingjiang Pharmaceutical Co.,Ltd.Huai'an223001,ChinaAbstract To optimize the process of hydrogenation reduction in the synthesis of apremilast(APST),3-nitroph⁃thalic anhydride(4)and(S)-1-(3-ethoxy-4-methoxyphenyl)-2-(methylsulfonyl)ethanamine-(S)-2-acetamido-4-methylpentanoate(7)were used as starting materials to synthesize(S)-2-(1-(3-ethoxy-4-methoxyphenyl)-2-(meth⁃ylsulfonyl)ethyl)-4-nitroisoindoline-1,3-dione(8)by amination.Then compound8was reduced to(S)-4-amino-2-(1-(3-ethoxy-4-methoxyphenyl)-2-(methylsulfonyl)ethyl)isoindoline-1,3-dione(9)with ammonium formate as hydrogen source and palladium hydroxide as catalyst.Finally,apremilast was obtained by the acetylation reaction with acetic anhydride.The structure of the products were verified by optical rotation,1H NMR,13C NMR,MS and elemental analysis.And the total yield of three steps was increased to67.0%.The improved reduction process can avoid the special reaction of hydrogenation and pressurization,and reduce the safety risk and production costs with high commercial value.Key words apremilast;phosphodiesterase-4inhibitors;ammonium formate;synthesis;productive technology improvement阿普斯特(apremilast,APST)化学名为(S)-2-[1-(3-乙氧基-4-甲氧基苯基)-2-甲磺酰基乙基]-4-乙酰基氨基异吲哚啉-1,3-二酮,是由美国Celgene 公司研发的一种磷酸二酯酶-4抑制剂,其作用机制是通过调控免疫细胞中的磷酸二酯酶-4的表达,使得磷酸腺苷增加,从而达到抑制免疫和炎症收稿日期2021-03-05通信作者*Tel:153****7999E-mail:520wangd@**Tel:133****6500E-mail:1026844919@ 536第52卷第5期王栋,等:阿普斯特的合成工艺改进反应[1-2]。
阿普斯特在中国上市了吗?阿普斯特长期用有没有肝肾毒性?阿普斯特对银屑病关节炎效果强劲!

阿普斯特在中国上市了吗?阿普斯特长期用有没有肝肾毒性?阿普斯特对银屑病关节炎效果强劲!2014年3月21日,FDA批准apremilast用于治疗中度至重度牛皮癣(又称斑块型银屑病或plaque psoriasis),剂型为片剂,规格为10mg,20mg,30mg。
2013年9月13日,EMA批准apremilast用于贝塞特病的治疗;2015年2月16日,再批准其单独或联合疾病改良抗风湿性关节炎药物(DMARDs),用于治疗成人患者的活动性银屑病关节炎(PsA)。
剂型为片剂,规格为10mg,20mg,30mg。
2016年12月19日,PMDA批准apremilast用于斑块型银屑病和银屑病关节炎的治疗,剂型为片剂,规格为10mg,20mg,30mg。
阿普斯特长期服用对肝肾功能有没有损害?老年人能长期服药吗?在健康受试者中,apremilast的血浆清除量约为10 L/hr,最终消除半衰期约为6-9小时。
口服放射性标记的阿普利末后,大约58%和39%的放射性分别在尿液和粪便中恢复。
阿普斯特的半衰期短,治疗如需中断,安全系数高。
因此,阿普斯特可应用于传统系统药物治疗无效或者有禁忌证的斑块状银屑病和关节病性银屑病患者以及对生物制剂疗效欠佳或依从性差的患者。
特定人群:肝损害者,apremilast的药动学不受中度或重度肝损害的影响。
肾损害者,阿普利末的药动学不受轻度或中度肾损害的影响。
在8名严重肾功能损害的受试者中,给予30mg apremilast单剂量时,apremilast的AUC和Cmax分别增加了约88%和42%年龄,研究对象为年轻成年人和老年人,每次口服30毫克的阿普利末。
年龄在65岁至85岁之间的老年受试者,与18岁至55岁的年轻受试者相比,AUC和Cmax分别高出约13%和约6%性别,在健康志愿者的药代动力学研究中,女性的暴露程度比男性高31%左右,Cmax比男性高8%左右。
在银屑病关节炎患者中临床研究主要终点是在第16周实现美国风湿病协会(ACR)20反应患者的百分率。
APREMILAST(阿普斯特)项目简介

APREMILAST原料及片剂工程简介南京艾德凯腾生物医药有限责任公司2018年02月一、品种基本情况1、药品名称通用名:阿普斯特(暂拟)英文名:APREMILAST英文商品名:OTEZLA结构式为:2、药理作用及作用机制阿普斯特是一种小分子磷酸二酯酶4(PDE4)抑制剂对环单磷酸腺苷(cAMP)特异性。
PDE4抑制作用导致细胞内cAMP水平增加。
阿普斯特在银屑病关节炎发挥的治疗作用的特异性机制尚未明确确定。
3、制剂的剂型及规格本品为片剂,规格:10mg、20mg、30mg。
可申报10、30mg。
4、拟用于临床的适应症及用法用量适应症:适用于为治疗有活动性银屑病关节炎的成年患者。
用量:(1)为减低胃肠道症状,按照以下给药时间表点滴调整至推荐剂量30 mg每天2次。
1)第1天:早晨10 mg2)第2天:早晨10 mg和傍晚10 mg3)第3天:早晨10 mg和傍晚20 mg4)第4天:早晨20 mg和傍晚20 mg5)第5天:早晨20 mg和傍晚30 mg6)第6天和其后:30 mg每天2次(2)在严重肾受损中的剂量:1)推荐剂量是30 mg每天1次2)对初始剂量的点滴调整,利用表1中列出仅是早晨时间表和跳过下午剂量5、品种概述2018年3月,Celgene生物技术公司开发的治疗关节炎药物apremilast获得了FDA的批准。
FDA批准其作为治疗银屑病性关节炎的口服药物上市。
二、立题背景银屑病关节炎(PsA)是一种与银屑病相关的炎性关节病,有银屑病皮疹并伴有关节和周围软组织疼痛、肿胀、压痛、僵硬和运动障碍。
部分患者可有骶髂关节炎和(或)脊柱炎,病程迁延,易复发。
晚期可有关节强直。
约75%的患者皮疹出现在关节炎之前,同时出现者约15%,皮疹出现在关节炎后的患者约10%。
该病可发生于任何年龄,高峰年龄为30~50岁,无性别差异,但脊柱受累以男性较多。
本病常有家庭聚集倾向,一级家属患病率高达30%,单卵双生子患病危险性为72%。
阿普斯特(Otelza, apremilast)的合成
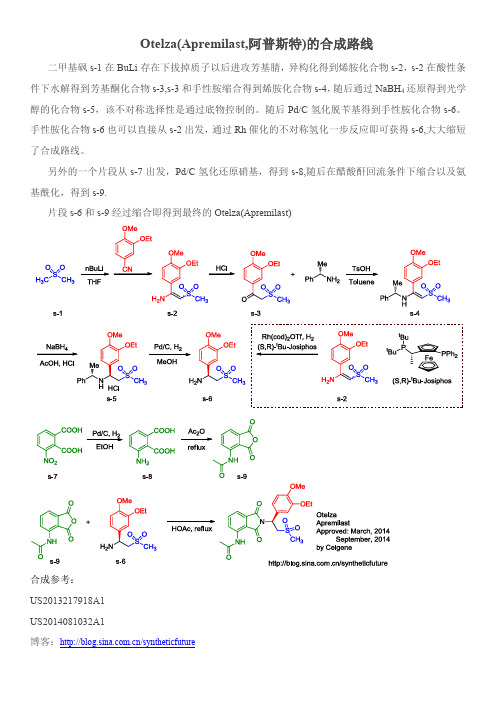
Otelza(Apremilast,阿普斯特)的合成路线
二甲基砜s-1在BuLi存在下拔掉质子以后进攻芳基腈,异构化得到烯胺化合物s-2,s-2在酸性条件下水解得到芳基酮化合物s-3,s-3和手性胺缩合得到烯胺化合物s-4,随后通过NaBH4还原得到光学醇的化合物s-5,该不对称选择性是通过底物控制的。
随后Pd/C氢化脱苄基得到手性胺化合物s-6。
手性胺化合物s-6也可以直接从s-2出发,通过Rh催化的不对称氢化一步反应即可获得s-6,大大缩短了合成路线。
另外的一个片段从s-7出发,Pd/C氢化还原硝基,得到s-8,随后在醋酸酐回流条件下缩合以及氨基酰化,得到s-9.
片段s-6和s-9经过缩合即得到最终的Otelza(Apremilast)
合成参考:
US2013217918A1
US2014081032A1
博客:/syntheticfuture。
阿普斯特及片注册情况
阿普斯特及片CDE承办情况(2015.1.23更新)
名称:阿普斯特片英文名:apremilast
商品名:Otezla
上市时间:2014年3月25日,美国
剂型及规格:片剂,10mg、20mg、30mg
适应症:(1)适用于治疗有活动性银屑病关节炎的成年患者
(2)适合光疗和系统疗法的中度至重度斑块型银屑病成人患者的治疗
中国注册情况(截止2015年1月):
1.瑞阳制药:国家局CDE首家承办
2.广州艾格生物:国家局CDE第2家承办
3.重庆医药工业研究院:国家局CDE第3家承办
项目优势:(1)FDA批准的首个PDE4抑制剂,是一个全新作用机制的口服抗风湿药物。
目前该适应症治疗以注射用为主,副作用大。
(2)临床开发多个适应症——类风湿性关节炎、银屑病关节炎、Crohn病、溃疡性结肠炎等,此次FDA批准了两个适应症--成人活动性银屑病关节炎以及光疗和系统疗法的中度至重度斑块型银屑病成人患者的治疗。
首个也是唯一获准用于治疗斑块状银屑病的PDE4抑制剂。
EvaluatePharma预测2018年销售额为12.19亿美元。
FDA批准Otezla新适应症后,业界预期,Otezla 的销售峰值有望突破20亿美元。
阿普米司特片作用功效
阿普米司特片作用功效
阿普米司特片是一种常见的药物,它属于一类被称为巴比妥类药物的镇静剂。
阿普米司特片具有以下作用和功效:
1. 镇静作用:阿普米司特片能够影响中枢神经系统,使人感到放松和镇静,有助于安宁和缓解紧张情绪。
2. 催眠作用:该药物可以诱导睡眠,并延长睡眠时间。
因此,它常被用于治疗失眠和其他与睡眠相关的问题。
3. 抗焦虑作用:阿普米司特片对焦虑症状有一定的缓解作用。
它可以减轻焦虑、紧张和恐惧感。
4. 抗惊厥作用:阿普米司特片常被用于防止或减少癫痫发作,其镇静和抗焦虑作用有助于控制异常电活动。
5. 肌肉松弛作用:该药物可以通过抑制中枢神经系统来产生肌肉松弛作用,因此常被用于治疗肌肉痉挛和痉挛性疾病。
需要注意的是,阿普米司特片应在医生的指导下使用,并遵循正确的剂量和用药频率,以避免副作用和依赖性的发生。
阿普斯特合成路线图解
阿普斯特合成路线图解
叶琼仙;罗统有;邓吉聪;谭志聪
【期刊名称】《江西化工》
【年(卷),期】2024(40)1
【摘要】阿普斯特是美国Celgene公司研发的一种口服类的选择性磷酸二酯酶4(PDE4)抑制剂,通过调节胞内促炎与抗炎因子,抑制参与银屑病发病机制中的多个炎症的活性,从而有效治疗银屑病。
阿普斯特分别获得FDA、EMA监管机构批准用于活动性银屑病关节炎和中度至重度斑块型银屑病的治疗。
因此对其研究具有重要的意义。
本文对阿普斯特的合成路线进行了总结,利用图解的方式对阿普斯特合成路线进行了综述和评价。
【总页数】4页(P12-15)
【作者】叶琼仙;罗统有;邓吉聪;谭志聪
【作者单位】广东华南药业集团有限公司;广东先强药业有限公司
【正文语种】中文
【中图分类】R914.5
【相关文献】
1.普瑞玛尼合成路线图解
2.普仑司特合成路线图解
3.普卢利沙星合成路线图解
4.群多普利合成路线图解
5.依普利酮合成路线图解
因版权原因,仅展示原文概要,查看原文内容请购买。
英国警示使用阿普斯特存在自杀倾向风险
英国警示使用阿普斯特存在自杀倾向风险
徐晓涵
【期刊名称】《中国食品药品监管》
【年(卷),期】2017(0)3
【摘要】英国药品和医疗产品管理局(MHRA)警示服用阿普斯特(Apremilast)存在增加部分患者精神症状(如抑郁和自杀意念)的风险。
阿普斯特是一种磷酸二酯酶-4-抑制剂,抗风湿病药,用来治疗中到重度的慢性应答不佳的成人慢性斑块型银屑病或活动性银屑病性关节炎(PsA)患者。
相对于一般人群,抑郁、自杀意念和
自杀行为在银屑病和银屑病关节炎患者中较为常见。
【总页数】1页(P78-78)
【关键词】自杀意念;银屑病关节炎;斑块型银屑病;自杀倾向;磷酸二酯酶;自杀行为;
抗风湿;医疗产品;自杀企图;临床试验
【作者】徐晓涵
【作者单位】北京大学药学院
【正文语种】中文
【中图分类】D919.3
【相关文献】
1.英国警示艾维雷韦/克比司特因治疗失败和母婴传播HIV\r的风险避免在孕期使
用 [J],
2.英国警示托伐普坦(Samsca)有导致血清钠升高过快及严重神经系统不良事件的
风险 [J],
3.英国警示阿普斯特自杀倾向风险 [J],
4.英国警示艾维雷韦/克比司特存在治疗失败及母婴传播HIV的风险应避免在孕期使用 [J],
5.英国发布非那雄胺存在抑郁和自杀倾向的信息 [J], 徐晓涵
因版权原因,仅展示原文概要,查看原文内容请购买。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(1)原料小试工艺研究
(2)制剂预实验
(1)样品的质量标准研究。
2、技术可行性分析
(1)合成工艺:
应为塞尔基因在沙利度胺结构上开发的一系列产品
(2)制剂工艺:本品规格为10、20、30mg,按申报规模,应需800g/批的原料规模。
推测为包衣片。辅料为乳糖一水合物,微晶纤维素,交联羧甲基纤维素钠,硬脂酸镁,聚乙烯醇,二氧化钛,聚乙二醇,滑石粉,氧化铁(黄、黑)。
本品目前原研尚未申报,但按照泊马度胺的进度来看,原研在2014年内将有很大可能申报,宜早动早报。
2、
除了手性,看上去没有什么特别的难点。
六
1、针对病因、副作用小。
2、尚在寻求新的适应症,未来有扩大适应症的潜力。
3、专利期适中,且有3+6的可能性。
2014年3月,Celgene生物技术公司开发的治疗关节炎药物apremilast获得了FDA的批准。FDA批准其作为治疗银屑病性关节炎的口服药物上市。
二、立题背景
银屑病关节炎(PsA)是一种与银屑病相关的炎性关节病,有银屑病皮疹并伴有关节和周围软组织疼痛、肿胀、压痛、僵硬和运动障碍。部分患者可有骶髂关节炎和(或)脊柱炎,病程迁延,易复发。晚期可有关节强直。约75%的患者皮疹出现在关节炎之前,同时出现者约15%,皮疹出现在关节炎后的患者约10%。该病可发生于任何年龄,高峰年龄为30~50岁,无性别差异,但脊柱受累以男性较多。
APREMILAST
原料及片剂项目简介
南京艾德凯腾生物医药有限责任公司
2014年02月
一、品种基本情况
1、药品名称
通用名:阿普斯特(暂拟)
英文名:APREMILAST
英文商品名:OTEZLA
结构式为:
2、药理作用及作用机制
阿普斯特是一种小分子磷酸二细胞内cAMP水平增加。阿普斯特在银屑病关节炎发挥的治疗作用的特异性机制尚未明确确定。
主要拓展为类风湿关节炎和特异性皮炎。
2、
目前常用的治疗药物包含了非甾体抗炎药、慢作用抗风湿药(DMARDs)等。近年来已使用单抗类制剂进行治疗。
3、
四、项目的研究内容及技术可行性
1、项目的研究内容
本项目的研究内容,主要为按化学药品3+3类的申报要求完成全套申报资料及样品的试制工作。预实验的研究内容集中原料小试工艺研究,制剂的预实验、质量标准的研究。
3、制剂的剂型及规格
本品为片剂,规格:10mg、20mg、30mg。可申报10、30mg。
4、
适应症:适用于为治疗有活动性银屑病关节炎的成年患者。
用量:
(1)为减低胃肠道症状,按照以下给药时间表点滴调整至推荐剂量30 mg每天2次。
1)第1天:早晨10 mg
2)第2天:早晨10 mg和傍晚10 mg
3)第3天:早晨10 mg和傍晚20 mg
4)第4天:早晨20 mg和傍晚20 mg
5)第5天:早晨20 mg和傍晚30 mg
6)第6天和其后:30 mg每天2次
(2)在严重肾受损中的剂量:
1)推荐剂量是30 mg每天1次
2)对初始剂量的点滴调整,利用表1中列出仅是早晨时间表和跳过下午剂量
5、品种概述
(3)质量研究:本品结构中有含氮碱基,应可采用滴定法控制原料含量,有共轭基团,应可采用高效液相色谱法控制有关物质及含量。其为手性化合物,需控制中间体和成品的手性。
(4)药毒理资料:本品的药理、毒理、药代动力学、临床资料,可参考FDA公布的资料。
五
1、
本品化合物专利CN16527722023年到期。
以“斯特”、“司特”、“Apremilast”在CDE进行查询,均未见相关申报。
本病常有家庭聚集倾向,一级家属患病率高达30%,单卵双生子患病危险性为72%。国内报告有家族史者为10%~23.8%,国外报道为10%~80%。本病是常染色体显性遗传,伴有不完全外显率,但也有人认为是常染色体隐性遗传或性联遗传。
在白人中约为1%-2%,亚非人种较为罕见。
美国FDA药物评价和研究中心的药物评价II部办公室主任Curtis Rosebraugh,M.D.,M.P.H.说:“对于有活动性银屑病关节炎患者重要治疗目标是缓解疼痛和炎症和改善身体机能,”“Otezla为患这种疾病患者提供一种新的治疗选择。”
三、市场综合分析
目前银屑病性关节炎市场上的药物一般是抗TNF类药物,例如艾博维生产的Humira,这种药物具有很大的副作用会导致患者出现严重不良反应。因此Celgene公司的apremilast具有很大的优势。不过apremilast能取得多大的成功还取决于FDA,Celgene公司将于9月份再次向FDA提交申请,扩大apremilast的适用人群。一旦获得批准,apremilast的销售额预计最高将达到20亿美元。
