中国药典版纯化水检验记录.pdf
2010版《中国药典》纯化水标准及检测项目
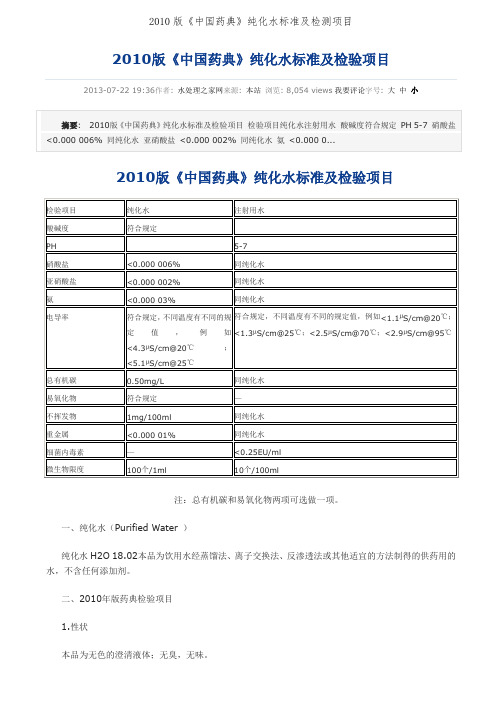
2010版《中国药典》纯化水标准及检验项目2013-07-22 19:36作者: 水处理之家网来源: 本站浏览: 8,054 views我要评论字号: 大中小注:总有机碳和易氧化物两项可选做一项。
一、纯化水(Purified Water )纯化水H2O 18.02本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的供药用的水,不含任何添加剂。
二、2010年版药典检验项目1.性状本品为无色的澄清液体;无臭,无味。
取本品10ml,加甲基红指示液2滴,不得显红色;另取10ml,加溴麝香草酚蓝指示液5滴,不得显蓝色。
3.硝酸盐取本品5ml置试管中,于冰浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液[取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml相当于1μgNO3)]0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后的颜色比较,不得更深(0.000 006%)。
4.亚硝酸盐取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液(1→100)1ml及盐酸萘乙二胺溶液(0.1→100)1ml,产生的粉红色,与标准亚硝酸盐溶液[取亚硝酸钠0.750g(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,摇匀,再精密量取1ml,加水稀释成50ml,摇匀,即得(每1ml相当于1μgNO2))0.2ml,加无亚硝酸盐的水9.8ml,用同一方法处理后的颜色比较,不得更深(.0000 02%)。
5.氨取本品50ml,加碱性碘化汞钾试液2ml,放置15分钟;如显色,与氯化铵溶液(取氯化铵31.5mg,加无氨水适量使溶解并稀释成1000ml)1.5ml,加无氨水48ml与碱性碘化汞钾试液2ml制成的对照液比较,不得更深(0.000 03%)。
中国药典2020版二部纯化水微生物检查

中国药典2020版二部纯化水微生物检查我国药典2020版二部纯化水微生物检查一、前言我国药典2020版二部纯化水微生物检查是当前药品行业中的重要标准之一。
纯化水作为制药过程中不可或缺的重要原料,其微生物检查的质量标准直接关系到药品的安全性和有效性。
本文将围绕我国药典2020版二部纯化水微生物检查这一主题展开讨论,通过全面评估和深入分析,帮助读者对该标准有更深入的理解。
二、我国药典2020版二部纯化水微生物检查的内容概述1. 我国药典2020版中纯化水微生物检查的重要性在药品制造中,纯化水被广泛应用于药品配制、清洁消毒等生产工艺中。
然而,在疫苗、注射剂、眼用制剂等高风险药品中使用的水质则对微生物污染的敏感度要求更高。
我国药典2020版二部纯化水微生物检查作为衡量纯化水质量的重要标准,对保障药品生产过程和药品质量安全具有重要意义。
2. 我国药典2020版中纯化水微生物检查的具体内容我国药典2020版二部中对纯化水微生物检查的内容主要包括微生物总数检查、大肠菌群检查和致病菌检查。
这些检查项目的严格执行,能够有效地保障纯化水的微生物污染水平处于合理的范围内,符合药品生产的要求。
三、对我国药典2020版二部纯化水微生物检查的深入分析1. 微生物总数检查微生物总数检查是评价水质中微生物总体污染水平的重要指标。
根据我国药典2020版二部的相关规定,微生物总数检查采用膜过滤法,通过将一定容积的水样过滤到膜上,再将膜培养于富含营养物质的培养基中,最终统计出微生物菌落总数。
这一检查项目的严谨性和科学性直接关系到纯化水的微生物质量。
2. 大肠菌群检查大肠菌群检查是评价水质中是否存在粪肠道致病菌的关键指标之一。
我国药典2020版二部中对大肠菌群检查的相关要求十分严格,如规定了检测方法、培养基的配制等方面的内容。
这一检查项目的合格与否,直接影响着纯化水的可靠性和安全性。
3. 致病菌检查致病菌检查是对纯化水中致病菌的检测和评价。
《中国药典》2015年版纯化水质量检验操作规程

本品为饮用水蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的制药用水,不含任何添加剂。
1、性状:本品为无色的澄明液体;无臭。
2、检查:2.1酸碱度取本品10ml,加甲基红指示液2滴,不得显红色;另取10ml,加溴麝香草酚蓝指示液5滴,不得显蓝色。
2.2 硝酸盐取本品5ml置试管中,于冰浴中冷却,加10%氯化钾溶液0.4ml 与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸 5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液[取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,再精密量取)0.3ml,加无硝10ml,加水稀释成100ml,摇匀,即得(每1ml相当于1μg NO3酸盐的4.7ml,用同一方法处理后的颜色比较,不得更深(0.000006%)。
2.3 亚硝酸盐取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液(1→100)1ml与盐酸萘乙二胺溶淮(0.1→100)1ml,产生的粉红色,与标准亚硝酸盐溶液[取亚硝酸钠0.750g(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,摇匀,再精密量取1ml,加水稀释成)]0.2ml,加无亚酸盐的水9.8ml,用50ml,摇匀,即得(每1ml相当于1ugNO2同一方法处理后的颜色比较,不得更深(0.000002%)。
2.4氨取本品50ml,加碱性磺化汞钾试液2ml,放置15分钟;如显色,与氯化铵溶液(取氯化铵31.5mg,加无水氨水适量使溶解并稀释成1000ml)1.5ml,加无氨水48ml与碱性磺化钾试液2ml制成的对照液比较,不得更深(0.00003%)。
2.5 电导率应符合规定(通则0681)2.6 总有机碳不得过0.50mg/L(通则0682)。
2.7 易氧化物取本品100ml,加稀硫酸10ml,煮沸后,加高锰酸钾滴定液(0.02mol/L)0.10ml,再煮沸10分钟,粉红色不得完全消失。
纯化水(药典标准)

纯化水Chunhuashui Purified waterH2O 18.02本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的制药用水,不含任何添加剂。
【性状】本品为无色的澄清液体;无臭、无味。
【检查】酸碱度取本品10ml加甲基红指示液2滴,不得显红色;另取10ml,加溴麝香草酚蓝指示液5滴,不得显蓝色。
硝酸盐取本品5ml置试管中,于冰浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液〔取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml相当于1μgNO3)〕0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后的颜色比较,不得更深(0.000 006%)亚硝酸盐取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液(1→100)lml与盐酸萘乙二胺溶液(0.1→100)lml,产生的粉红色,与标准亚硝酸盐溶液〔取亚硝酸钠0.750g(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取1ml,加水稀释至100ml,摇匀,再精密量取1ml,加水稀释成50ml,摇匀,即得(每1ml相当于1μgNO2 )〕0.2ml,加无亚硝酸盐的水9.8ml,用同一方法处理后的颜色比较,不得更深(0.000 002%)氨取本品50ml,加碱性碘化汞钾试液2ml,放置15分钟;如显色,与氯化铵溶液(取氯化铵31.5mg,加无氨水适量使溶解并稀释成1000ml)1.5ml,加无氨水48ml与碱性碘化汞钾试液2ml制成的对照液比较,不得更深(0.000 03%)电导率应符合规定(附录ⅧS)总有机碳不得超过0.50mg/l(附录ⅧR)易氧化物取本品100ml,加稀硫酸10ml,煮沸后,加高锰酸钾滴定液(0.02mol/L)0.10ml,再煮沸10分钟,粉红色不得完全消失。
纯化水检验原始记录(2020版药典)

检查方法:取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液﹙1→100﹚1ml与盐酸萘乙二胺溶液﹙0.1→100﹚1ml,产生的粉红色,与标准亚硝酸盐溶液[取亚硝酸钠0.750g(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取lml,加水稀释成 100ml,摇匀 ,再精密量取lml,加水稀释成 50ml,摇勻,即得(每1ml相当于1μg NO2)]0.2ml,加无硝酸盐的水9.8ml,用同一方法处理后的颜色比较,供试品溶液。
硝酸盐
检查方法:取本品5ml置试管中,于水浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液液[取硝酸钾0.163g ,加水溶解并稀释至100ml,摇匀,精密量取lml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得 (每1ml相当于1μgNO3)]0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后的颜色比较,供试品溶液。 (标准规定:不得更深0.000006%)
电导率
检查方法:取本品照制药用水电导率测定法标准操作规程25℃测得电导率为μS/cm 。 (标准规定:25℃不得大于5.1μSl,加稀硫酸10ml,煮沸后,加高锰酸钾滴定液﹙0.02mol/L﹚0.10ml,再煮沸10分钟,溶液的粉红色消失。
(标准规定:粉红色不得完全消失)
检验日期: 年 月 日;
检品名称:
纯化水
检品编号:
车 间:
取样日期:
取 样 点:
报告日期:
检验依据:
《中国药典》2020年版二部
检验项目:
全检
【性状】:本品为,无臭。
纯化水理化检验原始记录
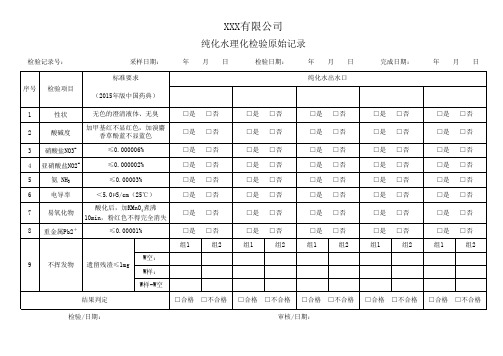
纯化水理化检验原始记录
检验记录号: 采样日期: 标准要求 序号 检验项目 (2015年版中国药典) 1 2 3 4 5 6 7 8 性状 酸碱度 硝酸盐NO3亚硝酸盐NO2 氨 NH3 电导率 易氧化物 重金属Pb2+
-
年
月
日
检验日期:
年
月
日
完成日期:
年
月
日
纯化水出水口
无色的澄清液体、无臭 加甲基红不显红色,加溴麝 香草酚蓝不显蓝色 ≤0.000006% ≤0.000002% ≤0.00003% <5.0µS/cm(25℃) 酸化后,加KMnO4煮沸 10min,粉红色不得完全消失 ≤0.00001%
□是 □是 □是 □是 □是 □是 □是 □是 组1
□否 □否 □否 □否 □否 □否 □否 □否 组2
□是 □是 □是 □是 □是 □是 □是 □是 组1
□否 □否 □否 □否 □否 □否 □否 □否 组2
□是 □是 □是 □是 □是 □是 □是 □是 组1
□否 □否 □否 □否 □否 □否 □否 □否 组2
□合格
□不合格
□合格
□不合格
□合格
□不合格
审核/日期:
□是 □是 □是 □是 □是 □是 □是 □是 组1
□否 □否 □否 □否 □否 □否 □否 □否 组2
□是 □是 □是 □是 □是 □是 □是 □是 组1
□否 □否 □否 □否 □否 □否 □否 □否 组2
9
不挥发物
遗留残渣≤1mg
W空: W样: W样-W空
结果判定 检验 □不合格
纯化水 注射用水《中国药典》2010版
《中国药典》2010版纯化水本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的制药用水,不含任何添加剂。
【性状】本品为无色的澄明液体;无臭,无味。
【检查】酸碱度取本品10ml,加甲基红指示液2滴,不得显红色;另取10ml,加溴麝香草酚蓝指示液5滴,不得显蓝色。
硝酸盐取本品5ml置试管中,于水浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液﹝取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml相当于1μg NO3)﹞0.3ml,加无硝酸盐的水4.7ml,用同一办法处理后的颜色比较,不得更深(0.000.006%)。
亚硝酸盐取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液(1→100)1ml与盐酸萘乙二胺溶液(0.1→100)1ml,产生的粉红色,与标准硝酸盐溶液﹝取亚硝酸钠0.750g (按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,摇匀,再精密量取1ml,加水稀释成50ml,摇匀,即得(每1ml相当于1μgNO2)﹞0.2ml,加无硝酸盐的水9.8ml,用同一方法处理后的颜色比较,不得更深(0.000 002%)氨取本品50ml,加碱性碘化汞钾试液2ml,放置15分钟;如显色,与氯化铵溶液(取氯化铵31.5mg,加无氨水适量使溶解并稀释成1000ml)1.5ml,加无氨水48ml与碱性碘化汞钾试液2ml制成的对照液比较,不得更深(0.000 03%)。
电导率应符合规定(附录Ⅷ S)。
总有机碳不得过0.50mg/L(附录Ⅷ R)。
易氧化物取本品100ml,加稀硫酸10ml,煮沸后,加高锰酸钾滴定液(0.02mol/L)0.10ml,再煮沸10分钟,粉红色不得完全消失。
2010版《中国药典》纯化水标准及检测项目
2010版《中国药典》纯化水标准及检验项目2013-07-22 19:36作者: 水处理之家网来源: 本站浏览: 8,054 views我要评论字号: 大中小注:总有机碳和易氧化物两项可选做一项。
一、纯化水(Purified Water )纯化水H2O 18.02本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的供药用的水,不含任何添加剂。
二、2010年版药典检验项目1.性状本品为无色的澄清液体;无臭,无味。
取本品10ml,加甲基红指示液2滴,不得显红色;另取10ml,加溴麝香草酚蓝指示液5滴,不得显蓝色。
3.硝酸盐取本品5ml置试管中,于冰浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50℃水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液[取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每1ml相当于1μgNO3)]0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后的颜色比较,不得更深(0.000 006%)。
4.亚硝酸盐取本品10ml,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液(1→100)1ml及盐酸萘乙二胺溶液(0.1→100)1ml,产生的粉红色,与标准亚硝酸盐溶液[取亚硝酸钠0.750g(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取1ml,加水稀释成100ml,摇匀,再精密量取1ml,加水稀释成50ml,摇匀,即得(每1ml相当于1μgNO2))0.2ml,加无亚硝酸盐的水9.8ml,用同一方法处理后的颜色比较,不得更深(.0000 02%)。
5.氨取本品50ml,加碱性碘化汞钾试液2ml,放置15分钟;如显色,与氯化铵溶液(取氯化铵31.5mg,加无氨水适量使溶解并稀释成1000ml)1.5ml,加无氨水48ml与碱性碘化汞钾试液2ml制成的对照液比较,不得更深(0.000 03%)。
纯化水《中国药典》2015年版 第二部
中国药典2015年版溶液的澄清度与颜色取本品,加水制成每lml中约含阿魏酸钠20m g的溶液,溶液应澄清无色;如显浑浊,与1号池度标准液(通则0902第一法)比较,不得更浓;如显色,与黄色或黄绿色3号标准比色液(通则0901第一法)比较,不得更深。
有关物质避光操作。
取本品,加流动相溶解并稀释制成每l m l中约含0. 7m g的溶液,作为供试品溶液;精密量取lm l,置200m l量瓶中,用流动相稀释至刻度,摇勻,作为对照溶液。
照阿魏酸钠有关物质项下的方法测定。
供试品溶液的色谱图中如有杂质峰,各杂质峰面积的和不得大于对照溶液的主峰面积(0.5%)。
水分取本品,照水分测定法(通则0832第一法1)测定,含水分应为13.0%〜16.0%(供无菌粉末用)或应不超过3.0%(供无菌冻干品用)。
热原取本品,加灭菌注射用水制成每l m l中含阿魏酸钠5m g的溶液,依法检查(通则1142),剂量按家兔体重每l k g 缓慢注射3m l,应符合规定。
无菌照阿魏酸钠项下的方法检査,应符合规定。
其他应符合注射剂项下有关的各项规定(通则0102)。
【含置测定】避光操作。
取装量差异项下的内容物约0.15g,精密称定,加冰醋酸20m l使阿魏酸钠溶解,照阿魏酸钠项下的方法,自“加醋酐3m l”起,依法测定。
每l m l高氣酸滴定液(0.lm o l/L)相当于25.22mg的C10H9N a04•2H20。
【类别】同阿魏酸钠。
【规格】(1)0. lg(2)0. 3g【贮藏】遮光,密封保存。
纯化水ChunhuashuiPurified WaterH2018.02本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的制药用水,不含任何添加剂。
【性状】本品为无色的澄清液体;无臭。
【检査】酸碱度取本品10m l,加甲基红指示液2滴,不得显红色;另取10m l,加溴麝香草酚蓝指示液5滴,不得显蓝色。
硝酸盐取本品5m l置试管中,于冰浴中冷却,加10%氣化钾溶液0.4m l与0.1%二苯胺硫酸溶液0.1m l,摇匀,缓缓滴加硫酸5m l,摇勻,将试管于50T:水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液[取硝酸钾0.163g,加水溶解并稀释至100m l,摇匀,精密量取l m l,加水稀释成100m l,再精密量取10m l,加水稀释成100m l,摇匀,即得(每l m l相当于1吨N03)]0.3m l,加无硝酸盐的水4.7m l,用同一方法处理后纯化水的颜色比较,不得更深(0.000006%)。
纯化水微生物限度检查法验证
目录A、验证方案1.概述2.适用范围3.验证目的4.验证小组及职责分工4.1 验证小组4.2 职责分工5.验证内容6.漏项与偏差及采取的纠偏措施.7.验证结论8.验证方案批准B、验证报告1.概述2.适用范围3.验证目的4.验证小组及职责分工4.1 验证小组4.2 职责分工5.确证内容6.漏项与偏差及采取的纠偏措施.7.验证结论8.最终批准9. 再验证周期与年度回顾性验证1 概述由于某些供试品抗菌活性,在建立测定方法或原测定法的检验条件发生改变时,可能影响检验结果的准确性,必须对供试品的抑菌活性及测定方法的可靠性、重现性进行验证。
验证时,按供试液的制备和细菌、霉菌及酵母菌计数所规定的方法进行。
对各试验菌的回收率应逐一进行验证。
2 适用范围纯化水微生物限度检查——薄膜过滤法的验证。
3 验证目的验证纯化水微生物限度检查——薄膜过滤法符合《中国药典》2005年版二部的规定要求。
4 验证小组及职责分工5 验证内容5.1 品种:纯化水5.2 验证方法:《中国药典》2005年版二部微生物限度检查——薄膜过滤法5.3 计数方法的验证5.3.1 验证试验用菌种验证试验用的菌株传代次数不得超过5代(从菌种保存中心获得的冷冻干燥菌种为第0代),并采用适宜的菌种保藏技术,以保证试验菌株的生物学特性。
大肠埃希菌(Escherichia coli)〔CMCC(B) 44 102〕金黄色葡萄球菌(Staphylococcus aureus) CMCC(B) 26 003〕枯草芽孢杆菌(Bacillus subtilis)〔CMCC(B) 63 501〕白色念珠菌(Candida albicans)〔CMCC(F) 98 001〕黑曲霉(Aspergillus niger)〔CMCC(F)98 003〕5.3.2 菌液制备取经32.5℃培养18~24小时的大肠埃希菌、金黄色葡萄球菌与枯草芽孢杆菌营养肉汤液体培养物,用0.9%无菌氯化钠溶液制成每1ml含菌数为50~100cfu的菌悬液。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
广东惠德勤药业有限公司
纯化水检验记录REC-(Q-30-007-F)-V06 页次1/10
广东惠德勤药业有限公司
纯化水检验记录REC-(Q-30-007-F)-V06 页次2/10
广东惠德勤药业有限公司
纯化水检验记录REC-(Q-30-007-F)-V06 页次3/10
纯化水检验记录REC-(Q-30-007-F)-V06 页次4/10
纯化水检验记录REC-(Q-30-007-F)-V06 页次5/10
广东惠德勤药业有限公司
纯化水检验记录REC-(Q-30-007-F)-V06 页次6/10
广东惠德勤药业有限公司
纯化水检验记录REC-(Q-30-007-F)-V06 页次7/10
广东惠德勤药业有限公司
纯化水检验记录REC-(Q-30-007-F)-V06 页次8/10
广东惠德勤药业有限公司
纯化水检验记录REC-(Q-30-007-F)-V06 页次9/10
学无止境
广东惠德勤药业有限公司
纯化水检验记录REC-(Q-30-007-F)-V06 页次10/10
检验人:复核人:。
