乙二醇及其水溶液二元体系理化性能数据的测定
工业用乙二醇酸度定滴定法试验方法

工业用乙二醇酸度定滴定法试验方法警告:本部分并不是旨在说明与其使用有关的所有安全问题。
使用者有责任采取适当的安全与健康措施,保证符合国家有关法规的规定。
1 范围本部分规定了工业用乙二醇酸度测定的手动滴定法和电位滴定法。
本部分手动滴定法适用于酸度为(2~200) mg/kg的工业用乙二醇的测定, 电位滴定法适用于酸度为(1~200) mg/kg的工业用乙二醇的测定。
2 规范性引用文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T 601 化学试剂标准滴定溶液的制备GB/T 603 化学试剂试验方法中所用制剂及制品的制备GB/T 3723 工业用化学产品采样安全通则GB/T 6680 液体化工产品采样通则GB/T 6682 分析实验室用水规格和试验方法GB/T 8170 数值修约规则与极限数值的表示和判定3 试验方法A---手动滴定法3.1 方法提要将乙二醇样品溶于水中,用氢氧化钠标准溶液滴定试样中的酸,采用酚酞指示液变色来指示滴定终点,根据消耗的氢氧化钠标准溶液的量计算样品的酸度,以乙酸(mg/kg)计。
3.2 试剂与材料3.2.1 除另有注明外,所用试剂均为分析纯,所用标准溶液、制剂均按GB/T 601或GB/T 603制备,所用水均符合GB/T 6682中规定的三级水的规格。
3.2.2 氢氧化钠标准滴定溶液:c(NaOH)=0.01 mol/L。
3.2.3 酚酞指示液:10 g/L。
3.2.4 氮气:纯度不低于99.99%(体积分数)。
3.3 仪器与设备3.3.1 分析天平:感量为0.0001 g。
3.3.2 锥形瓶:500 mL,带开口磨口塞和氮气吹管,如图1。
3.3.3 量筒:100 mL。
3.3.4 碱式滴定管:5 mL,分度为0.02 mL。
图1 锥形瓶图3.4 采样按照GB/T 3723和GB/T 6680规定的要求采取样品。
乙二醇和丙二醇分析的标准试验方法

乙二醇和丙二醇分析的标准试验方法引言乙二醇(Ethylene Glycol)和丙二醇(Propylene Glycol)是常用的有机化合物,广泛应用于化工、医药、食品等领域。
准确分析乙二醇和丙二醇的含量对于检测产品质量、保证工艺流程以及控制生产过程至关重要。
本文将介绍一种标准的试验方法,以帮助实验人员准确快速地分析乙二醇和丙二醇的含量。
试验目的本试验方法的目的是确定样品中乙二醇和丙二醇的含量,为产品质量控制和工艺改进提供准确的数据支持。
试验原理本试验方法基于酸碱滴定原理,利用酸碱滴定反应的终点变化现象,来测定乙二醇和丙二醇的含量。
具体原理如下:1.样品溶液中的乙二醇和丙二醇与对应的酸性溶液反应,生成酸性羧酸。
2.酸性羧酸与标准的碱溶液滴定反应,反应终点时酸性羧酸与碱溶液的中和反应完全。
3.通过溶液中酸性羧酸与酸碱指示剂的反应,可以通过颜色变化确定乙二醇和丙二醇的含量。
试验步骤试剂准备1.准备0.1mol/L的盐酸(HCl)溶液。
2.准备0.1mol/L的氢氧化钠(NaOH)溶液。
3.准备适用于乙二醇和丙二醇测定的酸碱指示剂。
样品准备1.将待测样品称取适量,加入容量瓶中。
2.加入适量酸性溶液,并摇匀使其溶解。
滴定操作1.使用准确的容量管量取待测溶液。
2.将溶液转移至滴定瓶中。
3.在滴定操作过程中,加入适量的酸碱指示剂。
4.在滴加氢氧化钠滴液的过程中,观察溶液颜色的变化,并搅拌溶液。
5.当溶液颜色变化到终点颜色时,记录所消耗的氢氧化钠滴液的体积。
结果计算根据滴定操作中氢氧化钠滴液的消耗量,结合标准的滴定反应等当量关系,计算得出乙二醇和丙二醇的含量。
实验注意事项1.实验过程中需严格控制试剂和样品的操作温度,以免影响滴定结果。
2.滴定过程中需反复搅拌溶液,确保反应充分。
3.为了获得准确的滴定结果,每次实验需进行至少三次重复测定,并取平均值。
结论通过本标准试验方法,可以准确快速地分析乙二醇和丙二醇的含量。
乙二醇冰点

汽车防冻剂冬季气温低,为使汽车在冬季低温下仍能继续使用,发动机冷却液都加入了一些能够降低水冰点的物质作为防冻剂,保持在低温天气时冷却系统不冻结。
因此人们有时把冷却液称作“防冻液”或“不冻液”。
防冻液的全称应该叫防冻冷却液,意为有防冻功能的冷却液。
简介乙二醇型;浓度配比为:55%——液45%——水、沸点:107℃;冰点:-40℃。
根据所需预防的温度,可以配入1~3倍的水,通常当水按1:1的比例混合使用时,将使冷却液的冰点降至-36.7℃。
乙二醇—水型的防冻液的最大使用浓度为75%,切记不可超过此浓度。
水分子之间是通过氢键的缔合而成为分子簇的,具有较高的冰点,在冬季若单以水为冷却液,低于0℃就会结冰而无法流动,启动时非但起不到循环冷却的作用,而且由于水变成冰晶是一个体积增大的过程,通常同样质量的水在变成冰时提及要增大9%~10%。
产生的膨胀力会胀裂散热器及管路等部件,在含有乙二醇的防冻液中,由于乙二醇的存在,起始冰点就远比水低,当达到冰点时析出的冰晶成浆状,而且这些冰晶中的乙二醇的含量较低,显然大部分的乙二醇仍然留在了未凝固的液相之中,其结果是使得仍未结晶的溶液的冰点更低,正是由于乙二醇的这个特性,所以含有乙二醇的防冻液使用的实际温度比测定的冰点还可以再降一些。
当然在超过最低点(-69℃,乙二醇的浓度68%)后冰点会有所上升,所以,以为增加乙二醇的浓度以求更低的冰点的做法,到最后是徒劳无效的。
种类乙二醇一水防冻液乙二醇是一种无色微粘的液体,沸点是197.4℃,冰点是-11.5℃,能与水任意比例混合。
混合后由于改变了冷却水的蒸气压,冰点显著降低。
其降低的程度在一定范围内随乙二醇的含量增加而下降。
当乙二醇的含量为68%时,冰点可降低至- 68℃,超过这个极限时,冰点反而要上升。
乙二醇防冻液在使用中易生成酸性物质,对金属有腐蚀作用。
因此,应加入适量磷酸氢二钠等以防腐蚀。
乙二醇有毒,但由于其沸点高,不会产生蒸气被人吸入体内而引起中毒。
二元气液平衡数据测定_实验指导书

化工专业实验报告实验名称:二元气液平衡数据的测定实验人员:同组人:实验地点:实验时间:班级:学号:指导教师:实验成绩:二元气液平衡数据的测定一、 实验目的1. 测定苯—正庚烷二元体系在常压下的气液平衡数据2. 通过实验了平衡釜的结构,掌握气液平衡数据的测定方法和技能 3. 应用Wilson 方程关联实验数据 二、 实验原理与循环法测定气液平衡数据的平衡釜基本原理相同,如下图所示,体系达到平衡时,两个容器的组成不随时间变化,这时从A 和B 两容器中取样分析,可得到一组平衡数f i L =f i V (1)φi py i =γi f i 0x i常压下,气相可视为理想气体,再忽略压力对液体逸度的影响,f i =p i 0从而得出低压下气液平衡关系为:py i =γi p i 0x i (2)式中,p ——体系压力(总压);p i 0——纯组分I 在平衡温度下饱和蒸汽压,可用安托尼(Antoine )公式计算; x i 、y i ——分别为组分I 在液相和气相中的摩尔分率; γi ——组分i 的活度系数。
由实验测得等压下气液平衡数据,则可用ii i i p x py =γ (3)计算出不同组成下的活度系数。
本实验中活度系数和组成关系采用Wilson 方程关联。
Wilson 方程为: lnγ1=-ln 22121)(x x x +Λ+)(121221212112x x x x Λ+Λ-Λ+Λ (4)lnγ2=-ln )()(21211212122111212x x x x x x x Λ+Λ-Λ+Λ+Λ+ (5)Wilson 方程二元配偶参数12Λ和21Λ采用非线形最小二乘法,由二元气液平衡数据回归而得。
目标函数选为气相组成误差的平方和,即F=∑=mj 1(y1实-y 1计)2j +(y 2实-y 2计)2j (6)三、实验装置和试剂1. 平衡釜一台(平衡釜的选择原则:易于建立平衡、样品用量少、平衡温度测定准确、气相中不夹带液滴、液相不返混及不易暴沸等。
电子烟雾化液中甲醇、乙二醇、二甘醇的测定

电子✕雾化液甲醇、乙二醇、二甘醇的测定B.1 原理采用含有内标的乙醇溶液稀释样品,使用带有氢火焰离子化检测器的气相色谱仪(GC-FID)测定,内标法定量,采用气相色谱-质谱确证阳性结果。
B.2 试剂B.2.1 乙醇,色谱纯。
B.2.2 甲醇,纯度不低于99.9%。
B.2.3 乙二醇,纯度不低于99.9%。
B.2.4 二甘醇,纯度不低于99.9%。
B.2.5 异丁醇,纯度不低于99.9%。
B.2.6 内标储备液准确称取0.1 g(精确至0.0001g)异丁醇(B.2.5)置于100mL容量瓶中,用乙醇(B.2.1)溶解定容,得到浓度为1000 mg/L的内标储备液。
储存于2℃~4℃条件下,有效期为3个月。
B.2.7 标准储备液分别准确称取0.1g(精确至0.0001g)甲醇(B.2.2)、乙二醇(B.2.3)、二甘醇(B.2.4)于100mL 容量瓶中,用乙醇(B.2.1)溶解定容,得到浓度均为1000 mg/L的甲醇、乙二醇和二甘醇混合储备液。
储存于2℃~4℃条件下,有效期为3个月。
B.2.8 标准工作溶液分别移取50μL 、100μL、200μL、500μL、1000μL的标准储备液(B.2.5)于10mL容量瓶中,再分别准确加入200μL内标储备液(B.2.6),用乙醇(B.2.1)稀释定容,得到浓度为5 mg/L、10 mg/L、20 mg/L、50 mg/L和100 mg/L系列标准溶液。
即配即用。
B.3 仪器与材料B.3.1 分析天平,感量为0.1mg。
B.3.2 气相色谱仪,配置有氢火焰离子化检测器,进样口应具有分流进样方式。
进样口、柱箱和检测器应分别配有独立可控制的加热单元。
B.3.3 容量瓶,A级,10mL、100mL。
B.3.4 涡旋振荡器,最大涡旋速度不小于2000r/min。
B.4 分析步骤B.4.1 样品前处理准确称取1.0 g(精确至0.0001g)电子雾化液于10mL容量瓶(B.3.3)中,加入200μL内标储备液(B.2.6)后,以乙醇(B.2.1)定容至刻度,加盖密封后置于涡旋振荡器(B.3.4)中,以2000r/min的速度涡旋振荡提取10 min,取萃取液转移到色谱分析瓶中进行仪器分析。
二元完全互溶液体蒸馏过程气液相折光率的测定

乙醇-丙醇系统沸点及气-液两相组成折光率数据
液相 样品编号 沸点t/℃ n tD 纯乙醇 — — 100ωB(丙醇) 0 n tD — —
气相冷凝液 100ωB(丙醇) 0
纯丙醇
—
100
—
100
六、思考题
一、在测定乙醇、丙醇各混合物沸点的顺序如何安排? 二、测定混合物两相组成时,先取气相样还是先取液相样?为什么?
纯液体物质,组成一定的A、B两液体的混合物,在恒定的压力 下沸点为确定值,液体混合物的沸点随组成不同而改变,因同样温 度下,各组分挥发能力不同,即具有不同的饱和蒸气压,故平衡共 存的气、液两相的组成通常并不相同。 测定混合物组成的方法分为物理法和化学法。物理法是通过测定 与系统组成有一定关系的某一物理性质(如电导、折射率、旋光度、 吸收光谱、体积、压力等)而求出系统组成方法。本实验是采用测 定折射率的方法,采用此法是因为液体乙醇与丙醇的折射率较大, 而且它们的液体混合物的折射率与其组成有较好的线性关系。 2. 沸点测定仪 各种沸点仪的具体构造虽各有特点,但其设计思想则都集中于 如何正确测定沸点、便于取样分析、防止过热及避免分馏等方面。 本实验所用的沸点仪如下图所示.这是一只带回流冷凝管的长颈圆底 烧瓶。冷凝管底部有一半球形小室,用以收集冷凝下来的气象样品 象,还能防止暴沸。小玻璃管有利于降低周围环境对温度计读数可 能造成的波动。
无水乙醇(分析纯)
四、实验步骤
1.开启供折射仪使用的超级恒温槽,调节温度控 制器,使达到实验所需温度。 2.如上图所示,将干燥的沸点仪安装好。检查 带有温度计的软木塞是否塞紧,电热丝要靠近烧 瓶底部的中心。温度计水银球的位置应处在支管 之下,但至少要高于电热丝2cm。 3.在干燥的蒸馏瓶中倒入适量的纯乙醇液体, 液面约在支管口下1cm左右,安放电热丝及温度 计(注 意两者不要接触,使两者浸入液体中)。接好冷 凝管,通入冷水。接通电源,徐徐旋转调压器转 盘,控制 电压≤20V,开始电压可稍高些,使液体加热至沸 腾之后再调电压至合适的大小,使之保持微沸, 并使冷凝液回流速度不要太快,1~2s内1滴为宜。
水 乙二醇的性能与使用注意事项
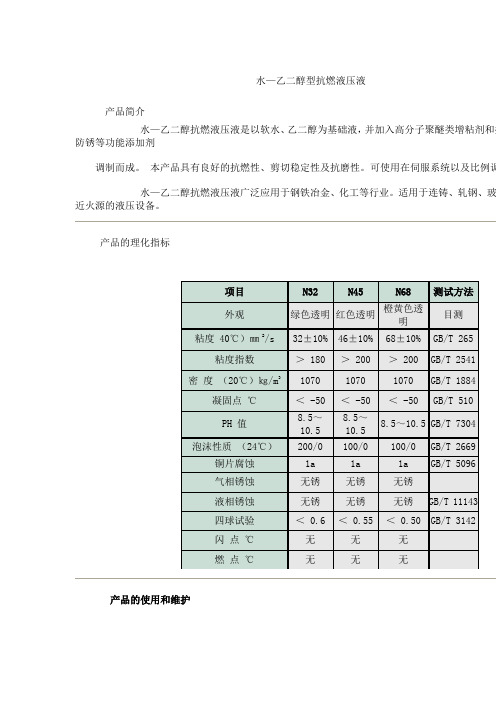
水—乙二醇型抗燃液压液产品简介水—乙二醇抗燃液压液是以软水、乙二醇为基础液,并加入高分子聚醚类增粘剂和抗磨、等功能添加剂调制而成。
本产品具有良好的抗燃性、剪切稳定性及抗磨性。
可使用在伺服系统以及比例调节水—乙二醇抗燃液压液广泛应用于钢铁冶金、化工等行业。
适用于连铸、轧钢、玻璃成型的液压设备。
产品的理化指标项目N32N45N68测试方法外观绿色透明红色透明橙黄色透明目测粘度40℃)㎜2/s 32±10% 46±10% 68±10% GB/T 265 粘度指数> 180 > 200 > 200 GB/T 2541 密度(20℃)㎏/m31070 1070 1070 GB/T 1884 凝固点℃ < -50 < -50 < -50 GB/T 510PH 值8.5~10.58.5~10.58.5~10.5 G B/T 7304泡沫性质(24℃)200/0 100/0 100/0 GB/T 2669铜片腐蚀1a 1a 1a GB/T 5096气相锈蚀无锈无锈无锈液相锈蚀无锈无锈无锈GB/T 11143四球试验< 0.6 < 0.55 < 0.50 GB/T 3142闪点℃ 无无无燃点℃ 无无无产品的使用和维护◆准备工作在设计和旧设备选用水—乙二醇抗燃液压液时,应考虑如下问题,并使液压系统适应水醇抗燃液压液的要求。
材质要求:水—乙二醇抗燃液压液属碱性物质,材料的适应性一表中列出部份金属,在会产生化学反应,系统中不能使用,表中不相容的过滤材料和密封材料也不能使用。
液压泵要求:柱塞泵、齿轮泵、螺杆泵、离心泵、往复泵、叶片泵均可使用。
考虑到磨单作用叶片泵,不平衡型重负荷滚动轴承的使用,应与本公司取得联系。
因水——乙二醇抗燃液压液的比重较矿物油高,故在设计时应考虑泵的功率,一般应按的 70%考虑。
过滤器要求:为防止泵抽空造成流量,压力不稳和泵的磨损,泵入口应选用粗过滤器(目),出口选用10~25μm的精滤器。
GBT 14571.2-93 二乙二醇和三乙二醇的测定方法

GBT 14571工业用乙二醇中二乙二醇和三乙二醇含量的测定气相色谱法GB/T 14571.2-93Monoethylene glycol for industrial use-Determination of diethylene glycol and triethyleneglycol - Gas chromatographic method主题内容与适用范畴本标准规定了工业用乙二醇中二乙二醇和三乙二醇含量的测定的气相色谱法。
本方法适用于工业用乙二醇中二乙二醇和三乙二醇含量的测定,其最小检测浓度分别为0.01%和0.02%。
引用标准GB/T 6680液体化工产品采样通则方法原理试样通过微量注射器注入,并被载气带入色谱柱,使各组分得到分离,用氢火焰离子化检测器检测。
采纳外标法运算二乙二醇和三乙二醇的含量。
必要时也可用内标法定量(见附录A)。
材料及试剂4.1载气:高纯氮气或氦气,纯度大于99.999%。
4.2辅助气:4.2.1氢气,纯度大于99.99%。
4.2.2空气,经硅胶及5A分子筛干燥、净化。
4.3固定液:聚乙二醇-20M。
4.4载体:Chromosorb W AW—DMCS,粒径为0.149~0.1 77mm(80~100目)或其他性能类似的载体。
4.5乙二醇:商品乙二醇径减压蒸馏提纯,收集中间30%的馏分备用。
该馏分按本标准规定条件进行分析,应检不出二乙二醇和三乙二醇。
4.6二乙二醇和三乙二醇,纯度应大于99%(必要时可按4.5条所述进行提纯)。
仪器为配有分流装置及氢火焰离子化检测器的气相色谱仪,该色谱仪对本标准规定最小检测浓度的二乙二醇和三乙二醇所产生的峰高应至少大于仪器噪声的两倍。
5.1汽化室:应配置石英或玻璃内衬管。
5.2色谱柱:举荐的色谱柱及其典型操作条件见表1。
能达到同等分离效能的其他色谱柱也可使用。
5.3记录装置:记录仪、积分仪或色谱数据处理机。
5.4微量注射器1或10μL。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
乙二醇及其水溶液二元体系理化性能数据的测定
乙二醇是一种重要的有机化合物,在现代化工领域非常重要。
为了研究其理化性能,采用乙二醇及其水溶液二元体系开展实验,检测其活化能、折射率、保温性等数据,为进一步的应用提供保障。
从理论上讲,乙二醇具有很强的溶解能力,溶解度取决于温度和其他因素,在实验中,需要把它与普通的水进行混合,以获得水溶液二元体系,检测所得的活化能,折射率和保温性参数,以揭示其理化性能特征。
实验当中,采用常规设备,如HR-GC、HR-GC/MS、粒度分析仪等,对乙二醇及其水溶液二元体系的理化性能特征进行测定分析,由于其优良的性质,它的测定结果以最高精度与准确度呈现,表现出易操作、快速可靠等特点。
总而言之,采用乙二醇及其水溶液二元体系理化性能数据测定,不仅可以有效研究开发化工新产品,还可以评估溶剂材料的性能特征,从而使有效利用其特殊功能,是现代化工领域获得科学研究成果及快速发展提供了可靠的技术依据。
