2019年精选高中化学选修6 实验化学实验2-5 乙酸乙酯的制备及反应条件探究人教版习题精选第八十八篇
实验2-5乙酸乙酯的制备及反应条件的探究
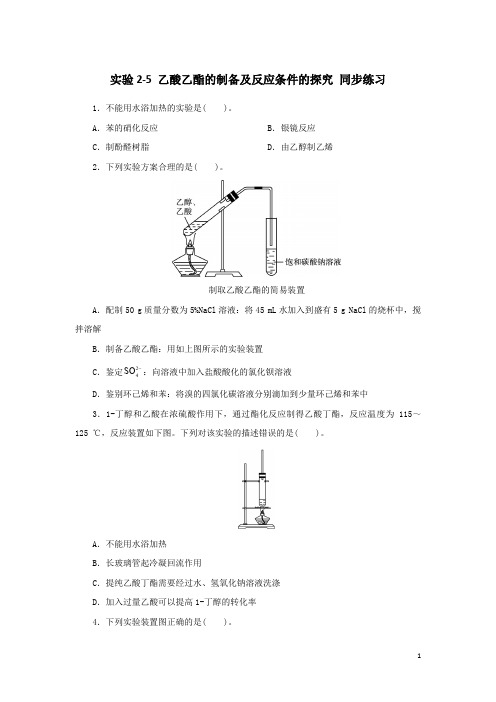
实验2-5 乙酸乙酯的制备及反应条件的探究同步练习1.不能用水浴加热的实验是( )。
A.苯的硝化反应B.银镜反应C.制酚醛树脂D.由乙醇制乙烯2.下列实验方案合理的是( )。
制取乙酸乙酯的简易装置A.配制50 g质量分数为5%NaCl溶液:将45 mL水加入到盛有5 g NaCl的烧杯中,搅拌溶解B.制备乙酸乙酯:用如上图所示的实验装置SO :向溶液中加入盐酸酸化的氯化钡溶液C.鉴定24D.鉴别环己烯和苯:将溴的四氯化碳溶液分别滴加到少量环己烯和苯中3.1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125 ℃,反应装置如下图。
下列对该实验的描述错误的是( )。
A.不能用水浴加热B.长玻璃管起冷凝回流作用C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤D.加入过量乙酸可以提高1-丁醇的转化率4.下列实验装置图正确的是( )。
5.油脂皂化后,使肥皂和甘油从混合液里面充分分离,可以采用:(1)分液、(2)蒸馏、(3)过滤、(4)盐析、(5)渗析,组合正确的是( )。
A.(1)(2) B.(3)(4) C.(4)(3)(2) D.(3)(2)(5) 6.以下实验能获得成功的是( )。
A.用乙醇和乙酸混合共热制取乙酸乙酯B.将铁屑、溴水、苯混合制溴苯C.在苯中滴入浓硝酸制硝基苯D.将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色7.酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、黏合剂及印刷、纺织等工业。
乙酸乙酯的实验室和工业制法常采用如下反应:CH3COOH+C2H5OH CH3COOC2H5+H2O请根据要求回答下列问题:(1)欲提高乙酸的转化率,可采取的措施有________________、________________等。
(2)若用下图所示装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为____________________、________________________等。
2.2物质的制备第2课时乙酸乙酯的制备及反应条件探究氢氧化铝的制备课件(人教版选修6)

解析:浓硫酸与其它液体混合时,通常将浓硫酸 加入到其它液体中;在乙酸乙酯制取中,饱和 Na2CO3溶液能够降低酯在水中的溶解度、除去酯 中混有的乙酸和乙醇。 答案: (1) 浓 H2SO4 慢慢倒入乙醇和乙酸的混合溶 液中 (2)降低酯在水中的溶解度,除去酯中混有的乙酸 和乙醇以利于分层 (3)小 水果香 (4)乙醚
2.实验步骤 乙醇 ,然后边振荡边缓慢加 在试管中加入3 mL_____ 浓硫酸 和2 mL______ 乙酸 。连接仪器,用 入2 mL_________ 酒精灯缓慢加热,将产生的气体经导管通到 饱和碳酸钠 溶液的液面上。反应停止后,用 ______________ 直尺测量有机层的厚度。 3.实验现象 无色油状 液 Na2CO3 饱和溶液的液面上有透明的 _________ 体产生,并可闻到______ 香味 。
解析:选 D。以上5种物质均既能与强酸反应,又 能与强碱溶液反应。如: NaHCO3 与盐酸可以反 应生成氯化钠、水、二氧化碳气体,与氢氧化钠 溶液反应生成正盐 ( 碳酸钠 ) 和水; (NH4)2S 与盐酸 反应生成H2S气体和氯化铵,与氢氧化钠溶液反应 生成硫化钠和氨水; Al2O3 、 Al(OH)3 都是两性物 质, Al 在金属中也具有特殊性,既能与强酸反应, 又能与强碱溶液反应。
思考感悟
2.用强碱氢氧化钠溶液和可溶性铝盐或用强酸硫
酸溶液和可溶性偏铝酸盐反应制取Al(OH)3可以吗?
为什么?
【提示】 不可以,因为氢氧化铝溶于强酸、强
碱,在操作过程中加入的NaOH或H2SO4有可能过 量,造成生成的Al(OH)3溶解而损失。
自主体验
1 .下列物质中既能跟稀盐酸反应,又能跟氢氧 化钠溶液反应的是( ) ①NaHCO3 ②(NH4)2S ③Al2O3 ④Al(OH)3 ⑤Al A.③④ B.③④⑤ C.①③④⑤ D.全部
人教版高中化学选修6第二单元 实验2-5 乙酸乙酯的制备及反应条件的探究 同步测试

人教版高中化学选修6第二单元实验2-5 乙酸乙酯的制备及反应条件的探究同步测试一、单选题(共10题;共20分)1.在西安一座西汉古墓中出土了50多斤西汉时期的古酿,当开启酒坛的封口时,散发出的香味把在场的品酒师都醉倒了,这些酒深藏地下历经两千年,不仅没有变质,反而变得香气更浓.这种香味是由哪种物质引起的()A. 乙醇B. 乙酸C. 乙酸乙酯D. 乙醛2.某有机物X能发生水解反应,水解产物为Y和Z.Y和Z的相对分子质量相同,化合物X可能是()A. 甲酸乙酯B. 甲酸丙酯C. 乙酸甲酯D. 乙酸乙酯3.下列有机物的酸性由强到弱排列正确的是()A. 碳酸、甲酸、乙酸、苯酚B. 乙酸、甲酸、碳酸、苯酚C. 甲酸、碳酸、乙酸、苯酚D. 甲酸、乙酸、碳酸、苯酚4.丙酸钠是常用的防腐剂之一,该物质可以由丙酸与烧碱反应制得.下面有关丙酸和丙酸钠的说法中不正确的是()A. 丙酸有多种同分异构体B. 丙酸与乙酸互为同系物C. 检验一种添加剂是丙酸钠还是氯化钠可以用pH试纸D. 丙酸分子中三个碳原子和两个氧原子一定在同一个平面上5.某酯A,其分子式C6H12O2,已知又知B、C、D、E均为有机物,D不与Na2CO3溶液反应,E不能发生银镜反应,则A结构可能有()A. 3种B. 4种C. 5种D. 6种6.下列物质中,属于饱和一元脂肪酸的是()A. 乙二酸B. 苯甲酸C. 硬脂酸D. 石炭酸7.下列有机物中,易溶于水的是()A. 乙酸B. 溴乙烷C. 四氯化碳D. 乙酸乙酯8.人剧烈运动时,骨骼肌组织会供氧不足,导致葡萄糖无氧氧化,产生大量酸性物质(分子式为C3H6O3),如果该物质过度堆积于腿部,会引起肌肉酸痛.体现该物质酸性的基团是()A. 羟基B. 甲基C. 乙基D. 羧基9.下面是4种有机弱酸,强弱顺序为:下列说法中不正确的是()A. 等浓度等体积的4种酸中和碱的能力:B. 等浓度的4种酸溶液中水电离出的c水(H+):>CH2ClCOOH>>CHCl2COOHC. 反应+2CH2ClCOO﹣→ +2CH2ClCOOH一定能够发生D. 由题中信息可推知酸性:CH2FCOOH>CH2ClCOOH10.下列说法正确的是()A. 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OHB. 乙酸乙酯和食用植物油均能水解生成乙醇C. 乙酸乙酯、油脂与NaOH溶液反应均有醇生成D. 能与NaOH溶液发生反应,分子式为C2H4O2的有机化合物一定是羧酸二、填空题(共3题;共14分)11.A、B两种有机物的分子式均为C6H12O2,A水解后得到C和D,C能发生银镜反应,D不能发生消去反应;B水解后得到E和F,F不能氧化产生E,但其同分异构体经氧化后可得E.请判断:(1)A的结构简式 ________ B的结构简式 ________(2)写出C发生银镜反应的方程式 ________12.羧酸的 ________反应的逆反应是 ________的水解反应.在无机酸存在下,该水解反应的产物为 ________;在碱存在下,该水解反应的产物为 ________.酸存在下水解反应的程度 ________碱存在下水解反应的程度,这是因为 ________13.甲酸具有下列性质:①挥发性②酸性③比碳酸的酸性强④还原性⑤能发生酯化反应下列各实验中,分别填出表现甲酸相应性质的编号:(1)在碳酸钠溶液中加入甲酸有气体放出,说明甲酸具有 ________;(2)在甲酸钠晶体中加入浓磷酸,加热后放出能使湿润蓝色石蕊试纸变红的气体,说明甲酸具有 ________;(3)与乙醇、浓硫酸混和后共热,能闻到一种香味,说明甲酸具有 ________;(4)在甲酸溶液中加入氢氧化铜,能看到溶液变蓝色,说明甲酸具有 ________;(5)在新制氢氧化铜中加入甲酸溶液,加热看到有红色沉淀生成,说明甲酸具有 ________三、实验探究题(共1题;共5分)14.乙酸乙酯是重要的化工原料,沸点约77℃.其水解反应方程式为:CH3COOC2H5+H2O⇌CH3COOH+C2H5OH,酸和碱均可用作该反应的催化剂.某兴趣小组对NaOH溶液催化乙酸乙酯水解进行了探究.实验步骤:向试管中加入8mLNaOH溶液,再加入2mL乙酸乙酯,用直尺量出乙酸乙酯的高度.再把试管放入70℃的水浴中,每隔1min将其取出,振荡,静置,立即测量并记录剩余酯层的高度.再迅速放回水浴中继续加热,如此反复进行.改变NaOH溶液浓度,重复实验.数据记录:乙酸乙酯水解后剩余的高度/min回答下列问题:(1)完成上述对比实验时,每组实验都必须控制不变的因素有________(2)分析上述数据,得到乙酸乙酯水解速率的结论是:①________.②乙酸乙酯水解速率先快后慢,一段时间后达到平衡状态.(3)结论②的理论解释是________(4)欲使乙酸乙酯完全水解,可采取的措施是________(5)有同学认为有必要用蒸馏水代替NaOH溶液重复试验,对数据进行修正,主要原因是________四、综合题(共2题;共20分)15.有以下一系列反应,最终产物为乙二酸。
人教版化学高二选修6第二单元实验2-5乙酸乙酯的制备及反应条件探究同步练习D卷

人教版化学高二选修6第二单元实验2-5乙酸乙酯的制备及反应条件探究同步练习D卷姓名:________ 班级:________ 成绩:________一、选择题 (共20题;共40分)1. (2分) 1﹣丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如图.下列对该实验的描述错误的是()A . 控制温度不可以用水浴加热B . 长玻璃管起冷凝回流作用C . 提纯乙酸丁酯需要经过氢氧化钠溶液洗涤D . 加入过量乙酸可以提高1﹣丁醇的转化率2. (2分)(2018·海南) 实验室常用乙酸与过量的乙醇在浓硫酸催化下合成乙酸乙酯。
下列说法正确的是()A . 该反应的类型为加成反应B . 乙酸乙酯的同分异构体共有三种C . 可用饱和的碳酸氢钠溶液鉴定体系中是否有未反应的乙酸D . 该反应为可逆反应,加大乙醇的量可提高乙酸的转化率3. (2分) (2018高二上·怀柔期末) 以下说法正确的是:()A . 制备乙酸乙酯的实验中,盛接酯的小试管中盛放了一定量的氢氧化钠溶液B . 实验室制乙烯时应将无水乙醇缓慢加入到浓硫酸中C . 在酸性重铬酸钾溶液中加入少量乙醇,橙色溶液变红D . 为减缓反应速率,将饱和食盐水滴加到烧瓶中的电石上来制取乙炔4. (2分) (2017高三上·汕头期中) 下列与实验相关的叙述正确的是()A . 用苯萃取溴水中的Br2时,有机层从分液漏斗的下端放出B . 检验溶液中是否含有SO42﹣,依次滴入Ba(NO3)2溶液和稀盐酸C . 配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出D . 配制AlCl3溶液时,将AlCl3溶解在较浓的盐酸中,再用水稀释到所需浓度5. (2分)下面哪个图是以乙酸(沸点:118℃)、浓硫酸和乙醇(沸点:78.5℃)为原料合成乙酸乙酯(沸点:77℃)的最佳装置()A .B .C .D .6. (2分)现由含硫酸镁和泥沙的粗食盐提纯氯化钠,可将粗食盐溶于水,然后进行下列操作:①过滤②加过量氢氧化钠溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液⑥蒸发结晶.正确的操作顺序是()A . ②④⑤①③⑥B . ⑤④②①③⑥C . ⑤④②③①⑥D . ②④⑤③①⑥7. (2分) (2018高二下·北京期中) 下列说法错误的是()A . 顺-2-丁烯和反-2-丁烯的加氢产物不同B . 用重结晶的方法提纯苯甲酸时应趁热过滤C . 邻二甲苯只有一种结构能说明苯分子的结构中,碳碳键不是单、双键交替的事实D . 的结构中含有酯基8. (2分)既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的乙烯,得到纯净乙烷的方法是()A . 与足量溴蒸气反应B . 通入足量溴水中C . 在一定条件下通入氢气D . 分别进行燃烧9. (2分)下列实验基本操作中,正确的是()A . 倾倒液体B . 过滤C . 加热液体D . 熄灭酒精灯10. (2分)设计学生实验要注意安全、无污染、现象明显。
人教版化学高二选修6第二单元实验2-5乙酸乙酯的制备及反应条件探究同步练习B卷

人教版化学高二选修6第二单元实验2-5乙酸乙酯的制备及反应条件探究同步练习B卷姓名:________ 班级:________ 成绩:________一、选择题 (共20题;共40分)1. (2分)实验室用图所示的装置制取乙酸乙酯,下列说法正确的是()A . 向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加冰醋酸B . 用CH3CH218OH与乙酸反应制取乙酸乙酯,18O 存在于水中C . 试管b中的液体是饱和NaHCO3溶液D . 实验时加热试管a的目的之一是及时将乙酸乙酯蒸出,使平衡向生成乙酸乙酯的方向移动2. (2分)下列说法不正确的是()A . 利用地沟油制肥皂的实验中,可以用玻璃棒蘸取反应液滴入有热水的试管中,振荡,若无油滴浮在液面上,说明反应液中的地沟油已完全皂化B . 制备乙酸乙酯时试剂添加的顺序为乙酸、浓硫酸和乙醇,同时为了防暴沸可以添加少量碎瓷片或小火均匀加热C . 可以利用溶液褪色的快慢来判断不同温度下同体积0.10mol•L﹣1酸性KMnO4溶液与0.01mol•L﹣1草酸稀溶液反应的快慢D . 燃料电池实验中,用KNO3 溶液或Na2SO4溶液代替蒸馏水,效果要好得多3. (2分) (2018高三上·海淀期末) 某同学利用右图所示装置制备乙酸乙酯。
实验如下:()① 向浓H2SO4乙醇混合液中滴入乙酸后,加热试管A② 一段时间后,试管B中红色溶液上方出现油状液体③ 停止加热,振荡试管B,油状液体层变薄,下层红色溶液褪色④ 取下层褪色后的溶液,滴入酚酞后又出现红色结合上述实验,下列说法正确的是A . ①中加热利于加快酯化反应速率,故温度越高越好B . ③中油状液体层变薄主要是乙酸乙酯溶于Na2CO3溶液所致C . ③中红色褪去的原因可能是酚酞溶于乙酸乙酯中D . 取②中上层油状液体测其,共有3组峰4. (2分) (2015高一上·德州月考) 除去下列物质中含有的少量杂质(括号中的物质)的方法,错误的是()A . NH4Cl溶液(I2)用CCl4萃取B . NO(NH3)通过水洗涤C . NaCl(NH4Cl)加热固体混合物D . N2(NO2)通过水洗涤5. (2分) (2016高二下·通榆期中) 1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~l25℃,反应装置如图.下列对该实验的描述错误的是()A . 不能用水浴加热B . 长玻璃管起冷凝回流作用C . 提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤D . 加入过量乙酸可以提高1﹣丁醇的转化率6. (2分) (2016高一下·汕头期末) 下列说法不正确的是()A . 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出B . 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口下沿处C . 蒸发结晶时应将溶液蒸干D . 能用CCl4从碘水中萃取碘是由于CCl4与H2O互不相溶且碘在CCl4中溶解度比在水中的大7. (2分)利用组成物质的原子、离子或分子的一些特征性质,检验组成化学物质的元素,是研究物质组成的常用方法。
《实验2-5 乙酸乙酯的制备及反应条件的探究》教学设计(湖北省市级优课)

《乙酸乙酯的制备》说课稿各位评委,各位同仁:大家上午好!我说课的题目是——《乙酸乙酯的制备》,下面我将从以下六个部分进行说课。
一、教材分析1、教材地位:本实验选自人教版高中化学必修二第三章的第三节《乙酸》的性质,也是普通高中课程标准实验探究活动的内容。
本节课以学生所学有机化合物常识为基础,提倡学生的生活经验出发,在介绍了有机物-乙醇、乙酸基础上引入的,通过本节的探究学习,既巩固前面所学的知识,也为以后学习更复杂的有机合成打下基础,通过实验能培养学生的探究能力、操作能力、观察能力、分析能力等。
本节有着承上启下的作用,是有机化学中的有机合成方法重点之一,也是高考重要考点,2018年高考单独一选择题考到。
2、教材内容:现有教材采用传统方法,以乙醇和乙酸为原料,浓硫酸为催化剂来制备乙酸乙酯。
该方法经学生讨论存在以下缺陷:直接用酒精灯加热不易控制反应温度,易产生副反应使乙酸乙酯收率低;浓硫酸具有强腐蚀性,增加了学生实验的危险性等。
因此,从绿色化学的角度出发,本实验将从装置的创新和催化剂的广泛性上进行探究,以乙酸和乙醇为原料制备乙酸乙酯。
3、实验原理:酯化反应指的是在少量酸催化下,羧酸和醇反应生成酯。
质子(H+)是反应中的催化剂,能提供H+催化剂的有质子酸和路易斯酸。
质子酸有硫酸、盐酸、硝酸、磷酸、硫酸氢钠等,路易斯酸包括铁盐、铝盐等。
二、教学目标在与教材传统方法的对比归纳指导下:1、采用控制变量法,探究制备乙酸乙酯的装置的改进和催化剂的广泛性。
2、通过学生设计实验,并对教材实验装置和原理存在缺陷的思考,联系生活实际,拓宽学生的思维宽度,提升学生的思维深度。
3、通过师生交流合作,激发学生学习化学的热情,体验化学来源于生活并服务于生活的科学情感,充分发挥学生的主体作用。
三、学情分析本节课的主要针对高二的学生,在心理认知方面,学生兴趣(直觉—操作—认知)逐步迁移,渴望探究性体验;在理论实验技能方面,对乙醇、乙酸等有机物有一定的认识,具备一定的实验技能、分析推理能力。
实验2-5乙酸乙酯的制备及反应条件探究课件
乙醇
易溶
0.789 -117.3 78.5
乙酸乙酯 难溶
0.894 -83.6 77.1
乙醚
难溶 0.7134 -116.3
34.6
基础 回顾
1.反应原理:
2.反应特点:
2.原理分析
O CH3-C-OH +H-O-C2H5
浓H2SO4 △
O CH3-C-O -C2H5 +H2O
取代反应 反应速率很慢
密度/g·cm-3 1.2659 1.05
0.789
熔点/℃
122 -34.6 -117.3
沸点/℃
249 212.6 78.5
制取苯甲酸乙酯能否使用制取乙酸乙酯的简易装置?
原料乙醇的沸点低于苯甲酸乙酯的沸点,若使用制备乙酸 乙酯的产生装置,会使原料乙醇大量蒸馏出去,实验效率 大大降低。
(一)控制反应条件避免损失 1.三颈烧瓶+冷凝回流+反应温度指导
加热温度以溶液 刚好回流为宜!(一)控制反应条件避免损失
2.恒压滴液漏斗+分批滴加+搅拌器+水浴加热+延长时 间 恒压滴液漏斗 滴速过快可能造反应温度降落过快或
放热反应升温过快
搅拌器+延长回流时间 使原料反应更充分 分批滴加 原料利用率更高
水浴加热 温度控制更精确
(一)控制反应条件避免损失
2.恒压滴液漏斗+分批滴加+搅拌器+水浴加热+延长时 间
类型
规律 酸脱羟基醇脱氢
酯化 反应
速率 平衡 反应可逆、产率低
3.如何“多快好省”的提高乙酸乙酯的产率,措施有哪些 快(速率角度):浓硫酸作催化剂并加热 多(平衡角度):增加乙醇的量(更经济)、浓硫酸吸水、加 热蒸出乙酸乙酯等,促使平衡正向移动,提高产率。
高中化学 2.2.2乙酸乙酯的制备及反应条件探究每课一练 新人教版选修6
2.2.2 乙酸乙酯的制备及反应条件探究每课一练(人教版选修6)[基础过关]一、乙酸乙酯的性质1.炒菜时,往往加入一些料酒和食醋,这样可使菜变得味香可口,你认为其中的原因是( ) A.有盐类物质生成B.有酸类物质生成C.有醇类物质生成D.有酯类物质生成2.用分液漏斗可以分离的一组液体混合物是 ( ) A.溴乙烷和乙醇B.乙酸乙酯和乙酸C.溴苯和水D.乙醇和水3.酯类物质广泛存在于香蕉、梨等水果中。
某实验小组从梨中分离出一种酯,然后将分离出的酯水解,得到了乙酸和另一种化学式为C6H13OH的物质。
以下分析不正确的是( ) A.C6H13OH分子中含有羟基B.C6H13OH可与金属钠发生反应C.实验小组分离出的酯可表示为CH3COOC6H13D.不需要催化剂,这种酯在水中加热即可大量水解二、乙酸乙酯的制备4.若乙酸分子中的氧都是18O,乙醇分子中的氧都是16O,二者在浓H2SO4作用下发生反应,一段时间后,分子中含有18O的物质有 ( ) A.1种B.2种C.3种D.4种5.如图在试管甲中先加入2 mL 95%的乙醇,并在振荡下缓慢加入2 mL浓硫酸,充分摇匀,冷却后再加入2 g无水乙酸钠(CH3COONa)。
将试管甲固定在铁架台上,在试管乙中加入5 mL饱和碳酸钠溶液,按图连接好装置进行实验,当试管乙中有明显现象时停止实验。
试回答:(1)实验时,应对试管甲缓慢加热,其目的是____________________________________________________________________________________________________________。
(2)写出试管甲中发生反应的化学方程式:______________________________________________________________________________________________________________。
《实验2-5 乙酸乙酯的制备及反应条件的探究》教学设计(广东省县级优课)
乙酸乙酯的制备教学设计一、教学目标知道乙酸乙酯的物理性质和分子结构。
知道酯化反应的概念通过乙酸乙酯的制备实验,培养独立思考、分析现象的能力激发学生的学习兴趣和求知欲,培养学生更好的科学作风和求实进取的优良品质,培养学生勇于探索的科学精神。
二、教学重点和难点重点、难点:乙酸的酯化反应三、教学方法:联系实际生活,演示实验六、教学流程【实验探究】乙酸乙酯的制备药品:碎瓷片仪器:试管乙醇 3mL 铁架台浓硫酸 2mL 导管乙酸 2mL 酒精灯饱和的Na2CO3溶液胶头滴管录制好实验后,反复播放让【学生思考】1、装药品的顺序如何?2、碎瓷片的作用是什么?3、浓硫酸的作用是什么?4、得到的实验产物是否纯净?主要杂质是什么?5、饱和碳酸钠溶液的作用是什么?6、导管为什么要高于液面?7、从刚才得实验中,我们观察到了什么现象?【叙述】这种无色的液体我们称为乙酸乙酯,我们一起来写一下这个反应的化学方程式。
【板书】【叙述】我们可以知道乙酸和乙醇反应生成了乙酸乙酯和水,我们就把这种酸跟醇起作用,生成酯和水的反应称为酯化反应。
不仅仅乙酸和乙醇能发生酯化反应,其他的酸和醇之间也能发生酯化反应【应用】在我们生活中,醋能够解酒,其原因是什么?【板书设计】乙酸的酯化反应酯化反应:酸跟醇起作用,生成酯和水的反应称为酯化反应1818O O CH 3—C —OH+H —O —C 2H CH 3—C —O —C 2H 5+ H 2O 1818O OCH 3—C —OH+H —O —C 2H CH 3—C —O —C 2H 5+ H 2O。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
最新教育资料精选
1 / 9
2019年精选高中化学选修6 实验化学实验2-5 乙酸乙酯的制备及反应条件探究
人教版习题精选第八十八篇
第1题【单选题】
分子式为C9H18O2的有机物A有下列变化关系( )
其中B、C的相对分子质量相等,则A的可能结构有
A、9种
B、8种
C、7种
D、6种
【答案】:
【解析】:
第2题【单选题】
白蚁分泌的蚁酸的化学性质与盐酸相似,能腐蚀很多建筑材料.下列材料中最不容易被白蚁蛀蚀的是
( )
A、钢
B、铜
C、大理石
最新教育资料精选
2 / 9
D、生铁
【答案】:
【解析】:
第3题【单选题】
下列说法正确的是( )
A、在酸性条件下,CH3CO^18OC2H5的水解产物是CH3CO^18OH和C2H5OH
B、乙酸乙酯和食用植物油均能水解生成乙醇
C、乙酸乙酯、油脂与NaOH溶液反应均有醇生成
D、能与NaOH溶液发生反应,分子式为C2H4O2的有机化合物一定是羧酸
【答案】:
【解析】:
第4题【单选题】
在西安一座西汉古墓中出土了50多斤西汉时期的古酿,当开启酒坛的封口时,散发出的香味把在场的
品酒师都醉倒了,这些酒深藏地下历经两千年,不仅没有变质,反而变得香气更浓.这种香味是由哪种物
质引起的( )
A、乙醇
B、乙酸
C、乙酸乙酯
最新教育资料精选
3 / 9
D、乙醛
【答案】:
【解析】:
第5题【单选题】
下列有关说法正确的是( )
A、2,2﹣二甲基丁烷与2,4﹣二甲基戊烷的一氯代物种类相同
B、乙烷、苯、葡萄糖溶液均不能使酸性高锰酸钾溶液褪色
C、苯的密度比水小,但由苯反应制得的溴苯、硝基苯、环己烷的密度都比水大
D、乙酸乙酯在碱性条件下的水解反应称为皂化反应
【答案】:
【解析】:
第6题【单选题】
下列与有机物的结构、性质有关的叙述中正确的是( )
A、在酸性条件下,CH3CO^18OC2H5的水解产物是CH3CO^18OH和C2H5OH
B、甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应
C、分子式为C5H12O且可与金属钠反应放出氢气的有机物有8种(不考虑立体异构)
D、乙醇、乙酸均能与Na反应放出H2 , 二者分子中官能团相同
最新教育资料精选
4 / 9
【答案】:
【解析】:
第7题【单选题】
有机物具有下列性质:能发生银镜反应,滴入石蕊试液不变色,加入少量碱液并滴入酚酞试液,共煮
后红色消失.原有机物是下列物质中的( )
A、甲酸乙酯
B、乙酸甲酯
C、乙醛
D、甲酸
【答案】:
【解析】:
最新教育资料精选
5 / 9
第8题【单选题】
分子式为C10H20O2的酯在酸性条件下水解,所得酸A和醇B,且B经氧化可得A。符合此条件的酯的
同分异构体数目为 ( )
A、4
B、8
C、16
D、32
【答案】:
【解析】:
第9题【单选题】
下列物质中,属于饱和一元脂肪酸的是( )
A、乙二酸
B、苯甲酸
C、硬脂酸
D、石炭酸
【答案】:
【解析】:
最新教育资料精选
6 / 9
第10题【单选题】
增塑剂DCHP可由环已醇制得。环已醇和DCHP的结构简式如图所示,下列说法正确的是( )
A、DCHP的分子式为C20H14O4
B、环已醇和DCHP的二氯代物均有4种
C、1molDCHP水解时消耗2molNaOH
D、环己醇分子中的所有碳原子可能共平面
【答案】:
【解析】:
第11题【单选题】
下列烃的衍生物可以发生加成反应的是( )
A、乙醛
B、乙酸
C、乙醇
D、乙酸乙酯
最新教育资料精选
7 / 9
【答案】:
【解析】:
第12题【单选题】
下列有机物的酸性由强到弱排列正确的是( )
A、碳酸、甲酸、乙酸、苯酚
B、乙酸、甲酸、碳酸、苯酚
C、甲酸、碳酸、乙酸、苯酚
D、甲酸、乙酸、碳酸、苯酚
【答案】:
【解析】:
第13题【填空题】
A、B两种有机物的分子式均为C6H12O2 , A水解后得到C和D,C能发生银镜反应,D不能发生消
去反应;B水解后得到E和F,F不能氧化产生E,但其同分异构体经氧化后可得E.请判断:
(1)A的结构简式______ B的结构简式______
(2)写出C发生银镜反应的方程式______
【答案】:
最新教育资料精选
8 / 9
【解析】:
第14题【填空题】
已知硬脂酸C17H35COOH为饱和高级脂肪酸,硬脂酸甘油酯在碱性条件下发生水解反应.
(1)该油脂能否使溴水褪色:______(填“能”或“不能”).
(2)写出该油脂在NaOH热溶液中水解的几种产物的结构简式______
【答案】:
【解析】:
最新教育资料精选
9 / 9
第15题【填空题】
甲、乙、丙三人分别将乙酸与乙醇反应得到的酯提纯.在未用指示剂的情况下,他们都是先加入NaOH
溶液中和过量的酸,然后用蒸馏法将酯分离出来.但他们的结果却不同:
①甲得到了不溶于水的中性酯②乙得到显酸性的酯的混合物③丙得到大量水溶性物质,试分析产生
上述各种结果的原因.
①______②______③______
【答案】:
【解析】:
