吡啶双恶唑啉配体的制备新方法
恶唑类化合物的合成方法综述之欧阳数创编

第一章:噁唑类化合物的合成方法综述1.引言:含有两个杂原子且其中一个杂原子为N的五元环体系叫唑,数目很多。
根据杂原子在环中位置不同,有可分为1,2唑和1,3唑。
五元环中杂原子为N、O的化合物是噁唑类化合物,其种类较多,有噁唑(1)、噁唑啉(2)、噁唑烷(3)、噁唑酮、苯并噁唑(4)等。
噁唑类化合物是一类重要的杂环化合物,一些具有噁唑环的化合物具有生物活性[1]。
例如2氨基噁唑具有杀真菌、抗菌、抗病毒作用[2]。
同时它们在中间体、药物合成中也具有广泛的用途[3,4,5]。
分子结构中含有噁唑环的聚苯并噁唑(5)是耐高温的高聚物[6]。
噁唑(1)是1,3位含有O、N原子的五元环,为有像吡啶一样气味且易溶于水的液体,是非常稳定的化合物,它在热的强酸中很稳定,不发生自身氧化反应,不参与任何的正常的生物化学过程。
其二氢和四氢杂环化合物叫做噁唑啉或4,5-二氢唑啉(2)和噁唑烷或四氢噁唑啉(3)。
虽然噁唑环这个名称还是Hantzsch在1887[1]年确定的,但一向没有人作过大量深入的研究,因为这个环系不常见于天然产物中,而且制备也相当困难。
直到青霉素的出现,才推动了噁唑的研究。
青霉素本身虽没有噁唑环,但它最初是疑为是属于这个环系的。
青霉素实际含有一个噻唑环,而噁唑是噻唑的氧的类似物。
因为青霉素是一个很重要的药品,研究的范围也由噻唑推广到了噁唑。
下面我们就将噁唑类化合物的合成方法进行综述。
2.合成方法噁唑类化合物可由提供N,O原子的化合物来合成。
2.1.Cornforth法合成噁唑环1947年由Cornforth等人首次合成第一个含有噁唑环的化合物[7]。
其过程如下:据此设计合成噁唑4羧酸乙酯的路线如下[7]。
2.2. 碱催化酰氨基磺酰烯关环合成法用3酰氨基2碘1苯磺酰烯在碱催化下关环可得到噁唑化合物[8]。
2.3.由西佛碱氧化法合成在温和的反应条件下,用二醋酸碘苯作氧化剂可以以良好产率将西佛碱氧化生成2芳基5甲氧基噁唑化合物[9]。
2-乙醇吡啶的制备

2-乙醇吡啶的制备
乙醇吡啶是一种常用的有机合成试剂,其制备通常有两种方法:
1. 通过乙醇和吡啶的反应制备。
将一定量的吡啶溶解在乙醇中,然后加入适量的无水乙醇溶液。
反应在常温下进行,反应物按摩尔比1:1.1-1.5混合,通常需要搅拌反应2-3小时。
反应结束后,产物可以通过结晶、蒸馏或萃取等方法分离和提纯。
2. 通过2-氰基乙醇与吡啶的反应制备。
首先将2-氰基乙醇溶
解在醇类溶剂中,然后加入适量的吡啶,并加热至反应温度。
反应温度通常在80-100摄氏度之间,反应时间约为2-3小时。
反应结束后,产物可以通过结晶、蒸馏或萃取等方法分离和提纯。
需要注意的是,在进行乙醇吡啶的制备过程中,要注意溶剂选择、反应条件的优化以及产物的分离与提纯等因素,以提高产率和纯度。
【国家自然科学基金】_恶唑啉_基金支持热词逐年推荐_【万方软件创新助手】_20140801
2012年 序号
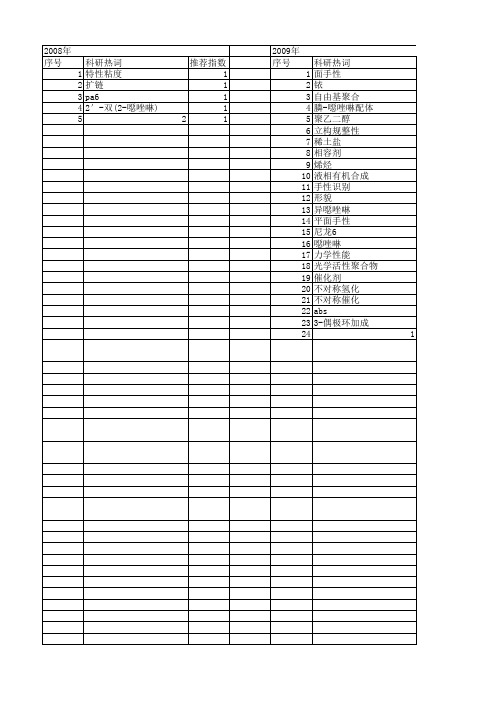
科研热词 推荐指数 1 异噁唑啉 2 2 合成 2 3 1 2 4 阴离子识别 1 5 选择性 1 6 超氧化物歧化酶模拟物 1 7 腈氧化物 1 8 脂质体 1 9 脂肪族聚酯酰胺 1 10 聚(2-乙基-2-噁唑啉) 1 11 紫外可见吸收光谱 1 12 糖蛋白 1 13 糖苷内切酶 1 14 糖肽 1 15 糖基噁唑啉 1 16 生物活性 1 17 环境友好 1 18 环化 1 19 环加成反应 1 20 氮蓝四唑光照法 1 21 氧化腈 1 22 扩链反应 1 23 手型诱导 1 24 己内酰胺 1 25 己二酸 1 26 吲哚嗪 1 27 吡啶双噁唑啉配体 1 28 吡啶单噁唑啉配体 1 29 化学酶法合成 1 30 乙醇胺 1 31 乙烯基膦酸酯 1 32 n-甲基异噁唑四氯化铁酸盐 1 33 michael加成 1 34 hso41 35 6-吡啶二甲酸二甲酯 1 36 3-偶极环加成 1 37 3-二羰基化合物 1 38 2 1
2008年 序号 1 2 3 ቤተ መጻሕፍቲ ባይዱ 5
科研热词 特性粘度 扩链 pa6 2′-双(2-噁唑啉)
推荐指数 1 1 1 1 2 1
2009年 序号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24
科研热词 面手性 铱 自由基聚合 膦-噁唑啉配体 聚乙二醇 立构规整性 稀土盐 相容剂 烯烃 液相有机合成 手性识别 形貌 异噁唑啉 平面手性 尼龙6 噁唑啉 力学性能 光学活性聚合物 催化剂 不对称氢化 不对称催化 abs 3-偶极环加成 1
推荐指数 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1
具有C2对称的氮磷-氧磷配体双恶唑啉磷乙烷的合成及在不对称催化加氢中的应用

GONG . — u Da Ch n W ANG , iS a Ta— h n ZHOU, a Hu W E , ig IPn
OUYANG, i g Ka Pn — i
(C lg h m s n i cec, hn he re nvri , h n 4 0 1 ol e fC e i r a d f S i e C i T re e o t y Le n a Gogs i sy Hca g 3 0 ) U e t 4 (C l g L e c n e n h r c, aj gU i ri cn lg , aj g20 0 ) ol e f i i c d amayN ni nv s o T h o y N ni 1 0 9 e o fS e a P n e t fe y o n (S a g a stt o g nc hmir, hns cd m Scn eS a g a 03 ) h n h intuefOra i C e s y C iee a e y f iec,h n h i 0 0 2 I i t A o 2
( MP ) 体 具 有 更 高 的 对 映选 择 性 .在 这 四个 新 的配 体 中配 体 (,) hB AP () A P配 尺尺 一 — O E 2 的催 化 性 能 最 优 .催 化 剂 P
恶唑类化合物的合成方法综述之欧阳语创编

第一章:噁唑类化合物的合成方法综述1.引言:含有两个杂原子且其中一个杂原子为N的五元环体系叫唑,数目很多。
根据杂原子在环中位置不同,有可分为1,2唑和1,3唑。
五元环中杂原子为N、O的化合物是噁唑类化合物,其种类较多,有噁唑(1)、噁唑啉(2)、噁唑烷(3)、噁唑酮、苯并噁唑(4)等。
噁唑类化合物是一类重要的杂环化合物,一些具有噁唑环的化合物具有生物活性[1]。
例如2氨基噁唑具有杀真菌、抗菌、抗病毒作用[2]。
同时它们在中间体、药物合成中也具有广泛的用途[3,4,5]。
分子结构中含有噁唑环的聚苯并噁唑(5)是耐高温的高聚物[6]。
噁唑(1)是1,3位含有O、N原子的五元环,为有像吡啶一样气味且易溶于水的液体,是非常稳定的化合物,它在热的强酸中很稳定,不发生自身氧化反应,不参与任何的正常的生物化学过程。
其二氢和四氢杂环化合物叫做噁唑啉或4,5-二氢唑啉(2)和噁唑烷或四氢噁唑啉(3)。
虽然噁唑环这个名称还是Hantzsch在1887[1]年确定的,但一向没有人作过大量深入的研究,因为这个环系不常见于天然产物中,而且制备也相当困难。
直到青霉素的出现,才推动了噁唑的研究。
青霉素本身虽没有噁唑环,但它最初是疑为是属于这个环系的。
青霉素实际含有一个噻唑环,而噁唑是噻唑的氧的类似物。
因为青霉素是一个很重要的药品,研究的范围也由噻唑推广到了噁唑。
下面我们就将噁唑类化合物的合成方法进行综述。
2.合成方法噁唑类化合物可由提供N,O原子的化合物来合成。
2.1.Cornforth法合成噁唑环1947年由Cornforth等人首次合成第一个含有噁唑环的化合物[7]。
其过程如下:据此设计合成噁唑4羧酸乙酯的路线如下[7]。
2.2. 碱催化酰氨基磺酰烯关环合成法用3酰氨基2碘1苯磺酰烯在碱催化下关环可得到噁唑化合物[8]。
2.3.由西佛碱氧化法合成在温和的反应条件下,用二醋酸碘苯作氧化剂可以以良好产率将西佛碱氧化生成2芳基5甲氧基噁唑化合物[9]。
8羟基喹啉生产工艺

8羟基喹啉生产工艺
8羟基喹啉是一种重要的精细化学品,广泛应用于制药、农药、染料等领域。
下面介绍一种常用的8羟基喹啉生产工艺。
首先,原料准备。
8羟基喹啉的主要原料是吡啶和高锰酸钾。
吡啶是一种常见的化工中间体,可通过乙酰乙酸酯和氮气经过催化剂催化反应合成;高锰酸钾是氧化剂,可通过氯化钾和高锰酸钠反应制得。
其次,反应步骤。
8羟基喹啉的合成一般经历三个步骤:氮气
氧化、酰化反应和还原反应。
1. 氮气氧化:将吡啶溶于适量的溶剂中,加入氮气进行氧化反应。
氮气能氧化吡啶中的氢原子,生成4,6-二氧代-2-吡啶酮。
这一步骤需要控制反应温度和反应时间,同时添加合适的催化剂来提高反应效率。
2. 酰化反应:将4,6-二氧代-2-吡啶酮与多功能羧酸反应,生成8羟基喹啉的中间体。
多功能羧酸可以选择丙二酸、乙酸等。
反应条件需要在适当的温度和溶剂中进行,同时添加酰化剂催化反应。
3. 还原反应:将8羟基喹啉中间体与还原剂反应,还原成最终产物8羟基喹啉。
常用的还原剂有亚硫酸氢钠和金属还原剂。
最后,产品提取和纯化。
反应结束后,通过合适的方法将产物从溶液中提取出来,然后经过精制工艺,如结晶、升华、再结
晶等纯化方法,获得高纯度的8羟基喹啉产品。
以上就是8羟基喹啉的生产工艺的基本步骤。
当然,具体的工艺参数和步骤可能因制造厂家和实际情况而有所不同。
在实际生产中,需要根据具体情况进行优化和调整,以提高产物收率和产品质量。
同时,也需要严格遵守安全操作规程,确保生产过程的安全性。
咪唑并[1 2-a]吡啶的合成与表征
咪唑并[1 2-a]吡啶的合成与表征咪唑并[1 2-a]吡啶(Imidazo[1,2-a]pyridine)是一类具有广泛生物活性的杂环化合物,被广泛用于制药、农药和材料科学领域。
因此,其合成方法备受关注。
本文将介绍几种咪唑并[1 2-a]吡啶的合成方法及其表征。
菲咯啉是一种含硝基的芳香胺,常常用来制备咪唑并[1 2-a]吡啶。
具体反应过程如下:首先,用甲醇将菲咯啉氧化为相应的醛基化合物;随后,将醛基化合物与酰胺反应,生成中间体;最后,在酸的催化下,将中间体脱水,就得到了目标产物咪唑并[1 2-a]吡啶。
该方法具有简单、高收率等优点,但需要使用大量的化学试剂,存在环境、经济和安全等问题。
2014年,一篇研究报道了一种大环化学反应,可用于合成咪唑并[1 2-a]吡啶。
该反应需要进行三次基本反应:多成环哌啶化、N-烷基化和O-烷基化。
具体反应过程如下:溶液法合成咪唑并[1 2-a]吡啶是近年来发展的一种新方法。
该方法基于有机溶剂作用下的滴加反应,通过添加多种组分反应,产生中间体,在酸催化下生成目标产物。
具体反应过程如下:首先,将四甲基异硫脲放入DMSO溶液中,并加入红酒酸到酸性,生成中间体;随后,将其他试剂–取代双苯醚、氯气和三环化加入溶液中,并在缓慢搅拌的条件下反应;最后,加入酸性催化剂,得到目标产物咪唑并[1 2-a]吡啶。
该方法具有原料易得、无毒、对环境无害等优点,但需要精确控制反应条件,且反应时间较长。
表征方法:为了确认所合成的咪唑并[1 2-a]吡啶的结构,需要进行多种表征方法。
主要包括:核磁共振(NMR)谱、红外光谱(IR)谱、质谱(MS)谱等。
这些表征手段能够确定目标产物的化学结构、分子量和元素组成等。
综上所述,通过不同的合成方法,可以有效地制备咪唑并[1 2-a]吡啶。
同时,针对不同的科研要求,可以选择适合自己的表征手段,以确保实验结果的准确性和可靠性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第48卷2012年第5期V01.482012No.5西北师范大学学报(自然科学版)JournalofNorthwestNormalUniversity(NaturalScience)57
·本刊特约藕·吡啶双嗯唑啉配体的制备新方法
王克虎,吴滢,黄丹凤,胡雨来。(西北师范大学化学化工学院,甘肃省赢分子材料重点实验室,甘肃兰姆730070)
摘要:介绍了一种以2,6一吡啶二甲酸二甲酯为原料经两步反应制备吡啶双嚷唑啉配体的新方法.以2,6一吡啶一二甲酸二甲酯为初始原料,与不同手性氨基醇反应生成关键中阃体吡啶一2,6~二酸双酰胺,再经舍环得到最终产物.结果表明,该方法反应产物单一、产率高,且避免了催化荆的使用;原料易得、成本较低;反应周期短、效率较高;污染排放轻、对环境友好.关键词:吡啶双曝哇啉配体;2,6-吡啶二甲酸二甲酯;合成;环化;环境友好中图分类号:O626文献标识码:A文章编号:1001—988X(2012.)05—0057—04
Newsynthetic
methodof
pyridinebis(oxazoline)
WANGKe-hu,WUYing,HUANGDan-feng,HUYu-lai
(KeyLaboratoryofPolymerMaterialsofGansuProvince,
CollegeofChemistryandChemicalEngineering,NorthwestNormalUniversity,Lanzhou730070,Gansu,China)
Ahstract:Anewmethodforthesynthesisofpybox,whichisobtainedfrompyridine一2,6一dicarboxylatebytwosteps。isdescribed.Reactedwithdifferentchiralaminoalcohols,pyridine-2,6-dicarboxylateis
convertedtobisamides,andthenpyboxisobtainedbycyclization
ofbisamidesinthepresenceofTsCI/
Et3N.Theresultsshowthatthismethodhastheadvantagesofhighyieldsavoidingtheuseofcatalyst,cheaprawmaterials,lowerCost,shortreactiontime,andenvironmentallybenign.
Keywords:.pyridinebis(oxazoline);pyridine一2,6-dicarboxylate;synthesis;cyclization;environmentallybenign
具有C一2对称轴的手性吡啶双嗯唑啉类配体已经广泛应用于不对称催化反应中,表现出优异的手性诱导作用:如Henry反应[1]、AIdol反应∽J、Michael加成[引、D-A反应卧焉3等.手性吡啶双嗯唑啉作为手性配体的优点在于易于制备、价格低廉,它可以由手性氨基醇为原料制备得到,而手性氨基醇可由自然界广泛存在的手性氨基酸通过加氢还原得到.另外,嗯唑啉作为手性配体的手性基团离配位中心很近,因此在金属离子催化过程中可起到直接的手性诱导作用.关于手性双噫唑啉配体的合成,国内外文献报道较多,根据所用的制备原料主要可分为2种:1)以2,6一吡啶二甲酰氯为原料.1989年Nishiyama等[63提出以2,6一吡啶二甲酰氯和手性氨基醇反应生成酰胺化合物,然后用二氯亚砜将羟基氯代保持手型碳原子构型不变,最后在碱性条件下环合生成手性双嗯唑啉吡啶类化合物(图1).该方法所用原料2,6一毗啶二甲酰氯稳定性差,不易
收稿日期:2012—08—20基金项目:国家自然科学基金资助项目(20272047,20572086):甘肃省自然科学基金资助项目(3ZS051一A25—001);甘肃省财政厅高校基本科研业务费项目作者简介:王克虎(1971一),男,甘肃古浪人,副教授,博士,硕士研究生导师.主要研究方向为不对称合成、金属有机化学.E-mail:wangkh@DWTILI.edu.cn*通讯联系人,教授,博士,博士研究生导师,E-mail:huyl@nwnu.edu.CFI
万方数据58西北师范大学学报(自然科学版)
JournalofNorthwestNormalUniversity(NaturalScience)第48卷V01.48
储存,且该法合成步骤繁琐,总产率较低.2)以2,6一吡啶二腈为原料.1999年,Chelucci等‘71以吡啶二腈为原料,在ZnCl2催化下,当氨基醇与二元腈的物质的量比为1:1时,同时生成单嗯唑啉配体(产率26%~44%)与双嗯唑ClooCl/oHR2JR,、NH2CnzCl2,NEt3啉配体(产率20%~30%);当氨基醇与二元腈的物质的量比为3:1时,只得到双嗯唑啉配体(图2).该法虽然步骤简单,但原料吡啶二腈非常昂贵,因此不适合工业化生产.
R2SOCl2-—·—--—·--—--●retlux.一一——图1以2,6吡啶二甲酰氯为原料合成手性双嗯唑啉配体的反应路线Fig1Syntheticrouteofpyboxfrompyridine一2,6-dicarbonyldichlorideN正心NZnCl2,PhCLrefluxRR图2以2,6一吡啶二腈为原料合成手性双嗯唑啉配体的反应路线Fig2Syntheticrouteofpyboxfrompyridine一2,6-dicarbonitrile鉴于以上考虑,笔者以廉价易得且容易储存的2,6-吡啶二甲酸二甲酯为初始原料,与手性氨基醇反应生成关键中间体吡啶一2,6一二甲酸双酰胺,再经合环得到最终目标产物(图3).经氢谱、碳谱等№似C。。№畿1实验部分R波谱数据进行表征.该方法反应产物单一、产率高,且避免了催化剂的使用;原料易得、成本较低;反应周期短、效率较高;污染排放轻、对环境友好.
2aR=Bn12bR=Ph2eR=CH,甲基苯磺酰三乙胺二氯甲烷回流,12h3aR=Bn3bR2Ph3cR=CHt
图3以2,6一吡啶二甲酸二甲酯为原料合成手性双嗯唑啉配体的反应路线
Fig3Synthetic
route
ofpyboxfrom
pyridine一2,6-dicarboxylate
1.1仪器和试剂.熔点在X一4型显微熔点仪上测定,温度计未校正;红外光谱在FTS3000FT—IR型红外光谱仪上测定(KBr压片);核磁共振谱在Mercury400plus型核磁共振仪上测定,TMS为内标,CDCl。为溶剂;质谱在ESQUIRE6000型液一质联用仪上测定.三乙胺、无水硫酸钠、无水硫酸镁、2,6一吡啶二甲酸、L一苯甘氨醇、L一苯丙氨醇、L一氨基丙醇、对甲苯磺酰氯、二氯甲烷、甲苯等均为分析纯试剂.石油醚(PE)、乙酸乙酯(EA)为重蒸的工业级试剂,其中石油醚的沸程控制在60~90℃.柱层
析硅胶为200~300目.甲苯用无水氯化钙预干燥,再加入金属钠回流,常压蒸馏,加分子筛密封保存.
HHdN义RR
万方数据2012年第5期2012No.5王克虎等:吡啶双噶唑啉配体的制备新方法Newsyntheticmethodofpyridinebis(oxaz01ine)59
二氯甲烷用无水氢化钙预干燥,常压蒸馏.1.2实验步骤1.2.1吡啶类双酰胺的合成将2,6一吡啶二甲酸二甲酯(8.80g,0.04t001)和L一氨基醇(0.1m01)加入到250mL的单口瓶中,加入200mL甲苯,在120℃回流24h.蒸去甲苯后,硅胶柱层析(EA:PE一2:1)分离得目标产物.2a白色固体17.6g,产率95%,m.P.87~88℃;1HNMR(CDCl3,400MHz)艿:8.35(d,,一8.8Hz,2H),8.17(d,,一8.0Hz,1H),7.95(S,2H),7.30~7.15(rrl,10H),4.33~4.29(In,2H),3.75(t,J=12.OHz,4H),3.00~2.93(m,4H),1.95(S,2H);13(2NMR(CDCl3,100MHz)占:160.5,149.9,139.0,138.1,128.9,128.2,126.1,125.0,65.8,54.5,39.2.2b白色固体16.5g,产率95%,m.P.117~119℃;1HNMR(CDCl。,400MHz)艿:8.37(d,J=8.4Hz,2H),8.19(d,J一8.0Hz,1H),7.99(S,2H),7.32~7.18(m,10H),4.37~4.33(m,2H),3.80(t,.,一12.0Hz4H),1.97(S,2H);”CNMR(CDCl。,100MHz)8:163.4,146.7,141.7,137.4,128.8,127.8,126.8,126.3,75.5,70.3.2c白色固体12.1g,产率98%,m.P.196~198℃;1HNMR(CDCI。,400MHz)占:8.35(d,J一8.8Hz,2H),8.26(d,J一8.0Hz,2H),8.12(S,2H),4.27~4.22(rrl,2H),3.70~3.63(131,4H),1.96(S,2H),1.30(d,J一8.OHz,6H);”CNMR(CDCl。,100MHz)占:160.5,149.9,139.0,125.0,68.4,46.1,17.1.1.2.2吡啶类双酰胺环化合成手性吡啶双嚷唑啉配体将吡啶一2,6一二酸双酰胺(0.02m01)和60mL二氯甲烷加入250mL单口瓶中,再分批加入对甲苯磺酰氯(o.05m01),0℃下缓慢滴加三乙胺(0.3m01),搅拌过夜,在60℃回流12h,TLC检测原料消失,过滤分离出对甲苯磺酰氯,然后将剩余的混合物氧化铝(EA:PE=2:1)过柱,得目标产物.3a白色固体,产率96%,rn.P.175~177℃;1HNMR(CDCl。,400MHz)艿:8.2(d,J=8.0Hz,2H),7.89(t,J一16.0HZ,1H),7.24~7.33(m,10H),4.61~4.69(m,2H),4.46(t,歹一20.0Hz,2H),4.25(t,J=16.0Hz,2H),3.27(d,J一16.0Hz,2H),2.75(d,J一24.oHz,2H);”CNMR(CDCl,,100MHz)d:162.6,146.8,137,7,137.3,129.1,128.5,126.5,125.8,72.6,68.0,41.6.3b白色固体,产率92%,rn.P.174~176℃;HNMR(CDC【3,400MHz)艿:8.34(d,J一8.0Hz,2H),7.92(t,I,一16.0Hz,1H),7.26~7.39(m,
