液相法制备纳米颗粒的机制.
铝纳米粒子的液相化学还原法制备与表征

于能 量 密度 大 、 耗 氧 量低 及 高 的反应 活性 而 成 为 火 箭
推进 剂 和火 炸 药 配 方 独 特 的 成 分 之 一 ;此 外 , 金 属 纳米 粒子 掺 杂 复 合 材 料 纤 维 也 可 用 作 z箍 缩 丝 阵
2 实验 部 分
2 . 1 试 剂 与 仪 器
材料
关键词 : 应 用化学 ; 分 散 稳 定 剂 ;液 相 化 学 还 原 法 ; 铝 纳米 粒 子 ; 制备 ; 表 征 中图 分 类 号 : T J 5 5 ; T G1 4 6; O6 9 文 献 标 识 码 :A D OI : 1 0 . 3 9 6 9 / j _ i s s n . 1 0 0 6 — 9 9 4 1 . 2 0 1 3 . 0 3 . 0 1 3
炸 、 激 光 感 应 、 等离 子体 或 电子 束 辐 射 等 加
二醇( 分子量 为 4 0 0 0) , 分析纯 , 成都 市 科 龙 化工 试 剂
厂 ;聚 乙二 醇 二 甲醚 ( 分子 量为 2 5 0 ) , 分析 纯 , 阿 拉 丁
热方 式 实现 原子 蒸发 , 在惰 性气 氛 中冷凝 沉积 , 所得 产 品纯 度 高 、 结 晶组 织好 , 但设 备要 求 高 。液 相化 学法 是 在溶 剂 体系 中 , 将 铝 烷类 前 驱 体 加 热 分 解 。 。 , 或 者 将 铝盐 还 原 … 实 现 AI NP s 的 合成 ;该 方 法 对 实 验 设 备 要 求不 高 , 可实 现实验 室化 学合 成 , 但 存 在 的缺点是 制 备 过程 中产 物易 被氧 化 , 易 发生 团 聚 , 以及 容 易包覆 副 产物 L i C I 杂 质 等 。 目前 采 用 液 相 化 学 法 制 备 A I NP s
气相与液相法制备纳米材料
液相制备纳米材料的原理、方法、形成机理和结构液相法实在液体状态下通过化学反应制取纳米材料方法的总称,又称为湿化学法或溶液法。
现在,有各种各样的制备方法,文献中无公认一致的分类方法,相反还有些凌乱。
为清晰醒目,特点明显,便于理解。
这里将液相材料的纳米制备方法分为:沉淀法、溶胶-凝胶(sol-gel)法、水热法、化学还原法、化学热分解法、微乳胶法、声化学法、电化学法和水中放电法等中。
3.1 沉淀法3.1.1 共沉淀和分步沉淀不论溶液中有一种还是几种离子,都能够同时生成沉淀的反应,就是共沉淀。
一般沉淀法的工艺流程可表示为图3.1所示。
分步沉淀则是反应中有多种可能的沉淀物,依次一个个地进行沉淀,称之为分步沉淀。
Raming等人就用了共沉淀和分步沉淀两种方法制备了掺Y的四方Zr+Fe3O4纳米粉末。
在共沉淀中,他们将ZrOCl2.8H2O和YCl3与FeCl3.6H2O的混合溶液,缓慢的加入到剧烈搅拌含有质量分数为25%、PH值约为14的氨水中,产生出的金属与氢氧化物混合的直接沉淀物。
在分步沉淀法中,他们用了两种不同的步骤。
第一种是先沉淀三氧化二铁,再沉淀氧化锆,简写成SPHZ;第二种则倒过来,先沉淀氧化锆,再沉淀氧化铁,简写成SPZH。
第一种具体操作是,将八水氯酸锆和YCl3的水溶液加到碱性的悬浮着氧化铁粒子的溶液中,因此是先沉淀氧化铁,再沉淀氧化锆。
第二种分步沉淀则是将六水氯化铁水溶液加到悬浮有氧化锆粉末粒子的碱性溶液中,因此是先沉淀氧化锆,再沉淀氧化铁。
这两种分步沉淀中,都是在剧烈搅拌中,将酸性的金属离子加入到碱性的氨水中,在悬浮液中导致金属氢氧化物的爆炸式成核。
经水洗后,在100℃下干燥成胶状,再在500-700℃温度内煅烧2h,以得到完全的晶体物质。
3.1.2 均匀沉淀无论是在CP还是在SP中,由于沉淀剂在金属溶液中的加入,哪怕是沉淀剂加入量很少,并不断的搅拌,在局部溶液中的沉淀剂浓度都可以变得很高,于是这些地方就首先沉淀,使沉淀变得不均匀,必须在溶液中消除不均匀的沉淀,而使整个溶液中均匀的生成沉淀。
纳米材料的制备方法(液相法)

05
液相法制备纳米材料的前景与展 望
新材料开发与应用
液相法制备纳米材料在新型材料开发 中具有广泛应用,如高分子纳米复合 材料、金属氧化物纳米材料等。
随着科技的发展,液相法制备的纳米 材料在能源、环保、生物医学等领域 的应用前景广阔,如燃料电池、太阳 能电池、生物传感器等。
提高制备效率与质量
液相法制备纳米材料具有较高的生产效率和可控性,能够实 现规模化生产。
通过优化制备条件和工艺参数,可以进一步提高纳米材料的 性能和质量,如粒径分布、结晶度等。
降低制备成本与能耗
液相法制备纳米材料具有较低的成本和能耗,能够降低生 产成本,提高经济效益。
通过改进制备技术和设备,可以进一步降低液相法制备纳 米材料的成本和能耗,实现绿色可持续发展。
THANKS
感谢观看
微乳液法
总结词
通过将前驱体溶液包含在微小的水或油滴中来制备纳米材料的方法。
详细描述
微乳液法是一种制备纳米材料的有效方法。在微乳液法中,将前驱体溶液包含在微小的水或油滴中, 形成微乳液。通过控制微乳液的尺寸和前驱体的反应条件,可以制备出具有特定形貌和尺寸的纳米材 料。微乳液法可以用于制备有机或无机纳米材料,具有较高的应用价值。
液相法具有操作简便、成本低、 可大规模生产等优点,适用于制 备多种纳米材料,如金属、氧化 物、硫化物等。
液相法的分类
01
02
03
化学还原法
通过化学还原剂将金属盐 或氧化物还原成金属纳米 粒子。
沉淀法
通过控制溶液的pH值、温 度等条件,使金属离子或 化合物沉淀为纳米粒子。
微乳液法
利用微乳液作为反应介质, 通过控制微乳液的组成和 反应条件,合成纳米粒子。
纳米功能材料的制备与表征

纳米功能材料的制备与表征近年来,纳米技术发展日新月异,纳米材料的制备与应用也得到了广泛的关注。
纳米功能材料的制备与表征是纳米科技中不可缺少的环节,在纳米科技的各个领域中都有着重要的应用。
今天,我们就一起来了解一下纳米功能材料的制备与表征的相关知识。
一、纳米功能材料的制备方法在制备纳米功能材料时,通常需要通过一些特殊的方法来实现纳米级精度。
其中,主要有以下几种方法:1. 物理制备方法物理制备方法是指通过物理手段来制造纳米材料,主要包括机械法、热处理法、蒸发法、溅射法等。
机械法是指通过机械力将材料切割成纳米级别的微粒。
常用的机械制备方法有球磨法、流化床法等。
热处理法是指将材料在高温下进行一系列的热处理,使其形成纳米级别的颗粒。
常用的热处理方法有高温还原法、热分解法等。
蒸发法是指将材料在真空条件下蒸发成薄膜,然后使用一些特殊的手段将其压缩成纳米级别的颗粒。
常用的蒸发法有电子束蒸发法、磁控溅射法等。
溅射法是指将材料放置在真空室中,在电子束或离子束的轰击下,使其形成纳米级别的颗粒。
常用的溅射法有磁控溅射法、光致发光溅射法等。
2. 化学制备方法化学制备方法是指通过化学反应来制备纳米材料,主要包括沉淀法、胶体溶胶法、微乳液法等。
沉淀法是指通过化学反应将材料溶液中的金属离子还原成金属颗粒,形成纳米级别的粒子。
常用的沉淀法有化学沉淀法、共沉淀法等。
胶体溶胶法是指在液相中制备纳米颗粒,主要通过控制反应条件来控制颗粒的大小和形态。
常用的胶体溶胶法有溶胶凝胶法、微乳液法等。
微乳液法是指在反应体系中加入表面活性剂,形成微胶团来控制粒子的大小和形态。
常用的微乳液法有水合胶体微乳液法、反应交替微乳液法等。
二、纳米功能材料的表征方法在研究纳米材料的表征时,常采用一些特殊的方法来观察其物理化学性质和结构特征。
其中,主要采用以下几种方法:1. 电子显微镜电子显微镜是一种用来观察纳米材料的表面形貌和结构的仪器。
主要包括扫描电子显微镜(SEM)、透射电子显微镜(TEM)等。
纳米材料的制备方法及原理 (整理)

使介质温度出现宏观上的升高
可见微波加热是介质材料自身损耗电磁场能量而发热
10/372
6) 电弧加热
在两个电极间加一电压,当电源提供较大功率的电能时, 若极间电压不高 ( 约几十伏 ) ,两极间气体或金属蒸气中可 持续通过较强的电流 ( 几安至几十安 ) ,并发出强烈的光辉, 产生高温(几千至上万度),这就是电弧放电。 电弧放电最显著的外观特征是明亮的弧光柱和电极斑点。
分子水平的操作。21Βιβλιοθήκη 3727、等离子体加热蒸发法
等离子体的概念及其形成
物质各态变化:
固体→液体→气体→等离子体→反物质(负)+物质(正) (正负电相反,质量相同) 只要使气体中每个粒子的能量超过原子的电离能,电子将 会脱离原子的束缚而成为自由电子,而原子因失去电子成
为带正电的离子(热电子轰击)。这个过程称为电离。当
开始成核:其过程涉及到在含有可溶性的或悬浮盐的水或 非水溶液中的化学反应。液体变得饱和时,沉积就会借助 于均相或异相成核机制而发生。 成核之后:由扩散控制长大,此时溶液的浓度和温度在决 定粒子长大中起重要作用。 满足条件:所有的核必须几乎在同时生成,而且在接下来
的生长过程中必须没有进一步的成核或颗粒团聚。
23/372
8、溅射法
溅射法制备纳米微粒的原理
• 用两块金属板分别作为阳极和阴极,阴极为蒸发用的材料,在两电极
间充入Ar气(40~250 Pa),两电极间施加的电压范围为0.3~1.5 kV。
由于两电极间的辉光放电使 Ar 离子形 成,在电场的作用下Ar离子冲击阴极靶
材表面 (加热靶材 ),使靶材原子从其表
主要影响因素:反应液浓度、反应温度、溶液pH值、反应 物加到溶液中的顺序等。
纳米材料的制备方法及其原理

注意:对于金属材料,电磁场不能透入内部而 是被反射出来,所以金属材料不能吸收微波。 小块金属会发出电火花,注意安全!!! 水是吸收微波最好的介质,所以凡含水的物质 必定吸收微波。 特点:加热速度快;均匀加热;节能高效;易 于控制;选择性加热。
28/372
6) 电弧加热
在两个电极间加一电压,当电源提供较大功率的电能时, 若极间电压不高(约几十伏),两极间气体或金属蒸气中可 持续通过较强的电流(几安至几十安),并发出强烈的光辉, 产生高温(几千至上万度),这就是电弧放电。 电弧放电最显著的外观特征是明亮的弧光柱和电极斑点。 电弧放电可分为 3个区域:
23/372
化学法:利用大功率激光器的激光束照射于反应 物,反应物分子或原子对入射激光光子的强吸收, 在瞬间得到加热、活化,在极短的时间内反应分 子或原子获得化学反应所需要的温度后,迅速完 成反应、成核凝聚、生长等过程,从而制得相应 物质的纳米微粒。
24/372
• 激光加热蒸发法制备纳米粒子的优点:
❖ 我国近年来在纳米材料的制备、表征、性能及理论研究方面取 得了国际水平的创新成果,已形成一些具有物色的研究集体和 研究基地,在国际纳米材料研究领域占有一席之地。在纳米制 备科学中纳米粉体的制备由于其显著的应用前景发展得较快。
纳米材料的制备
纳米材料的合成与制备一直是纳米科学领域的一个重要研究课题,新材 料制备工艺过程的研究与控制对纳米材料的微观结构和性能具有重要的 影响。在所有纳米材料的制备方法中,最终目的是所制得的纳米颗粒具 有均一的大小和形状。理论上,任何能够制备出无定型超微粒子和精细 结晶的方法都可以用来制备纳米材料。如果涉及了相转移(例如,气相 到固相),则要采取增加成核以及降低在形成产品相过程中颗粒的增长 速率的步骤,从而获得纳米颗粒。一旦形成了纳米颗粒,则要防止其团 聚和聚结。此外,许多方法合成制备出的纳米材料都是结构松散、易团 聚的纳米超细微粒,这样只可得到纳米粉体。如果要获得纳米固体材料, 须将纳米颗粒压实才可得到致密的块材。因此,材料的压制工艺也是纳 米制备技术的重要部分。
9零维纳米材料的制备化学液相法沉淀法水热法
压片
纳米粉体
球磨
•纳米微粉大大降低了透明陶瓷的烧结温度; •La2O3 起到稳定陶瓷结构与组成的作用。
pH值对金属离子沉淀的影响
混合物共沉淀过程是非常复杂的.溶液中不同种类的阳离子不能同时 沉淀.各种离子沉淀的先后与溶液的pH值密切相关.
Zr、Y、Mg、Ca的盐溶液, 在不同浓度下,各种金属离子发
沉淀法
沉淀法的特点: 简单易行,但纯度低,颗粒半径大。适合制备氧化物。
沉淀物的粒径的影响因素: •沉淀物的溶解度,沉淀物的溶解度越小,相应粒子径也越小。 •形核与核长大的相对速度。即核形成速度低于核成长,那么生成的颗粒数 就少,单个颗粒的粒径就变大。
沉淀发生的物理过程: 存在于溶液中的离子A+和B-结合,形成晶核,由晶核生长和在重力的作用下 发生沉降,形成沉淀物。一般而言,当颗粒粒径成为1微米以上时就形成沉淀。
用无水乙醇清洗2次,除去沉淀中的水分
•透明Y2O3陶瓷在很宽的光谱范 围内都光学透明,在红外和远红 外具有较高的线透过率,作为激 光增益介质。
•采用一般的Y2O3微粉很难制备 出透明陶瓷,而且烧结温度大于 2000℃;
陶瓷
烘箱中干燥
纳米粉体样品的TEM照片
1450-1550C还原气氛下 烧结4 h
1000℃下煅烧4h
生沉淀所应的pH值范围
•对于同一种离子,离子浓度越 高,发生沉淀的pH值越低;
•对于不同离子,相同的浓度条 件下所对应的沉淀pH值各有不 同
沉淀剂和搅拌的影响
为了获得沉淀的均匀性,通常是将含多种阳离子的盐溶 液慢慢加到过量的沉淀剂中并进行搅拌,使所有沉淀离子的 浓度大大超过沉淀的平衡浓度,尽量使各组份按比例同时沉 淀出来,从而得到较均匀的沉淀物。
液相化学法制备贵金属纳米颗粒的研究进展
里面加入还原剂还原高价金属离子到金属单质 , 然后经过洗涤 、 过滤 、 干燥 、 煅烧等处理得到催化剂纳米粉体 。还原法中的还原
剂 可 以是 将 高 价 贵 金 属 物 种 还 原 为 零 价 原 子 的 任 意 一 种 , 机 有
学和航 空等领域展现 出极其广 阔的应用前 景。因此 , 纳米技 术
摘 要 关 键 词 纳 米 贵 金 属 粒 子 因具 有 大 的 比表 面积 、 良好 的 界 面 效 应 及 小 尺 寸 效 应 等独 特 的性 能 , 催 化 领 域 备 受 关 在 液相化学法 贵金属 纳米颗粒
注, 尤其是铂族贵金 属催化 剂的纳米材料 。主要概 述 了液相 法制备贵金属( 、 g P 、 d 纳米颗粒的研 究状况 。 Au A 、 tP )
优 异 的 电学 、 磁学 及 光 学 性 能 , 之 发 挥 更 大 的作 用 。 使
度应大 于贵金属前体物质的浓度才 有利 于其 与贵金属离子的完
全 反 应 , 成 粒 径 较 小 的 纳 米 粒 子 ; 且 随还 原 剂浓 度 的 增 加 , 生 并
a d lr e s e i c s r a e a e t , ih h v t r c e r e e r h r n c t ltc f l , s e i l p a i u g o p n a g p cf u f c r a e c wh c a e a ta td mo e r s a c e s i a a y i i d e p cal i e y, ltn m- r u me a ( t l PGM )n n p ria s I h sp p r t e r s a c t t so ep e a a i n o M ( a o a t l. n t i a e , h e e r h sa u f h r p r to fP c t Au, Ag, t P )n n p ril sb P , d a o at e y c c e c l iu d p a em eh d i i to u e e u p i ey h mia l i- h s t o s n r d c d r s m t l. q v
液相法制备纳米微粒
溶胶、凝胶和淀物的区分
(1)溶胶的制备 有两种方法制备溶胶
先将部分或全部组分用适当沉淀剂先沉淀出来, 经解凝,使原来团聚的沉淀颗粒分散成原始颗粒。 因这种原始颗粒的大小一般在溶胶体系中胶核的 大小范围,因而可制得溶胶 。
通过对沉淀过程的仔细控制,使首先形成的颗 粒不致团聚为大颗粒而沉淀,从而直接得到胶体 溶胶。
(ⅱ)金属卤化物与醇反应.金属不能与醇直接反应可以 用卤化物代替金属.
(a)直接反应(B,Si,P) MCl3+3C2H5OH→M(OC2H5)3+HCl 氯离子与烃氧基(RO)完全置换生成醇化物。
(b)碱性基加入法.多数金属氯化物与醇的反应,仅部 分C1- 离子与(RO)基发生置换.则必须加入NH3、吡啶、 三烷基胺、醇钠等碱性基,使反应进行到底。
将溶胶在一定条件下(温度、酸碱度等)进行老化 处理,得到透明状的冻状物即称凝胶(gel)。
溶胶-凝胶法可精确控制各组分的含量,使不同 组分之间实现分子/原子水平上的均匀混合,而且 整个过程简单,工艺条件容易控制。
溶胶(Sol)是由孤立 的细小粒子或大分子 组成,分散在溶液中 的胶体体系。
凝胶(Gel)是一种由 细小粒子聚集而成三 维网状结构的具有固 态特征的胶态体系。
完全沉淀的方法称共沉淀法。
(i)单相共沉淀:沉淀物为单一化合物或单相固溶体 时,称为单相共沉淀。
例如,在Ba,Ti的硝酸盐溶液中加入草酸沉淀剂 后这 种,方形法成的了缺单点相是化适合用物范B围aT很iO窄(,C2仅H2对)有2·4限H的20 沉草淀酸; 盐沉淀适用。
(ⅱ)混合物共沉淀 如果沉淀产物为混合物时,称为混合物共沉
溶胶—凝胶法是60年代发展起来的一种制备 玻璃、陶瓷等无机材料的新工艺。其基本原理是: 将金属醇盐或无机盐经水解直接形成溶胶,然后 使溶质聚合凝胶化,再将凝胶干燥、焙烧去除有 机成分,最后得到无机材料。
激光液相烧蚀制备TiO2纳米颗粒的研究
V0 1 . 2 6 NO .L 1 De ( 、 . 2 01 4
激 光 液 相烧 蚀 制 备 Ti O2 纳 米 颗粒 的研 究
何国庆 张丙元 高学喜 王国菊 刘云龙 王文军
( 聊城大学 物理与信息工程学院 ; 山 东 省 光 通信 科 学 与技 术 重 点 实 验 室 , 山东 聊 城 2 5 2 0 5 9 )
摘 要 利 用脉 冲激 光 器对金 属钛 靶进 行 液 相烧 蚀 , 在 不 同的激 光 烧蚀 功 率 下 , 削备 出 了 Ti O 2 纳米颗 粒. 利用 原子 力显 微 镜 、 X 射 线衍 射 对 T i O 。纳 米 颗 粒 的形 貌 、 结 构 进 行 了表 征 , 讨论 了
第 4期
何国庆等 : 激 光 液 相 烧 蚀 制 备 F i ( ) : 纳 米 颗 粒 的 研 究
3 9
参 考 文 献
[ 1 ] C h r y s i c o p o u l o u P ,D a v a z o g l o u D,T r a p a l i s C, e t a 1 . Op t i c l a p r o p e r t i e s o f v e r y t h i n (  ̄1 0 0 n m)s o l — g e 1 Ti O 2 i f l ms [ J ] .Th i n S o l i d F n ms ,
的制 备 、 以及其 性能 的研究 备受 人们 的关 注r 6 ] . 目前 , 二 氧化钛 纳米 颗粒 的制备 方法 主要 有 两种 : 物 理 方法 和化 学 方法 . 其 中化 学 方 法 主 要有 : 沉 淀
法、 溶 胶一 凝胶 法 、 微 乳 液法 、 水 热法 等. 采 用化 学 法 很难 控 制其 反应 方 向和 反应 速 率及 所 生成 的颗 粒 大
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
液相法制备纳米颗粒的机制液相法是在液体状态下通过化学反应制备纳米材料方法的总称,又称为湿化学法或溶液法。
纳米材料的液相制备方法分为:沉淀法、溶胶-凝胶(Sol-Gel)法、水热法、化学还原法、化学热分解法、微乳液法、声化学法、电化学法和水中放电法等9种。
用液相化学法合成纳米颗粒能够较好地控制颗粒大小、形状和粒径分布。
为了充分利用化学法的优点,需要充分了解这种方法制备纳米颗粒的形成机制,这涉及到:晶体化学、热力学、相平衡以及反应动力学的基本原理。
从液相中生成固相颗粒,要经过成核、生长、凝结、团聚等过程。
1 液相中生成固相颗粒的机理1.1 成核为了从液相中析出大小均匀一致的固相颗粒,必须使成核和长大这两个过程分开,以便使已成核的晶核同步地长大,并在生长过程中不再有新核形成。
在纳米颗粒形成的最初阶段,都需要有新相的核心形成。
新相的形核过程可以被分为两种类型,即自发形核与非自发形核过程。
所谓自发形核指的是整个形核过程完全是在相变自由能的推过下进行的,而非自发形核则指的是除了有相变自由能作推动力之外,还有其他的因素起到了帮助新相核心生成的作用。
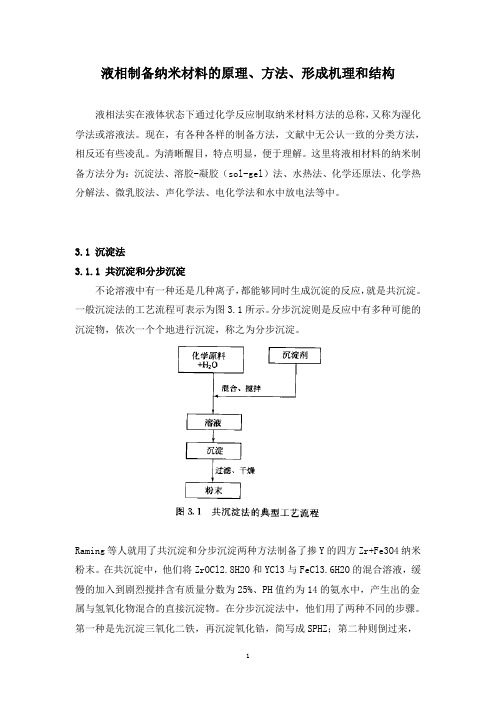
图1 析出固体时液相中溶质浓度随时间的变化情况如图1所示,在整个成核和生长过程中液相内与析出物相应的物质的量浓度是变化的。
在阶段Ⅰ浓度尚未达到成核所要求的最低过饱和浓度*min c ,因此无晶核形成。
当液相中溶液浓度超过*min c 后即进入成核阶段Ⅱ。
作为自发形核的例子,我们考虑一个从过饱和溶液中析出一个球形的固相核心的过程。
设新相核心的半径为r ,因而形成一个新相核心时体自由能将变化343C r G π∆,其中C G ∆为从溶液中析出单位体积晶核时伴随的自由能变化。
0ln C Tc G V c κ∆=- (1-1)上式还可以写成:()ln 1C TG s V κ∆=-+ (1-2)其中,c 为过饱和溶液的浓度;0c 为饱和溶液的浓度;V 晶体中单个分子所占的体积;()00s c c c =-是液相的过饱和度。
当过饱和度为零时,0C G ∆=,这时将没有新相的核心可以形成,或者已经形成的新相核心不能获得长大。
当液相存在过饱和现象时,0C G ∆<,它就是新相形核的驱动力。
在新的核心形成的同时,还将伴随有新的固-液相界面的生成,它导致相应界面能的增加,其数值为24r πγ,其中γ为单位面积的界面能。
综合上面两项能量之后,我们得到系统的自由能变化为:32443C G r G r ππγ∆=∆+ (1-3)将上式对r 微分,求出使得自由能G ∆为零的条件为: *2C r G γ=-∆ (1-4)它是能够平衡存在的最小的固相核心半径,又称为临界核心半径。
当*r r <时,在热涨落过程中形成的这个新相核心将处于不稳定状态,它将可能再次消失。
相反,当*r r >时,新相的核心将处于可以继续稳定生长的状态,并且生长过程将使得自由能下降。
将式(1-4)代入(1-3)后,可以求出形成临界核心时系统的自由能变化:3*2163C G G πγ∆=∆ (1-5)图2 新相形核过程的自由能变化随核心半径的变化趋势图2中画出了形核自由能变化随新相核心半径的变化曲线。
我们看到,形成临界核心的临界自由能变化*G ∆实际上就相当于形核过程的能垒。
热激活过程提供的能量起伏将使得某些原子集团具备了*G ∆大小的自由能涨落,从而导致了新相核心的形成。
液相中均匀成核的核生长速率可用式(1-6)表示:0exp exp C D G G J J T T κκ∆∆⎛⎫⎛⎫= ⎪ ⎪⎝⎭⎝⎭ (1-6)式中,0J 为分子的跃迁频率;D G ∆为晶核在液相中的扩散活化自由能;C G ∆为从溶液中析出晶核时伴随的自由能变化;κ为玻耳兹曼常数;T 为热力学温度。
核的生长速率随的变化而很快地变化。
非均匀成核时,在相界表面上(如外来质点、容器壁以及原有晶体表面上)形成晶核,称非均匀成核,临界核生成的自由能变化为*C G ∆。
可用式(1-7)式表示:()()2*2cos 1cos 4C C G G θθ⎡⎤+-∆=∆⎢⎥⎢⎥⎣⎦(1-7) 式中,θ是液体和固体形成的接触角,由于()()22cos 1cos 41θθ+-<,所以*CG ∆比均匀成核的C G ∆要小。
非均匀核的成核速率可用式(1-8)表示:()()()22231222cos 1cos 2162exp 34CV CV V V V V J n P m T G T G θθσπσππκκ-⎡⎤+-⎛⎫=-⨯⎢⎥ ⎪∆∆⎢⎥⎝⎭⎣⎦(1-8) 式中,V n 为蒸汽或液相的密度;P 为压强;V G ∆为亚稳相中单相原子或分子转变为稳定相中单个原子或分子所引起的自由能的变化;m 为分子的质量;CV σ为比表面能。
从式(1-8)可以看出,核生长速率对V G ∆值是非常敏感的,不均匀核生成比均匀核的生成容易。
式(1-8)对液相或气相中的非均匀成核皆适用。
阶段Ⅲ是生长阶段,晶体的生长是在生成的晶核上吸附原子或分子而使其长大。
1.2 生长1.2.1 四种界面模型(1)完整光滑界面结构模型(Kossel 模型)1927年,Kossel 提出了完整光滑界面结构模型。
模型认为,晶体是理想完整的,生长界面在原子层次上没有凹凸不平,固相和液相之间是突变的。
晶体生长时,光滑面上首先发生二维成核,一旦晶核形成,生长界面上就会出现台阶,在台阶上必然存在三面角位置(称为扭折)。
这些位置束缚能最大,最容易吸附原子。
对应于完整光滑界面的晶体生长包括以下过程:①原子从稀薄环境相向扭折处作三维扩散;②吸附原于在生长界面上向扭折处作二维扩散;③扭折的延伸,台阶的扩展,界面逐渐铺满原于,进而转变成为新的完整光滑界面。
晶面的生长速率取决于界面上扭折密度以及扭折处吸附原子的能力。
Kossel 模型选用了简单的立方结构晶体,仅考虑单个原子在生长界面上的叠合,因此是一种非常简单化的理想界面,与实际晶体生长有很大的距离。
(2)非完整光滑界面结构模型1949年,Frank提出了非完整光滑面界面结构模型,它是Kossel-Stranski 理论的发展。
模型认为晶体生长界面不是理想完整的,界面上存在一定数量的位错。
如果一个纯螺旋型位错和光滑的奇异面相交,在晶面上就会产生一个永不消失的台阶源。
在晶体生长过程中,台阶将逐渐变成螺旋状,使晶面不断向前推移。
后来,Burton、Cabrera和Frank进一步发展了该模型,形成了较为完整的Burton-Cabrera-Frank晶体生长理论(简称为BCF理论)。
(3)粗糙化界面结构模型1958年,Jackson提出了粗糙化界面模型,其基础是考察恒温恒压条件下,生长界面层中流体相原子转变为晶相原子所引起的自由能变化。
模型假设晶体生长界面为单原子层,生长界面中包含的晶相和流体相原子都位于品格位置上;吸附原子进入到生长界面是随机的,液体是连续的流体,流体原子之间、晶相原子与流体原子之间没有相互作用,表面键能只考虑吸附原子之间最近邻的相互作用。
根据统计热力学近似计算,可以判断固/液界面的平衡结构性质。
判断其是光滑界面(界面层全部为晶相原子)还是粗糙界面(界面层晶相原子和流体相原子各占一半)。
一般来讲,如果晶体相变熵小于2,生长界面为粗糙界面;如果晶体相变熵大于4,生长界面为光滑界面;如果晶体相变熵在2—4之间,生长界面是光滑还是粗糙界面,不仅取决于相变熵,而且还取决于生长界面的取向因素等。
(4)弥散界面结构模型1966年,Temkin提出了弥散界面结构模型(又称为多层界面模型)。
模型考虑正方晶系晶体,认为生长界面由多个原子层组成,界面晶格位置由晶相原子和流体相原子所占据,在整个生长过程中,“晶相块”仅能在晶相块上堆积,仅考虑“晶相块”和“流体相块”之间、“晶相块”之间和“流体相块”之间最近邻的相互作用。
弥散界面结构模型具有以下特点:①和Jackson单原子层模型相比,模型没有限制原子层数,因此更“贴近”实际晶体生长情况;②使用平衡热力学基本原理,处理较为简单;③模型不仅适用于固/液生长界面,也适用于固/气或固熔体生长界面。
弥散界面结构模型是目前应用最广的晶体生长界面模型。
1.2.2 生长机理研究(1)二维成核生长模型当晶体在气相或溶液中生长时,若生长界面为原子级完整光滑界面时,晶体生长遵循二维成核生长机制。
原子或分子被吸附到生长界面后,通过扩散聚集而形成二维晶核。
二维晶核一旦出现,体系就增加了棱边能。
此棱边能效应与三维晶核中界面能效应完全类似,构成了二维晶核的热力学势垒。
因此,只有当尺寸达到临界大小时,二维晶核才能自发生长。
以n t 表示连续两次二维成核时间间隔,以s t 表示1个二维临界晶核的台阶“扫过”整个生长界面所需要的时间,根据n t 和s t 的关系,可把二维成核生长分为两种类型“。
一是单二维成核生长,即当n s t t ≥时,在新的二维成核再次形成以前,有足够时间让该晶核的台阶“扫过”整个生长界面;二是多二维成核生长,即当n s t t ≤时,单二维晶核的台阶扫过整个生长界面所需要的时间远远超过连续两次成核的时间间隔,即生长界面每增长1个原子层,需要2个以上的二维品核。
根据原于(分子)成核方式,二维成核又分为表而扩散二维成核(Surface Diffusion two-Dimensional Nucleation)和直接在扭折处叠合二维成核(Direct Integration two-Dimensional Nucleation)。
(2)螺位错生长模型若生长界面上有螺位错露头点,晶体生长机制与二维成核机制不同。
此时,晶体生长起源于生长界面上螺旋位错露头点的台阶,在生长过程中台阶永不消失,螺旋位错露头点提供了一个连续起作用的台阶源,生长界面为一连续的螺旋面。
假设台阶高度为h ,相邻螺旋之间的距离为1919c r kTs λγ==Ω,形成螺旋状生长丘的斜度p h λ=。
如果台阶运动速率为ν,晶体生长的法向生长速率为:n R h p υλν==,与二维成核生长相似,螺旋位错生长也分为表面扩散和直接在扭折处叠合两种形式。
(3)体扩散控制生长模型将在生长界面上吸附结晶的粒子或粒子团称为生长基元,将生长基元在结晶相(即已形成的晶体)内的扩散速度称为体扩散速度。
如果生长基元的体扩散速度小于其在生长界面上的扩散速度,或者小于在生长界面扭折处叠合(结晶)的速度时,晶体生长的速度就由体扩散速度决定,相应的晶体生长称为体扩散控制的生长。
1.2.3 界面生长晶体界面生长,是生长基元不断从流体相通过界面进入晶格位置的过程,也是晶体和流体界面不断向流体中推移的过程,即晶体界面生长的过程是气相或者液相的原子或分子扩散到晶体表面附着并进入晶格。
