铁、钴、镍实验报告
实验二十四:第一过渡系元素(二)(铁、钴、镍)
实验二十四:第一过渡系元素(二)(铁、钴、镍)〔实验目的〕1.试验并掌握二价铁、钴、镍的还原性和三价铁、钴、镍的氧化性;2.试验并掌握铁、钴、镍配合物的生成及性质。
〔实验原理〕铁、钴、镍的高氧化态化合物多是以含氧酸盐或配盐形式存在,如Na2FeO4、K3CoO4、K2NiF6,这类化合物在水溶液中都是不稳定的。
一、铁的化合物1.铁的化合物铁有3种氧化物,红棕色的氧化铁,黑色的氧化亚铁和黑色的四氧化三铁。
它们都不溶于水,灼烧后的氧化铁不溶于酸,氧化亚铁能溶于酸。
四氧化三铁是二价铁和三价铁的混合型氧化物,具有磁性。
铁化合物列于下表中:物质颜色和状态性质FeCl3黑褐色晶体以共价键为主的化合物,它的蒸气为双聚分子Fe2Cl6。
Fe(NO3)3 = Fe2O3 + 6NO2 + 3/2O2 (600~700ºC) Fe(NO3)3•H2O 淡紫色晶体 2FeCl2•4H2O 淡蓝色晶体在空气中易被氧化为草绿色FeSO4•7H2O 淡绿色晶体加热分解为三氧化硫,水溶液易被氧化。
(NH4)2Fe(SO4)2•6H2O 绿色晶体摩尔氏盐,在潮湿空气和水溶液中较稳定。
2.溶液中Fe(Ⅲ)、Fe(Ⅱ)的反应⑴溶液中Fe3+的重要反应还原剂如I-,SO2,H2S,Sn2+,Fe,Cu,等――――――――――――――――→ Fe2+OH-Δ⇌ Fe(OH)3(s)(棕色)→ Fe2O3NH3•H2O———→ Fe(OH)3(s)(棕色)NH3•H2O+NH4Cl——————→ Fe(OH)3(s)(棕色)Fe2+(NaOH,80ºC) O2——————→ Fe3O4• x H2O → Fe2O3CO32-ClO-——→ Fe(OH)3——→ FeO42-NH3•H2O+(NH4)2S H+――――――→Fe2O3(黑色)―→ FeS(黑色)H2S――→Fe2+ + SNCS-过量F-――→[Fe(NCS)]2+(血红色)―→ [FeF6]3-(无色)[Fe(CN)6]4-+ K+――――――→ [KFe(CN)6Fe]x(蓝色)K2C2O4(浓),加热――――――→ [Fe(C2O4)3]3-(黄色)不稳定,见光分解⑵溶液中Fe2+的重要反应氧化剂如Cr2O72-,浓HNO3等―――――――――――→ Fe3+OH-O2⇌ Fe(OH)2(s)(纯白色)→Fe(OH)3(s)(棕色)NH3•H2O――→ Fe(OH)2(s)(纯白色)NH3•H2O+NH4Cl――――――→无沉淀CO32-H2O + CO2 O2――→ FeCO3(白色)――→ Fe(HCO3)2―→Fe(OH)3(s)(NH4)2S―――→ FeS(黑色)NO――→[Fe(NO)( H2O)5]2+( 棕色)H2O2 +过量F-―――――→ [FeF6]3-(无色)NCS-――→无溶液、无颜色CN-过量CN-Cl2―→Fe(CN)2(s) (白色) ――→[Fe(CN)6]4-――→[Fe(CN)6]3-[Fe(CN)6]3-+ K+――――――→ [KFe(CN)6Fe]x(蓝色)二、钴的化合物1. 钴的化合物钴的氧化物与铁的氧化物类似,为暗褐色的Co2O3•xH2O和灰绿色的CoO。
铁、钴、镍实验报告
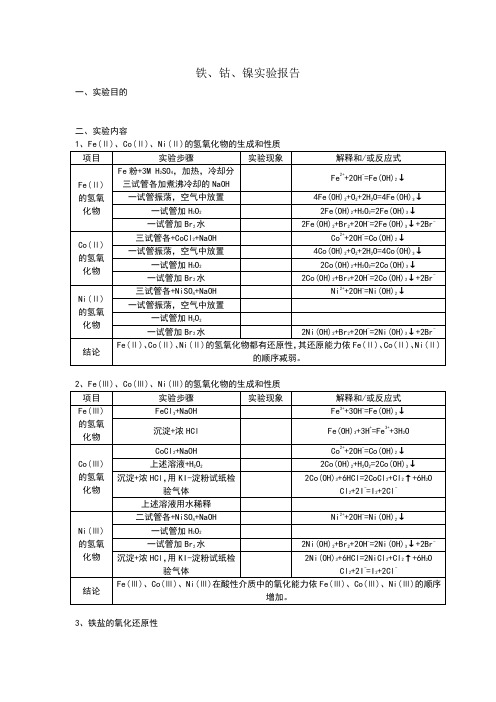
一试管加Br2水
2Co(OH)2+Br2+2OH-=2Co(OH)3↓+2Br-
Ni(Ⅱ)的氢氧化物
三试管各+NiSO4+NaOH
Ni2++2OH-=Ni(OH)2↓
一试管振荡,空气中放置
一试管加H2O2
一试管加Br2水
2Ni(OH)2+Br2+2OH-=2Ni(OH)3↓+2Br-
CoCl2+OH-=Co(OH)Cl↓+Cl-
上述溶液+过量NH3水
Co(OH)Cl+6NH3=[Co(NH3)6]2++OH-+Cl-
4[Co(NH3)6]2++O2+2H2O=4[Co(NH3)6]3++4OH-
NiSO4+适量NH3水
2Ni2++2OH-+SO42-=Ni2(OH)2SO4↓
上述溶液+过量NH3水
Fe(OH)3+3H+=Fe3++3H2O
Co(Ⅲ)的氢氧化物
CoCl2+NaOH
Co2++2OH-=Co(OH)2↓
上述溶液+H2O2
2Co(OH)2+H2O2=2Co(OH)3↓
沉淀+浓HCl,用KI-淀粉试纸检验气体
2Co(OH)3+6HCl=2CoCl2+Cl2↑+6H2O
Cl2+2I-=I2+2Cl-
Ni2(OH)2SO4+12NH3=2[Ni(NH3)6]2++2OH-+SO42↓
铁、钴、镍实验报告

Co(Ⅲ)的氢氧化物
CoCl2+NaOH
Co2++2OH-=Co(OH)2↓
上述溶液+H2O2
2Co(OH)2+H2O2=2Co(OH)3↓
沉淀+浓HCl,用KI-淀粉试纸检验气体
2Co(OH)3+6HCl=2CoCl2+Cl2↑+6H2O
Cl2+2I-=I2+2Cl-
一试管加H2O2
2Fe(OH)2+H2O2=2Fe(OH)3↓
一试管加Br2水
2Fe(OH)2+Br2+2OH-=2Fe(OH)3↓+2Br-
Co(Ⅱ)的氢氧化物
三试管各+CoCl2+NaOH
Co2++2OH-=Co(OH)2↓
一试管振荡,空气中放置
4Co(OH)2+O2+2H2O=4Co(OH)3↓
结论
Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)的氢氧化物都有还原性,其还原能力依Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)的顺序减弱。
2、Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)的氢氧化物的生成和性质
项目
实验步骤
实验现象
解释和/或反应式
Fe(Ⅲ)的氢氧化物
FeCl3+NaOH
Fe3++3OH-=Fe(OH)3↓
沉淀+浓HCl
Ni2(OH)2SO4+12NH3=2[Ni(NH3)6]2++2OH-+SO42↓
与SCN-形成的配合物
FeCl3+KSCN
整理铁、钴、镍的性质

整理铁、钴、镍的性质-CAL-FENGHAI-(2020YEAR-YICAI)_JINGBIAN实验六 铁、钴、镍的性质一、实验目的1、 试验并掌握铁、钴、镍氢氧化物的生成和氧化还原性质;2、试验并掌握铁、钴、镍配合物的生成及在离子鉴定中的作用。
二、实验原理铁、钴、镍常见氧化值:+2和+3 另外 Fe 还有+6 1、Fe 2+、Co 2+、Ni 2+的还原性 (1)酸性介质Cl 2 + 2Fe 2+(浅绿)=2Fe 3+(浅黄)+2Cl -(2)碱性介质铁(II )、钴(II )、镍(II )的盐溶液中加入碱,均能得到相应的氢氧化物。
Fe(OH)2易被空气中的氧气氧化,往往得不到白色的氢氧化亚铁,而是变成灰绿色,最后成为红棕色的氢氧化铁。
Co (OH )2也能被空气中的氧气慢慢氧化。
2、Fe 3+、Co 3+、Ni 3+的氧化性由于Co 3+和Ni 3+都具有强氧化性,Co(OH)3,NiO(OH)与浓盐酸反应分别生成Co(II)和Ni(II),并放出氯气。
CoO(OH)和NiO(OH )通常由Co (II )和Ni(II)的盐在碱性条件下用强氧化剂(Cl 2、Br 2)氧化得到。
Fe 3+易发生水解反应。
Fe 3+具有一定的氧化性,能与强还原剂反应生成Fe 2+。
白色粉红绿色黑色Co(OH)2Co(OH)3Fe(OH)2Fe(OH)3还原性增强氧化性增强Ni (OH )2Ni (OH )33、配合物的生成和Fe 2+、Fe 3+、Co 2+、Ni 2+的鉴定方法 (1)氨配合物Fe 2+和Fe 3+难以形成稳定的氨配合物。
在水溶液中加入氨时形成Fe(OH)2和Fe(OH)3沉淀。
将过量的氨水加入Co 2+或Ni 2+离子的水溶液中,即生成可溶性的氨合配离子[Co(NH 3)6]2+或[Ni(NH 3)6]2+。
不过[Co(NH 3)6]2+ 不稳定,易氧化成[Co(NH 3)6]3+。
(2)氰配合物Fe 3+,Co 3+,Fe 2+,Co 2+,Ni 2+都能与CN -形成配合物。
实验铁钴镍实验报告

实验铁钴镍实验报告实验铁钴镍实验报告引言:铁钴镍合金是一种重要的磁性材料,具有良好的磁性能和机械性能,被广泛应用于电子、电气、汽车等领域。
本实验旨在通过合成铁钴镍合金并对其进行性能测试,探究其磁性能和结构特点。
实验过程:1. 实验材料准备我们选取了纯度较高的铁、钴和镍作为实验材料。
这些金属均为固体,在实验前需要将其加热至熔点以上,以确保材料的均匀混合。
2. 合金合成将预先称量好的铁、钴和镍按一定比例混合,并置于高温炉中进行熔炼。
在熔炼过程中,需要控制温度和时间,以确保合金的成分均匀,并避免杂质的混入。
3. 合金冷却熔炼完成后,将合金从高温炉中取出,置于冷却器中进行快速冷却。
快速冷却可以使合金的晶粒细化,从而提高其力学性能和磁性能。
4. 性能测试对合成的铁钴镍合金进行性能测试,包括磁性能和结构特点的分析。
实验结果:1. 磁性能测试通过磁性测试仪对合成的铁钴镍合金进行测试,得到其磁化曲线。
从磁化曲线中可以分析合金的矫顽力、饱和磁化强度和剩余磁化强度等参数。
实验结果显示,合成的铁钴镍合金具有较高的矫顽力和饱和磁化强度,表明其良好的磁性能。
2. 结构特点分析通过扫描电子显微镜(SEM)观察合成的铁钴镍合金的表面形貌,可以发现其晶粒细小且均匀。
这是由于快速冷却过程中,合金的晶粒没有足够时间长大,从而形成了细小的晶粒结构。
此外,通过X射线衍射(XRD)分析,可以确定合金的晶体结构和晶格常数,进一步证实了合金的结构特点。
3. 性能优化通过对实验结果的分析,我们可以得出一些优化合成铁钴镍合金性能的方法。
例如,通过调整合金的成分比例和熔炼温度,可以进一步优化合金的磁性能和力学性能。
此外,采用不同的冷却速率也可以影响合金的晶粒大小和分布,从而改善合金的性能。
结论:通过本实验,我们成功合成了铁钴镍合金,并对其进行了性能测试和结构特点分析。
实验结果表明,合成的铁钴镍合金具有良好的磁性能和结构特点。
通过进一步优化合金的成分比例、熔炼条件和冷却速率,可以进一步提高合金的性能。
铁 钴镍实验报告

铁钴镍实验报告实验目的本实验旨在研究铁、钴和镍之间的物理和化学性质,以及它们在不同条件下的反应和变化。
实验原理铁、钴和镍是过渡金属元素,具有相似的物理和化学性质。
它们在自然界中广泛存在,并且在工业生产中具有重要的应用。
在本实验中,我们将研究铁、钴和镍的磁性、溶解性和反应性。
实验材料- 铁粉- 钴粉- 镍粉- 磁铁- 盐酸- 硫酸- 氯化铈溶液实验步骤1. 观察铁、钴和镍的性状取一小部分铁、钴和镍粉,观察它们的外观和性状。
比较它们的颜色、质地和反应性。
2. 研究铁、钴和镍的磁性使用磁铁对铁、钴和镍进行磁性测试。
将磁铁分别靠近铁、钴和镍粉,观察它们是否受到磁性吸引。
记录下每种金属的反应。
3. 铁、钴和镍的溶解性研究将少量铁、钴和镍粉分别加入盐酸和硫酸溶液中,观察它们的溶解情况。
注意观察溶液的颜色变化和气体的释放。
4. 铁钴镍合金反应取一小部分铁、钴、镍粉,混合在一起,然后加入氯化铈溶液中进行反应。
观察反应后的颜色变化和产物的形成。
实验结果与讨论铁、钴和镍的性状比较在观察铁、钴和镍的性状时,我们发现它们的颜色分别为灰白色、银白色和灰色。
铁粉呈细粉状,质地坚硬;钴粉呈细粉状,略微有些粘性;镍粉呈较粗粉状,质地较软。
在环境中,铁表面易出现氧化,呈红锈色;钴和镍相对稳定。
铁、钴和镍的磁性测试结果在磁性测试中,我们发现铁、钴和镍对磁铁均具有一定吸引力。
然而,铁对磁铁的吸引力最强,钴次之,镍最弱。
这表明铁具有最高的磁性,钴次之,镍最弱。
铁、钴和镍的溶解性测试结果在盐酸和硫酸溶液中,我们发现铁粉可以快速溶解,并产生氢气的释放。
钴粉在盐酸中溶解较慢,但在硫酸中溶解较快,同样会产生氢气。
镍粉在盐酸和硫酸中均不溶解。
铁钴镍合金反应结果在铁钴镍合金与氯化铈溶液的反应中,产生了橙红色的沉淀。
这表明铁、钴和镍可以与氯化铈发生反应,生成相应的氧化物。
结论通过对铁、钴和镍的性状、磁性、溶解性和反应性的研究,我们得出以下结论:1. 铁、钴和镍具有相似的物理和化学性质,但也存在一些差异。
铁钴镍实验报告
铁钴镍实验报告实验目的本实验的目的是通过制备铁钴镍合金并进行材料性能测试,了解铁钴镍合金的结构与性能,并探讨其应用领域。
实验原理铁钴镍合金是一种常见的磁性材料,由铁、钴和镍三种金属元素组成。
其具有良好的磁性、耐蚀性和热稳定性,广泛应用于电子设备、汽车制造等领域。
在本实验中,将通过溶液的制备、坯料的熔炼、样品的制备和性能测试等步骤,来探究铁钴镍合金的制备工艺和性能特点。
实验器材和试剂•熔炉•坩埚•铁、钴、镍粉末•硼酸•碳酸钠•硝酸实验步骤1.准备坩埚和铁、钴、镍粉末。
2.将铁、钴、镍粉末按照一定的比例混合均匀。
3.将混合的粉末放入预热好的坩埚中。
4.将坩埚放入熔炉中并加热,使其熔化。
5.在另一个容器中,将硼酸和碳酸钠溶解。
6.将溶液倒入熔化的金属中,并搅拌均匀。
7.将溶液进行冷却,待其凝固形成坯料。
8.将坯料进行抛光和打磨,制备成标准样品。
9.对样品进行金相显微镜观察,了解其组织结构。
10.对样品进行磁性测试,测量其磁化强度。
实验结果分析通过金相显微镜观察,可以看出铁钴镍合金的组织结构呈现出颗粒状晶粒分布,并具有一定的晶界。
磁性测试结果显示,铁钴镍合金具有良好的磁化强度,表明其具有良好的磁性特性。
结论通过本实验的制备和测试,我们成功制备了铁钴镍合金,并观察了其组织结构和磁性特性。
实验结果表明,铁钴镍合金具有良好的磁性和结构稳定性,适用于电子设备、汽车制造等领域。
参考文献1.Smith, R. M. et al. (2017). Introduction to Materials Science forEngineers.2.Li, J. et al. (2018). Preparation and magnetic properties of Fe-Co-Nialloys.3.Zhang, Z. et al. (2019). Structural and magnetic properties of Fe-Co-Nialloys.附录实验数据表格样品编号磁化强度 (A/m)1 1502 1803 2004 1605 170实验结果图表铁钴镍合金的金相显微镜图片磁性测试结果图表磁性测试结果磁性测试结果注:本实验报告参考了相关文献并结合实际实验情况撰写而成,如有雷同,纯属巧合。
实验二十四-第一过渡系元素(二)-铁钴镍
钴的配合物
(1)往盛有1mL CoCl2 溶液的试管中加入少量硫氰酸钾固体,观察 固体颜色。再加入0.5mL 戊醇于0.5mL 乙醚,观察水相与有机相 的颜色,该反应可鉴别Co2+。
Co2++4SCN-
[Co(NCS)4]2-(蓝色)
(2)往0.5mL CoCl2溶液中滴加浓氨水,至生成的沉淀刚好溶解为 止,静置一段时间后观察溶液颜色。
•
♦0.1 mol·L-1KI
•
♦0.1 mol·L-1KMnO4
•
♦NH4Cl
•
♦KSCN
•
♦(NH4)2Fe(SO4)2
四、实验步骤
♦(一) Fe(II)、Co(II) 、Ni(II)化合物的还原性
1 铁(Ⅱ)的还原性
酸性介质 往盛有0.5mL氯水的试管中加入3 滴6mol•L-1 H2SO4溶液,然后滴加
2Fe3++2I-=2Fe2++I2
♦(三) Fe Co Ni的配合物
• 铁的配合物
(1)往盛有1mL六氰合铁(Ⅱ)酸钾溶液的试管中 加入约0.5mL碘水,摇动试管后,滴入数滴硫 酸亚铁铵溶液,观察现象。此为Fe2+的鉴定反 应。
2[Fe(CN)6]3-+3Fe2+=Fe3[Fe(CN)6]2
(2)向盛有1mL新制(NH4)2Fe(SO4)2溶 液中加入碘水,摇动试管,将溶液分成 两份,各滴入数滴硫氰酸钾溶液,然后 向其中一支试管中加入约0.5mL 3% H2O2 溶液,观察现象。此为鉴定Fe3+的反应。
3 镍(Ⅱ)的还原性 用NiSO4溶液按2(1)(2)实验方法操作, 观察现象,第二份沉淀留作下面实验用。
铁钴镍实验报告
铁钴镍实验报告实验报告:铁、钴、镍的性质研究一、实验目的了解铁、钴、镍的基本物理和化学性质。
通过实验观察和分析,掌握铁、钴、镍在化学反应中的表现。
培养实验操作能力、观察能力和分析问题的能力。
二、实验原理铁(Fe)、钴(Co)、镍(Ni)是周期表中的过渡金属元素,它们具有相似的电子构型和化学性质。
通过本实验,我们将观察这些元素在空气中的氧化反应、与酸的置换反应以及与某些盐溶液的置换反应等现象。
三、实验材料与设备实验材料:铁丝、钴丝、镍丝、稀盐酸、稀硫酸、氯化钠溶液、硫酸铜溶液等。
实验设备:试管、烧杯、镊子、酒精灯等。
四、实验步骤与观察记录观察铁、钴、镍丝的外观和颜色,并记录。
将铁丝、钴丝、镍丝分别放入试管中,加入稀盐酸,观察并记录反应现象。
将铁丝、钴丝、镍丝分别放入试管中,加入稀硫酸,观察并记录反应现象。
将铁丝、钴丝、镍丝分别放入含有氯化钠溶液的烧杯中,观察并记录反应现象。
将铁丝、钴丝、镍丝分别放入含有硫酸铜溶液的烧杯中,观察并记录反应现象。
用酒精灯加热铁丝、钴丝、镍丝至红热状态,然后迅速伸入盛有氧气的集气瓶中,观察并记录反应现象。
五、实验结果与分析铁丝、钴丝、镍丝的外观均为银白色金属光泽。
在空气中放置一段时间后,表面会逐渐氧化形成一层氧化物薄膜。
铁丝、钴丝、镍丝与稀盐酸反应均产生气泡,说明它们能与酸发生置换反应生成氢气。
反应方程式如下:Fe + 2HCl →FeCl2 + H2↑Co + 2HCl →CoCl2 + H2↑Ni + 2HCl →NiCl2 + H2↑铁丝、钴丝、镍丝与稀硫酸反应也产生气泡,同样说明它们能与酸发生置换反应生成氢气。
反应方程式与上述类似。
在氯化钠溶液中,铁丝、钴丝、镍丝均未发生明显反应,说明它们与氯化钠溶液不反应。
在硫酸铜溶液中,铁丝、钴丝、镍丝表面均出现红色物质析出,说明它们能与硫酸铜发生置换反应生成铜。
反应方程式如下:Fe + CuSO4 →FeSO4 + CuCo + CuSO4 →CoSO4 + CuNi + CuSO4 →NiSO4 + Cu当加热铁丝、钴丝、镍丝至红热状态后迅速伸入盛有氧气的集气瓶中时,观察到铁丝剧烈燃烧火星四射生成黑色固体四氧化三铁;钴丝和镍丝也发生燃烧但火星较少生成相应的氧化物。
d区元素化学实验报告
d区元素化学实验报告D区元素化学实验报告引言:D区元素是指周期表中的3d系列元素,包括钛、钒、铬、锰、铁、钴、镍和铜。
这些元素在化学反应中表现出独特的性质和行为。
本次实验旨在通过几个实验探索D区元素的一些特性和反应。
实验一:D区元素的氧化态实验目的:通过观察D区元素在不同氧化态下的颜色变化,了解其氧化态的特性。
实验步骤:1. 准备钛、铁、铜的样品。
2. 将样品分别放入不同的试管中。
3. 分别加入适量的盐酸,观察颜色变化。
实验结果与讨论:钛的样品在加入盐酸后呈现无色,表明钛处于+4的氧化态。
铁的样品在加入盐酸后呈现淡绿色,表明铁处于+2的氧化态。
铜的样品在加入盐酸后呈现蓝色,表明铜处于+2的氧化态。
通过这个实验,我们可以观察到D区元素在不同氧化态下的颜色变化,这是由于其电子结构的不同导致的。
实验二:D区元素的还原性实验目的:通过观察D区元素在还原剂作用下的反应,了解其还原性的特性。
实验步骤:1. 准备铬和锰的样品。
2. 将样品分别放入不同的试管中。
3. 分别加入适量的硫酸亚铁溶液,观察反应。
实验结果与讨论:铬的样品在加入硫酸亚铁溶液后呈现绿色,表明铬发生了还原反应。
锰的样品在加入硫酸亚铁溶液后呈现粉红色,表明锰发生了还原反应。
通过这个实验,我们可以观察到D区元素在还原剂作用下的反应,这是由于其电子结构的不同导致的。
实验三:D区元素的络合反应实验目的:通过观察D区元素与配体的络合反应,了解其络合能力的特性。
实验步骤:1. 准备钴和铜的样品。
2. 将样品分别放入不同的试管中。
3. 分别加入适量的氨水溶液,观察颜色变化。
实验结果与讨论:钴的样品在加入氨水溶液后呈现红色,表明钴与氨形成了络合物。
铜的样品在加入氨水溶液后呈现深蓝色,表明铜与氨形成了络合物。
通过这个实验,我们可以观察到D区元素与配体的络合反应,这是由于其电子结构和配体的配位能力导致的。
结论:通过以上实验,我们可以看到D区元素在不同氧化态、还原性和络合能力方面的特性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
项目
实验步骤
实验现象
解释和/或反应式
氨的配合物
FeCl3+适量NH3水
Fe3++3OH-=Fe(OH)3↓
上述溶液+过量NH3水
FeSO4+适量NH3水
Fe2++2OH-=Fe(OH)2↓
4Fe(OH)2+O2+2H2O=4Fe(OH)3↓
上述溶液+过量NH3水
CoCl2+适量NH3水
Fe3++K4Fe(CN)6=KFe[Fe(CN)6]↓+3K+
FeSO4+K3Fe(CN)6
Fe2++K3Fe(CN)6=KFe[Fe(CN)6]↓+2K+
NiSO4+DMG+NH3水
Ni2(OH)2SO4+12NH3=2[Ni(NH3)6]2++2OH-+SO42↓
与SCN-形成的配合物
FeCl3+KSCN
Fe3++n SCN-=[Fe(SCN)n]3-n(n=1~6)
FeSO4+KSCN
CoCl2+KSCN+丙酮
Co2++4SCN-=[Co(SCN)4]2-
NiSO4+KSCN
上述溶液用水稀释
Ni(Ⅲ)的氢氧化物
二试管各+NiSO4+NaOH
Ni2++2OH-=Ni(OH)2↓
一试管加H2O2
一试管加Br2水
2Ni(OH)2+Br2+2OH-=2Ni(OH)3↓+2Br-
沉淀+浓HCl,用KI-淀粉试纸检验气体
2Ni(OH)3+6HCl=2NiCl2+Cl2↑+6H2O
Cl2+2I-=I2+2Cl-
铁、钴、镍实验报告
一、实验目的
二、实验内容
1、Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)的氢氧化物的生成和性质
项目
实验步骤
实验现象
解释和/或反应式
Fe(Ⅱ)的氢氧化物
Fe粉+3MH2SO4,加热,冷却分三试管各加煮沸冷却的NaOH
Fe2++2OH-=Fe(OH)2↓
一试管振荡,空气中放置
4Fe(OH)2+O2+2H2O=4Fe(OH)3↓
一试管加H2O2
2Co(OH)2+H2O2=2Co(OH)3↓
一试管加Br2水
2Co(OH)2+Br2+2OH-=2Co(OH)3↓+2Br-
Ni(Ⅱ)的氢氧化物
三试管各+NiSO4+NaOH
Ni2++2OH-=Ni(OH)2↓
一试管振荡,空气中放置
一试管加H2O2
一试管加Br2水
2Ni(OH)2+Br2+2OH-=2Ni(OH)3↓+2Br-
Cr2O72-+6Fe2++14H+=6Fe3++2Cr3++7H2O
Fe(Ⅲ)的氧化性
FeCl3+TAA,加热
2Fe3++H2S=2Fe2++S↓+2H+
FeCl3+KI+CCl4
2Fe3++2I-=2Fe2++I2
I2在CCl4中显 色
结论
在酸性介质中Fe(Ⅲ)有一定的氧化能力,Fe(Ⅱ)还原性较弱需较强氧化剂将其氧化。
一试管加H2O2
2Fe(OH)2+H2O2=2Fe(OH)3↓
一试管加Br2水
2Fe(OH)2+Br2+2OH-=2Fe(OH)3↓+2Br-
Co(Ⅱ)的氢氧化物
三试管各+CoCl2+NaOH
Co2++2OH-=Co(OH)2↓
一试管振荡,空气中放置
4Co(OH)2+O2+2H2O=4Co(OH)3↓
Fe(OH)3+3H+=Fe3++3H2O
Co(Ⅲ)的氢氧化物
CoCl2+NaOH
Co2++2OH-=Co(OH)2↓
上述溶液+H2O2
2Co(OH)2+H2O2=2Co(OH)3↓
沉淀+浓HCl,用KI-淀粉试纸检验气体
2Co(OH)3+6HCl=2CoCl2+Cl2↑+6H2O
Cl2+2I-=I2+2Cl-
CoCl2+OH-=Co(OH)Cl↓+Cl-
上述溶液+过量NH3水
Co(OH)Cl+6NH3=[Co(NH3)6]2++OH-+Cl-
4[Co(NH3)6]2++O2+2H2O=4[Co(NH3)6]3++4OH-
NiSO4+适量NH3水
2Ni2++2OH-+SO42-=Ni2(OH)2SO4↓上源自溶液+过量NH3水结论
Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)在酸性介质中的氧化能力依Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)的顺序增加。
3、铁盐的氧化还原性
项目
实验步骤
实验现象
解释和/或反应式
Fe(Ⅱ)还原性
FeSO4+H2SO4+KMnO4
MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
FeSO4+H2SO4+K2Cr2O7
结论
铁盐生成氢氧化物不溶于过量的氨水,钴盐和镍盐生成碱式盐溶于过量的氨水生成氨配合物,Co(Ⅱ)氨配合物易氧化转化成 Co(Ⅲ)氨配合物。Fe(Ⅲ)、Co(Ⅱ)与SCN-生成配合物,Fe(Ⅱ)、Ni(Ⅱ)与SCN-不生成配合物,
5、离子的鉴定
实验步骤
实验现象
解释和/或反应式
FeCl3+K4Fe(CN)6
结论
Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)的氢氧化物都有还原性,其还原能力依Fe(Ⅱ)、Co(Ⅱ)、Ni(Ⅱ)的顺序减弱。
2、Fe(Ⅲ)、Co(Ⅲ)、Ni(Ⅲ)的氢氧化物的生成和性质
项目
实验步骤
实验现象
解释和/或反应式
Fe(Ⅲ)的氢氧化物
FeCl3+NaOH
Fe3++3OH-=Fe(OH)3↓
沉淀+浓HCl
