分子平均平动动能
理想气体分子的平均平动动能与温度

微观量的统计平均值
宏观可测量量
温度 T 的物理意义
1 2 3 k m v kT 2 2
1) 温度是分子平均平动动能的量度 (反映热运动的剧烈程度).
k T
2)温度是大量分子的集体表现,个别分子无意义. 3)在同一温度下,各种气体分子平均平动动能均 相等。 热运动与宏观运动的区别:温度所反 注意 映的是分子的无规则运动,它和物体的整 体运动无关,物体的整体运动是其中所有 分子的一种有规则运动的表现.
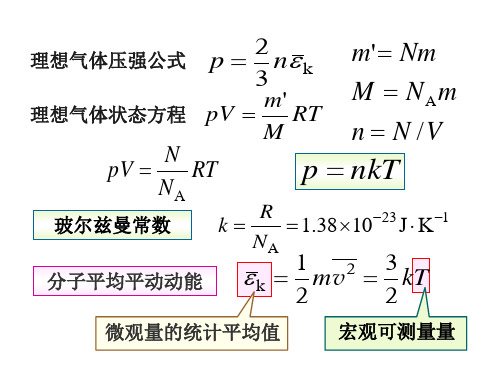
2 m' Nm 理想气体压强公式 p n k 3 M NAm m' 理想气体状态方程 pV RT M n N /V N pV RT p nkT NA
玻尔兹曼常数 分子平均平动动能
R k 1.38 1023 J K 1 NA
1 3 2 k m v kT 2 T , 一个分子 的质量为 m ,k 为玻尔兹曼常量,R 为摩 尔气体常量,则该理想气体的分子数为:
(A)
pV m
(B) pV (D)pV
(kT )
(m T )
(C) pV
( RT )
解
p nkT
pV N nV kT
讨论
一瓶氦气和一瓶氮气密度相同,分子平均平动动 能相同,而且它们都处于平衡状态,则它们 (A)温度相同、压强相同。
(B)温度、压强都不同。 (C)温度相同,但氦气的压强大于氮气的压强. (D)温度相同,但氦气的压强小于氮气的压强.
N k 解 p nkT kT T V m p( N 2 ) p(He) m( N 2 ) m(He)
分子的平均平动动能

F引 F引
r0
F合
r
F引
r0 平衡距离
F斥
(2)当r<r0时,随r的减小,F引、F斥都增大,F斥比F引增 大得快,F斥>F引,分子力表现为斥力,r减小,分子力增大
F
F斥
r>r0
F斥
F引
F引
F斥
0
r0
F合
r
F引
(3)当r>r0时,随r 的增加,F引、F斥都减小,F斥 比F引减小得快,F斥<F引,分子力表现为引力
第四步: 计算N个分子给器壁的平均冲力:
mv m N 2 vx F Fi l x i 1 lx i i 1
该面所受压强
F 1 P S l x l y lz
N
2 x
Nm 1 ( mv V N i
N 2 ix
2 v ix ) nm v i
N
_____
2 x
定义分子速率平均值
v
则
v
i
i
N
;
定义分子速率平方的平均值
vx v y vz ; 2 v i 2
v
2 z
i
N
; v2
v v v ;
2 x 2 y 2 z
则
1 2 v v v v ; v x v y vz v 3
2 2 x 2 y
2
2
2
注意:统计规律有涨落 (fluctuation), 统计对象的数量越大,涨落越小。
微观理论,从分子热运动观点出发,依赖微 观粒子的力学规律,运用统计方法研究气体 分子热运动的宏观性质和变化规律。寻求宏 观量与微观量之间的关系,揭示气体宏观热 现象及其规律的微观本质。
理想气体分子的平均平动动能与温度
3 2
kT
1) 温度是分子平均平动动能的量度 k T
(反映热运动的剧烈程度). 2)温度是大量分子的集体表现,个别分子无意义.
3)在同一温度下,各种气体分子平均平动动能均 相等。
注意
热运动与宏观运动的区别:温度所反 映的是分子的无规则运动,它和物体的整
体运动无关,物体的整体运动是其中所有 分子的一种有规则运动的表现.
例 理想气体体积为 V ,压强为 p ,温度为 T , 一个分子 的质量为 m ,k 为玻尔兹曼常量,R 为摩 尔气体常量,则该理想气体的分子数为:
(A) pV m (C) pV (RT )
(B)pV (kT )
(D)pV (mT )
解 p nkT
N nV pV kT
讨论
一瓶氦气和一瓶氮气密度相同,分子平均平动动 能相同,而且它们都处于平衡状态,则它们
(A)温度相同、压强相同。来自(B)温度、压强都不同。
(C)温度相同,但氦气的压强大于氮气的压强.
(D)温度相同,但氦气的压强小于氮气的压强.
解
p nkT N kT k T
V
m
m(N2 ) m(He) p(N2 ) p(He)
理想气体压强公式 理想气体状态方程
p
2 3
n k
pV m' RT
M
m' Nm M NAm n N /V
pV N RT NA
p nkT
玻尔兹曼常数
k R 1.381023J K1
NA
分子平均平动动能
k
1 mv2 2
3 kT 2
微观量的统计平均值
宏观可测量量
温度 T 的物理意义
k
1 mv2 2
分子平均平动动能-精品

12-4 理想气体分子平均平动动能与温度的关系
第五版
理想气体压强公式
p
2 3
n k
理想气体物态方程 p nkT
分子平均平动动能:
k
1mv2 2
3kT 2
微观量的统计平均 宏观可测量量
第十二章 气体动理论
1
物理学
12-4 理想气体分子平均平动动能与温度的关系
第五版
温度 T 的物理意义
第十二章 气体动理论
4
物理学
12-4 理想气体分子平均平动动能与温度的关系
第五版
2 理想气体体积为 V ,压强为 p ,温度为 T . 一个分子 的质量为 m ,k 为玻耳兹曼常 量,R 为摩尔气体常量,则该理想气体的分 子数为:
(A) pV m (B) pV(kT)
(C) pV(RT) (D) pV(mT)
k
1mv2 2
3kT 2
(1)温度是分子平均平动动能的量度.
k T
(2)温度是大量分子的集体表现.
(3)在同一温度下各种气体分子平均平 动动能均相等.
第十二章 气体动理论
2
物理学
12-4 理想气体分子平均平动动能与温度的关系
第五版
注意
热运动与宏观运动的区别:温度所 反映的是分子的无规则运动,它和物体 的整体运动无关,物体的整体运动是其 所有分子的一种有规则运动的表现.
解 p nkT
N nV pV kT
第十二章 气体动理论
5
第十二章 气体动理论
3
物理学
12-4 理想气体分子平均平动动能与温度的关系
第五版
讨论
1 一瓶氦气和一瓶氮气质量密度相同,分子 平均平动动能相同,且都处于平衡状态,则:
12-4理想气体分子的平均平动动能与温度的关系

1 2
m 1 v12
1 2
m2
v22
v12 m2
v22
m1
•当温度T=0时,气体的平均平动动能为零,这时气体
分子的热运动将停止。然而事实上是绝对零度是不可 到达的(热力学第三定律),因而分子的运动是用不停 息的。
第十二章 气体动理论
3
物理学
12-4 理想气体分子平均平动动能与温度的关系
第五版
注意
(A) pV m (B) pV (kT )
(C) pV (RT ) (D) pV (mT )
解 p nkT
N nV pV kT
第十二章 气体动理论
6
分子平均平动动能:
k
1 2
mv2
3 2
kT
微观量的统计平均 宏观可测量量
第十二章 气体动理论
1
物理学
12-4 理想气体分子平均平动动能与温度的关系
第五版
温度 T 的物理意义
k
1 mv2 2
3 kT 2
(1)温度的微观本质:温度是分子平均平动动能的量度.
k T
(2)温度是大量分子的集体表现.单个分子的温度无意义。
大学物理124理想气体分子的平均平动动能与温度的关系理学院物理系2019323方均根速率ms气体种类第十二章气体动理论124理想气体分子平均平动动能与温度的关系物理学第五版a温度相同压强相同
物理学
12-4 理想气体分子平均平动动能与温度的关系
第五版
理想气体压强公式
p
2 3
n k
理想气体物态方程 p nkT
(3)同一温度下各种气体分子平均平动动能均相等.
(4)温度的实质:分子热运动剧烈程度的宏观表现。
理想气体分子的平均平动动能与温度的关系

V
m
第十二章 气体动理论
4
物理学
12-4 理想气体分子平均平动动能与温度的关系
第五版
2 理想气体体积为 V ,压强为 p ,温度为 T . 一个分子 的质量为 m ,k 为玻耳兹曼常 量,R 为摩尔气体常量,则该理想气体的分 子数为:
(A) pV m (B) pV (kT )
(C) pV (RT ) (D) pV (mT )
第十二章 气体动理论
3
物理学
12-4 理想气体分子平均平动动能与温度的关系
第五版
讨论
1 一瓶氦气和一瓶氮气密度相同,分子平均 平动动能相同,而且都处于平衡状态,则:
(A)温度相同、压强相同.
(B)温度、压强都不同.
(C)温度相同,氦气压强大于氮气压强.
(D)温度相同,氦气压强小于氮气压强.
解 p nkT N kT k T
解 p nkT
N nV pV kT
第十二章 气体动理论
5
k
1 mv2 2
ห้องสมุดไป่ตู้
3 kT 2
(1)温度是分子平均平动动能的量度.
k T
(2)温度是大量分子的集体表现.
(3)在同一温度下各种气体分子平均平 动动能均相等.
第十二章 气体动理论
2
物理学
12-4 理想气体分子平均平动动能与温度的关系
第五版
注意
热运动与宏观运动的区别:温度所 反映的是分子的无规则运动,它和物体 的整体运动无关,物体的整体运动是其 中所有分子的一种有规则运动的表现.
物理学
12-4 理想气体分子平均平动动能与温度的关系
第五版
理想气体压强公式
分子平均平动动能:
分子平均平动动能:分子平均平动动能是描述分子热运动的一种物理量,它揭示了分子在热运动过程中的平均运动情况。
在我们日常生活中,热能是无处不在的,分子的平动动能是构成热能的基本要素之一。
本文将从定义、计算方法以及一些实际应用等方面来详细介绍分子平均平动动能。
首先,我们来看一下分子平均平动动能的定义。
分子平均平动动能是指一个系统中所有分子平动动能的平均值。
根据动能的定义,分子平均平动动能可以用公式K_avg = (1/2) mv^2 来表示,其中m是分子的质量,v是其速度。
这个公式表明,分子的运动速度越大,分子的平动动能也就越大。
那么如何计算分子平均平动动能呢?我们需要用到统计物理学中的一些基本概念和理论。
首先,我们需要知道系统中分子的数目N和总的平动动能E,那么分子平均平动动能K_avg =E/N。
在理论计算中,可以采用玻尔兹曼分布定律来确定分子速度的分布概率,进而计算出分子平均平动动能。
实际上,分子平均平动动能不仅仅是一个理论概念,它在很多实际应用领域都有很大的作用。
首先,分子平均平动动能是理解物质的热性质和热传导的基础。
在热力学中,平动动能的增加意味着系统的温度升高,而热传导则是分子平均平动动能在不同物体之间的传递。
此外,分子平均平动动能还在研究化学反应动力学和速率论方面具有重要意义。
在化学反应中,分子发生碰撞并因此发生反应。
分子平均平动动能的高低会对化学反应的速率和动力学过程产生影响。
分子平均平动动能还与气体的压力有密切关系。
根据理想气体状态方程,P V = N k T,其中P是气体的压力,V是气体的体积,N是气体的分子数,k是玻尔兹曼常量,T是气体的温度。
由此可见,温度升高和分子平均平动动能的增加,会导致气体的压强增加。
最后需要注意的是,分子平均平动动能只是热能的一部分,还有分子的转动动能和振动动能等。
这些能量组成了分子的总动能。
而热能是分子或粒子的总动能的表现形式,它包括热力学性质(如温度、热容等)和能量传递机制的研究。
12-4理想气体分子的平均平动动能与温度的关系讲解
则 pV NkT 或 p nkT
温度的微观本质
p
nkT 与压强公式
P
2 3
n k
比较
得
k
1 2
v2
3 2
kT
处于平衡态的理想气体,分子的平均平 动动能与气体的温度成正比。
例1 计算标准状态下,任何气体在1cm3体积中 含有的分子数 。
1 2 3
若各种气体的分子数密度分别为 n1,n2,n3,…
则混合气体的分子数密度为
n=n1+n2+n3+…
将n代入 p 2n / 3 ,得
p
2 3
n
2 3
(n1
n2
n3
)
p
2 3
n11
2 3
n2 2
2 3
n3 3
即 p p1 p2 p3
—— 道尔顿分压定律。
其中
p1
2 3
n11,
p2
2 3
n2 2 ,
p3
2 3
n3 3 ,
例3 有一容积为 10 cm3 的电子管,当温度为
300 K时用真空泵抽成高真空,使管内压强为 5×10-6 mmHg。求 (1) 此时管内气体分子的
数目; (2) 这些分子的总平动动能。
解 (1) 由理想气体状态方程得
N
pV kT
5106 133.3105 1.381023 300
12.4 温度的微观本质
一、理想气体温度与分子平均平动动能的关系
理想气体分子的平均平动动能为
1 v2 1 3kT
2
2
3 kT
2
理想气体分子平均平动动能与温度的关系
四、理想气体分子平均平动动能与温度的关系(可以用一个公式加以概括)k ε=kT v m 23212=1.简单推导:理想气体的物态方程:RT m N m N RT M m PV A ''== 而⎪⎭⎫ ⎝⎛=⎪⎭⎫ ⎝⎛=2221322132v m V N v m n P n=N/V 为单位体积内的分子数,即分子数密度, k =R /N A =1.38×10-23J·K -1称为玻尔斯曼常量。
所以:kT v m 23212= 这就是理想气体分子的平均平动动能与温度的关系,是气体动理论的另一个基本公式。
它表明分子的平均平动动能与气体的温度成正比。
气体的温度越高,分子的平均平动动能越大;分子的平均平动动能越大,分子热运动的程度越剧烈。
因此,温度是表征大量分子热运动剧烈程度的宏观物理量,是大量分子热运动的集体表现。
对个别分子,说它有多少温度,是没有意义的。
从这个式子中我们可以看出2.温度的统计意义该公式把宏观量温度和微观量的统计平均值(分子的平均平动动能)联系起来,从而揭示了温度的微观本质。
关于温度的几点说明1.由kT v m 23212=得021 02=v m T =,=ε,气体分子的热运动将停止。
然而事实上是绝对零度是不可到达的(热力学第三定律),因而分子的运动是用不停息的。
2.气体分子的平均平动动能是非常小的。
J K T 2110,300-==ε J K T 15810 ,10-==ε例1. 一容器内贮有氧气,压强为P=1.013×105Pa ,温度t=27℃,求(1)单位体积内的分子数;(2)氧分子的质量;(3)分子的平均平动动能。
解:(1)有P=nkT得 ()3252351045.2273271038.110013.1--⨯=+⨯⨯⨯==m kT P n (2)kg N M m A 262331031.51002.61032--⨯=⨯⨯==(3)J kT k 21231021.6)27327(1038.12323--⨯=+⨯⨯⨯==ε例2. 利用理想气体的温度公式说明Dalton 分压定律。
分子的平均平动动能
分子的平均平动动能分子的平均平动动能是指分子在三维空间内做自由运动时,其平均动能的大小。
分子的平均平动动能与温度密切相关,当温度升高时,分子的平均平动动能也会增加。
下面将对分子的平均平动动能进行详细解释:一、分子平均平动动能的定义分子的平均平动动能是指在某个温度下,各个分子在空间中做自由运动时,其动能的平均值。
由于气体分子随机运动,因此各个分子的动能大小不同,但在一个温度下,所有分子的平均动能是相同的。
二、分子平均平动动能的计算公式分子的平均平动动能可以用下面的公式进行计算:E_k = 1/2 * m * v^2其中,E_k表示平均平动动能,m表示分子的质量,v表示分子的速度。
由此可见,分子的动能与其质量和速度有关,质量越大、速度越快的分子,其动能也就越大。
三、分子平均平动动能与温度的关系在同一体积的气体中,温度越高,分子的平均平动动能也就越大,因为分子的能量是由其速度和质量共同决定的,而温度提高会导致分子的速度增加。
根据分子的平均平动动能和温度的关系,可以得出一个公式:E_k = 3/2 * k_b * T其中,k_b表示玻尔兹曼常数,T表示温度。
这个公式说明,分子的平均平动动能与温度成正比,温度升高,分子的平均平动动能也会增加。
四、应用举例气温的测量:根据气体分子的平均平动动能与温度的关系,可以设计出一些测量气温的方法。
例如,可以测量气体分子的速度,从而计算出气体的温度。
材料科学:研究材料的热学性质时,需要考虑分子的平均平动动能,因为分子的动能会影响材料的热膨胀、热导率等性质。
总之,分子的平均平动动能是一个非常重要的物理量,对于研究和应用都具有重要意义。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
