苯乙酮的制备1
苯乙酮的制备研究

苯乙酮的制备研究苯乙酮,在有机化学中也称为酮类。
它是一种重要的中间体,广泛用于食品、化妆品和药物等领域。
苯乙酮的制备方法有许多种,其中比较常用的方法包括芳香族酰胺水解法、芳香族硫醇氧化法、苄基溴化为酮等。
芳香族酰胺水解法是苯乙酮的一种重要制备方法。
该方法的反应物是苯乙酰胺和水,在催化剂的促进下,苯乙酰胺与水发生水解反应,即生成苯乙酮和氨。
水解反应的方程式为:C6H5CONH2 + H2O => C6H5COCH3 + NH3。
催化剂通常是醋酸或硫酸,反应进行时需要保持适当的温度和pH值。
使用醋酸作为催化剂时,反应温度通常保持在80~100℃之间,反应溶液的pH值控制在3~4之间。
苯乙酸在水中较为容易溶解,所以水解反应可以在水相中进行。
反应完成后,将产物分离出来,并通过蒸馏和结晶等步骤进行纯化。
该反应通常在10%氢氧化钾和乙醇混合溶液中进行催化,反应温度保持在50℃左右。
苯乙酮和水可以形成混合溶液,通过蒸馏、结晶等步骤进行分离和纯化,得到高纯度的苯乙酮。
该反应需要在大量溴和催化剂存在的情况下进行,其中催化剂通常使用过渡金属催化剂如Pd、Pt等。
反应温度较高,通常在80~120℃之间。
反应后,通常需要进行萃取和纯化等步骤来提高产物的纯度。
以上几种制备苯乙酮的方法,各有优缺点。
芳香族酰胺水解法是简单易行、成本低,但产物纯度有限。
芳香族硫醇氧化法产物纯度高,但反应较为复杂。
苄基溴化为酮反应条件苛刻,但产物纯度较高。
选择何种方法制备苯乙酮,应根据具体需求和实验条件进行选择。
苯乙酮的制备1

答:加酸的目的是使苯乙酮析出;其反应如下:
O
_CCH3. AlCl3 H+ ,H2O
O
_CCH3 + AlCl3
• 1.实验装置图:
• 2.实验步骤:
• ⑴制备:
• 安装好仪器;在干燥的三口烧瓶中加入13g无水三氯化铝和 16ml苯..在搅拌下逐滴加入4ml乙酸酐;控制加入速度;使 烧瓶刚刚感到发热为准..然后对三口烧瓶进行水浴加热;保 持反应容器微沸;直至没有氯化氢放出为止..
• ⑵精制:
• 将反应混合物冷却到室温;在搅拌下倒入盛有18ml浓盐酸 和35g碎冰的烧杯中;溶解完成后..
• 用分液漏斗分离有机层和水层;水层用8ml苯萃取两次;合 并有机相..
• 有机相依次用等体积5%氢氧化钠和水洗涤;再用无水硫酸 镁干燥..
• 在水浴上加热;蒸馏出大量的苯;再换成石棉网加热;蒸馏出 残留的苯;冷却后用石棉网加热;改成空气冷凝管;蒸馏收集 188~192℃曲靖的馏分..
纯苯乙酮为无色透明油状液体;bp为202℃;mp为20.5℃;nD201.5372
• 5.由于最终产物不多;宜选用较小的蒸馏瓶;苯溶液可用分液漏斗分批 加入蒸馏瓶中..
• 6.滴加苯乙酮和乙酐混合物的时间以10min为宜;滴的太快温度不易控 制
七、思考题
1、在苯乙酮的制备中;水和潮气对本实验有何影响 在仪器装置和操作中应注意哪些事项..答:破坏试剂 影响产率;导致失败因三个试剂都属无水..应采取措施 :⑴药品仪器均需干燥..⑵回流冷凝管上装一个干燥 管..⑶整个装置密合不漏气..
五、实验结果
1. 计算产率理论产量以醋酸酐为准计算
2.也可用减压蒸馏..苯乙酮在不同压力下的沸点列表如下:
苯乙酮的制备(精)
苯乙酮的沸点文献值为202.0℃,熔点为20.5℃, 折光率l.5372。
图1、带滴 液漏斗和 气体吸收 装置的反 应装置
乳胶管联结 气体吸收
NaOH水 溶 液
苯乙酮的制备
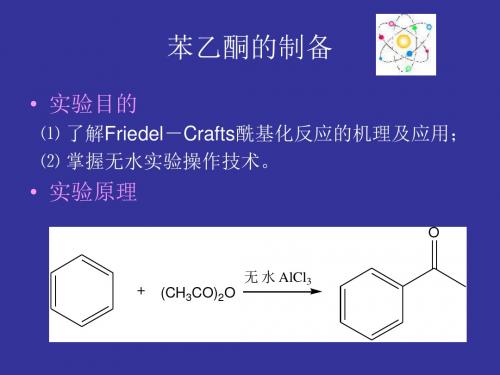
• 实验目的
⑴ 了解Friedel-Crafts酰基化反应的机理及应用; ⑵ 掌握无水实验操作技术。• Fra bibliotek验原理O
+
无 水 AlCl3 (CH3CO)2O
操作步骤
迅速称取25g经研碎的无水AlCl3(放入三颈瓶中)+ 30 mL 经金属钠干燥过的苯,启动搅拌,由滴液漏斗滴加重新 蒸馏过的醋酸酐6mL(约6.5g,0.06mol)和无水苯10mL的 混合溶液(约20min滴完)。反应立即开始,伴随有反应混 合液发热及氯化氢急剧产生。控制滴加速度,勿使反应过 于激烈。滴加完后,在水浴(或电热套)上回流0.5h, 至无氯化氢气体逸出为止(此时三氯化铝溶完)。
将三颈瓶冷却,在搅拌下慢慢滴加100 mL冷却的稀盐酸。 当瓶内固体物质完全溶解后,分出苯层。水层每次用 15mL苯萃取两次。合并苯层,依次用5%的氢氯化钠溶 液、水各20mL洗涤,然后用无水硫酸钠(镁)干燥。
将干燥后的粗产物过滤,蒸去苯以后(温度升到140 ℃左右,停止加热) ,将粗产物转移到50mL的蒸馏
思考题
1、水和潮气对本实验有何影响?在仪器的装 置和操作中应注意哪些事项?为什么要迅速称 取研磨三氯化铝? 2、反应完成后为什么要加入冷却的稀盐酸? 3、指出如何由傅—克反应制备下列化合构:(1) 二苯甲烷;(2)苄基苯基酮;(3)对硝基二苯酮。
苯乙酮的制备研究

苯乙酮的制备研究苯乙酮,也叫丙酮苯,是一种有机化合物,化学式为C6H5COCH3,具有强烈的香气和刺激性。
因其广泛应用于工业和医药领域,因此对其制备方法进行深入研究,具有很高的实用价值。
本文对苯乙酮的制备研究进行探讨,介绍其常用的制备方法以及反应机理。
1.酸催化法该方法是通过酸性催化剂催化苯与丙酮反应生成苯乙酮。
常用的酸性催化剂有硫酸、磷酸、五氧化二磷等。
反应机理:酸性催化剂可以将丙酮中的α-氢离子去除,形成羰基负离子,然后与苯发生亲核加成反应,最终得到苯乙酮。
2.氧化偶联法该方法是通过将苯和丙酮溶于碱性氧化剂中进行氧化反应,生成苯甲基酮,然后再将其经过酸催化偶联反应,得到苯乙酮。
二、苯乙酮的反应机理苯乙酮是一种α-酮,其含有酮基和苯环,可以经过多种反应。
1.酮的加成反应苯乙酮的酮基可以发生羰基加成反应。
例如,苯乙酮与氨在氧化铜的催化下发生反应,生成咪唑类物质。
反应机理:氧化铜催化下,苯乙酮中的羰基吸引了氨中的一个氢离子,生成一种带负电荷的羰基中间体,接着,中间体进一步与氨发生亲核加成反应,得到产物。
2.催化加氢反应反应机理:在铂等贵金属催化剂作用下,氢气分子可以在铂催化剂表面吸附,然后分解成氢原子,接着,氢原子在催化剂表面反应,生成苯乙醇。
3.酮的羟醛化反应苯乙酮可以经过羟醛化反应变成苯乙醛。
例如,苯乙酮经过氢气和催化剂的作用下,可以生成苯乙醛。
反应机理:在催化剂的作用下,苯乙酮中的羰基吸引氢离子,然后经过析出水产生α,β-不饱和醛。
最后,α,β-不饱和醛在氢气的作用下,被还原成为苯乙醛。
苯乙酮广泛应用于工业和医药领域,如:1.工业领域苯乙酮作为有机合成材料,广泛应用于合成香料、染料、药物、树脂、柔性泡沫材料等领域。
2.医药领域总之,苯乙酮的制备方法和反应机理的研究,具有很高的实用价值,在生产和科研领域都有广泛的应用和重要的作用。
苯乙酮的制备研究

苯乙酮的制备研究苯乙酮,又称丙酮苯,是一种无色液体有机化合物,化学式为C6H5COCH3。
它具有独特的香味,在化工领域有着广泛的应用。
苯乙酮通常用作香水、药品和塑料制造的原料,也被用来生产染料,树脂和农药等化工产品。
苯乙酮的生产工艺以及制备方法在化工领域一直备受关注。
本文着重研究苯乙酮的制备方法,探究其生产工艺和优化措施。
一、苯乙酮的制备方法苯乙酮的制备方法主要包括酸碱法、酸酮偶合法、苯甲酮氧化、苯甲酮硝化等多种工艺。
其中以酸碱法和酸酮偶合法较为成熟和广泛应用。
1.酸碱法酸碱法是苯乙酮生产的传统工艺,也是经济实用的一种制备方法。
其反应如下:2 C6H5CH2Cl + 2 NaOH → C6H5COCH3 + 2 NaCl + 2 H2O苯乙酮生产工艺在操作和控制上较为简单,但废气处理较为复杂。
目前,酸碱法苯乙酮生产工艺已经具备较高的稳定性和成熟度,但由于产物纯度较低、副反应严重等问题,越来越多的企业将目光转向其他更为先进的制备方法。
二、苯乙酮的生产工艺苯乙酮的生产工艺主要包括原料处理、反应制备、产品分离等多个环节,整个工艺复杂且关联紧密。
1.原料处理苯乙酮的原料处理主要包括底物氧化、催化剂制备等多个环节。
底物氧化是指将前体物质如乙苯氧化为苯乙酮,该步骤需要合适的氧化剂以及适当的催化剂参与反应。
催化剂的制备则需要先进的制备工艺以及严格的质量控制,以确保产品的稳定生产。
2.反应制备反应制备是苯乙酮生产的核心环节,其反应条件的控制和催化剂的添加对产品质量影响极大。
目前,酸酮偶合法生产苯乙酮的反应制备中,催化剂的选取和稳定性是重点研究的方向。
3.产品分离产品分离是苯乙酮生产工艺中的最后一步,该环节直接影响产品的质量和产率。
目前,常用的产品分离方法主要包括单级结晶、溶剂萃取等。
三、苯乙酮的制备技术改进苯乙酮的制备技术改进主要包括反应条件的优化、催化剂的改进以及产品分离技术的改进等多个方面。
1.反应条件的优化反应条件的优化是苯乙酮制备中的重点方向之一,通过对底物浓度、反应温度、反应时间等参数进行调整,可以提高产品的产率和纯度。
《苯乙酮的制备》课件

苯乙酮是一种重要的化学品,在化学催化、医药和食品工业中得到广泛应用。
苯乙酮介绍
物理特性
白色晶体,微溶于水,易溶于乙醇、甲醇等有机溶剂。
化学性质
可以发生自由基反应、亲电加成反应和亲核取代反应等多种化学反应。
产业应用
主要应用于日化、医药、化学合成、生物科技等领域。
苯乙酮合成
醋苯的羟基化
通过将醋苯与顺式双羟乙基苯烷加热反应后,加入 氢氧化钠使其分解生成苯乙酮。
苯乙酮的应用
作为光引发剂
苯乙酮可用作照相学中的无色光敏剂和非黄色变色 剂,还可用于固化丙烯酸等工业生产中。
作为防晒剂
由于苯乙酮对紫外线有很强的吸收能力,所以它经 常被用于防晒产品中。
作为香料
苯乙酮是一种有醇香的化合物,常用于制作香囊、 蜡烛等香氛产品。
在食品工业中的应用
苯乙酮可以用作饮料、寿司、口香糖、果酱等食品 的防腐剂。
结论和未来方向
结论
在本次课程中,我们学习了苯乙酮的制备、性质、 合成和应用等方面的知识,并了解了苯乙酮的环保 和健康问题。
未来方向
虽然苯乙酮在许多领域都有广泛的应用,但其环保 和与人类健康有关的问题不能忽视,我们需要在制 备和应用过程中寻找更加环保和健康的替代方法。
将三氯化铝和醋酸加入反应瓶中,并加
入适量的苯,将硫酸的冷却溶液加入反
应瓶,同时滴加苯乙烯。
3
反应过程
ቤተ መጻሕፍቲ ባይዱ
将反应瓶密封后在沸水中进行加热,观
察溶液的颜色变化。反应结束后,冷却
分离与提纯
4
至室温。
通过蒸馏、结晶和有机相和水相的分离, 获得初步纯化的苯乙酮产物。
苯乙酮的分析
检查项目 蒸汽压 密度 折射率
苯乙酮的制备研究

苯乙酮的制备研究苯乙酮,也被称为乙苯酮,是一种有机化合物,化学式为C8H8O。
它是一种常用的有机合成中间体,广泛应用于医药、香料以及化妆品等领域。
本文将介绍苯乙酮的制备方法研究。
目前,苯乙酮的制备方法主要有四种:烯丙基化、芳香亲核取代、还原反应和酸解反应。
1. 烯丙基化法:烯丙基化法通过烯丙基基团与苯基团的偶联反应来制备苯乙酮。
一种常用的烯丙基化试剂是苯乙炔,它和很多齐聚试剂(如醇、醛、酮等)反应可以得到苯乙酮。
苯乙炔可以与酮类反应,生成相应的苯乙酮。
2. 芳香亲核取代法:芳香亲核取代法通过芳香化合物与酸、酰基化合物或酰化试剂反应制备苯乙酮。
常用的亲核试剂有醇、胺和硫氢化物等。
芳香亲核取代法的一个优点是可以采用氢氧化钠或碳酸钠等碱性条件作为催化剂,从而使得反应条件温和。
3. 还原反应法:还原反应法通过将酮化合物还原为相应的醇,然后进一步氧化为醛或酮,从而制备苯乙酮。
常用的还原剂有金属氢化物(如锂铝氢化物)、酸性溶液(如硫酸和亚硫酸)等。
4. 酸解反应法:酸解反应法通过酸催化将醇酮类化合物加水分解得到苯乙酮。
乙醇醇酮可以经过酸解反应得到苯乙酮。
酸解反应法的优点是操作简单,但副反应较多,需要选择适当的酸和反应条件,以提高产率。
还有很多其他的方法也可以用于苯乙酮的制备,如金属催化的氨基还原反应、过渡金属催化的C-H键取代反应等。
这些方法相对较新,需要更多的研究来完善优化。
苯乙酮的制备方法多种多样,可以根据需要选择适合的方法进行实验研究。
在制备苯乙酮的过程中,需要考虑反应的选择性、产率、操作简便性等因素,以达到高效、高产的目的。
未来的研究还可以通过改进催化剂、溶剂以及反应条件等方面,进一步提高制备苯乙酮的效率和选择性。
苯乙酮的制备

实验六苯乙酮的制备一、实验目的1.掌握傅瑞德尔-克拉夫茨酰基化反应;2.学习电动搅拌器的安装、使用以及减压蒸馏操作方法。
二、实验原理傅瑞德尔-克拉夫茨反应是指芳香烃在无水三氯化铝等催化剂存在下,同卤代烃、酰氯或酸酐作用,在苯环上发生亲电取代反应而引入烷基或酰基的反应。
(CH3CO)2O CH3COOH 无水AlClCH3O三、主要仪器和试剂1.仪器:电动搅拌器、电热套、三口瓶、球形冷凝管、分液漏斗、温度计、园底烧瓶、氯化钙干燥管;2.试剂:苯35g、无水三氯化铝20g、乙酸酐6.5g 、浓硫酸、浓盐酸、5%氢氧化钠溶液。
四、实验仪器及装置图五、实验操作流程搭建装置填料回流1小时冰水浴冷却加盐酸苯萃取洗涤,无水硫酸镁干燥常压蒸馏140度停热稍冷减压蒸馏,收集92~96度六、实验操作步骤现象、解释1、干燥仪器,及保证药品的无水。
2、20g无水三氯化铝和30ml苯,在滴液漏斗中加6ml乙酸酐和10ml苯的混合物;搅拌下缓慢滴加,反应开始,放出氯化氢气体,三氯化铝溶解,体系升温,控制温度,加料时间约20min。
3、加完乙酸酐关闭滴液漏斗旋塞,用电热套加热保持缓缓回流1h。
4、回流后,将三口瓶用冰水浴冷却至5~10℃,不断搅拌下滴加80ml20%盐酸至固体溶解。
分液漏斗分出苯层,水层用30ml苯分两次萃取。
用20ml氢氧化钠溶液洗涤,再用水洗涤。
分出苯层,用无水硫酸镁干燥。
5、将含苯的粗产物放入100ml圆底烧瓶,加沸石,蒸出苯,温度升到140℃左右,停止加热。
收集116~120℃/8.00kPa的馏分。
七、产率的计算,n D 20=1.5372。
纯苯乙酮,无色油状液体,熔点20℃,沸点202℃,d204=1.026。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一、 实验目的
1学习傅克反应的原理和方法,学习付克酰基化制备芳 学习傅克反应的原理和方法, 香酮的方法; 香酮的方法 2 .掌握有机合成的无水操作; 掌握有机合成的无水操作; 掌握有机合成的无水操作 3.掌握搅拌器的使用方法 掌握搅拌器的使用方法; 掌握搅拌器的使用方法 4. 进一步熟练蒸馏、液体的干燥、萃取等操作; 进一步熟练蒸馏、液体的干燥、萃取等操作;
苯 醋酸酐 苯乙酮
102.09 -73.1 120.15 20.5
四、实验操作步骤
• 1.实验装置图: 实验装置图: 实验装置图
• 2.实验步骤: 实验步骤: 实验步骤 • ⑴制备: 制备: • 安装好仪器,在干燥的三口烧瓶中加入13g无水三氯化铝 安装好仪器,在干燥的三口烧瓶中加入 无水三氯化铝 乙酸酐, 和16ml苯。在搅拌下逐滴加入 苯 在搅拌下逐滴加入4ml乙酸酐,控制加入速度, 乙酸酐 控制加入速度, 使烧瓶刚刚感到发热为准。然后对三口烧瓶进行水浴加热, 使烧瓶刚刚感到发热为准。然后对三口烧瓶进行水浴加热, 保持反应容器微沸,直至没有氯化氢放出为止。 保持反应容器微沸,直至没有氯化氢放出为止。 • ⑵精制: 精制: • 将反应混合物冷却到室温,在搅拌下倒入盛有 将反应混合物冷却到室温,在搅拌下倒入盛有18ml浓盐 浓盐 酸和35g碎冰的烧杯中,溶解完成后。 碎冰的烧杯中, 酸和 碎冰的烧杯中 溶解完成后。 • 用分液漏斗分离有机层和水层,水层用 用分液漏斗分离有机层和水层,水层用8ml苯萃取两次, 苯萃取两次, 苯萃取两次 合并有机相。 合并有机相。 • 有机相依次用等体积 氢氧化钠和水洗涤,再用无水硫 有机相依次用等体积5%氢氧化钠和水洗涤 氢氧化钠和水洗涤, 酸镁干燥。 酸镁干燥。 • 在水浴上加热,蒸馏出大量的苯,再换成石棉网加热,蒸 在水浴上加热,蒸馏出大量的苯,再换成石棉网加热, 馏出残留的苯,冷却后用石棉网加热,改成空气冷凝管, 馏出残留的苯,冷却后用石棉网加热,改成空气冷凝管, 蒸馏收集188~192℃(曲靖)的馏分。 曲靖) 蒸馏收集 ℃ 曲靖 的馏分。
七、思考题
1、在苯乙酮的制备中,水和潮气对本实验有何影响 ?在仪器装置和操作中应注意哪些事项。答:破坏试 答 剂影响产率,导致失败因三个试剂都属无水。应采取 措施:⑴药品仪器均需干燥。⑵回流冷凝管上装一个 干燥管。⑶整个装置密合不漏气。 2、反应完成后,为什么要加入浓盐酸和冰水的混合 液? 答:加酸的目的是使苯乙酮析出,其反应如下:
• 二 、实验原理 • 主要反应
+ (CH3CO)2O AlCl3 COCH3 + CH3COOH
副反应: 副反应:乙酸酐和氯化铝的水解反应
三、主要物料及其物理常数
化合物 分子 量 78.11 熔点 (℃) 5.5 沸点 (℃) 80.1 139.55 202 密度 溶解性 (g/cm3) (水) 0.8786 1.0820 1.5318 不溶 微溶 不溶
纯苯乙酮为无色透明油状液体, 为 纯苯乙酮为无色透明油状液体,bp为202℃,mp为20.5℃,nD201.5372 ℃ 为 ℃
五、实验结果
1. 计算产率(理论产量以醋酸酐为准计算)
2.也可用减压蒸馏。苯乙酮在不同压力下的沸点列表如下:
压力 /mmHg 沸点/℃ 压力 /mmHg 沸点/℃ 4 60 30 102 5 64 40 109.4 6 68 50 115.5 7 71 60 120 8 73 100 133.6 9 76 150 146 10 78 200 155 25 98
• 六. 注意事项
• 1.仪器必须是干燥的,否则影响反应顺利进行,而且反应容器要与空 1.仪器必须是干燥的,否则影响反应顺利进行, 仪器必须是干燥的 气隔绝,装置中凡是和空气相通的部位,应装置干燥管。 气隔绝,装置中凡是和空气相通的部位,应装置干燥管。 • 2.反应混合物与水混合时,一定要注意安全,会放出大量的氯化氢气 2.反应混合物与水混合时 一定要注意安全, 反应混合物与水混合时, 体。 • 3.注意不要将产品洒落,苯和苯乙酮都是有毒的,而且味道比较大。 3.注意不要将产品洒落 苯和苯乙酮都是有毒的,而且味道比较大。 注意不要将产品洒落, • 4.无水三氯化铝的质量是实验成败的关键之一,研细、称量及投料均 4.无水三氯化铝的质量是实验成败的关键之一,研细、 无水三氯化铝的质量是实验成败的关键之一 需迅速,避免长时间暴露在空气中(可在带塞的锥形瓶中称量)。 需迅速,避免长时间暴露在空气中(可在带塞的锥形瓶中称量)。 • 5.由于最终产物不多,宜选用较小的蒸馏瓶,苯溶液可用分液漏斗分 5.由于最终产物不多 宜选用较小的蒸馏瓶, 由于最终产物不多, 批加入蒸馏瓶中。 批加入蒸馏瓶中。 • 6.滴加苯乙酮和乙酐混合物的时间以10min为宜,滴的太快温度不易 6.滴加苯乙酮和乙酐混合物的时间以10min为宜, 滴加苯乙酮和乙酐混合物的时间以10min为宜 控制
O _CCH . AlCl 3 3
H+ ,H 2O
O _CCH + AlC
