制 程 稽 核 准 则(中英文对照版)
医学影像专业名词中英文对照

医学影像专业名词中英文对照学习必备欢迎下载学习必备欢迎下载Unit 4on cologycorresp ondingtherapy?肿瘤学on cologycorresp ondingtherapy对应的【医】疗法;治疗,疗效electro nproto n电子【物】(正)质子;氕核,氢核始基;朊胨prot on decay质子衰变n eutr on中子n eutr on bomb中子弹n eutr on capture中子俘获n eutr on nu mber【原物】(核内)中子数curre ntly现时,当前dose(药的)剂量,用量;一剂;投配量;【物】放射能剂量mi ni mizi ng极小化;求最小参数值tissue【生】组织;【医】组织培养;培养出来的组织target目标,靶子;对阴极(X射线中的靶),对[中间]电极beam【无】射线,射束;波束;(扩音器的)最大有效范围modality模态,形态,样式enhance增加(价值、价格、力量、吸引力等);提咼;增进;放大overall全部的,总的in itiate引进inten sity强度,密度,应力,亮度;强烈,剧烈modulate调节,调整tumor肿块,肿瘤dyn amic动力的;动力学的;动态的;电动的defi nitive 丨决定性的;最后的;明显的esse ntial本质的,实质的,基本的fuse熔化;使融合;合并,结合一起radioactivity放射性;放射现象;放射能力;放射学categorize加以类别,分类exter nal外部的;外面的brachytherapy短程治疗;近距治疗;浅部治疗;短距离放射治疗lin ear accelerator线性加速器,直导轨发射装置[核子]直线加速器gan try构台,桶架collimator【物】平行光管,视准仪;准直仪;准直光管rotate旋转;循环dime nsional空间的an atomy解剖学;解剖体;解剖体组织构造;解剖lesi on【医】(机体、器官等的)损害;损害,损伤irradiati on放射,照射modifier调节剂;调节器;改良[变性]剂;改变装置parameter参数criteria标准margin【医】缘in ternal内部的;在内部的cli nical 临床(教学)的;病房(用)的;诊所的in corporate(使)合并,并入metabolize产生代谢变化porti on一部分;区划[段]detect察觉,发觉,侦查,探测detector array检测器阵列metastasis〈医〉转移briefly暂时地,简要地laboratory实验室;化学实验室disti nctio n不同;区别conven ti onal惯例的,常规的simulator模拟器,假装者diag no stic诊断的,用于诊断的roun ded 全面的,圆形的gan try构台,桶架bore钻孔diameter直径accommodate供应,供给,向…提供,容纳,immobilizatio n固定,定位posture姿势,姿态;tube管,筒coronal冠;花冠;冠状物sagittal弧矢的,矢状的,径向的spatial空间的man datory命令的,强制的atte nuati on变薄,稀薄化,变细,衰减coefficie nt共同作用的voxel=(si ngle)volume eleme nt(CT image display)]( 一)容量成分(CT显影)virtual实际[质]上的,事实上的,可能的alig n排成直线;排成行tattoo(皮肤上)刺花纹,文身reference(与to连用)提及;涉及utilize利用correlate(使)相互关联illustrate举例说明,图解,加插图于,阐明prescribe optimal in teractive multiple parameter radiographic algorithm orthogo nal spectroscopic 指示,规定,处(方),开(药)最适宜的;最理想的;最好的相互作用[影响,配合,干扰]的,交互性的复合的;多样的参数,参量X光线照相术的[数]运算法则直角的;互相垂直的;正交的[物]分光镜的,借助分光镜的molecule分子;克分子;微点;微粒;一点点microscopic vomit显微镜的;用显微镜可见的呕吐,吐出nausea dem on strate pathological alterati on inferior极度的厌恶;引起人极度厌恶的东西示范,证明,论证由疾病引起的;伴杂疾病的变更,改变差的,次的interpretation surgery nasopharyngeal emission metabolic解释,阐明外科,外科学[解]鼻咽的(光、热等的)散发,发射,喷射代谢作用的,新陈代谢的abnormally diagnosis inadequate insulin prior hybrid morphologicradioisotope thorax dominant反常地,不规则地诊断不充分的,不适当的胰岛素优先的,在前的杂种,混血儿,混合物形态学(上),语形学的放射性同位素胸,胸腔,胸廓,胸部支配的abdome n decay morphologic compressor residual elimi nate suspend reproducible phase ultras ono graphy ultraso und腹部腐朽,腐烂,衰减形态学(上),语形学的?【医】收缩肌剩余的,残留的排除,消除吊,悬挂能繁殖的,可再生的,可复写的阶段,状态,相,相位[医]超声波检查法,超声波扫描术超频率音响comp onent tran sducer sonic成分传感器,变频器,变换器音速的obstetric sonographypreg nancy deli neati ng prostate discrepa ncy impleme nt pen etrate coefficie nt pan el bony prostate opaque bio compatibility fluoroscopic volumetric产科的[医]超声波检查法,超声波扫描术怀孕描绘前列腺的;前列腺相差,差异,矛盾贯彻,实现穿透,渗透[数]系数面板,嵌板,仪表板,多骨的,瘦骨嶙峋的前列腺的,前列腺不透明物个人简历(biography 的缩写)[计]兼容性荧光镜的,荧光检查法的测定体积的coronal sagittal cone冠,花冠,冠状物弧矢的,矢状的,径向的锥形物,圆锥体,beam geometry therapeutic feasible perpe ndicular algorithm梁,桁条,(光线的)束,柱,电波,横梁几何学治疗的,治疗学的,治疗剂,治疗学家可行的,切实可行的垂直的,正交的,垂线[数]运算法则rotate adjace nt collimator(使)旋转邻近的,接近的瞄准仪portal electrical imagi ng device入口电的,有关电的成像设备,装置,RT modifier slot=Radioisotope Tracer 放射性同位素指示剂,放射性示踪物修正的人,改造者,[语]修饰语,修饰成分缝,狭槽,compe nsator moun ted simulta neous con trast un dergo补偿者安在马上的,裱好的同时的,同时发生的对比,对照,(对照中的)差异经历,遭受,忍受Utrecht乌得勒支(何兰城市)outer外部的,外面的,远离中心的ring环,环形物,环状,superb庄重的,堂堂的,华丽的,极好的magn etic 磁的,有磁性的,有吸引力的dempster英国曼岛的法官(共两位)cobalt钴类颜料,由钴制的深蓝色prototype原型sole noid[电]螺线管robust精力充沛的nano表示极小[十亿分之一]imagi ng成像molecular分子的,由分子组成的。
稽核作业指导书(二)

引言概述:稽核作业是一项重要的管理活动,旨在确保组织内部业务运作的合规性、有效性和高效性。
稽核作业指导书是对稽核作业的具体步骤和要求进行规范和说明的工具,有助于稽核人员正确进行工作,并提高工作的质量。
本文将为您详细介绍稽核作业指导书的使用方法和内容要点。
正文内容:一、稽核目标与范围1.明确稽核目标:在开始稽核作业之前,要明确稽核的目标是什么,例如检查某个业务流程的合规性或评估某个部门的风险管理能力等。
2.确定稽核范围:确定稽核的范围是非常重要的,可以避免稽核人员的工作超范围或遗漏重要内容。
二、稽核计划和准备1.编制稽核计划:根据稽核目标和范围,制定详细的稽核计划,明确稽核的时间安排、人员分配、稽核程序等。
2.收集稽核准备资料:稽核作业需要相关的准备资料,例如文件、记录、数据等,稽核人员要提前收集并整理好这些资料,确保稽核工作的顺利进行。
三、稽核实施1.明确稽核程序:根据稽核计划,稽核人员要按照规定的程序进行稽核,例如了解被稽核对象的情况、收集证据、进行数据分析等。
2.采取合适的稽核方法:根据稽核的性质和目标,选择相应的稽核方法,例如文件审查、系统检查、询问当事人等。
3.及时沟通与报告:稽核过程中,稽核人员要与被稽核对象进行沟通,了解业务情况,同时要及时向上级主管报告稽核进展和发现的问题。
四、稽核结果评价与反馈1.结果评价:在稽核完成后,稽核人员要对稽核结果进行评价,判断业务运作的合规性和有效性,并提出改进意见或建议。
2.问题跟踪与整改:对于发现的问题,稽核人员要进行跟踪和整改,确保问题得到解决,并预防类似问题的再次发生。
3.主管评审和决策:稽核结果和意见要提交给上级主管,供其进行评审和决策,以采取适当的措施或纠正措施。
五、稽核总结与报告1.总结经验教训:稽核工作结束后,稽核人员要总结工作经验教训,包括稽核中遇到的问题、工作中的不足以及改进措施等。
2.编写稽核报告:将稽核过程、结果和评价等内容整理成稽核报告,报告要具有清晰、准确、全面的特点,并呈交给上级主管和相关部门。
内部稽核制度(5篇)

内部稽核制度一、目的:为加强财务监督机制,提高内部财务管理水平,确保集团资产安全完整,制定本制度二、权限1、对发现的会计凭证、会计账簿、会计核算、会计报表和其他资料的问题,属于会计业务的要求会计人员限期改正。
2、对发现内部管理缺陷,分析拟写内控稽核报告,提出修改完善业务流程制度建议,送呈有关部门讨论修订整改方案,并____整改工作进展。
3、对发现的不合法、不真实的原始凭证有权要求经办人员提供真实合法的原始凭证,对有损企业、集团利益的行为及时上报集团处理。
4、参与各公司内部财产清查,库存盘点,有价证券清理等专项稽核工作,调查有关经济事项。
5、____企业制度流程实施效果,保证企业、集团经营目标的实现。
三、稽核工作方法:1、一般性复核。
稽核相关联的原始记录,利用其对应的逻辑关系稽核有关原始凭证、记账凭证、账簿报表及其他会计资料的真实性、准确性。
稽核经济业务内容真实性、合理性、完整性、数字计算准确性。
稽核会计科目运用的正确性。
2、实地调查,对有疑问或不清楚的经济业务,可以深入现场进行实地调查,掌握经济事项的相关信息,取得真实数据。
稽核财务资料的真实性、合法性、合理性四、稽核的方式:1、对稽核发现的问题应积极分析原因,并提出改进措施,督促有关人员整改。
2、对有损集团利益的行为要逐级上报,未果情况可越级上报。
五、稽核的工作范围:1、稽核会计凭证各项要素完整,摘要描述清晰准确,印鉴及有关审批签章齐全,数字(包括大小写、金额、日期)准确,业务内容真实,会计凭证具有可靠性。
2、稽核会计报表的准确性,符合集团的统一要求和财务制度3、稽核收、付款流程,会计核算方式,资产定期盘点制度的执行情况。
4、稽核其他会计资料、各种票据、收付款、合同等管理情况的合规性及规范性。
5、稽核预算执行、考核情况,保证企业实现经营目标。
6、稽核年度财务预决算事项。
内部稽核制度(二)1、实行内部稽核制度,是为了加强会计人员相互制约,相互核对,提高会计工作的质量,防止会计事务处理中发生的失误和差错以及营私舞弊等行为。
IATF16949-中英文对照版2017-10-13NEW

d)产品安全相关特性的识别;
e)产品及制造时安全相关特性的识别和控制;
f)控制计划和过程FMEA的特殊批准;
g)反应计划(见第9。1。1。1条);
h)包括最高管理者在内的,明确的职责,升级过程和信息流的定义,以及顾客通知;
i)组织或顾客为与产品安全有关的产品和相关制造过程中涉及的人员确定的培训;
a)优化材料的流动和搬运,以Fra bibliotek对空间场地的增值利用,包括对不合格品的控制,并且
b)在适用时,便于材料的同步流动。
应开发并适时对新产品或新操作的制造可行性进行评价的方法.制造可行性评估应包括产能策划。这些方法还应适用于评价对现有操作的提议更改.
组织应保持过程有效性,包括定期风险复评,以纳入在过程批准、控制计划维护(见第8.5。1。1条)及作业准备的验证(见第8。5。1。3条)期间做出的任何更改。
h)改进过程和质量管理体系。
组织应确保所有的产品和过程,包括服务件及外包的产品和过程,符合一切适用的顾客和法律法规要求(见8。4。2.2条).
组织应有形成文件的过程,用于与产品安全有关的产品和制造过程管理;形成文件的过程包括但不限于(在适用情况下):
a)组织应对产品安全法律法规要求的识别;
b)向顾客通知a)项中的要求;
d)作为应急计划的补充,包含一个通知顾客和其他相关方的过程,告知影响顾客作业的任何情况的程度和持续时间;
e)定期测试应急计划的有效性(如:模拟,视情况而定);
f)利用包括最高管理者在内的跨部门小组对应急计划进行评审(至少每年一次),并在需要时进行更新;
g)对应急计划形成文件,并保留描述修订以及更改授权人员的形成文件的信息。
那些不适用组织的质量管理体系要求,不能影响组织确保产品和服务合格以及增强顾客满意的能力或责任,否则不能声称符合本标准的要求.
订单合同评审程序中英文对照版

订单评审程序Purchase order Review Procedure1、目的Purpose为保证公司能满足客户的要求,并能及时合理安排生产,故对客户所下之订单进行有效评审,特制定本程序。
This procedure is stipulated in order to meet customers’ requirements,assort production reasonable and timely and ensure to review customers’order and requirements effectively.2、适用范围Scope适用于公司所有客户订单的评审。
Be applicable to all customers' order review.3、定义Definition无No4、订单评审过程图Purchase order review flow chart输入部门:外部客户 Input: External customer 过程客户:外部客户 Process clients: customer 支持部门:工厂技术使用资源 Resources 1、 计算机网络Computer & internet 2、 电话过程责任者: Related principle:市场部经理。
其能力和资格见《岗位职务说明书》 Market manager, Specified requirements see job6、附加说明Additional notes市场部应每月按时将本月的客户订单和已交货订单汇总后交财务部,以便财务部做财务报表和成本分析。
Market dept. supervisor should collect customer order information like delivered or not delivered to financial dept。
【免费下载】工厂中英文对照
全檢 Follow up
跟進
Reject rate
不合格率 Manufacturability
可生產性
Pass rate
合格率 Questionnaire
問卷調查
Random check
隨機檢查 QA(Quality Assurance)
品質保証
Acceptance rate
可接收率 IQC(Incoming Quality Control)來料質量控制
Customer Complaint
客戶投訴 CPI(Continuous Process Improvement)
不斷的過程改制
Internal audit
內部審核 Non-conformance
不符合
Check list
檢查表 In-process control
制程中控制
CAR(Corrective Action Request)改進行動 Supplier Assessment
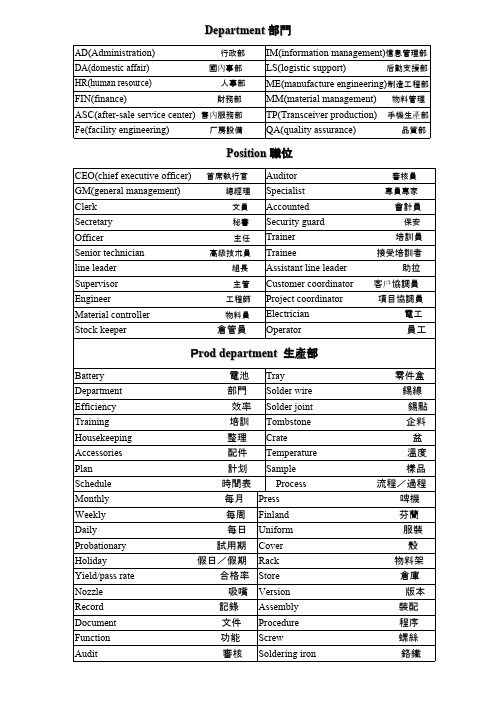
Department 部門
AD(Administration)
行政部
DA(domestic affair)
國內事部
HR(human resource)
人事部
FIN(finance)
財務部
ASC(after-sale service center) 售內服務部
Fe(facility engineering)
QA(quality assurance)
品質部
Position 職位
对全部高中资料试卷电气设备,在安装过程中以及安装结束后进行高中资料试卷调整试验;通电检查所有设备高中资料电试力卷保相护互装作置用调与试相技互术关,系电,力根保通据护过生高管产中线工资敷艺料设高试技中卷术资配,料置不试技仅卷术可要是以求指解,机决对组吊电在顶气进层设行配备继置进电不行保规空护范载高与中带资负料荷试下卷高总问中体题资配,料置而试时且卷,可调需保控要障试在各验最类;大管对限路设度习备内题进来到行确位调保。整机在使组管其高路在中敷正资设常料过工试程况卷中下安,与全要过,加度并强工且看作尽护下可关都能于可地管以缩路正小高常故中工障资作高料;中试对资卷于料连继试接电卷管保破口护坏处进范理行围高整,中核或资对者料定对试值某卷,些弯审异扁核常度与高固校中定对资盒图料位纸试置,.卷编保工写护况复层进杂防行设腐自备跨动与接处装地理置线,高弯尤中曲其资半要料径避试标免卷高错调等误试,高方要中案求资,技料编术试5写交卷、重底保电要。护气设管装设备线置备4高敷动调、中设作试电资技,高气料术并中课3试中且资件、卷包拒料中管试含绝试调路验线动卷试敷方槽作技设案、,术技以管来术及架避系等免统多不启项必动方要方式高案,中;为资对解料整决试套高卷启中突动语然过文停程电机中气。高课因中件此资中,料管电试壁力卷薄高电、中气接资设口料备不试进严卷行等保调问护试题装工,置作合调并理试且利技进用术行管,过线要关敷求运设电行技力高术保中。护资线装料缆置试敷做卷设到技原准术则确指:灵导在活。分。对线对于盒于调处差试,动过当保程不护中同装高电置中压高资回中料路资试交料卷叉试技时卷术,调问应试题采技,用术作金是为属指调隔发试板电人进机员行一,隔变需开压要处器在理组事;在前同发掌一生握线内图槽部纸内故资,障料强时、电,设回需备路要制须进造同行厂时外家切部出断电具习源高题高中电中资源资料,料试线试卷缆卷试敷切验设除报完从告毕而与,采相要用关进高技行中术检资资查料料和试,检卷并测主且处要了理保解。护现装场置设。备高中资料试卷布置情况与有关高中资料试卷电气系统接线等情况,然后根据规范与规程规定,制定设备调试高中资料试卷方案。
生产制程稽核行为标准_双语中英文对照版_
PROCESS AUDIT GUIDELINES制 程 稽 核 准 则SUGGESTED CONTENT包含的内容WORK INSTRUCTIONS作业指导书Available at each process step每个步骤是否被执行Work Instruction under revision control and at current revision level作业指导书是否有版本管制及当前版本。
Calls out current production part number and revision level有没有注明产品编号及版本。
Calls out direct materials P/N, description, usage, and designator有无直接罗列所用材料料号,规格,用量,点位。
Calls out operation machine name & station number, machine program name & revision, fixtures name/part number & revision有无机器名称/编号,机器程序名/版本,治具名/编号/版本。
Call out tools/gages with part number or name, indirect materials with detailed description, and their working conditions有无罗列所用工具及计量器名称或编号,以及用到的间接材料(如胶,锡丝)有无具体说明,包括他们工作条件。
Calls out work process/instruction for the station每一站有无罗列作业步骤及作业指导。
Call out highlights/special notes for the operation在作业指导书中有没有对相关注意事项做重点标识。
血站核酸检测工作导则(2016版)
血站核酸检测工作导则核酸检测技术用于血液筛查概述1.筛查项目目前用于血液筛查的核酸检测项目包括:人类免疫缺陷病毒核糖核酸(Human Immu nodeficie ncy Virus Rib onu cleic Acid, HIV RNA )、丙型肝炎病毒核糖核酸(Hepatitis C Virus Ribonucleic Acid,HCV RNA )和乙型肝炎病毒脱氧核糖核酸(Hepatitis B Virus Deoxyribo nucleic acid,HBV DNA )。
2.检测方式核酸检测技术(NAT筛查可通过两种方式进行:单人份检测(IDT)和混合样本检测(Pooled Testi ng )。
混合样本检测方法是先将献血者样本进行不多于8人份混合,然后进行核酸分离纯化和扩增检测。
对于反应性的混合样本再进行拆分检测,若拆分出反应性样本(可为一个或多个),则呈反应性反应的血液进入隔离程序;呈阴性反应的血液可进入合格放行程序;如全部样本检测结果均为阴性,则全部血液均可进入合格放行程序。
]混合样本检测模式宜在进行血清学检测后,将血清学检测阴性的样本进行混合样本检测。
单人份检测模式,是对单个样本进行检测的模式,其中对单个样本同时三个项目的检测而无法区分反应性项目的检测称为联合检测。
对于反应性的样本可进行鉴别试验以确定结果。
对于联检阳性样本不需等待鉴别结果,可以直接进入血液的隔离程序。
3.应用原则实验室的检测策略应该以有效保证阳性样本的检出为目的。
与血清学抗原抗体检测相结合才能真正起到提高血液安全性的作用,核酸检测对于早期感染的检测效果与当地的流行病学状况和献血人群是相关的,因此在选择检测体系与检测模式时应从检测通量、检测系统性能、检测成本、献血人群流行状况、业务工作流程等几个方面进行综合分析,选择适合的检测模式。
二、检测技术人员要求1.人员的配备与资质应有与核酸检测业务相适应的岗位设置和人员配备,满足从血液样本采集、接收到实验室报告发出的整个核酸检测过程及其支持保障等需求。
21CFR211中英文对照版(SMART)
PART 211 211部分- CURRENT GOOD MANUFACTURING PRACTICE FOR—制剂药品的CGMPFINISHED PHARMACEUTICALSSubpart A--General Provisions A.总 则§211.1 - Scope.211∙1范围§211.3 - Definitions.211∙3定义Subpart B--Organization and Personnel B.组织与人员§211.22 - Responsibilities of quality control unit.211∙22质量控制部门的职责§211.25 - Personnel qualifications.211∙25人员资格§211.28 - Personnel responsibilities.211∙28人员职责§211.34 - Consultants.211∙34顾问Subpart C--Buildings and Facilities C.厂房和设施§211.42 - Design and construction features.211∙42设计与建造特征§211.44 - Lighting.211∙44照明§211.46 - Ventilation, air filtration, air heating and211∙46通风、空气过滤、空气加热与冷却§211.48 - Plumbing.211∙48管件§211.50 - Sewage and refuse.211∙50污水和废料§211.52 - Washing and toilet facilities.211∙52洗涤和盥洗设备§211.56 - Sanitation.211∙56卫生§211.58 - Maintenance.211∙58保养Subpart D--Equipment D.设备§211.63 - Equipment design, size, and location.211∙63设备的设计、尺寸及位置§211.65 - Equipment construction.211∙65设备构造§211.67 - Equipment cleaning and maintenance.211∙67设备清洁与保养§211.68 - Automatic, mechanical, and electronic211∙68自动化设备、机械化设备和电子设备equipment.§211.72 - Filters.211∙72过滤器Subpart E--Control of Components and DrugE.成分、药品容器和密封件控制Product Containers and Closures§211.80 - General requirements.211∙80总要求§211.82 - Receipt and storage of untested211∙82未检验的成份、药品容器和密封件的接收与贮存components, drug product containers, and closures.§211.84 - Testing and approval or rejection of211∙84成份、药品容器和密封件的试验、批准或拒收components, drug product containers, and closures.§211.86 - Use of approved components, drug product211∙86获准的成份、药品容器和密封件的使用containers, and closures.§211.87 - Retesting of approved components, drug211∙87获准的成份、药品容器和密封件的复检product containers, and closures.§ 211.89 - Rejected components, drug product211∙89拒收的成份、药品容器和密封件containers, and closures.§ 211.94 - Drug product containers and closures.211∙94药品密封容器和密封件Subpart F--Production and Process Controls F .生产和加工控制§211.100 - Written procedures; deviations.211∙100成文的规程、偏差§211.101 - Charge-in of components.211∙101成分的控制§211.103 - Calculation of yield.211∙103 产量计算§211.105 - Equipment identification.211∙105设备鉴别§211.110 - Sampling and testing of in-process211∙110中间体和药品的取样与检验materials and drug products.§211.111 - Time limitations on production.211∙111生产时间限制§211.113 - Control of microbiological contamination.211∙113微生物污染的控制§211.115 - Reprocessing.211∙115返工Subpart G--Packaging and Labeling Control G.包装和标签控制§211.122 - Materials examination and usage criteria.211∙122材料的检查和使用标准§211.125 - Labeling issuance.211∙125标签的发放§211.130 - Packaging and labeling operations.211∙130包装和贴签操作§211.132 - Tamper-evident packaging requirements211∙132人用非处方药(OTC)保险包装的要求for over-the-counter (OTC) human drug products.§211.134 - Drug product inspection.211∙134药品检查§ 211.137 - Expiration dating.211∙137有效期Subpart H--Holding and Distribution H.贮存和销售§ 211.142 - Warehousing procedures.211∙142入库程序§ 211.150 - Distribution procedures.211∙150销售程序Subpart I--Laboratory Controls I∙实验室控制§ 211.160 - General requirements.211∙160总要求§ 211.165 - Testing and release for distribution.211∙165销售前的检验与发放§ 211.166 - Stability testing.211∙166稳定性试验§211.167 - Special testing requirements.211∙167特别检验要求§ 211.170 - Reserve samples.211∙170留样§ 211.173 - Laboratory animals.211∙173实验动物§ 211.176 - Penicillin contamination.211∙176青霉素污染Subpart J--Records and Reports J.记录和报告§ 211.180 - General requirements.211∙180总要求§ 211.182 - Equipment cleaning and use log.211∙182设备清洁和使用记录§ 211.184 - Component, drug product container,211∙184成份、药品容器、密封件及标签记录closure, and labeling records.§ 211.186 - Master production and control records.211∙186主要生产和控制的记录§ 211.188 - Batch production and control records.211∙188批生产和控制记录§ 211.192 - Production record review.211∙192产品记录复查§ 211.194 - Laboratory records.211∙194实验室记录§ 211.196 - Distribution records.211∙196销售记录§ 211.198 - Complaint files.211∙198客户投诉档案Subpart K--Returned and Salvaged Drug Products K.退货的药品和回收处理§ 211.204 - Returned drug products.211∙204退货的药品§ 211.208 - Drug product salvaging.211∙208 药品的回收利用Subpart A-General Provisions A.总 则§ 211.1 Scope211∙1范围(a) The regulations in this part contain the minimum current good manufacturing practice for preparation of drug products for administration to humans or animals.(a)本部分的条例包含人用或兽用药品制备的现行最低限度的药品生产质量管理规范(GMP)(b) The current good manufacturing practice regulations in this chapter, as they pertain to drug products, and in parts 600 through 680 of thischapter, as they pertain to biological products for human use, shall be considered to supplement, not supersede, the regulations in this part unless the regulations explicitly provide otherwise. In the event it is impossible to comply with applicable regulations both in this part and in other parts of this chapter or in parts 600 through 680 of this chapter, the regulation specifically applicable to the drug product in question (b)在本章里的这些针对药品的现行GMP条例和本章600至800的所有部分针对人用生物制品的现行GMP条例,除非明确另有说明者外,应认为是对本部分条例的补充,而是不代替。
WHO偏差处理和质量风险管理-中英文对照版-2013
25
质量风险管理实例
6.
Training 培训
28
7.
Conclusions 结论
29
8.
Glossary 术语
29
9.
References 文献
33
10. Acknowledgements 致谢
33
3
1) Purpose 目的
The aim of this guidance document is to contribute to the understanding of a quality risk management approach in the handling of deviations from a practical perspective as per WHO expectations on the matter. This proposal does not have the intent to be prescriptive in any way.
作为全面纠正和预防措施计划的一部分一旦发现偏差就需要立即采取措施即更正必要时确定其根本原因实施系统措施即纠正措施以防止未来相同或类似的不符合项
Deviation Handling and Quality Risk Management
偏差处理和质量风险理
A note for guidance for the manufacture of prequalified vaccines for supply to United Nations agencies
20
5.1.5 Purpose of Quality Risk Management 质量风险管理的目
20
的
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
PROCESS AUDIT GUIDELINES制程稽核准则SUGGESTED CONTENT包含的内容WORK INSTRUCTIONS作业指导书Available at each process step每个步骤是否被执行Work Instruction under revision control and at current revision level作业指导书是否有版本管制及当前版本。
Calls out current production part number and revision level有没有注明产品编号及版本。
Calls out direct materials P/N, description, usage, and designator有无直接罗列所用材料料号,规格,用量,点位。
Calls out operation machine name & station number, machine program name & revision, fixtures name/part number & revision有无机器名称/编号,机器程序名/版本,治具名/编号/版本。
Call out tools/gages with part number or name, indirect materials with detailed description, and their working conditions有无罗列所用工具及计量器名称或编号,以及用到的间接材料(如胶,锡丝)有无具体说明,包括他们工作条件。
Calls out work process/instruction for the station每一站有无罗列作业步骤及作业指导。
Call out highlights/special notes for the operation在作业指导书中有没有对相关注意事项做重点标识。
OPERATOR作业员Is operator certified for operation作业员是否有受过相关作业资格培训If operator is in training, verify adequate supervision在训新员工上线是否有人做足够的监督检查Ongoing program for re-certification of operators对作业员是否有再认证计划.Is operation staffed per Work Instructions作业指导书是否规定各操作负责人员.Is operation being performed per Work Instructions作业指导书上规定的操作是否都被执行.Is the operator monitored for his/her performance作业员的绩效是否被考核MATERIALS材料Production materials for each operation specified in Work Instructions and under A VL control 作业指导书是否有罗列出每站所需用到的生产材料, 并列入管制.Verify production materials are revision controlled & current检查生产材料是否有版本管制及目前版本状况Handling & storage guidelines called out in Work Instruction作业指导书中是否定义材料处理&存储办法.Compliance with handling & storage guidelines documented材料处理&存储办法是否被有效执行Scrap and nonconforming material is isolated from normal production废料和不良品是否与良品隔离Material preparation operations documented and controlled备料动作有无文件说明并被控制Controlled by an effective FIFO system是否有一个有效的先进先出的系统,并被执行Verify traceability of materials验证材料的可追溯性Self audit system to ensure correct material usage有无自检系统以确保材料的正确使用Materials are clearly marked/identified on line and storage area在产线上及存储区的材料是否有清楚的鉴别标识EQUIPMENT / TOOLING / FIXTURES仪器/工具/治具Calibration校准Preventive maintenance (PM) records and schedules, maintenance log预防保养履历记录,时间表,保养日志Hour log maintained between PM’s, replacement, etc.预防保养,更换等有无做时间记录,按小时数实施Tooling & fixtures identified by part number and revision工治具编号与版本Operating procedure available at each operation是否有对应于每一操作的作业程序Cycle count management / hour log for tooling对工具模具有无做周期循环/小时数管理ECO/ECN tracking工程变更单/工程变更通知跟踪Machine & tool capability studies performed and on file是否完成仪器工具性能研究并保存相关文件ESD CONTROL (IF APPLICABLE)静电管制(如可适用)Training records for all personnel对所有相关人员的培训记录Daily test logs in place现场测试日报All ESD systems in good working order and are properly installed and maintained所有正常控制的静电系统是否被恰当地安装并保养维护ESD earth ground rod is checked for grounding impedance and recorded on annual basis是否每年检查ESD接地棒对地阻抗并记录ESD grounding main system is checked for grounding impedance and recorded on monthly basis是否每月检测ESD接地系统对地阻抗并记录Instrument/fixtures/benches are checked for grounding impedance and recorded on weekly basis是否每周检测并记录仪器设备/治具/椅子等对地阻抗Wrist/heel strip, and/or conductive shoes are checked and recorded by shift是否每班检测并记录静电手环或传导鞋。
Wireless wrist strip is not allowed unless used with ionic blower and conductive floor无线手环是不被允许的,除非在离子吹风机和传导地板环境中使用All semiconductor materials are in ESD free container, package or bin when/during storage, transfer, and handling所有半导体材料在存储,运输及搬运中必须用防静电容器,防静电袋等进行静电防护。
People, semiconductor materials, machines, instrument, tools, fixtures, and working benches at ESD sensitive operation stations are grounded在静电敏感站的人员,半导体材料,机器,工具,治具及工作桌椅必须接地。
QUALITY CONTROL品质控制Effective SPC in place and closed loop corrective action is taken when out-of-control occurs 现场是否有做有效的SPC管制,当超出管制点时是否做CLCA。
Control limits of control chart are reviewed on monthly basis是否每月审查管制图之上下限Effective Continuous Improvement Process (CIP) in place现场是否实施有效持续改进过程Quality acceptance/rejection criteria established for each process step每段制程是否建立允收/拒收标准Effective quality inspection and measurement capability in place at each inspection station 在每一个检验站是否有进行有效的品质检验与测量Evidence that operators receive quality feedback and are responsible for the quality of their work是否保证作业员可收到品质反馈并改进他们作业品质。
Self audit system in place and effective是否有自我稽核系统并有效实施PRODUCTION PROCESS / FLOW生产制程/流程Does layout prevent misrouting of product and minimize handling线体设置是否能保证制程顺畅(产品不滞流)以达成最少的人工处理。
Evaluate physical layout for proper line balance and potential bottlenecks线体规划有无对其平衡及潜在瓶颈进行评估Is flow of defective product documented是否有文件定义不良品的处理流程Is line stop criteria documented and enforced to prevent excessive buildup of defectiveproduct是否有文件定义停线标准以强迫防止生产额外不良品Is customer’s process flow documented是否文件化客户制程流程TEST PROCESS测试过程Verify that test process is documented检查测试步骤方法是否文件化Is test equipment and software under revision control是否有对测试仪器与软件进行版本管制Test yield and defect data collection system exists, is automated and collects all data现有的测试单元及不良数据收集系统是否是自动化以及是否能够收集到所有数据Feedback to the defect source from test yields and defect data for improvement测试区域是否能及时反馈不良以加以改善Test process and production flow prevents test escapes or misrouting of product测试过程以及生产流程是否可以防止测试漏失及保证生产顺畅FAILURE ANALYSIS PROCESS不良分析过程Is process documented该制程是否文件化Are production materials and repair materials effectively controlled to prevent misrouting or wrong parts being used对生产及维修材料进行有效地控制以防止用错料。
