9D 铁盐检查法 2010年版中国药典一部附录
医学临床三基训练药师药物分析基本知识2_真题-无答案

医学临床三基训练药师药物分析基本知识2(总分140,考试时间600分钟)一、选择题A型题1. 重金属检查法中,若以硫代乙酰胺为显色剂,溶液最适宜的pH值为()A. 3~3.5B. 4~4.5C. 5~5.5D. 6~6.5E. 2~2.52. 《中国药典》(2010年版)铁盐检查法中,需将供试品中的Fe2+氧化成Fe3+,常用氧化剂是()A. 溴水B. 硝酸C. 硫酸D. 过硫酸铵E. 过氧化氢3. 在氯化物检查中,反应溶液需在“暗处”放置5分钟后再比较浊度,目的是()A. 避免碳酸银沉淀生成B. 避免单质银析出C. 避免氯化银沉淀生成D. 使生成的氯化银沉淀溶解E. 避免氯化银沉淀析出4. 二乙基二硫代氨基甲酸银(Ag—DDC)法检查砷盐的原理是()A. 砷盐与Ag(DDC)吡啶溶液作用,使Ag(DEC)中的DDC还原为红色胶态溶液B. 砷化氢与Ag(DDC)吡啶溶液作用,使Ag(DDC)中的银还原为银原子沉淀C. 砷盐与Ag(DDC)吡啶溶液作用,使Ag(DDC)中的银还原为红色胶态银D. 砷盐与Ag(DDC)吡啶溶液作用,使Ag(DDC)中的DDC还原为紫色溶液E. Ag(DDC)吡啶溶液与砷盐作用,使As3+还原为红色胶态砷5. 检查高锰酸钾中的氯化物时,需使高锰酸钾褪色后检查,所用试剂是()A. 硫化钠溶液B. 乙醇C. 过氧化氢溶液D. 维生素CE. 硝酸6. 《中国药典》中检查阿司匹林中的水杨酸的方法是()A. 三氯化铁反应B. 分光光度法C. 分离后酸碱滴定法D. 重氮化—偶合比色法E. 非水滴定法7. 《中国药典》检查布洛芬中有关物质,采用的方法是()A. 薄层色谱法B. 非水滴定法C. 高效液相色谱法D. 挥发法E. 重量法8. 用两步滴定法滴定阿司匹林片的含量,是因为()A. 片剂中有硬脂酸镁影响测定B. 阿司匹林片易水解C. 方法简便,结果准确D. 是片剂就要两步滴定法E. 片剂中有枸橼酸、酒石酸等稳定剂影响测定9. 盐酸普鲁卡因加氢氧化钠试液,加热,逸出的气体为()A. 二氧化硫B. 二氧化碳C. 氨气D. 二乙胺基乙醇E. 三乙胺10. 检查对乙酰氨基酚中的特殊杂质时,使用的试剂是()A. 氯化铜B. 亚硝基铁氰化钠C. 三硝基苯酚D. 三氯化铁E. 硫氰酸按11. 盐酸普鲁卡因注射液中应检查()A. 间氨基酚B. 对氯乙酰苯胺C. 对氨基苯甲酸D. 对氨基酚E. 对氨基水杨酸12. 与铜吡啶试液作用,生成绿色配位化合物的药物是()A. 戊巴比妥B. 异戊巴比妥C. 司可巴比妥D. 苯巴比妥E. 硫喷妥钠13. 《中国药典》(2010年版)中采用银量法测定苯巴比妥的含量时,指示终点的方法是()A. 自身指示法B. 铁铵矾指示剂法C. 邻二氮菲指示剂法D. 电位法E. 酚酞指示剂法14. 下列药物中可用溴量法测定含量的是()A. 水杨酸B. 司可巴比妥C. 枸橼酸钠D. 链霉素E. 苯巴比妥15. 于新制的碳酸钠溶液中加硝酸银试液,开始生成白色沉淀经振摇即溶解,继续加硝酸银试液,生成的沉淀不再溶解,则该药物应是()A. 庆大霉素B. 盐酸吗啡C. 青霉素D. 维生素CE. 苯巴比妥16. 亚硝酸钠—硫酸反应鉴别苯巴比妥药物的现象是()A. 生成蓝色产物,并随即转变为绿色B. 生成橙红色产物,并随即溶解C. 生成橙黄色产物,并随即转变为橙红色D. 生成黑色产物,并溶于氨试液E. 生成红色产物,并随即转变为黄色17. 磺胺甲噁唑中有关物质的检查时采用的方法是()A. 气相色谱法B. 高效液相色谱法C. 非水滴定法D. 银量法E. 薄层色谱法18. 《中国药典》中磺胺嘧啶的鉴别反应是()A. 重氮化—偶合反应B. 麦芽酚反应C. 三氯化铁反应D. Vitali反应E. 硫色素反应19. 《中国药典》测定诺氟沙星软膏的含量时采用的方法是()A. 紫外分光光度法B. 气相色谱法C. 薄层色谱法D. 高效液相色谱法E. 非水滴定法20. 异烟肼可由原料反应不完全或储藏中的降解反应而引入的杂质为()A. 对氨基酚B. 其他甾体C. 对氨基苯甲酸D. 游离肼E. 酮体21. 利用奥沙西泮水解产物进行的鉴别反应是()A. 坂口反应B. 三氯化铁反应C. 芳伯胺反应D. 沉淀反应E. 高锰酸钾反应22. 溴酸钾法测定异烟肼含量时,溴酸钾与异烟肼的摩尔比为()A. 3:2B. 1:3C. 1:2D. 2:1E. 2:323. 硫酸阿托品中莨菪碱的检查是利用了两者()A. 吸附性差异B. 紫外吸收光谱差异C. 旋光性质的差异D. 溶解度差异E. 酸碱性的差异二、选择题B型题A.硫代乙酰胺法B.第二法C.硫化钠法D.微孔滤膜法E.第五法重金属检查时:24. 难溶于稀酸,但能溶于碱性水溶液的药物采用()25. 在实验条件下,供试液澄清无色,对检查无干扰的药物采用()26. 仅含有2~5µg重金属杂质的药物采用()27. 难溶于水或稀醇的有机药物应采用()28. 中药制剂中重金属检查常采用()A.发生FeCl2反应B.水解后发生FeCl3反应C.发生麦芽酚反应D.发生重氮化—偶合反应E.水解后发生重氮化—偶合反应29. 链霉素()30. 水杨酸()31. 盐酸普鲁卡因()32. 阿司匹林()33. 对乙酰氨基酚()A.紫外分光光度法B.铈量法C.气相色谱法D.溴量法E.银量法34. 维生素E制剂的含量测定适宜采用()35. 苯巴比妥含量测定采用()36. 注射用硫喷妥钠含量测定采用()37. 葡萄糖酸亚铁原料药含量测定采用()38. 司可巴比妥钠含量测定采用()A.与亚硝酸—硫酸反应B.在稀硝酸中与银离子反应生成白色沉淀C.与碘试液的反应D.在氢氧化钠试液中与铅离子反应生成白色沉淀E.与硫酸反应39. 可用于鉴别硫喷妥钠的反应是()40. 可适用于鉴别氯化物的反应是()41. 可用于鉴别苯巴比妥的反应是()42. 可用于鉴别司可巴比妥钠的反应是()A.米黄色沉淀B.草绿色沉淀C.紫色沉淀D.绿色沉淀E.黄绿色沉淀,放置后为紫色43. 硫喷妥钠与铜盐反应生成()44. 磺胺甲噁唑与铜盐反应生成()45. 磺胺嘧啶与铜盐反应生成戊()46. 巴比妥与铜盐反应生成()A.硫代乙酰胺试液B.硫氰酸铵试液C.硝酸银试液D.硫化钠试液E.碘化钾试液47. 磺胺嘧啶中氯化物检查采用的试液是()48. 磺胺甲噁唑中重金属检查采用的试液是()49. 磺胺嘧啶中重金属检查采用的试液是()50. 右旋糖酐20中重金属检查采用的试液是()51. 葡萄糖中微量铁检查采用的试剂是()A.硝苯地平衍生物B.间氯二苯胺C.游离肼D.对氨基酚E.2—甲氨基—5—氯二苯酮分解产物52. 盐酸氯丙嗪有关物质检查主要控制物有()53. 硝苯地平中检查的有关杂质是()54. 地西泮注射液检查()55. 异烟肼检查()A.苯基—1,4—二氢吡啶B.吡啶环C.苯并二氮杂环D.硫氮杂蒽母核E.喹琳环56. 地西泮分子结构中有()57. 奋乃静分子结构中有()58. 硝苯地平分子结构中有()59. 异烟肼分子结构中有()60. 硫酸奎宁分子结构中有()A.银镜反应B.Vitali反应C.双缩脲反应D.三氯化铁反应E.坂口反应下列药物可采用的鉴别方法为:61. 异烟肼()62. 盐酸麻黄碱()63. 链霉素()64. 硫酸阿托品()65. 苯甲酸()三、选择题X型题66. 阿司匹林原料药中应检查的项目有()A. 重金属B. 醋酸C. 易碳化物D. 溶液的澄清度E. 游离水杨酸67. 能与三氯化铁试液显紫堇色的药物有()A. 阿司匹林B. 阿托品C. 丙磺舒D. 水杨酸E. 麻黄碱68. 两步滴定法测定阿司匹林片含量时,第一步消耗的氢氧化钠的作用是()A. 中和游离水杨酸B. 中和片剂中可能加入的有机酸C. 水解酯键D. 中和阿司匹林分子中的游离酸E. 中和游离醋酸69. 氯化物检查法中使用的试剂有()A. 硝酸银试液B. 稀盐酸C. 酸性氯化亚锡D. 25%氯化钡溶液E. 稀硝酸70. 《中国药典》(2010年版)肾上腺素采用的鉴别方法有()A. 坂口反应B. 与三氯化铁反应C. 重氮化—偶合反应D. 与硝酸银试液的反应E. 与过氧化氢反应71. 对乙酰氨基酚的含量测定方法有()A. 亚硝酸钠滴定法B. 双相滴定法C. 高效液相色谱法D. 紫外分光光度法E. 非水溶液滴定法72. 巴比妥类药物的鉴别反应包括()A. 与银盐的反应B. 与汞盐的反应C. 三氯化铁反应D. 与铜盐的反应E. 与甲醛—硫酸反应73. 属于苯巴比妥的鉴别反应有()A. 与硝酸银反应B. 与三氯化铁反应C. 与亚硝酸钠—硫酸反应D. 与盐酸羟胺反应E. 与甲醛—硫酸反应74. 《中国药典》采用银量法测定苯巴比妥含量时,选用的试剂有()A. 硝酸银试液B. 甲醇C. 醋酸D. 甲基橙指示液E. 3%新制无水碳酸钠溶液75. 采用溴量法测定司可巴比妥钠的含量时必须具备的条件是()A. 加入定量过量溴滴定液B. 在盐酸介质中进行滴定C. 用硫代硫酸钠滴定液滴定D. 用淀粉指示剂指示终点E. 加入过量的碘化钾溶液76. 《中国药典》中采用亚硝酸钠滴定法测定含量的药物有()A. 磺胺嘧啶B. 盐酸氯丙嗪C. 磺胺甲噁唑D. 盐酸麻黄碱E. 盐酸普鲁卡因77. 磺胺类药物的鉴别方法包括()A. 红外光谱法B. 与碘试液的反应C. 重氮化—偶合反应D. 三氯化铁反应E. 与硫酸铜的反应78. 溴酸钾法测定异烟肼含量的方法是()A. 1mol的溴酸钾相当于3/2mol的异烟肼B. 可用于异烟肼制剂的含量测定C. 在酸性条件下滴定D. 采用永停滴定法指示终点E. 属于氧化还原反应79. 紫外分光光度法测定盐酸氯丙嗪注射液的含量,下列说法中正确的有()A. 在最大吸收波长254nm附近处直接测定盐酸氯丙嗪的含量B. 利用百分吸收系数测定盐酸氯丙嗪的含量C. 在306nm处,维生素C有干扰D. 用对照品作对照来测定盐酸氯丙嗪的含量E. 在306nm处测定盐酸氯丙嗪的含量80. 异烟肼具有的性质和反应包括()A. 三氯化铁反应B. 还原性C. 弱碱性D. 与芳醛缩合呈色反应E. 重氮化—偶合反应四、是非选择题81. 《中国药典》分为凡例、正文、附录、索引四部分。
药物检验工(高级)理论试卷(四)
职业技能鉴定国家题库 药物检验工(高级)理论知识试卷 注 意 事 项 1、考试时间:120分钟。
2、请首先按要求在试卷的标封处填写您的姓名、准考证号和所在单位的名称。
3、请仔细阅读各种题目的回答要求,在规定的位置填写您的答案。
4、不要在试卷上乱写乱画,不要在标封区填写无关的内容。
一、单项选择(第1题~第80题。
选择一个正确的答案,将相应的字母填入题内的括号中。
每题1分,满分80分。
) 1、中国药典从( )年开始分为三部。
A 、1953 B 、1995 C 、2000 D 、2005 E 、1990 2、 药品检验工作程序是()。
A 、性状、检查、含量测定、检验报告 B 、鉴别、检查、含量测定、原始记录 C 、取样、检验(性状、鉴别、检查、含量测定)、记录与报告 D 、取样、鉴别、检查、含量测定 E 、性状、鉴别、含量测定、检验报告 3、 一般杂质检查方法收载在药典的( )。
A 、凡例 B 、品名目次 C 、正文 D 、附录 E 、索引 4、 中国药典2010年版附录中的内容不包括()。
A 、试药、试液 B 、质量检定有关的共性问题 C 、滴定液 D 、标准品 E 、对照品 5、分光光度法中不影响摩尔吸收系数的因素是( )。
A 、溶液的温度 B 、溶液的浓度 C 、入射光的波长 D 、物质的性质 6、由于产品要进行检测,需要从399件产品中抽取样品,那么需要随机抽取( )件样品进行检测。
A. 14B. 3C. 12D. 10E. 117、 中国药典规定的一般杂质检查中不包括的项目是()。
考 生 答 题 不 准超过此 线A、硫酸盐B、氯化物C、溶出度D、重金属8、药品抽样时一般不得少于检测用量的()倍。
A、1B、2C、3D、5E、随机抽取多少9、显色反应是指()。
A. 将无色混合物转变为有色混合物B. 向无色物质中加入有色物质C. 将无机物转变为有机物D. 将待测离子或分子转变为有色化合物10、某有色物质的摩尔吸收系数ε较大,则表示()。
《中国药典》2015年版通则编码与2010年版附录编码对照表
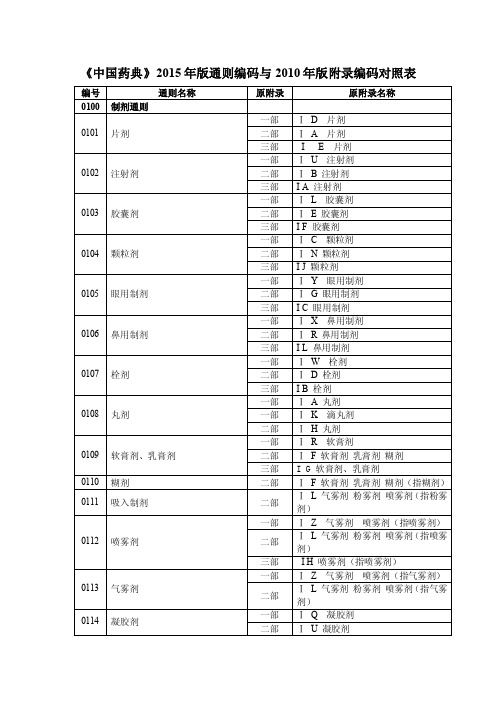
0500 色谱法 0501 纸色谱法
0502 薄层色谱法 0511 柱色谱法 0512 高效液相色谱法
一部 二部 三部 一部 二部 一部 二部 一部 二部
ⅥA ⅤA ⅢA ⅥB ⅤB ⅥC ⅤC ⅥD ⅤD
二部 Ⅷ R 制药用水中总有机碳测定法
一部 二部 一部 二部 二部 一部 二部 三部
一部
Ⅷ A 电位滴定法与永停滴定法 Ⅶ A 电位滴定法与永停滴定法 Ⅷ B 非水溶液滴定法 Ⅶ B 非水溶液滴定法 Ⅶ C 氧瓶燃烧法 Ⅸ L 氮测定法 Ⅶ D 氮测定法 Ⅵ A 氮测定法
Ⅸ M 乙醇量测定法
二部
二部 一部 二部 二部 二部 二部
《中国药典》2015 年版通则编码与 2010 年版附录编码对照表
编号
通则名称
0100 制剂通则
0101 片剂
0102 注射剂
0103 胶囊剂
0104 颗粒剂
0105 眼用制剂
0106 鼻用制剂
0107 栓剂
0108 丸剂
0109 软膏剂、乳膏剂 0110 糊剂 0111 吸入制剂
0112 喷雾剂
0113 气雾剂 0114 凝胶剂
0115 散剂
0116 糖浆剂
0117 搽剂
0118 涂剂
0119 涂膜剂
0120 酊剂
0121 贴剂 0122 贴膏剂
口服溶液剂 口服混悬剂 口服乳 0123 剂 0124 植入剂 0125 膜剂 0126 耳用制剂 0127 洗剂
0128 冲洗剂 0129 灌肠剂 0181 合剂 0182 锭剂 0183 煎膏剂(膏滋) 0184 胶剂 0185 酒剂 0186 膏药 0187 露剂 0188 茶剂 0189 流浸膏剂与浸膏剂
《中国药典》2015年版通则编码与2010年版附录编码对照表

1141 异常毒性检查法
1142 热原检查法
1143 细菌内毒素检查法 1144 升压物质检查法 1145 降压物质检查法 1146 组胺类物质检查法 1147 过敏反应检查法 1148 溶血与凝聚检查法
二一二三一三一二一二二三新部部部部部部部部部部部部增
ⅩⅢ ⅪⅫⅩⅢCF ⅪⅫⅩⅢDD ⅪⅫⅪⅩⅢEEF ⅪG
A A B B
非非电电水水位位溶溶滴滴液液定定滴滴法法定定与与法法永永停停滴滴定定法法
4
《中国药典》2015年版通则编码与2010年版附录编码对照表
编号
0703
氧瓶燃烧法
0704 氮测定法
通则名称
0711 乙醇量测定法
0712 甲氧基、乙氧基与羟丙氧基测定法 0713 脂肪与脂肪油测定法
二二二一三一一二二原部部部部部部部部部附录
0600 物理常数测定法 0601 相对密度测定法 0611 馏程测定法 0612 熔点测定法 0613 凝点测定法 0621 旋光度测定法 0622 折光率测定法
0631 pH值测定法
0632 渗透压摩尔浓度测定法
一二一二一二一二一二一二三一二三二一部部部部部部部部部部部部部部部部部部
ⅥⅦⅥⅦⅦⅥⅦⅥⅦⅥⅦⅥⅦⅥⅤⅪⅨⅤ
E异异常常毒毒性性检检查查法法 异常毒性检查法 A热原热检原查检法查法 热原检查法 D细菌细内菌毒内素毒检素查检法查法 细菌内毒素检查法 升压物质检查法 F降降压压物物质质检检查查法法
二一一二部部部部
ⅩⅢ ⅪⅩⅢK ⅪL
G过敏过反敏应反应检查检法查法 H溶血溶与血凝与聚凝检聚查检法查法
1200
1201 1202 1205 1206 1207 1208 1209 1210 1211 1212 1213
砷盐检查法操作规程

目的:制订砷盐检查法操作规程,明确其检查法的操作。
依据:《中华人民共和国药典》2010年版;《中国药品检验标准操作规范》2010年版。
范围:砷盐检查法的操作。
责任:质检室主任、化验员。
内容:1简述1.1砷盐检查法(《中国药典》2010年版二部附录Ⅷ J)适用于药品中微量砷盐(以A S计)的限量检查。
1.2砷盐检查法中的第一法(古蔡氏法)用作药品中砷盐的限量检查;第二法(二乙基二硫代氨基甲酸银法)既可检查药品中砷盐的限量,又可以作砷盐的含量测定;两法并列,应根据《中国药典》品种项下规定的方法选用。
1.3古蔡氏法是利用金属锌与酸作用产生新生态的氢与药品中微量亚砷酸盐反应生成具有挥发性的砷化氢,遇溴化汞试纸产生黄色至棕色的砷斑,与同一条件下定量标准砷溶液所产生的砷斑比较,以判定砷盐的限量。
1.4二乙基二硫代氨基甲酸银法是将生成的砷化氢气体导入盛有二乙基二硫代氨基甲酸银试液的管中,使之还原为红色胶态银,与同一条件下定量的标准砷溶液所制成的对照液比较,或在510nm的波长处测定吸光度,以判定含砷盐的限度或测定含量。
2仪器与用具见下图。
图1 第一法仪器装置 图2 第二法仪器装置(古蔡氏法) (二乙基二硫代氨基甲酸银法)第一法仪器装置说明:A 为100ml 标准磨口锥形瓶;B 为中空的标准磨口塞;上连导气管C (外径8.0mm ,内径6mm ),全长约180mm ;D 为具孔的有机玻璃旋塞,其上部为圆形平面,中央有一圆孔,孔径与导气管C 的内径一致,其下部孔径与导气管C 的外径相适应,将导气管C 的顶端套入旋塞下部孔内,并使管壁与旋塞的圆孔相吻合,黏合固定;E 为中央具有圆孔(孔径6.0mm )的有机玻璃旋塞盖,与D 紧密吻合。
第二法仪器装置说明:A 为100ml 标准磨口锥形瓶;B 为中空的标准磨口塞,上连导气管C (一端外径为8mm ,内径为6mm ;另一端长为180mm ,外径为4mm ,内径为1.6mm ,尖端内径为1mm )。
[答案][西安交通大学]《药物分析》作业
![[答案][西安交通大学]《药物分析》作业](https://img.taocdn.com/s3/m/f05c53cf6edb6f1afe001f4e.png)
1.砷盐检查法中,醋酸铅棉花的作用是()[答案:D]A.消除锑对检查的干扰B.消除铅对检查的干扰C.消除铁对检查的干扰D.消除硫化物对检查的干扰E.消除氯化氢气体对检查的干扰2.《中国药典》(2010年版)将生物制品列入()[答案:C]A.第二部附录B.第二部C.第三部D.第一部附录E.第一部3.用酸度计测定溶液的pH值,测定前应用pH值与供试液较接近的一种标准缓冲液调节仪器旋钮,使仪器pH示值与标准缓冲液的pH值一致,此操作步骤为()[答案:E]A.调节零点B.调节斜率C.校正温度D.平衡E.定位4.按《中国药典》(2010年版)的规定,红外光谱仪校正的项目有()[答案:B]A.波数的准确性和杂散光B.波数的准确性和分辨率C.检测灵敏度和杂散光D.检测灵敏度和分辨率E.杂散光和分辨率5.检查药物中的残留溶剂,各国药典均采用()[答案:E]A.高效液相色谱法B.薄层色谱法C.紫外-可见分光光度法D.滴定分析法E.气相色谱法6.《中国药典》(2010年版)薄层色谱法在检查中主要应用于()[答案:A]A.溶液颜色的检查B.水分的测定C.有机溶剂残留量的测定D.有关物质的检查E.一般杂质检查7.《中国药典》(2010年版)检查对乙酰氨基酚中的对氨基酚及有关物质采用的方法是()[答案:A]A.高效液相色谱法B.薄层色谱法C.紫外分光光度法D.气相色谱法E.比色法8.测定某药物的比旋度,若供试品溶液的浓度为10.0mg/ml,样品管长度为2dm,测得的旋光度值为2.02,则比旋度为()[答案:E]A.202B.20.0C.2.02D.101E.10.19.适用于贵重药物和空气中易氧化药物干燥失重测定的方法是()[答案:C]A.电泳法B.热重分析法C.差示热分析法D.差示扫描量热法E.X-射线粉末衍射法10.盐酸氯丙嗪需检查溶液的颜色,此项目检查的杂质是()[答案:B]A.铁盐B.重金属C.因被还原而产生的杂质D.因被氧化而产生的杂质E.因聚合而产生的杂质11.取供试品,加氢氧化钠试液溶解后,加铁氰化钾试液和正丁醇,振摇,放置分层后醇层显强烈的蓝色荧光,加酸使成酸性,荧光消失,再加碱使成碱性,荧光又出现。
中级药品检验工理论考试
国家人力资源与社会保障职业技能鉴定湖南省药物检验工应知试卷(中级)模拟试题注意事项1、考试时间:120分钟。
2、请首先按要求在试卷的标封处填写你的姓名、准考证号和所在单位的名称。
3、请仔细阅读各种题目4一、单项选择题:共45分,每题1.5分(请从五个备选项中选取一个正确答案填写在括号中,错选、漏选、多选均不得分,也不反扣分)1、中国药典所规定的“精密称定”,系指称取重量应准确至所取重量的( C )A、百万分之一B、十万分之一C、万分之一D、千分之一E、百分之一2、中国药典(2010年版)规定铁盐的检查方法为( D )A、邻二氮菲法B、水杨酸显色法C、普鲁士蓝法D、硫氰酸盐法E、巯基醋酸法3、中国药典规定,称取“2.000g”系指(A )A、称取重量可为1.5~2.5 gB、称取重量可为1.95~2.05 gC、称取重量可为1.995~2.005gD、称取重量可为1.9995~2.0005gE、称取重量可为1~3 g4、温度对试验结果有显著影响者,除另有规定外,应以(D )A、10~30℃为准B、15~30℃为准C、20~30℃为准D、25±2℃为准E、26±2℃为准5、检验记录作为实验的第一手资料()A、应妥善保存,以备查B、应保存一年C、待检验报告发出后可销毁D、在必要时应作适当修改E、待复合无误后可自行处理6、药物中氯化物杂质检查,是使该杂质在酸性溶液中与硝酸银作用生成氯化物浑浊,所用的稀酸是(A )A、硝酸B、硫酸C、盐酸D、醋酸E、磷酸7、SD表示( b )A、回收率B、标准偏差C、误差度D、相对标准偏差E、变异系数8、杂质检查一般(B )A、检查最低量B、为限度检查C、为含量检查D、检查最大允许量E、用于原料药检查9、用古蔡氏法测定砷盐限量,对照管中加入标准砷溶液为( B )A 1mlB 2ml C、5ml D、依限量大小决定E、依样品取量及限量计算决定10、药典规定取用量为“约”若干时,系指取用量不得超过规定量的( E )A、±0.1%B、±1%C、±2%D、±5%E、±10%11、药品红外光谱图收集在药典的哪一部分内容中( E )A、凡例B、正文C、附录D、附在索引后E、不在药典中,另行出版12、在中国药典中,通用的测定方法收载在( C )A、凡例部分B、正文部分C、附录部分D、索引部分E、目录部分13、葡萄糖中存在的特殊杂质为(A )A、糊精B、砷盐C、氯化物D、重金属E、盐酸14、中国药典规定“微溶”系指( D )A、溶质(1g或1ml)能在溶剂1~不到10ml中溶解B、溶质(1g或1ml)能在溶剂10~不到30ml中溶解C、溶质(1g或1ml)能在溶剂30~不到100ml中溶解D、溶质(1g或1ml)能在溶剂100~不到1000ml中溶解E、溶质(1g或1ml)能在溶剂1000~不到10000ml中溶解15、Ag(DDC)法检查砷盐时,判断结果依据()A、砷斑颜色B、峰面积大小C、砷化氢气体多少D、Ag(DDC)法吡啶溶液的体积E、Ag(DDC)法吡啶吸收液的吸收度大小16、检查药物中杂质时,若药物溶液有颜色而干扰检查,常用内消法或外消法消除干扰。
新旧附录通则编码对照表
《中国药典》2015年版通则编码与2010年版附录编码对照表编号通则名称原附录原附录名称0100 制剂通则0101 片剂一部Ⅰ D 片剂二部Ⅰ A 片剂三部I E 片剂0102 注射剂一部ⅠU 注射剂二部Ⅰ B 注射剂三部I A 注射剂0103 胶囊剂一部ⅠL 胶囊剂二部Ⅰ E 胶囊剂三部I F 胶囊剂0104 颗粒剂一部Ⅰ C 颗粒剂二部ⅠN 颗粒剂三部I J 颗粒剂0105 眼用制剂一部ⅠY 眼用制剂二部ⅠG 眼用制剂三部I C 眼用制剂0106 鼻用制剂一部ⅠX 鼻用制剂二部ⅠR 鼻用制剂三部I L 鼻用制剂0107 栓剂一部ⅠW 栓剂二部Ⅰ D 栓剂三部I B 栓剂0108 丸剂一部Ⅰ A 丸剂一部ⅠK 滴丸剂二部ⅠH 丸剂0109 软膏剂、乳膏剂一部ⅠR 软膏剂二部Ⅰ F 软膏剂乳膏剂糊剂三部I G 软膏剂、乳膏剂0110 糊剂二部ⅠF 软膏剂乳膏剂糊剂(指糊剂)0111 吸入制剂二部ⅠL 气雾剂粉雾剂喷雾剂(指粉雾剂)0112 喷雾剂一部ⅠZ 气雾剂喷雾剂(指喷雾剂)二部ⅠL 气雾剂粉雾剂喷雾剂(指喷雾剂)三部I H 喷雾剂(指喷雾剂)0113 气雾剂一部ⅠZ 气雾剂喷雾剂(指气雾剂)二部ⅠL 气雾剂粉雾剂喷雾剂(指气雾剂)0114 凝胶剂一部ⅠQ 凝胶剂二部ⅠU 凝胶剂三部I M 凝胶剂0115 散剂一部Ⅰ B 散剂二部ⅠP 散剂三部I K 散剂0116 糖浆剂一部ⅠH 糖浆剂二部ⅠK 糖浆剂0117 搽剂一部ⅠV 搽剂洗剂涂膜剂(指搽剂)二部ⅠT 搽剂涂剂涂膜剂(指搽剂)0118 涂剂二部ⅠT 搽剂涂剂涂膜剂(指涂剂)三部I D 外用制剂0119 涂膜剂一部ⅠV 搽剂洗剂涂膜剂(指涂膜剂)二部ⅠT 搽剂涂剂涂膜剂(指涂膜剂0120 酊剂一部ⅠN 酊剂二部Ⅰ C 酊剂0121 贴剂一部Ⅰ I 贴膏剂 (指贴剂) 二部ⅠV 贴剂0122 贴膏剂一部ⅠI 贴膏剂0123 口服溶液剂口服混悬剂口服乳剂二部ⅠO 口服溶液剂口服混悬剂口服乳剂0124 植入剂二部ⅠJ 植入剂0125 膜剂二部ⅠM 膜剂0126 耳用制剂二部ⅠQ耳用制剂0127 洗剂一部ⅠV 搽剂洗剂涂膜剂(指洗剂)二部ⅠS洗剂冲洗剂灌肠剂(指洗剂)0128 冲洗剂一部ⅠV 搽剂洗剂涂膜剂(指洗剂)二部ⅠS洗剂冲洗剂灌肠剂(指冲洗剂)0129 灌肠剂二部ⅠS洗剂冲洗剂灌肠剂(指灌肠剂)0181 合剂一部ⅠJ 合剂0182 锭剂一部ⅠE 锭剂0183 煎膏剂(膏滋)一部ⅠF 煎膏剂(膏滋)0184 胶剂一部ⅠG 胶剂0185 酒剂一部ⅠM 酒剂0186 膏药一部ⅠP 膏药0187 露剂一部ⅠS 露剂0188 茶剂一部ⅠT 茶剂0189 流浸膏剂与浸膏剂一部ⅠO 流浸膏剂与浸膏剂0200 其他通则0211 药材和饮片取样法一部ⅡA 药材和饮片取样法0212 药材和饮片检定通则一部ⅡB 药材和饮片检定通则0213 炮制通则一部ⅡD 炮制通则0251 药用辅料二部附录Ⅱ药用辅料0261 制药用水一部附录ⅩⅣ制药用水二部附录ⅩⅥ制药用水0291 国家药品标准物质通则新增第二增补本03000301 一般鉴别试验一部附录Ⅳ一般鉴别试验二部附录Ⅲ一般鉴别试验0400光谱法一部附录Ⅴ分光光度法二部附录Ⅳ分光光度法三部附录Ⅱ分光光度法0401 紫外-可见分光光度法一部Ⅴ A 紫外-可见分光光度法二部Ⅳ A 紫外-可见分光光度法三部Ⅱ A 紫外-可见分光光度法0402 红外分光光度法一部Ⅴ C 红外分光光度法二部Ⅳ C 红外分光光度法0405 荧光分光光度法二部Ⅳ E 荧光分析法三部Ⅱ C 荧光分析法0406 原子吸收分光光度法一部Ⅴ D 原子吸收分光光度法二部Ⅳ D 原子吸收分光光度法三部Ⅱ B 原子吸收分光光度法0407 火焰光度法二部Ⅳ F 火焰光度法三部Ⅱ D 火焰光度法ⅦI 钾离子测定法ⅦJ 钠离子测定法0411 电感耦合等离子体原子发射光谱法一部Ⅺ E 电感耦合等离子体原子发射光谱法0412 电感耦合等离子体质谱法一部ⅪD 电感耦合等离子体质谱法0421 拉曼光谱法二部ⅩⅨL 拉曼光谱法指导原则0431 质谱法二部ⅨJ 质谱法0441 核磁共振波谱法二部ⅨK 核磁共振波谱法0451 X射线衍射法二部ⅨF X射线粉末衍射法0500色谱法0501 纸色谱法一部Ⅵ A 纸色谱法二部Ⅴ A 纸色谱法三部Ⅲ A 纸色谱法0502 薄层色谱法一部Ⅵ B 薄层色谱法二部Ⅴ B 薄层色谱法0511 柱色谱法一部Ⅵ C 柱色谱法二部Ⅴ C 柱色谱法0512 高效液相色谱法一部Ⅵ D 高效液相色谱法二部Ⅴ D 高效液相色谱法三部Ⅲ B 高效液相色谱法0513 离子色谱法一部ⅥG 离子色谱法二部ⅤJ 离子色谱法三部Ⅲ E 离子色谱法0514 分子排阻色谱法二部ⅤH 分子排阻色谱法三部Ⅲ D 分子排阻色谱法0521 气相色谱法一部Ⅵ E 气相色谱法二部Ⅴ E 气相色谱法三部Ⅲ C 气相色谱法0531 超临界流体色谱法新增0532 临界点色谱法新增0541 电泳法二部Ⅴ F 电泳法三部Ⅳ A 醋酸纤维素薄膜电泳法三部Ⅳ B 琼脂糖凝胶电泳法三部Ⅳ C SDS-聚丙烯酰胺凝胶电泳法三部Ⅳ D 等电聚焦电泳法0542 毛细管电泳法一部Ⅵ F 毛细管电泳法二部ⅤG 毛细管电泳法0600 物理常数测定法0601 相对密度测定法一部Ⅶ A 相对密度测定法二部Ⅵ A 相对密度测定法0611 馏程测定法一部Ⅶ B 馏程测定法二部Ⅵ B 馏程测定法0612 熔点测定法一部Ⅶ C 熔点测定法二部Ⅵ C 熔点测定法0613 凝点测定法一部Ⅶ D 凝点测定法二部Ⅵ D 凝点测定法0621 旋光度测定法一部Ⅶ E 旋光度测定法二部Ⅵ E 旋光度测定法0622 折光率测定法一部Ⅶ F 折光率测定法二部Ⅵ F 折光率测定法0631 pH值测定法一部ⅦG pH值测定法二部ⅥH pH值测定法三部Ⅴ A pH值测定法0632 渗透压摩尔浓度测定法一部Ⅺ F 渗透压摩尔浓度测定法二部ⅨG 渗透压摩尔浓度测定法三部ⅤH 渗透压摩尔浓度测定法0633 黏度测定法二部ⅥG 黏度测定法0661 热分析法二部ⅧQ 热分析法0681 制药用水电导率测定法二部ⅧS 制药用水电导率测定法0682 制药用水中总有机碳测定法二部ⅧR 制药用水中总有机碳测定法0700其他测定法Other Assays0701 电位滴定法与永停滴定法一部Ⅷ A 电位滴定法与永停滴定法二部Ⅶ A 电位滴定法与永停滴定法0702 非水溶液滴定法一部Ⅷ B 非水溶液滴定法二部Ⅶ B 非水溶液滴定法0703 氧瓶燃烧法二部ⅦC 氧瓶燃烧法0704 氮测定法一部ⅨL 氮测定法二部Ⅶ D 氮测定法三部Ⅵ A 氮测定法0711 乙醇量测定法一部ⅨM 乙醇量测定法二部Ⅶ E 乙醇量测定法0712 甲氧基、乙氧基与羟丙氧基测定法二部Ⅶ F 甲氧基、乙氧基与羟丙氧基测定法0713 脂肪与脂肪油测定法一部ⅨN 脂肪与脂肪油测定法二部ⅦH 脂肪与脂肪油测定法0721 维生素A测定法二部ⅦJ 维生素A测定法0722 维生素D测定法二部ⅦK 维生素D测定法0731 蛋白质含量测定法二部ⅦM 蛋白质含量测定法三部Ⅵ B 蛋白质测定法0800 限量检查法0801 氯化物检查法一部Ⅸ C 氯化物检查法二部Ⅷ A 氯化物检查法0802 硫酸盐检查法二部ⅧB 硫酸盐检查法0803 硫化物检查法二部ⅧC 硫化物检查法0804 硒检查法二部ⅧD 硒检查法0805 氟检查法二部ⅧE 氟检查法0806 氰化物检查法二部Ⅷ F 氰化物检查法三部ⅥX 氰化物残留量测定法0807 铁盐检查法一部Ⅸ D 铁盐检查法二部ⅧG 铁盐检查法0808 铵盐检查法二部ⅧK 铵盐检查法0821 重金属检查法一部Ⅸ E 重金属检查法二部ⅧH 重金属检查法0822 砷盐检查法一部Ⅸ F 砷盐检查法二部ⅧJ 砷盐检查法0831 干燥失重测定法一部ⅨG 干燥失重测定法二部ⅧL 干燥失重测定法三部ⅦL 干燥失重测定法0832 水分测定法一部ⅨH 水分测定法二部ⅧM 水分测定法三部Ⅶ D 水分测定法0841 炽灼残渣检查法一部ⅨJ 炽灼残渣检查法二部ⅧN 炽灼残渣检查法0842 易炭化物检查法二部ⅧO 易炭化物检查法0861 残留溶剂测定法二部ⅧP 残留溶剂测定法三部ⅥV 残留溶剂测定法0871 甲醇量检查法一部ⅨT 甲醇量检查法0872 合成多肽中的醋酸测定法二部ⅦN 合成多肽中的醋酸测定法0873 2-乙基己酸测定法二部ⅦL 2-乙基己酸测定法0900 物理特性检查法0901 溶液颜色检查法一部Ⅺ A 溶液颜色检查法二部Ⅸ A 溶液颜色检查法0902 澄清度检查法二部ⅨB 澄清度检查法0903 不溶性微粒检查法一部ⅨR 不溶性微粒检查法二部Ⅸ C 不溶性微粒检查法三部ⅤI 不溶性微粒检查法0904 可见异物检查法一部Ⅺ C 可见异物检查法二部ⅨH 可见异物检查法三部Ⅴ B 可见异物检查法0921 崩解时限检查法一部Ⅻ A 崩解时限检查法二部Ⅹ A 崩解时限检查法三部Ⅴ C 崩解时限检查法0922 融变时限检查法一部Ⅻ B 融变时限检查法二部Ⅹ B 融变时限检查法三部Ⅴ D 融变时限检查法0923 片剂脆碎度检查法二部ⅩG 片剂脆碎度检查法三部Ⅴ E 片剂脆碎度检查法0931 溶出度测定法(合并释放度测定法)二部Ⅹ C 溶出度测定法二部Ⅹ D 释放度测定法0941 含量均匀度检查法二部ⅩE 含量均匀度检查法0942 最低装量检查法一部Ⅻ C 最低装量检查法二部Ⅹ F 最低装量检查法三部Ⅴ F 最低装量检查法0951 吸入制剂微细粒子空气动力学特性测定法二部ⅩH 吸入气雾剂、吸入粉雾剂、吸入喷雾剂的雾滴(粒)分布测定法0952 粘附力测定法一部ⅫE 贴膏剂黏附力测定法二部ⅩJ 贴剂黏附力测定法0981 结晶性检查法二部ⅨD 结晶性检查法0982 粒度和粒度分布测定法一部Ⅺ B 粒度测定法二部Ⅸ E 粒度和粒度分布测定法三部ⅤG 粒度测定法0983 锥入度测定法二部ⅩK 锥入度测定法1000 分子生物学技术1100 生物检查法1101 无菌检查法一部ⅩⅢ B 无菌检查法二部ⅪH 无菌检查法三部Ⅻ A 无菌检查法1105 非无菌产品微生物限度检查:微生物计数法一部ⅩⅢ C 微生物限度检查法二部Ⅺ J 微生物限度检查法三部Ⅻ G 微生物限度检查法1106 非无菌产品微生物限度检查:控制菌检查法一部ⅩⅢ C 微生物限度检查法二部Ⅺ J 微生物限度检查法三部Ⅻ G 微生物限度检查法1107 非无菌药品微生物限度标准一部ⅩⅢ C 微生物限度检查法二部Ⅺ J 微生物限度检查法三部Ⅻ G 微生物限度检查法1121 抑菌效力检查法一部ⅩⅧ D 抑菌剂效力检查法指导原则二部ⅪⅩ N 抑菌剂效力检查法指导原则三部ⅩⅦ A 抑菌剂(防腐剂)效力检查法指导原则1141 异常毒性检查法一部ⅩⅢ E 异常毒性检查法二部Ⅺ C 异常毒性检查法三部Ⅻ F 异常毒性检查法1142 热原检查法一部ⅩⅢ A 热原检查法二部Ⅺ D 热原检查法三部Ⅻ D 热原检查法1143 细菌内毒素检查法一部ⅩⅢ D 细菌内毒素检查法二部Ⅺ E 细菌内毒素检查法三部Ⅻ E 细菌内毒素检查法1144 升压物质检查法二部ⅪF 升压物质检查法1145 降压物质检查法一部ⅩⅢ F 降压物质检查法二部ⅪG 降压物质检查法1146 组胺类物质检查法新增1147 过敏反应检查法一部ⅩⅢG 过敏反应检查法二部ⅪK 过敏反应检查法1148 溶血与凝聚检查法一部ⅩⅢH 溶血与凝聚检查法二部ⅪL 溶血与凝聚检查法1200 生物活性测定法1201 抗生素微生物检定法二部ⅪA 抗生素微生物检定法1202 青霉素酶及其活力测定法二部ⅪB 青霉素酶及其活力测定法1205 升压素生物测定法二部ⅫA 升压素生物测定法1206 细胞色素C活力测定法二部ⅫB 细胞色素C活力测定法1207 玻璃酸酶测定法二部ⅫC 玻璃酸酶测定法1208 肝素生物测定法二部ⅫD 肝素生物测定法1209 绒促性素生物测定法二部ⅫE 绒促性素生物测定法1210 缩宫素生物测定法二部ⅫF 缩宫素生物测定法1211 胰岛素生物测定法二部ⅫG 胰岛素生物测定法1212 精蛋白锌胰岛素注射液延缓作用检查法二部ⅫH 精蛋白锌胰岛素注射液延缓作用检查法1213 硫酸鱼精蛋白生物测定法二部ⅫJ 硫酸鱼精蛋白生物测定法1214 洋地黄生物测定法二部ⅫK 洋地黄生物测定法1215 葡萄糖酸锑钠毒力检查法二部ⅫL 葡萄糖酸锑钠毒力检查法1216 卵泡刺激素生物测定法二部ⅫM 卵泡刺激素生物测定法1217 黄体生成素生物测定法二部ⅫN 黄体生成素生物测定法1218 降钙素生物测定法二部ⅫO 降钙素生物测定法1219 生长激素生物测定法二部ⅫP 生长激素生物测定法1401 放射性药品检定法二部ⅩⅢ放射性药品检定法1421 灭菌法一部ⅩⅥ灭菌法二部ⅩⅦ灭菌法三部ⅩⅤ灭菌法1431 生物检定统计法二部ⅩⅣ生物检定统计法2000 中药相关检查方法2001 显微鉴别法一部ⅡC 显微鉴别法2101 膨胀度测定法一部ⅨO 膨胀度测定法2102 膏药软化点测定法一部ⅫD 膏药软化点测定法2201 浸出物测定法一部ⅩA 浸出物测定法2202 鞣质含量测定法一部ⅩB 鞣质含量测定法2203 桉油精含量测定法一部ⅩC 桉油精含量测定法2204 挥发油测定法一部ⅩD 挥发油测定法2301 药材和饮片杂质检查法一部ⅨA 杂质检查法2302 灰分测定法一部ⅨK 灰分测定法2303 酸败度测定法一部ⅨP 酸败度测定法2321 铅、镉、砷、汞、铜测定法一部ⅨB 铅、镉、砷、汞、铜测定法2322 汞和砷元素形态及其价态测定法新增2331 二氧化硫残留量测定法一部ⅨU 二氧化硫残留量测定法2341 农药残留量测定法一部ⅨQ 农药残留量测定法2351 黄曲霉毒素测定法一部ⅨV 黄曲霉毒素测定法2400 中药注射剂有关物质检查法一部ⅨS 注射剂有关物质检查法3000 生物制品相关检查方法(附后)待定3100 含量测定法3101 固体总量测定法三部ⅦM 固体总量测定法3102 唾液酸测定法三部ⅥC 唾液酸测定法3103 磷测定法三部ⅦA 磷测定法3104 硫酸铵测定法三部ⅦC 硫酸铵测定法3105 亚硫酸氢钠测定法三部ⅦE 亚硫酸氢钠测定法3106 氢氧化铝(或磷酸铝)测定法三部ⅦF 氢氧化铝(或磷酸铝)测定法3107 氯化钠测定法三部ⅦG 氯化钠测定法3108 枸橼酸离子测定法三部ⅦH 枸橼酸离子测定法3109 辛酸钠测定法三部ⅥK 辛酸钠测定法3110 乙酰色氨酸测定法三部ⅥW 乙酰色氨酸测定法3111 苯酚测定法三部ⅥM 苯酚测定法3112 间甲酚测定法三部ⅥN 间甲酚测定法3113 硫柳汞测定法三部ⅦB 硫柳汞测定法3114 对羟基苯甲酸甲酯、对羟基苯甲酸丙酯含量测定法三部ⅥT 对羟基苯甲酸甲酯、对羟基苯甲酸丙酯含量测定法3115 O-乙酰基测定法三部ⅥF O-乙酰基测定法3116 己二酰肼含量测定法三部ⅧK 己二酰肼含量测定法3117 高分子结合物含量测定法三部ⅧL 高分子结合物含量测定法3118 人血液制品中糖及糖醇测定法三部ⅥP 人血液制品中糖及糖醇测定法3119 人血白蛋白多聚体测定法三部ⅥQ 人血白蛋白多聚体测定法3120 人免疫球蛋白类制品IgG单体加二聚体测定法三部ⅥR 人免疫球蛋白类制品IgG单体加二聚体测定法3121 人免疫球蛋白类中甘氨酸含量测定法三部ⅥS 人免疫球蛋白中甘氨酸含量测定法3122 重组人粒细胞刺激因子蛋白质含量测定法三部ⅥU 重组人粒细胞刺激因子蛋白质含量测定法3123 组胺人免疫球蛋白中游离磷酸组胺测定法三部Ⅵ E 组胺人免疫球蛋白中游离磷酸组胺测定法3124 IgG含量测定法三部ⅪK IgG含量测定法3200 化学残留物测定法3201 乙醇残留量测定法三部ⅥD 乙醇残留量测定法3202 聚乙二醇残留量测定法三部ⅥG 聚乙二醇残留量测定法3203 聚山梨酯80残留量测定法三部ⅥH 聚山梨酯80残留量测定法3204 戊二醛残留量测定法三部ⅥI 戊二醛残留量测定法3205 磷酸三丁酯残留量测定法三部ⅥJ 磷酸三丁酯残留量测定法3206 碳二亚胺(EDAC)残留量测定法三部ⅥY 碳二亚胺(EDAC)残留量测定法3207 游离甲醛测定法三部ⅥL 游离甲醛测定法3208 人血白蛋白铝残留量测定法三部ⅦK 人血白蛋白铝残留量测定法3209 羟胺残留量测定法新增3300 微生物检查法3301 支原体检查法三部ⅫB 支原体检查法3302 病毒外源因子检查法三部ⅫC 病毒外源因子检查法3303 鼠源性病毒检查法三部ⅫH 鼠源性病毒检查法3400 生物测定法3401 免疫印迹法三部ⅧA 免疫印迹法3402 免疫斑点法三部ⅧB 免疫斑点法3403 免疫双扩散法三部ⅧC 免疫双扩散法3404 免疫电泳法三部ⅧD 免疫电泳法3405 肽图检查法三部ⅧE 肽图检查法3406 质粒丢失率检查法三部ⅨG 质粒丢失率检查法3407 SV40核酸序列检查法三部ⅨH SV40核酸序列检查法3408 外源性DNA残留量测定法三部ⅨB 外源性DNA残留量测定法3409 抗生素残留量检查法三部ⅨA 抗生素残留量检查法3410 激肽释放酶原激活剂测定法三部ⅨF 激肽释放酶原激活剂测定法3411 抗补体活性测定法三部ⅨK 抗补体活性测定法3412 牛血清白蛋白残留量测定法三部ⅧI 牛血清白蛋白残留量测定法3413 大肠杆菌菌体蛋白质残留量测定法三部Ⅸ C 大肠杆菌菌体蛋白质残留量测定法3414 假单胞菌菌体蛋白质残留量测定法三部Ⅸ D 假单胞菌菌体蛋白质残留量测定法3415 酵母工程菌菌体蛋白质残留量测定法三部Ⅸ E 酵母工程菌菌体蛋白质残留量测定法3416 类A血型物质测定法三部ⅨI 类A血型物质测定法3417 鼠IgG残留量测定法三部ⅨL 鼠IgG残留量测定法3418 无细胞百日咳疫苗鉴别试验三部ⅨS 无细胞百日咳疫苗鉴别试验3419 抗毒素、抗血清制品鉴别试验三部ⅨT 抗毒素、抗血清制品鉴别试验3420 A群脑膜炎球菌多糖分子大小测定法三部ⅧG A群脑膜炎球菌多糖分子大小测定法3421 伤寒Vi多糖分子大小测定法三部ⅧH 伤寒Vi多糖分子大小测定法3422 b型流感嗜血杆菌结合疫苗多糖含量测定法三部ⅧJ b型流感嗜血杆菌结合疫苗多糖含量测定法3423 人凝血酶活性检查法三部ⅨN 人凝血酶活性检查法3424 活化的凝血因子活性检查法三部ⅨO 活化的凝血因子活性检查法3425 肝素含量测定法三部ⅨP 肝素含量测定法3426 抗A、抗B血凝素测定法三部ⅨJ 抗A、抗B血凝素测定法3427 人红细胞抗体测定法三部ⅨQ 人红细胞抗体测定法3428 人血小板抗体测定法三部ⅨR 人血小板抗体测定法3429 猴体神经毒力试验三部ⅪL 猴体神经毒力试验3430 人血浆病毒核酸检测技术要求新增3431 单抗纯度茨顶方法-CE-SDS毛细管电泳(还原和非还原)新增3500 生物活性/效价测定法3501 重组乙型肝炎疫苗(酵母)体外相对效力检查法三部Ⅹ A 重组乙型肝炎疫苗(酵母)体外相对效力检查法3502 甲型肝炎灭活疫苗体外相对效力检查法三部ⅩS 甲型肝炎灭活疫苗体外相对效力检查法3503 人用狂犬病疫苗效价测定法三部ⅪA 人用狂犬病疫苗效价测定法3504 吸附破伤风疫苗效价测定法三部ⅪB 吸附破伤风疫苗效价测定法3505 吸附白喉疫苗效价测定法三部ⅪC 吸附白喉疫苗效价测定法3506 类毒素絮状单位测定法三部ⅪD 类毒素絮状单位测定法3507 白喉抗毒素效价测定法三部ⅪE 白喉抗毒素效价测定法3508 破伤风抗毒素效价测定法三部ⅪF 破伤风抗毒素效价测定法3509 气性坏疽抗毒素效价测定法三部ⅪG 气性坏疽抗毒素效价测定法3510 肉毒抗毒素效价测定法三部ⅪH 肉毒抗毒素效价测定法3511 抗蛇毒血清效价测定法三部ⅪI 抗蛇毒血清效价测定法3512 狂犬病免疫球蛋白效价测定法三部ⅪJ 狂犬病免疫球蛋白效价测定法3513 人免疫球蛋白中白喉抗体效价测定法三部ⅩO 人免疫球蛋白中白喉抗体效价测定法3514 人免疫球蛋白Fc段生物学活性测定法三部ⅩP 人免疫球蛋白Fc段生物学活性测定法3515 抗人T细胞免疫球蛋白效价测定法(E玫瑰花环形成抑制试验)三部ⅩQ 抗人T细胞免疫球蛋白效价测定法(E玫瑰花环形成抑制试验)3516 抗人T细胞免疫球蛋白效价测定法(淋巴细胞毒试验)三部ⅩR 抗人T细胞免疫球蛋白效价测定法(淋巴细胞毒试验)3517 人凝血因子Ⅱ效价测定法三部ⅩJ 人凝血因子Ⅱ效价测定法3518 人凝血因子Ⅶ效价测定法三部ⅩK 人凝血因子Ⅶ效价测定法3519 人凝血因子Ⅸ效价测定法三部ⅩL 人凝血因子Ⅸ效价测定法3520 人凝血因子Ⅹ效价测定法三部ⅩM 人凝血因子Ⅹ效价测定法3521 人凝血因子Ⅷ效价测定法三部ⅩN 人凝血因子Ⅷ效价测定法3522 重组人促红素体内生物学活性测定法三部Ⅹ B 重组人促红素体内生物学活性测定法3523 干扰素生物学活性测定法三部ⅩC 干扰素生物学活性测定法3524 重组人白介素-2生物学活性测定法三部Ⅹ D 重组人白介素-2生物学活性测定法3525 重组人粒细胞刺激因子生物学活性测定法三部Ⅹ E 重组人粒细胞刺激因子生物学活性测定法3526 重组人粒细胞巨噬细胞刺激因子生物学活性测定法三部Ⅹ F 重组人粒细胞巨噬细胞刺激因子生物学活性测定法3527 重组牛碱性成纤维细胞生长因子生物学活性测定法三部ⅩG 重组牛碱性成纤维细胞生长因子生物学活性测定法3528 重组人表皮生长因子生物学活性测定法三部ⅩH 重组人表皮生长因子生物学活性测定法3529 重组链激酶生物学活性测定法三部ⅩI 重组链激酶生物学活性测定法3530 鼠神经生长因子生物学活性测定新增法3531 尼妥珠单抗生物学活性测定法新增3532 白介素-11-生物活性测定方法新增3600 特定生物原材料/动物3601 无特定病原体鸡胚质量检测要求三部ⅩⅢ A 无特定病原体鸡胚质量检测要求3602 实验动物微生物学检测要求三部ⅩⅢB 实验动物微生物学检测要求3603 实验动物寄生虫学检测要求三部ⅩⅢC 实验动物寄生虫学检测要求3604 新生牛血清检测要求三部ⅩⅢD 新生牛血清检测要求3611 细菌生化反应培养基三部ⅩⅣ细菌生化反应培养基8000 试剂与标准物质8001 试药一部ⅩⅤ A 试药二部ⅩⅤ A 试药8002 试液一部ⅩⅤ B 试液二部ⅩⅤ B 试液8003 试纸一部ⅩⅤ C 试纸二部ⅩⅤ C 试纸8004 缓冲液一部ⅩⅤ D 缓冲液二部ⅩⅤ D 缓冲液8005 指示剂与指示液一部ⅩⅤ E 指示剂与指示液二部ⅩⅤ E 指示剂与指示液8006 滴定液一部ⅩⅤ F 滴定液二部ⅩⅤ F 滴定液8061 标准物质一部ⅩⅤG 对照品对照药材对照提取物二部ⅩⅤG 标准品与对照品9000 指导原则9001 原料药与药物制剂稳定性试验指导原则二部ⅩⅨ C 原料药与药物制剂稳定性试验指导原则9011 药物制剂人体生物利用度和生物等效性试验指导原则二部ⅩⅨ B 药物制剂人体生物利用度和生物等效性试验指导原则9012 生物样品定量分析方法验证指导原则新增9013 缓释、控释和迟释制剂指导原则二部ⅩⅨ D 缓释、控释和迟释制剂指导原则9014 微粒制剂指导原则二部ⅩⅨ E 微囊、微球与脂质体制剂指导原则9015 药品晶型研究及晶型质量控制指导原则新增9101 药品质量标准分析方法验证指导一部ⅩⅧ A 中药质量标准分析方法验证原则指导原则二部ⅩⅨ A 药品质量标准分析方法验证指导原则9102 药品杂质分析指导原则二部ⅩⅨ F 药品杂质分析指导原则9103 药物引湿性试验指导原则二部ⅩⅨ J 药物引湿性试验指导原则9104 近红外分光光度法指导原则二部ⅩⅨK 近红外分光光度法指导原则9105 中药生物活性测定指导原则一部ⅩⅧC 中药生物活性测定指导原则9106 基于基因芯片药物评价技术指导原则新增9107 中药材DNA条形码分子鉴定法指导原则新增9201 药品微生物检验替代方法验证指导原则一部ⅩⅧ E 药品微生物检验替代方法验证指导原则二部ⅩⅨO 药品微生物检验替代方法验证指导原则三部ⅩⅦ B 药品微生物检验替代方法验证指导原则9202 非无菌药品微生物限度检查指导原则一部ⅩⅧ F 微生物限度检查法应用指导原则二部ⅩⅨP 微生物限度检查法应用指导原则9203 药品微生物实验室质量管理指导原则一部ⅩⅧG 药品微生物实验室规范指导原则二部ⅩⅨQ 药品微生物实验室规范指导原则9204 微生物鉴定指导原则新增9205 药品洁净实验室微生物监测和控制指导原则新增9206 无菌检查用隔离系统验证指导原则新增9301 注射剂安全性检查法应用指导原则一部ⅩⅧ B 中药注射剂安全性检查法应用指导原则二部ⅩⅨ M 化学药品注射剂安全性检查法应用指导原则9302 中药有害残留物限量制定指导原则新增9303 色素检测指导原则新增9304 中药中铝、铬、铁、钡元素测定指导原则新增9305 中药中真菌毒素测定指导原则新增9401 生物制品定量分析方法指导原则新增生物制品类预留位置。
《中国药典》2015年版通则编码与2010年版附录编码对照表
中国药典2015年版《中国药典》2015年版通则编码与2010年版附录编码对照表《中国药典》2015年版通则编码与2010年版附录编码对照表编号通则名称原附录原附录名称0100制剂通则一部工D片剂0101片剂二部I A片剂三部I E片剂一部I u注射剂0102注射剂二部I B注射剂三部I A注射剂一部I L胶囊剂0103胶囊剂二部I E胶囊剂三部I F胶囊剂一部I C颗粒剂0104颗粒剂二部I N颗粒剂三部I J颗粒剂一部I Y眼用制剂0105眼用制剂二部I G眼用制剂三部I c眼用制剂一部I X鼻用制剂0106鼻用制剂二部I R 鼻用制剂三部I L鼻用制剂一部I w栓剂0107栓剂二部I D栓剂三部I B栓剂一部I A丸剂0108丸剂一部I K滴丸剂二部I H丸剂一部I R 软音剂0109软裔剂乳裔剂二部I F软膏剂乳裔剂糊剂三部I G软裔剂、乳裔剂0110糊剂二部I F 软膏剂乳音剂糊剂(指糊剂)0111吸人制剂二部I L气雾剂粉雾剂喷雾剂(指粉雾剂)一部I Z气雾剂喷雾剂(指喷雾剂)0112喷雾剂二部I L气雾剂粉雾剂喷雾剂(指喷雾剂)三部I H喷雾剂一部I Z气雾剂喷雾剂(指气雾剂)0113气雾剂二部I L 气雾剂粉雾剂喷雾剂(指气雾剂)• 425《中国药典》2015年版通则编码与2010年版附录编码对照表中国药典2015年版续表编号通则名称原附录原附录名称一部I Q凝胶剂0114凝胶剂二部I U凝胶剂三部I M凝胶剂一部I B散剂0115散剂二部I P散剂三部I K散剂一部I H糖浆剂0116糖浆剂二部I K糖浆剂一部I V搽剂洗剂涂膜剂(指搽剂)0117搽剂二部I T搽剂涂剂涂膜剂(指搽剂)二部I T搽剂涂剂涂膜剂(指涂剂)0118涂剂三部I D外用制剂一部I V搽剂洗剂涂膜剂(指涂膜剂)0119涂膜剂二部I T搽剂涂剂涂膜剂(指涂膜剂)一部I N酊剂0120酊剂二部I C酊剂一部I I 贴音剂(指贴剂)0121贴剂二部I V贴剂0122贴裔剂一部I I贴音剂0123口服溶液剂口服混悬剂口服乳剂二部I o口服溶液剂口服混悬剂口服乳剂0124植人剂二部I J植人剂0125膜剂二部I M膜剂0126耳用制剂二部I Q耳用制剂-部I V搽剂洗剂涂膜剂(指洗剂)0127洗剂二部I s洗剂冲洗剂灌肠剂(指洗剂)一部I V搽剂洗剂涂膜剂(指洗剂)0128冲洗剂二部I S洗剂冲洗剂灌肠剂(指冲洗剂〉0129灌肠剂二部I S 洗剂冲洗剂灌肠剂(指灌肠剂)0181合剂一部I J 合剂0182锭剂一部I E锭剂0183煎膏剂(裔滋)一部I F煎裔剂(裔滋)0184胶剂一部I G胶剂0185酒剂—部I M酒剂0186裔药一部I P裔药0187露剂一部I S露剂0188茶剂一部I T茶剂0189流浸裔剂与浸資剂一部I o流浸裔剂与浸裔剂0200其他通则0211药材和饮片取样法一部n a药材和饮片取样法0212药材和饮片检定通则一部n b药材和饮片检定通则0213'炮制通则一部n d炮制通则0251药用辅料二部n药用辅料• 426 •中国药典2015年版《中国药典》2015年版通则编码与2010年版附录编码对照表续表.....编号通则名称原附录原附录名称0261制药用水-部m制药用水二部m制药用水0291国家药品标准物质通则新增第二增补本03000301一般鉴别试验一部w一般鉴别试验二部i n一般鉴别试验0400光谱法一部Y分光光度法二部W分光光度法三部n分光光度法0401紫外-可见分光光度法一部V A紫外-可见分光光度法二部IV A 紫外-可见分光光度法三部n a紫外-可见分光光度法0402红外分光光度法一部V c红外分光光度法二部i v c红外分光光度法0405荧光分光光度法二部N E荧光分析法三部n c荧光分析法0406原子吸收分光光度法一部V D原子吸收分光光度法二部IV D原子吸收分光光度法三部n b原子吸收分光光度法0407火焰光度法二部IV F火焰光度法三部n d火焰光度法0411电感耦合等离子体原子发射光谱法一部H E电感耦合等离子体原子发射光谱法0412电感耦合等离子体质谱法一部H D电感耦合等离子体质谱法0421拉曼光谱法二部XK L拉曼光谱法指导原则0431质谱法.二部IX J 质谱法0441核磁共振波谱法二部IX K 核磁共振波谱法0451X射线衍射法二部IX F X射线粉末衍射法0500色谱法0501纸色谱法一部YI A 纸色谱法二部V A纸色谱法三部m a纸色谱法0502薄层色谱法一部VI B 薄层色谱法二部V B薄层色谱法0511柱色谱法一部yi c柱色谱法二部v c柱色谱法0512髙效液相色谱法-部VI D髙效液相色谱法二部V D高效液相色谱法三部冚 B 髙效液相色谱法0513离子色谱法一部YI G离子色谱法二部V J 离子色谱法三部m e离子色谱法• 427《中国药典》2015年版通则编码与2010年版附录编码对照表中国药典2015年版续表编号通则名称原附录原附录名称0514分子排阻色谱法二部V H 分子排阻色谱法三部m d分子排阻色谱法一部V I E 气相色谱法0521气相色谱法二部V E 气相色谱法三部in c气相色谱法0531超临界流体色谱法新增0532临界点色谱法新增二部V F 电泳法三部W A 醋酸纤维素薄膜电泳法0541电泳法三部IV B 琼脂糖凝胶电泳法三部N C SD&聚丙烯酰胺凝胶电泳法三部IV D 等电聚焦电泳法0542毛细管电泳法一部二部V I F毛细管电泳法V G 毛细管电泳法0600物理常数测定法0601相对密度测定法一部1 A 相对密度测定法二部yi a相对密度测定法0611馏程测定法一部W B 馏程测定法二部V I B馏程测定法0612熔点测定法一部M C 熔点测定法二部*V I C 熔点测定法0613凝点测定法一部1D凝点测定法二部VI D凝点测定法0621旋光度测定法一部1E旋光度测定法二部E旋光度测定法0622折光率测定法一部m f折光率测定法二部V I F折光率测定法一部1G p H值测定法0631p H值测定法二部V I H p H值测定法三部V A p H值测定法一部X I F渗透压摩尔浓度测定法0632渗透压摩尔浓度测定法二部K G 渗透压摩尔浓度测定法三部V H渗透压摩尔浓度测定法0633黏度测定法二部V I G黏度测定法0661热分析法二部1Q 热分析法0681制药用水电导率测定法二部1S制药用水电导率测定法0682制药用水中总有机碳测定法二部1R 制药用水中总有机碳测定法0700其他测定法0701电位滴定法与永停滴定法一部1 A 电位滴定法与永停滴定法二部I A 电位滴定法与永停滴定法%0702非水溶液滴定法一部1B非水溶液滴定法二部M B 非水溶液滴定法• 428中国药典2015年版《中国药典》2015年版通则编码与2010年版附录编码对照表续表编号通则名称原附录原附录名称0703氧瓶燃烧法二部1 C 氧瓶燃烧法一部K L氮测定法0704氮测定法二部1D氮测定法三部M l A氮测定法一部K M乙醇量测定法0711乙醇量测定法二部\I E乙醇量测定法0712甲氧基、乙氧基与羟丙氧基测定法二部\l F甲氧基、乙氧基与羟丙氧基测定法一部IX N脂肪与脂肪油測定法0713脂肪与脂肪油测定法二部1H脂肪与脂肪油测定法0721维生素A测定法二部1J 维生素A测定法0722维生素D测定法二部1K维生素D测定法二部1M蛋白质含量测定法0731蛋白质含量测定法三部YI B蛋白质测定法0800限量检査法一部H C氯化物检査法0801氣化物检查法二部1A氯化物检查法0802硫酸盐检查法二部1B硫酸盐检查法0803硫化物检査法二部1 C 硫化物检查法0804硒检查法二部1D砸检查法0805氟检查法二部1E氟检查法二部1F氰化物检查法0806氰化物检查法三部YI X氮化物残留量测定法一部IX D铁盐检查法0807铁盐检查法二部1G铁盐检查法0808铵盐检查法二部1K铵盐检查法一部K E重金属检査法0821重金属检查法二部1H重金属检查法一部IX F砷盐检查法0822砷盐检査法二部1J 砷盐检查法一部K G干燥失重测定法0831干燥失重测定法二部1L干燥失重测定法三部W L干燥失重测定法一部K H水分测定法0832水分测定法二部坩M水分测定法三部\I D水分测定法一部K J 炽灼残渣检查法0841炽灼残渣检查法二部W N炽灼残渣检查法0842易炭化物检查法二部1C) 易炭化物检查法二部1P残留溶剂测定法0861残留溶剂测定法三部VI V残留溶剂测定法0871甲醇量检查法一部IX T甲醇量检查法0872合成多肽中的醋酸测定法二部1N合成多肽中的醋酸测定法429《中国药典》2015年版通则编码与2010年版附录编码对照表中国药典2015年版续表编号通则名称原附录原附录名称08732-乙基己酸测定法二部1L2-乙基己酸测定法0900特性检査法0901溶液颜色检查法一部H A溶液颜色检查法二部K A溶液颜色检查法0902澄清度检查法二部I X B澄清度检査法一部I X R不溶性微粒检查法0903不溶性微粒检查法二部I X c不溶性微粒检査法三部V I不溶性微粒检査法一部X I c可见异物检查法0904可见异物检査法二部I X H可见异物检查法三部V B 可见异物检査法一部M A崩解时限检查法0921崩解时限检查法二部\A崩解时限检查法三部V C崩解时限检查法一部1B融变时限检查法0922融变时限检査法二部I B融变时限检査法三部V D 融变时限检查法0923片剂脆碎度检查法二部X G片剂脆碎度检査法三部V E 片剂脆碎度检査法0931溶出度与释放度测定法二部X C溶出度测定法二部I D释放度测定法0941含量均匀度检查法二部X E 含量均匀度检查法—部a C最低装量检査法0942最低装量检查法二部\F最低装量检查法三部V F最低装量检查法0951吸人制剂微细粒子空气动力学特性测定法二部吸人气雾剂、吸人粉雾剂、吸入喷雾剂的雾滴(粒)X H分布测定法0952黏附力测定法一部1 E 贴膏剂黏附力测定法二部I J贴剂黏附力测定法0981结晶性检查法二部K D结晶性检查法一部X I B粒度测定法0982粒度和粒度分布测定法二部K E 粒度和粒度分布测定法三部V G粒度测定法0983锥入度测定法二部I K 锥入度测定法1100生物检査法一部I I B无菌检查法1101无菌检查法二部X I H 无菌检查法三部W A无菌检查法非无菌产品微生物限度检査:微生物计数法一部m c微生物限度检查法1105二部H J微生物限度检查法%三部I G微生物限度检査法• 430 •中国药典2015年版《中国药典》2015年版通则编码与2010年版附录编码对照表续表4编号通则名称原附录原附录名称非无菌产品微生物限度检查:控制菌检查法一部X I O c微生物限度检査法1106二部X I J微生物限度检査法三部M G微生物限度检查法一部X D I C微生物限度检查法1107非无菌药品微生物限度标准二部X I J微生物限度检査法三部M G微生物限度检査法一部X I D抑菌剂效力检查法指导原则1121抑菌效力检查法二部X I X N抑菌剂效力检査法指导原则三部X I A抑菌剂(防腐剂)效力检查法指导原则一部X f f l E异常毒性检查法1141异常毒性检查法二部X I c异常毒性检査法三部I F异常毒性检査法一部m a热原检査法1142热原检查法二部X I D热原检査法三部M D热原检查法一部X f f l D细菌内毒素检查法1143细菌内毒素检査法二部X I E细菌内毒素检査法三部1E细菌内毒素检查法1144升压物质检查法二部X I F升压物质检查法1145降压物质检查法一部m f降压物质检査法二部X I G降压物质检査法1146组胺类物质检查法新增1147过敏反应检查法一部X I I G过敏反应检査法二部X I K过敏反应检査法1148溶血与凝聚检查法—部X f f l H溶血与凝聚检査法二部X I L溶血与凝聚检查法1200生物活性测定法1201抗生素微生物检定法二部X I A抗生素微生物检定法1202青霉素酶及其活力测定法二部X I B青霉素酶及其活力测定法1205升压素生物测定法二部1A升压素生物测定法1206细胞色素C活力测定法二部I B细胞色素C活力測定法1207玻璃酸酶测定法二部m C玻璃酸酶测定法1208肝素生物测定法二部M D肝素生物测定法1209绒促性素生物测定法二部1E绒促性素生物测定法1210缩宫素生物测定法二部M F缩宫素生物测定法1211胰岛素生物测定法二部M G胰岛素生物测定法1212精蛋白锌胰岛素注射液延缓作用测定法二部I H精蛋白锌胰岛素注射液延缓作用测定法1213硫酸鱼精蛋白生物测定法二部1J硫酸鱼精蛋白生物测定法1214洋地黄生物测定法二部孤K洋地黄生物测定法1215葡萄糖酸锑钠毒力检查法二部I L葡萄糖酸锑钠毒力检查法1216卵泡刺激素生物测定法二部M M卵泡刺激素生物测定法1217黄体生成素生物测定法二部1N黄体生成素生物测定法431《中国药典》2015年版通则编码与2010年版附录编码对照表中国药典2015年版续表编号通则名称原附录原附录名称1218降钙素生物测定法二部1O降钙素生物测定法1219生长激素生物测定法二部1P 生长激素生物测定法1401放射性药品检定法二部X I放射性药品检定法一部n灭菌法1421灭菌法二部X I灭菌法三部XV 灭菌法1431生物检定统计法二部X W生物检定统计法2000中药其他方法2001显微鉴别法一部n c显微鉴别法2101膨胀度测定法一部IX () 膨胀度测定法2102裔药软化点测定法一部1D裔药软化点测定法2201浸出物测定法一部X A浸出物测定法2202鞣质含量测定法一部X B鞣质含量测定法2203桉油精含量测定法一部X c桉油精含量测定法2204挥发油测定法一部I D挥发油测定法2301杂质检査法一部IX A杂质检查法2302灰分测定法一部K K灰分测定法2303酸败度测定法一部IX P 酸败度测定法2321铅、镉、砷、汞、铜测定法一部IX B 铅、镉、砷、汞、铜测定法2322汞和砷元素形态及其价态测定法新增2331二氧化硫残留量测定法一部IX u二氧化硫残留量测定法2341农药残留量测定法一部IX Q农药残留量测定法2351黄曲霉毒素测定法一部IX V黄曲霉毒素测定法2400注射剂有关物质检查法一部K S 注射剂有关物质检查法3000生物制品相关检査方法3100含量测定法3101固体总量测定法三部1M固体总量测定法3102唾液酸测定法三部yi c唾液酸测定法3103磷测定法三部W A磷测定法3104硫酸铵测定法三部w c硫酸铵测定法3105亚硫酸氢钠测定法三部I E亚硫酸氢钠测定法3106氢氧化铝(或磷酸铝)测定法三部1F氢氧化铝(或磷酸铝)测定法3107氣化钠测定法三部I G氯化钠测定法3108枸橼酸离子测定法三部I H枸橼酸离子测定法3109钾离子测定法三部1I钾离子测定法3110钠离子测定法三部I J 钠离子测定法3111辛酸钠测定法三部V I K辛酸钠测定法3112乙酰色氨酸测定法三部VI W乙酰色氨酸测定法3113苯酚测定法三部V I M苯酚测定法3114间甲酚测定法三部VI N间甲酚测定法3115'硫柳汞测定法三部1B硫柳汞测定法432中国药典2015年版《中国药典》2015年版通则编码与2010年版附录编码对照表续表编号通则名称原附录原附录名称对羟基苯甲酸甲酯、对羟基苯甲酸丙酯含三部M l T对羟基苯甲酸甲酯、对羟基苯甲酸丙酯含量测定法3116量测定法3117O-乙酰基测定法三部M l F O乙酰基测定法3118己二酰肼含量测定法三部1K己二酰肼含量测定法3119高分子结合物含量测定法三部L高分子结合物含量测定法3120人血液制品中糖及糖醇测定法三部VI P人血液制品中糖及糖酵测定法3121人血白蛋白多聚体测定法三部yi Q人血白蛋白多聚体测定法人免疫球蛋白类制品Ig G单体加二聚体测三部yi r人免疫球蛋白类制品i g G单体加二聚体测定法3122定法3123人免疫球蛋白中甘氨酸含量测定法三部S 人免疫球蛋白中甘氨酸含量测定法3124重组人粒细胞刺激因子蛋白质含量测定法三部yi u重组人粒细胞刺激因子蛋白质含量测定法3125组胺人免疫球蛋白中游离磷酸组胺测定法三部V I E组胺人免疫球蛋白中游离磷酸组胺测定法3126I g G含量测定法三部H K I g G含量测定法3127单抗分子大小变异体测定法新增3200化学残留物测定法3201乙醇残留量测定法三部Y I D乙醇残留量测定法3202聚乙二醇残留量测定法三部V I G聚乙二醇残留量测定法3203聚山梨酯80残留量测定法三部Y I H聚山梨酯80残留量测定法3204戊二醛残留量测定法三部V I I戊二醛残留量测定法3205磷酸三丁酯残留量测定法三部V I J磷酸三丁酯残留量测定法3206碳二亚胺残留量测定法三部V I Y碳二亚胺残留量测定法3207游离甲醛测定法三部Y I L游离甲醛测定法3208人血白蛋白铝残留量测定法三部1K人血白蛋白铝残留量测定法3209羟胺残留童测定法新增3300微生物检査法3301支原体检査法三部M B支原体检查法3302外源病毒因子检査法三部1C病毒外源因子检査法3303鼠源性病毒检査法三部I H 鼠源性病毒检查法3304S V40核酸序列检査法三部I X H S V40核酸序列检査法3305猴体神经毒力试验三部X I L猴体神经毒力试验血液制品生产用人血浆病毒核酸检测技术新增3306要求3400生物澜定法3401免疫印迹法三部V I A 免疫印迹法3402免疫斑点法三部11 B 免疫斑点法3403免疫双扩散法1三部11 C免疫双扩散法3404免疫电泳法三部1 D 免疫电泳法3405肽图检查法三部1E肽图检查法3406质粒丢失率检査法三部I X G质粒丢失率检査法3407外源性D N A残留量测定法三部K B外源性D N A残留量测定法3408抗生素残留量检查法三部I X A抗生素残留量检查法3409激肽释放酶原激活剂测定法三部I X F激肽释放酶原激活剂测定法433《中国药典》2015年版通则编码与2010年版附录编码对照表中国药典2015年版续表编号通则名称原附录原附录名称3410抗补体活性测定法三部I X K抗补体活性测定法3411牛血清白蛋白残留量测定法三部1I牛血清白蛋白残留量测定法3412大肠杆菌菌体蛋白质残留量测定法三部I X C大肠杆菌菌体蛋白质残留量测定法3413假单胞菌菌体蛋白质残留量测定法三部I X D假单胞菌菌体蛋白质残留量测定法3414酵母工程菌菌体蛋白质残留量测定法三部K E酵母工程菌菌体蛋白质残留量测定法3415类A血型物质测定法三部K I类A血型物质测定法3416鼠I g G残留量测定法三部I X L鼠I g G残留量测定法3417无细胞百日咳疫苗鉴别试验三部I X s无细胞百日咳疫苗鉴别试验3418抗毒素、抗血清制品鉴别试验三部K T 抗毒素、抗血清制品鉴别试验3419A群脑膜炎球菌多糖分子大小测定法三部1G A群脑膜炎球菌多糖分子大小测定法3420伤寒V i多糖分子大小测定法三部I H 伤寒V i多糖分子大小测定法3421b型流感嗜血杆菌结合疫苗多糖含量测定法三部m J b型流感嗜血杆菌结合疫苗多糖含量测定法3422人凝血酶活性检查法三部I X N人凝血酶活性检查法3423活化的凝血因子活性检查法三部I X0活化的凝血因子活性检查法3424肝素含量测定法三部I X P 肝素含量测定法3425抗A、抗B血凝素测定法三部K J抗A、抗B血凝素测定法3426人红细胞抗体测定法三部I X Q人红细胞抗体测定法3427人血小板抗体测定法三部I X R人血小板抗体测定法3500生物活性/效价测定法3501重组乙型肝炎疫苗(酵母)体外相对效力检査法三部\A重组乙型肝炎疫苗(酵母)体外相对效力检查法3502甲型肝炎灭活疫苗体外相对效力检查法三部I S 甲型肝炎灭活疫苗体外相对效力检査法3503人用狂犬病疫苗效价测定法三部X I A人用狂犬病疫苗效价测定法3504吸附破伤风疫苗效价测定法三部XI B 吸附破伤风疫苗效价测定法3505吸附白喉疫苗效价测定法三部X I C吸附白喉疫苗效价测定法3506类毒素絮状单位测定法三部X I D 类毒素絮状单位测定法3507白喉抗毒素效价测定法三部XI E 白喉抗毒素效价测定法3508破伤风抗毒素效价测定法三部X I F破伤风抗毒素效价测定法3509气性坏疽抗毒素效价测定法三部X I G气性坏疽抗毒素效价测定法3510肉毒抗毒素效价测定法三部X I H 肉毒抗毒素效价测定法3511抗蛇毒血清效价测定法三部X I I抗蛇毒血清效价测定法3512狂大病免疫球蛋白效价测定法三部X I J 狂犬病免疫球蛋白效价测定法3513人免疫球蛋白中白喉抗体效价测定法三部I0人免疫球蛋白中白喉抗体效价测定法3514人免疫球蛋白F c段生物学活性测定法三部I P 人免疫球蛋白F c段生物学活性测定法3515抗人T细胞免疫球蛋白效价测定法(E玫瑰花环形成抑制试验)三部抗人T细胞免疫球蛋白效价测定法(E玫瑰花环形成X Q抑制试验)3516抗人T细胞免疫球蛋白效价测定法(淋巴细胞毒试验)三部抗人T细胞免疫球蛋白效价测定法(淋巴细胞X R毒试验)3517人凝血因子n效价测定法三部x j人凝血因子n效价测定法3518人凝血因子V I[效价测定法三部X K人凝血因子V I I效价测定法3519^人凝血因子I X效价测定法三部X L 人凝血因子K效价测定法3520人凝血因子X效价测定法三部X M人凝血因子X效价测定法• 434 •中国药典2015年版《中国药典》2015年版通则编码与2010年版附录编码对照表续表«编号通则名称原附录原附录名称3521人凝血因子V I E效价测定法三部X N人凝血因子1效价测定法3522重组人促红素体内生物学活性测定法三部I B重组人促红素体内生物学活性测定法3523干扰素生物学活性测定法三部I C 干扰素生物学活性测定法3524重组人白介素-2生物学活性测定法三部I D重组人白介素-2生物学活性测定法3525重组人粒细胞剌激因子生物学活性测定法三部X E重组人粒细胞刺激因子生物学活性测定法重组人粒细胞巨噬细胞剌激因子生物学活三部\F重组人粒细胞巨噬细胞剌激因子生物学活性测定法3526性测定法重组牛碱性成纤维细胞生长因子生物学活三部X G重组牛碱性成纤维细胞生长因子生物学活性测定法3527性测定法3528重组人表皮生长因子生物学活性测定法三部I H重组人表皮生长因子生物学活性测定法3529重组链激酶生物学活性测定法三部I I 重组链激酶生物学活性测定法3530鼠神经生长因子生物学活性测定法新增3531尼妥珠单抗生物学活性测定法新增3532重组人白介素-11生物学活性测定法新增3533A型肉毒毒素效价测定法新增3600特定生物原材料/动物3601无特定病原体鸡胚质量检测要求三部XII A无特定病原体鸡胚质量检测要求m b实验动物微生物学检测要求3602实验动物微生物学检测要求三部m c实验动物寄生虫学检测要求3603实验动物寄生虫学检测要求三部3604新生牛血淸检测要求三部XI D新生牛血清检测要求3605细菌生化反应培养基三部X I V细菌生化反应培养基37003701生物制品国家标准物质目录新增试剂与标准物质8000一部XV A试药8001试药二部XV A试药一部XV B试液8002试液二部I V B试液一部I V c试纸8003试纸二部I V C 试纸一部I V D缓冲液8004缓冲液二部X V D缓冲液一部XV E指示剂与指示液8005指示剂与指示液二部X V E指示剂与指示液一部XV F滴定液8006滴定液二部XV F滴定液8061对照品对照药材对照提取物—部X V G对照品对照药材对照提取物8062标准品与对照品二部I V G 标准品与对照品9000指导原则9001原料药物与制剂稳定性试验指导原则二部XIX c原料药与药物制剂稳定性试验指导原则• 435 •《中国药典》2015年版通则编码与2010年版附录编码对照表中国药典2015年版续表编号通则名称原附录原附录名称9011药物制剂人体生物利用度和生物等效性试验指导原则二部药物制剂人体生物利用度和生物等效性试验指导XIX B原则9012生物样品定量分析方法验证指导原则新增9013缓释、控释和迟释制剂指导原则二部XIX D 缓释、控释和迟释制剂指导原则9014微粒制剂指导原则二部XIX E 微襄、微球与脂质体制剂指导原则9015药品晶型研究及晶型质量控制指导原则新增9101药品质量标准分析方法验证指导原则一部二部X I A 中药质量标准分析方法验证指导原则m A 药品质量标准分析方法验证指导原则9102药品杂质分析指导原则二部XIX F 药品杂质分析指导原则9103药物引湿性试验指导原则二部X K J 药物引湿性试验指导原则9104近红外分光光度法指导原则二部XIX K 近红外分光光度法指导原则9105中药生物活性测定指导原则一部X I C 中药生物活性测定指导原则9106基于基因芯片的药物评价技术与方法指导原则新增9107中药材D N A条形码分子鉴定法指导原则新增一部X I E 药品微生物检验替代方法验证指导原则9201药品微生物检验替代方法验证指导原则二部XIX 0药品微生物检验替代方法验证指导原则三部X I B 药品微生物检验替代方法验证指导原则9202非无菌产品微生物限度检查指导原则一部二部11 F 微生物限度检查法应用指导原则XIX P 微生物限度检查法应用指导原则9203药品微生物实验室质量管理指导原则一部二部11G 药品微生物实验室规范指导原则XIX Q 药品微生物实验室规范指导原则9204微生物鉴定指导原则新增9205药品洁净实验室微生物监测和控制指导原则新增9206无菌检査用隔离系统验证指导原则新增9301注射剂安全性检査法应用指导原则—部二部I I B 中药注射剂安全性检查法应用指导原则XIX M 化学药品注射剂安全性检査法应用指导原则9302中药有害残留物限量制定指导原则新增9303色素测定法指导原则新增9304中药中铝、铬、铁、钡元素测定指导原则新增9305中药中真菌毒素测定指导原则新增9501正电子类放射性药品质量控制指导原则二部M G 正电子类放射性药品质量控制指导原则9502锝[99m T c]放射性药品质量控制指导原则二部XIX H 得[99™Tc]放射性药品质量控制指导原则9601药用辅料功能性指标研究指导原则新增9621药包材通用要求指导原则新增9622药用玻璃材料和容器指导原则新增9901国家药品标准物质制备指导原则新增第二增补本• 436。
药物分析课后答案
药物分析课后答案【篇一:药物分析课后习题答案】题1. b2. b3.b4. d5.c6. c7. d8. a9. b 10.c 11.c 12c 13b 14c 二、多项选择题1.acd2.bc3.bc4.bc5.bc6.acd7.ad8.bc9.abd 10.bcd11abc 12bcd 第三章一、单项选择题 bcdca二、多项选择题1acd 2acd3bd 4abcd 5abcd三、1 p452 p49第四章一、单项选择题1.c2.c3.b4.a5.c6.c7.b8.b9.b 10.d 11.c 12.a 13.d 14.d15.a 16.c 17.c 18.d 19.c 20.b 21c 二、多项选择题1.bcd2.acd3.ab4.ad5.bc6.abcd7.abd8. bcd9. cd10.acd 11.abd 12.abd 13.ab14.bcd15.abc 三、分析问答题1.答:判断滤纸上有无cl-或so42-的方法是:用少量无cl-或so42-蒸馏水agno3或bacl2,如果出现白色沉淀,说明滤纸上有cl -或42-。
消除的方法是:用含硝酸的水洗滤纸,至向最后的滤液中加入agno3或bacl2后,没有沉淀为止。
2.答:铁盐、铅盐、砷盐都要配成标准贮备液,临用时才能稀释成标准液使用,因为这些杂质在中性或碱性条件下易水解。
贮备液的特点是:高浓度,高酸性,抑制此类药物的水解。
3.答:杂质是在药物的生产和贮存过程中引入的。
有效控制杂质的方法包括: (1)改进生产工艺和贮存条件;(2)在确保用药安全、有效的前提下,合理制订杂质限量;(3)有针对性地检查杂质;应用类型特点(1)选用实际存在的待检杂质方法准确,但需要杂质对照品,不够方对照品法便。
2)选用可能存在的某种物质作较(1)方便,但仍需知道杂质种类,并为杂质对照品(3)高低浓度对比法需要对照品。
不需杂质对照品,方便,但杂质与药物薄层显色灵敏度应相近,否则误差大。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
附录Ⅸ D 铁盐检查法
除另有规定外,取各品种项下规定量的供试品,加水溶解使成25ml,移置50ml纳氏比色管中,加稀盐酸4ml与过硫酸铵50mg,用水稀释使成35ml后,加30%硫氰酸铵溶液3ml,再加水适量稀释成50ml,摇匀;如显色,立即与标准铁溶液一定量制成的对照溶液(取该品种项下规定量的标准铁溶液,置50ml 纳氏比色管中,加水使成25ml,加稀盐酸4ml与过硫酸铵50mg,用水稀释使成35ml,加30%硫氰酸铵溶液3ml,再加水适量稀释成50ml,摇匀)比较,即得。
如供试管与对照管色调不一致时,可分别移至分液漏斗中,各加正丁醉20ml提取,俟分层后,将正丁醇层移置50ml纳氏比色管中,再用正丁醇稀释至25ml,比较,即得。
标准铁溶液的制备称取硫酸铁铵〔FeNH4(SO4)2²12H2 O〕 0. 863g,置1000ml 量瓶中,加水溶解后,加硫酸2.5ml,用水稀释至刻度,摇匀,作为贮备液。
临用前,精密量取贮备液10ml,置100ml量瓶中,加水稀释至刻度,摇匀,即得(每1ml相当于10ng的Fe)。
