第二十八章重排反应
大学有机化学反应方程式总结重排反应

大学有机化学反应方程式总结重排反应反应方程式是有机化学中非常重要的一部分,它描述了化学反应中物质的转化过程。
在大学有机化学中,我们学习了各种各样的反应方程式,其中包括重排反应。
本文将对大学有机化学中的重排反应进行总结,介绍其机理和一些典型反应。
1. 环丙烷重排反应(C1C2速度放缓)在环丙烷分子中,碳原子1和碳原子2之间为一个甲基基团,环丙烷重排反应就是指这个甲基基团发生位移,形成其他异构体的过程。
环丙烷重排反应可以发生两种类型的重排:1,2-重排和1,3-重排。
1,2-重排:环丙烷中的甲基基团发生位移,形成丙烯和丙烯烷的异构体。
1,3-重排:环丙烷中的甲基基团发生位移,并且环丙烷的碳原子2和碳原子3之间的键断裂,形成丙烯和甲烯烷的异构体。
2.1-甲基移位反应1-甲基移位反应是指分子中一个碳原子上的甲基基团在反应中发生迁移,形成另一种异构体。
这种反应在很多有机化合物中都可以观察到,例如烷烃、烯烃等。
3. α,β-不饱和酮的Knoevenagel缩合反应Knoevenagel缩合反应是α,β-不饱和酮与活性甲基化合物(如甲醛、甲基丙烯酮等)在碱的催化下进行的加成反应。
这个反应的机理涉及羰基亲核加成和酸碱中和等步骤。
4. 列维架桥异构化反应列维架桥异构化反应发生在某些烯烃和孤立的单质金属之间的反应中。
该反应可以形成由金属和碳原子构成的稳定的配位化合物。
总结:大学有机化学中的反应方程式总结重排反应,包括环丙烷重排反应、1-甲基移位反应、α,β-不饱和酮的Knoevenagel缩合反应和列维架桥异构化反应等。
这些反应在有机合成中具有重要的地位,对于理解有机反应的机理和应用具有重要意义。
在学习和运用这些反应时,我们需要深入了解它们的机理,并且掌握相应的实验操作技巧。
大二有机化学课件重排反应

O
R C .N. OH
R N=C=O + OH H2O RNH2
19
从杂原子到碳原子的重排
在这类反应中,与杂原子(N,O,S等)相邻的碳原子,由于 受杂原子和周围吸电子基(Z)的影响,其活泼氢原子在强碱作 用下易形成碳负离子过渡态,然后杂原子上烃基通过分子内迁 移该碳负离子上,从而改变了分子骨架,以下列通式表示:
5
迁移基团 迁移顺序
OCH3
>
Cl
>
> R3C- > R2CH-
> RCH3- > CH3- > H-
CH3 H
Ph C C OTs
△
CH3 CH3
H3C
H C C Ph CH3 CH3
苯的迁移速度为甲基的3000倍
6
2、Pinacol rearrangement 频哪醇重排
在酸催化下,邻二叔醇失去一分子水,重排成醛或酮的反应
AlBr3 AlBr4
CH3
CH3
+
C CH2
CH3
1,2-烷基迁移
CH3
+
C CH2 CH3 CH3
转变成更稳定的正离 子是重排的一个动力
AlBr4 H+
CH3
Br C CH2 CH3 CH3
CH3 C CH CH3 CH3
4
C+ 的形成形式 (a)卤代烃 Ag+ AlCl3
(CH3)3C-CH2Cl Ag (AgNO3) (CH3)3C-CH2+AgCl
26 重排反应
1
定义:在同一分子内,某一原子或基团从一个原子迁移至另一 个原子而形成新分子的反应。
W AB
W AB
第二十八章重排反应

Ph
Ph
2. 半频哪醇重排
Ph
Ag+
HO
CH2 I
Me
O C CH2 Ph Me
HO
Ph Ph C HC NH2 Me
HNO2
Ph Ph
H O C CH
N+
N
Me
Me C CH2 Ph2 O
O
HO CN
HO CH2 NH2
HCN
LiAlH4
O HO CH2 NH2
HNO2,HCl
61%
频哪醇重排立体选择性很强:
_H
OH
H2SO4
Ac2O
7
O
2
10 SO3H
16
_H
HO
2
7 10
SO3H
16
3 45
3 45
H2SO4
3 2 OH
6
1 10 SO3H
54 7
半频哪醇重排重排
二、烃基由碳原子迁移到杂原子上
1. Hofmann重排、 Lossen重排、 Curtius重排、 Schmidt重排
1882年 霍夫曼
1899年, Wagner发现,在萜类的反应中环系发生变化。 例如:
HCl
Cl
Cl
莰烯
外-2-氯莰烷
α-蒎烯
HCl
Cl
内-2-氯莰烷
定义:醇或卤代烃在酸催化下进行亲核取代或消除反应 时,烯烃进行亲电加成时发生的重排。
萜类化合物中烃基的迁移叫做Nametkin(H S)重排(区别于 桥链的迁移),现在也包括在Wagner-Meewein重排中:
OO OH
Ar C C
Ar
OO Ar C C OH
药物合成讲稿重排反应
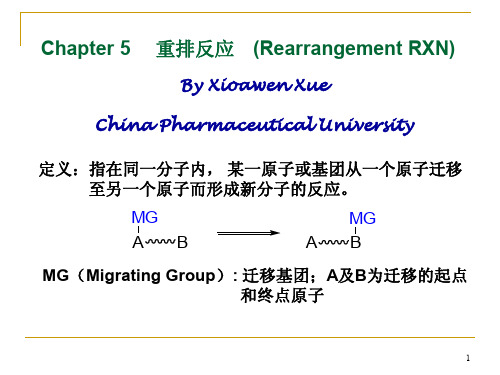
Me COOH OH
H
H
60-70%
27
b. 碱及溶剂
所用的碱通常为KOH, NaOH等无机碱,溶剂为水或含水乙 醇。如用醇的碱金属盐为碱,反应产物为酯。
28
在药物合成中的应用
抗癫痫药苯妥英钠
29
四. Beckmann 重排 定义:醛肟(Oxime)或酮肟在酸性催化剂作用下重排 成取代酰胺的反应称Beckmann 重排。
7
Mechanism
8
反应影响因素 a. 反应物结构:凡能生成正碳离子的化合物,如醇、卤 烃、 烯烃、胺及环氧化物等
OH NHTs PPh 3 DEAD ArCO2 NHTs OPPh3 NHTs
NHTs H
ArCO2-
9பைடு நூலகம்
CH3 CH3 CH3 TsOH
CH3
CH3 CH3 H3C
CH3 CH3
Chapter 5
重排反应 (Rearrangement RXN)
By Xioawen Xue
China Pharmaceutical University 定义:指在同一分子内, 某一原子或基团从一个原子迁移 至另一个原子而形成新分子的反应。
MG A
B
A
MG B
MG(Migrating Group): 迁移基团;A及B为迁移的起点 和终点原子
1
2
分类: 根据迁移起点及终点原子之间的位置,可分为1, 2-迁 移、1, 3-迁移…… 根据迁移起点及终点原子的种类,可分为从碳原子到碳 原子的重排、从碳原子到杂原子的重排以及从杂原子到 碳原子的重排。 根据反应机理, 可分为亲核重排、亲电重排、自由基 重排及协同反应(s迁移重排)。
高等有机化学重排反应公开课获奖课件

Me Me C CMe2
OH
H Me C CMe3 O
Me C CMe3 OH
第33页
脂环族氨基醇和脂环族卤代醇则发 生扩环或缩环反应
CH2NH2 HNO2
OH
-N2
CH2 OH
OH CH3 Ag AgI
I
OH
CH3 or
OH CH3
O-H CH3
OH H
O
OH CH3
H C CH3 OH
C CH3 O
机理:
(NH3存在时生成酰胺):
(EtO-)
R
H2 O CC
H C
R' EtONa
O
R
H C
C
H C
R ' -X
R
HH CC
C
'R E t O N a
HH RCC
aC
R'
b
X
a) R
H C
H C
R'
X
O
O
O Et
b) R
H C
H C
R'
COOEt
H
R
H2 H CC
R'
COOEt
E tO O C H
R
第46页
CH2 C CH2Cl
OH
O
OH
CH C CH3 Cl O
OH
O
CH2 CH2COOH ( A 比 B 稳定 )
CH CH2COOH A
CH CH2 COOH B
O
O
Cl C CH3
EtONa
O EtO
EtONa
C 所连接的取代基越少越稳定
COOEt CH2
重排反应

重排反应(rearrangement reaction)是分子的碳骨架发生重排生成结构异构体的化学反应,是有机反应中的一大类。
重排反应通常涉及取代基由一个原子转移到同一个分子中的另一个原子上的过程。
以下例子中取代基R由碳原子1移动至碳原子2:分子间重排反应也有可能发生。
按反应机理,重排反应可分为:基团迁移重排反应和周环反应。
基团迁移重排反应反应物分子中的一个基团在分子范围内从某位臵迁移到另一位臵的反应。
常见的迁移基团是烃基。
迁移基团的原来位臵称为迁移起点,迁移后的位臵称为迁移终点,这类反应又可按价键断裂方式分为异裂和均裂,前者重要得多,其中尤以缺电子重排最为重要。
缺电子重排反应是反应物分子先在迁移终点形成一个缺电子活性中心,从而促使迁移基团带着键裂的电子对发生迁移,并通过进一步变化生成稳定产物。
以频哪酮重排反应为例,反应物分子中的一个羟基与酸作用形成锌盐后失水变为缺电子活性中心正碳离子,促使邻位带羟基碳原子上的一个甲基带着电子对发生1,2-迁移,同时羟基氧原子上未共用电子对转移至碳?氧之间构成双键,最后失去质子而得产物(见上反应式)。
在迁移终点形成一个富电子活性中心后,促使迁移基团不带键裂电子对而转移,叫富电子重排反应,例如法沃斯基重排:a - 卤代酮在强碱作用下重排,生成碳架不同的羟酸酯,反应通过富电子活性中心负碳离子进行:环反应反应物因分子内共价键协同变化而发生重排Favorsky重排反应的反应,有电环化反应和δ迁移反应。
例如环丁烯经加热发生逆向电环化而得1,3-丁二烯,1,3-己二烯经加热发生氢原子1,5-迁移而得2,4-己二烯。
这类重排在合成中应用最多的是属于3,3-迁移的科普重排和克莱森重排。
科普重排是1,5-二烯受热重排为另一个1,5-二烯的反应。
例如内消旋-3,4-二甲基-1,5-己二烯经加热几乎定量地转变为(Z ,E)-2,6-辛二烯:克莱森重排反应是参与反应的体系中有一个氧原子代替了碳原子。
重排反应
R O C C R'
H2O R'OH O C CH R NH3 R'NH2
RCH2COOH RCH2COOR' RCH2CONH2 RCH2CONHR'
阿恩特-埃斯特尔特(Arndt-Eistert)合成
R'COOH R'COX CH2N2 R'COCH=N2 H2O R'CH2COOH
制备多一个碳的羧酸
第六章
重排反应
Rearrangement Reaction
定义:受试剂或介质的影响,同一有机分子内的一个基团
或原子从一个原子迁移到另一个原子上,使分子构架发生 改变而形成一个新的分子的反应称为重排反应。
W A B A W B
A:重排起点原子,B:重排终点原子,W:重排基团
分类: 离子型机理(亲核重排,亲电重排) 自由基重排 周环机理重排(σ-键迁移重排)
4
AlCl3
Et2O
PhCH2NHPh
2、Hofmann重排
酰胺用溴(或氯)和碱处理转变为少一个碳原子的伯胺的 反应。又叫Hofmann降解反应。
O R C NH2
NaOX
机理:
O R C NH2
or X2/NaOH O Br2 R C NH Br -HBr
RNH2
OH O R C N Br
-Br
O EtO EtONa
Cl
CH2COOEt C 所连接的取代基越少越稳定
CH3 Br H3C C EtONa C CH3 Br H3C C C O CH2 EtO Br H3C O C C OEt H3C EtOOC C CH2 CH2 Br C CH2
COOEt
重排反应_精品文档
重排反应7重排反应重排反应指同一分子内,其中一原子或基团从一个原子迁移到另一个原子形成新的分子的反应。
利用重排常常可以合成用其它方法难以合成的物质。
其反应机理不外乎亲核、亲电和自由基几种。
按其迁移的方式大致可分为从碳原子到碳原子的重排、从碳原子到杂原子的重排以及从杂原子到碳原子的重排等几种。
7。
1从碳原子到碳原子的重排从碳原子到碳原子的重排使碳骨架发生变化。
其中典型的重排包括亲核1,2-重排和亲电1,2-重排。
前者包括Wagner-Meerwein重排和Pinacol重排;后者包括Wolf和Arndt-Eitert重排等。
7。
1、1Wagner-Meerwein重排在质子酸或Lewi酸催化下形成的碳正离子中,烷基、芳基或氢从正离子相邻的碳原子上迁移到正离子上的反应,称为Wagner-Meerwein重排。
生成更稳定的碳正离子或产物成为重排的动力。
反应示例:双环二烯酮重排为四氢萘酚。
用质子酸处些环外烯烃可致重排。
7。
1、2Pinacol重排酸催化下,邻二醇脱水重排为醛或酮的反应称为Pinacol重排。
(1)四取代邻二醇的重排如果四个取代基相同,单一产物。
如果是对称的邻二醇,产物分配主要取决于迁移基团的迁移能力。
迁移能力可能与亲核能力正相关。
一般而言,芳基>烷基>氢。
对位供电子基取代的芳基>未取代的芳基>邻位取代的芳基(空间障碍)。
如果是不对称的邻二醇,产物分配主要取决于形成的碳正离子的稳定性,与迁移基团的迁移能力关系不大。
不对称Pinacol重排的选择性不是太好,常常得到混合物,在药物合成上的意义不太大。
(2)三取代邻二醇的重排对于三取代的邻二醇,其中的叔碳上形成的碳正离子较稳定,所以一般是仲碳上的基团(或氢原子)迁移。
如果需要叔碳上的基团迁移,可采用衍生物法在碱性条件下重排。
(3)脂环上的邻二醇重排羟基位于脂环上的邻二醇的重排常导致脂环结构的变化。
螺环形成:羟基共环的情形:如上,对于羟基共环的情形,总是处在离去的羟基反式的基团迁移,这在一定程度上说明Pinacol重排可按分子内SN2机理进行。
重排反应
重排过程中的立体因素:
Beckmann重排(反位基团)
重要的重排反应 迁移基向正碳离子的迁移
• 频哪醇重排 邻二醇在酸的作用下重排成醛和酮的反应
1)驱动力? 2)两个羟基中谁先离去?(生成的正碳离子稳定性) 3)立体化学上离去基与迁移基成反式共平面
半频哪醇重排
α-碳上有OH的碳正离子
实例
Taylor’s work
Chem. Commun., 2009, 3249
O N
N
OEt O N 98% (by 1HNMR)
O
O
O OEt
Benzil-Benzilic acid (二苯基乙二酮-二苯基羟基乙酸)重排
其他二酮类
Arndt-Eistert合成和Wolff重排
(Wolff重排)
重氮酮经加热、光解或者金属催化剂 作用下重排生成烯酮
基团向缺电子氮原子的迁移 Beckmann重排
Hoffmann重排
1)N上必须两个H 2)第三步重排中多数认为Br的离去和R的迁移是协同进行的,也有认 为Br先离去形成氮烯再迁移O Ar[O源自 -eNAr OH N
Ar [O] O -e-
H N
Ar Base O -H+ N
Ar O
O O O OEt 1.0 eq. Cu(OAc)2H2O 1.1 eq. KOtBu DMF, 110 oC 1h
1.0 eq. Cu(OAc)2H2O 1.1 eq. KOtBu OEt -H+ [O] O N O OEt N O O OEt [O] N OEt DMF, 110 oC 1h N 65% -H+ O O
环的扩大和缩小反应
脂环化合物环上碳原子带有正电荷,通过重排环会收缩 如果正碳离子位于环外α-位,则环会扩大
《有机化学重排反应》课件
THANKS
感谢观看
详细描述
重排反应通常涉及分子内部的重排,包括电子、质子和原子的重新排列,这种 重排可以发生在分子内或分子间,并伴随着键的断裂和形成。重排反应通常伴 随着键能的变化,需要一定的活化能来启动反应。
重排反应的重要性
总结词
重排反应在有机化学中具有重要的意义,它涉及到许多有机化合物的合成、转化和降解过程。
详细描述
重排反应的动力学与热力学
动力学研究
分析重排反应的动力学特征,如反应 速率常数、活化能等,以及如何影响 反应进程。
热力学研究
探讨重排反应的热力学性质,如反应 熵变、焓变等,以及与反应条件的关 系。
重排反应的历程与过渡态
历程研究
揭示重排反应的具体步骤和中间体,以及各 步骤之间的相互转化。
过渡态研究
分析重排反应过程中的过渡态结构,以及如 何影响反应活化能和产物形成。
贝克重排反应是一种有机化学反应,涉及环丙烷环系的重排过程。在反应中,环丙烷环系通过加热或 其他能量源的激发,发生重排,生成新的化合物。
沃尔夫-凯惜纳重排反应
总结词
涉及芳香族化合物的重排反应
详细描述
沃尔夫-凯惜纳重排反应是一种有机化学反应,涉及芳香族化 合物的重排过程。在反应中,芳香族化合物通过加热或其他 能量源的激发,发生重排,生成新的化合物。
计算化学的应用
利用计算化学方法预测和优化 重排反应的途径和产物,提高
反应效率。
06
参考文献
参考文献
《有机化学重排反应》第二版,作者
01
XXX,出版社:XXX。
《有机化学重排反应》第三版,作者
02
XXX,出版社:XXX。
"有机化学重排反应研究进展",作者
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
HO
O
N
H2NOH
O
H
NH
用质子酸(极性溶剂中)催化时存在异构化问题。
R
OH H
CN
R'
R
CN
R'
OH
(R和 R‘相差不大时,会发生异构化,但R=CH3, R'=Ph不会发生异构化)
例:
OH N
POCl3,吡啶 20%,H2SO4-H2O HCl,Et2O
+ NO
98% 43% 5%
N O
2%
57% 95%
PhCOCHN2
反应机理:
AgO,NH4OH
△
PhCH2CONH2 + N2
R
CH N +
N_
O
-N2 O C CHR
H R C_ N N
+ O
+ H2O
HO C CH2R O
4. 二苯乙醇酸重排
1838年Liebig J发现:
OO
NaOH
OH O
Ar C C Ar
△
Ar C C ONa
Ar
1928年Ingold C K 提出重排机理:
H2O
CH3
CH3 C C+ CH3 OH CH3
CH3
CH3 C C CH3 +OH CH3
CH3
H+
CH3 C C CH3 O CH3
生成最稳定的碳正离子:
Ph2C CH2 H+ Ph2C+ CH2
OH OH
OH
Ph2CH CH +OH
H+
Ph2CH
CH O
苯基优先迁移:
PhHC CHPh H+ PhHC
PCl3 OH
典型的Wagner-Meewein重排,3,3-二甲基-2-丁醇在酸催化 下脱水的反应机理:
CH3 H CH3 C C CH3 H
CH3 OH
CH3 H
CH3 C
-H2O
C CH3
CH3 OH2
CH3 H CH3 C C CH3
CH3
H
CH3 C
CH3 C CH3
H CH3 C
CH3
Ph
Ph
2. 半频哪醇重排
Ph
Ag+
HO
CH2 I
Me
O C CH2 Ph Me
HO
Ph Ph C HC NH2 Me
HNO2
Ph Ph
H O C CH
N+
N
Me
Me C CH2 Ph2 O
O
HO CN
HO CH2 NH2
HCN
LiAlH4
O HO CH2 NH2
HNO2,HCl
61%
频哪醇重排立体选择性很强:
-H
CH2OH +
OH
+
NH2 HNO2 -N2
CH2OH
H2O
OH +
-H
+
Demyano重排也可以归入Wagner-Meewein重排中。
Wagner-Meerwein重排在合成中的应用:
O7
10
2 16
H
7 10
HO
216
3 45
34 5
3
OH
6
10
21 54 7
H
Wagner-Meerwein重排
_H
OH
H2SO4
Ac2O
7
O
2
10 SO3H
16
_H
HO
2
7 10
SO3H
16
3 45
3 45
H2SO4
3 2 OH
6
1 10 SO3H
54 7
半频哪醇重排重排
二、烃基由碳原子迁移到杂原子上
1. Hofmann重排、 Lossen重排、 Curtius重排、 Schmidt重排
1882年 霍夫曼
亲核重排
R C N R'
R C N R' H2O RCONHR'
试剂:H2SO4 , HCl, PCl5,POCl3,SOCl2, TsCl, 甲酸,聚磷 酸等。其作用是将OH转变成离去倾向大的基团。
R
OH
PCl5 + R' C N
R RC
OPCl4 N
离去基团
环酮的Beckmann重排得到扩环产物:
EtOH EtOCNHR
1923年 施密特
O RCOH
_ N2
H, HN3
R H O C NH N N
O HOCNHR
OH
_ CO2
RNH3
(1)Hofmann重排
CONH2
Br2,PTC
NaOH-CH2Cl2, 25 ℃min PTC=Bu4N+HSO4-
NCO
H+,H2O
NCO 87%
NH2Biblioteka (2)Lossen重排Ph(CH2)2NH2 70%-90%
Ph(CH2)4CO2H NaN3,H2SO4,CHCl3 HO3S 40 ℃, 1 h
(CH2)4NH2
2. Beckmann重排
醛肟或酮肟在酸性试剂作用下重排生成取代酰胺的反应。
R
OH
R' C N
H
O R C NHR'
机理:
R
OH H
R' C N
R
OH2
R' C N
PhCH2CON3
EtOH △
PhCH2NHCO2Et O
(PhO)2 P+ N3 ,Et3N
HCl AcOH
PhCH2NH3+Cl80%
N COOH t-BuOH,reflux, 23 h
(4)Schmidt(施密特)重排
N NH CO2Bu-t 73%
NaN3,H2SO4 Ph(CH2)2CO2H
H2O R
R
R
R
H O+ H
R
OR
-H+
R C O + ROH
R
R
三、烃基由杂原子迁移到碳原子上 1. Stevens(斯提文)重排
CH3
OH
CH3
PhCOCH2 N CH3
PhCOCH N CH3
CH2Ph
CH2Ph
CH3 PhH2COCH N CH3
CH2Ph
分子内反应,其可能的机理:
CH3
PhCOCH N. CH3 . CH2Ph
CH3
PhCOC. H N CH3 . CH2Ph
两个自由基生成后同在溶剂 笼中,在逸出前即迅速结合
Sommelet(萨姆勒特)-Hauser(霍瑟)重排与Stevens(斯 提文)重排相似:
CH2N(CH3)3OH NaNH2-NH3
CH3 CH2N(CH3)2
其可能的机理为:
H2C
CH3
N CH3 NaNH2-NH3 CH3
CH3
CH3 C
CHPh
CH3
CH3 C CHPh CH3 CH3
迁移基团迁移顺序:
Product
CH3O > R3C
>
> Cl
> CH2=CH
> R2CH >CH3 > H
Demyano重排:
NH2 HNO2
N≡N
NH2 HNO2
N≡N
OH 48%
OH 47%
CH2NH2 HNO2 -N2
CH2 H2O
HO
OH OH
Ph O
注意:频哪醇重排机理还不是很清楚。
频哪醇重排可用于环的扩大、缩小和螺环化合物合成:
HO OH
O
H2SO4-H2O
Ph
OH
H+
OH
Ph
COPh Ph
频哪醇重排所用的原料可以由醛或酮的双分子还原得到:
O Al(Hg),CH2Cl2,回流
HO OH
Ph O O
Mg,MgCl2
Ph OH OH
1899年, Wagner发现,在萜类的反应中环系发生变化。 例如:
HCl
Cl
Cl
莰烯
外-2-氯莰烷
α-蒎烯
HCl
Cl
内-2-氯莰烷
定义:醇或卤代烃在酸催化下进行亲核取代或消除反应 时,烯烃进行亲电加成时发生的重排。
萜类化合物中烃基的迁移叫做Nametkin(H S)重排(区别于 桥链的迁移),现在也包括在Wagner-Meewein重排中:
OH OH
+
CHPh OH
Ph2CH CH +OH
H+
Ph2CH
CH O
应考虑两个问题:
1、决定哪个羟基离去,一般是能生成最稳定的碳 正离子的羟基离去。
2、哪一个基团迁移。
在表面相似条件下重排,产物却不同:
Ph Ph
Ph Ph
Ph
Ph C
C
浓H2SO4
Ph C
C H 40%H2SO4 Ph C
CH
H2C
CH3 N CH3 CH2
CH2
CH2N(CH3)2 H
CH3 CH2N(CH3)2
2. Wittig(魏狄希)重排
1942年, Wittig发现,醚与苯基锂反应生成锂化醚,
异构化而生成醇锂:
Li
R
PhCH2OR PhLi PhCHOR
Ph-CHOLi
Wittig重排反应机理与Stevens重排反应机理相似:
CH3 H
C CH3 CH3 C C CH2
