无机化学金属有机化合物的亲核反应
化学反应中的亲核取代反应

化学反应中的亲核取代反应化学反应是物质之间发生变化的过程,其中亲核取代反应是一种重要的反应类型。
亲核取代反应是指一个亲核试剂与一个电子不足的反应物发生反应,亲核试剂中的亲核基团取代掉反应物中的一个离去基团。
这种反应在有机合成中具有广泛的应用,可以用于合成各种有机化合物。
亲核取代反应可以分为两类:亲核试剂为中性物质的亲核取代反应和亲核试剂为离子的亲核取代反应。
中性物质的亲核取代反应通常发生在有机化合物中,而离子的亲核取代反应则发生在无机化合物或离子中。
中性物质的亲核取代反应中,亲核试剂通常是一种带有孤对电子的原子或分子,如氨、水、醇等。
这些亲核试剂通过与反应物中的电子不足的原子或分子发生反应,形成新的化学键。
例如,氨与醛反应可以生成胺,水与酰氯反应可以生成醛或酮。
离子的亲核取代反应中,亲核试剂通常是带有正电荷的离子,如氢离子、钠离子等。
这些亲核试剂通过与反应物中的带有负电荷的离子或原子发生反应,形成新的化学键。
例如,氢离子与氢氧根离子反应可以生成水,钠离子与氯离子反应可以生成氯化钠。
亲核取代反应的速率通常受到多种因素的影响,如反应物浓度、温度、溶剂等。
在一些情况下,亲核取代反应可能会出现竞争性反应,即不同的亲核试剂与反应物中的不同位置发生取代反应。
这时,反应的选择性就成为一个重要的问题。
在有机合成中,亲核取代反应可以用于合成各种有机化合物,包括药物、农药、染料等。
通过选择不同的反应条件和亲核试剂,可以实现对目标化合物的选择性合成。
亲核取代反应还可以用于构建碳-碳键和碳-杂原子键,从而构建复杂的有机分子。
总之,亲核取代反应是化学反应中的一种重要反应类型,广泛应用于有机合成中。
通过选择不同的亲核试剂和反应条件,可以实现对目标化合物的选择性合成。
亲核取代反应的研究对于发展新的有机合成方法和合成新的有机化合物具有重要意义。
[解答]无机化学反应之亲电反应与亲核反应详解
![[解答]无机化学反应之亲电反应与亲核反应详解](https://img.taocdn.com/s3/m/3f26693103020740be1e650e52ea551810a6c965.png)
[解答]无机化学反应之亲电反应与亲核反应详解亲电反应和亲核反应详解一、目的和要求通过本节课的学习,达到:1. 掌握共价键的断裂方式2. 掌握有机化学反应类型的分类3. 掌握亲电试剂和亲核试剂的概念4. 掌握亲电和亲核概念5. 掌握亲电和亲核反应的历程要求能够辨别亲电反应和亲核反应。
引言(提出问题)我们说乙炔和溴的四氯化碳溶液反应生成1,2—二溴乙烯,进一步反应生成1,1,2,2—四溴乙烷的反应为亲电加成,反应式如下:BrBrBrBrBr2CCl4CCHHCHCBr+(亲电加成)2HCHCHCCl4BrBr乙炔1,1,2,2-四溴乙烷 1,2-二溴乙烯同样是乙炔,在碱的存在下,和甲醇发生反应生成甲基乙烯基醚是亲核加成反应,反应式如下:KOH(亲核加成)HCCOCHOHCHHCHC23+3H加热、加压甲基乙烯基醚乙炔在有机化学的学习过程中,亲电和亲核是让很多同学困惑的概念,为了说明亲电和亲核的概念,让我们从共价键的断裂说起,来阐明亲核反应和亲电反应。
二、共价键的断裂方式有机化学反应的实质是旧键的断裂和新键的形成过程。
组成有机化合物的化学键主要是共价键,共价键是由电子云重叠而成,每根共价键由电子对(2个电子)构成,共价键的断裂方式有两种:1 均裂均裂:A:B ? A? , B?即构成共价键的电子对在断裂时平均分配到两个原子上,形成带有单电子的活泼原子或基团——游离基(又叫自由基),这种断裂方式称为共价键的均裂。
2 异裂-++- 异裂:A:B ? A ,B(或A , B)即构成共价键的电子对在断裂时完全转移到1个原子上,形成正离子和负离子,这种断裂方式称为共价键的异裂。
三、有机反应类型分类根据共价键断裂方式分类根据共价键的断裂方式分类,可分为协同反应、自由基反应、离子型反应: 协同反应:在反应过程中,旧键的断裂和新键的形成都相互协调地在同一步骤中完成的反应称为协同反应。
协同反应往往有一个环状过渡态。
它是一种基元反应。
有机化学反应机理总结

有机化学反应机理总结一、引言有机化学是研究有机物合成和反应规律的科学领域。
在有机化学中,了解反应机理对于准确预测反应产物以及设计新的合成路径至关重要。
本文将总结几种常见的有机化学反应机理,包括亲核取代、酸催化、碱催化和自由基反应等。
二、亲核取代反应机理亲核取代反应是指一个亲核试剂(通常是负电荷较高的电子富余分子)与一个受体分子发生反应,取代掉受体分子中的某个官能团。
这类反应的机理通常分为四个步骤:出发物生成电子富余中间体、亲核试剂攻击中间体、负离子生成和负离子与溶剂或其他分子反应。
亲核取代反应具有广泛的应用,例如取代烯烃、芳香化合物和醇等。
三、酸催化反应机理酸催化反应是指在酸性条件下进行的一系列有机化学反应。
酸催化反应机理通常包括质子化、核迁移、亲核试剂攻击和质子转移等步骤。
酸催化反应广泛应用于合成复杂有机分子,如酯化、缩合和环化反应等。
四、碱催化反应机理碱催化反应是指在碱性条件下进行的一系列有机化学反应。
碱催化反应机理通常包括质子解离、亲电试剂攻击、质子转移和负离子生成等步骤。
碱催化反应常见于酯水解、亲电取代和醇酸碱中和反应等。
五、自由基反应机理自由基反应是指在自由基存在下进行的一系列有机化学反应。
自由基反应机理通常包括自由基生成、自由基与稳定分子反应、自由基重组和自由基转移等步骤。
自由基反应广泛应用于合成烯烃和环化反应等。
六、结论有机化学反应机理的理解对于有机化学的学习和应用具有重要意义。
通过掌握亲核取代、酸催化、碱催化和自由基反应等常见反应的机理,我们能更好地理解有机化学反应中的规律,合理设计合成路线,并预测反应的产物。
在未来的有机化学研究和实践中,深入了解和掌握有机化学反应机理将会取得重要的成果。
考研化学无机化学重要反应总结

考研化学无机化学重要反应总结在考研化学中,无机化学是一个重要的科目。
熟练掌握无机化学的重要反应对于考研的成功非常关键。
下面我将对考研化学无机化学重要反应进行总结,希望能够对考生们有所帮助。
一、氧化还原反应氧化还原反应是无机化学中最重要的一类反应。
其中,常见的重要反应包括:1. 活动性金属与酸反应:活动性金属(如铁、锌、铝等)与酸(如盐酸、硫酸等)反应会生成相应金属的盐和氢气。
例如:2HCl + Zn → ZnCl2 + H22. 金属与非金属元素反应:金属与非金属元素的反应通常是氧化还原反应,其中金属元素被氧化,非金属元素被还原。
例如:2Mg + O2 → 2MgO3. 单质与氧化剂反应:单质与氧化剂反应的热稳定性变化可用来判断其是否是还原剂。
例如:2Cu + O2 → 2CuO4. 非金属氧化物与碱反应:非金属氧化物与碱反应会生成相应的盐和水。
例如:SO2 + 2NaOH → Na2SO3 + H2O二、配位化学配位化学是无机化学中另一个重要的分支。
其中,与配位化学相关的重要反应包括:1. 配位络合反应:配体与金属离子之间的反应称为配位络合反应。
在配位化学中,常见的络合反应有配体取代、加成、还原等反应。
例如:[Fe(H2O)6]3+ + 6NH3 → [Fe(NH3)6]3+ + 6H2O2. 配位置换反应:配位置换反应是指一个配体从金属离子中脱离,同时另一个配体与金属离子结合。
例如:[Cu(NH3)4]2+ + 2H2O → [Cu(H2O)4]2+ + 4NH3三、反应动力学反应动力学是研究化学反应速率和反应机理的科学。
了解反应动力学对于掌握无机化学重要反应非常重要。
下面是一些值得关注的重要反应动力学内容:1. 反应速率:反应速率描述了反应物的消耗和反应物产物的生成之间的关系。
例如:2NO2 → 2NO + O22. 反应速率常数:反应速率常数是描述反应速率与反应物浓度关系的常数。
例如:rate = k[NO2]^23. 反应机理:反应机理是描述反应物转化为产物的详细过程。
有机金属化合物的反应
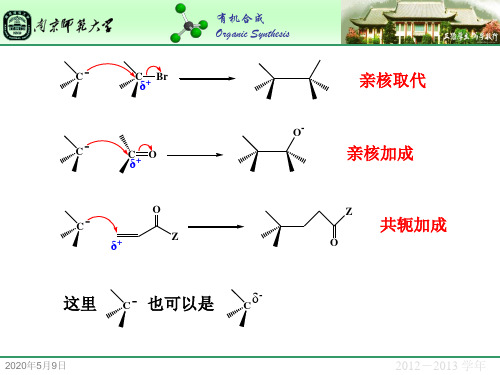
是一类活泼的亲核试剂,可以发生亲核取代、亲核加成、
共轭加成等反应。
2018年10月18日
2012-2013 学年
有机合成 Organic Synthesis
有机金属试剂的亲核反应活性取决于所连接的金属的活泼
性,它们的活性次序为:
R-K、 R-Na > R-Li > R-Mg > R-Zn > R-Cu
O H
+
C2H5MgBr
(1) 醚 (2) H2O
OH C2 H 5
O Ph
2018年10月18日
H
+
PhMgBr
(1) 醚 (2) H2O
OH Ph Ph
2012-2013 学年
有机合成 Organic Synthesis
b. 与 , 不饱和酮反应:
C2H5 O (1) C2H5MgBr (2) H2O O Ph (1) PhMgBr (2) H2O Ph Ph O OH Ph OH
① 有机钾、钠化合物是离子型的盐;
② 有机镁、锌、铜化合物中的金属-碳键是极性共价键,
它们可溶于乙醚、THF等有机溶剂中;
③ 有机锂化合物中的金属-碳键则介于以上两者之间。
2018年10月18日
2012-2013 学年
有机合成 Organic Synthesis
1.1.1 有机镁试剂
格利雅试剂 制备:
有机合成 Organic Synthesis
如果一论用哪一种格利雅试剂,都得到1,4-加成产物。
C2H5 O O Ph (1) PhMgBr (2) H2O (1) C2H5MgBr (2) H2O Ph
1,4-加成 100%
Ph Ph O
金属有机化学反应机理解析

金属有机化学反应机理解析金属有机化学是研究金属和有机化合物之间相互作用以及相关的反应机理的学科。
金属有机化合物广泛应用于有机合成、材料科学和均相催化等领域。
对金属有机化学反应机理的深入理解对于合成新型化合物、优化反应条件以及提高反应效率至关重要。
1. 金属有机化合物的形成机制金属有机化合物的形成机制主要包括基于配位键和基于氧化还原反应两种方式。
基于配位键的形成机制是指金属离子与有机配体形成化学键,产生稳定的配位化合物。
这种形成机制通常发生在溶液中,金属离子的电子轨道与配体的孤对电子进行共价键形成,使得金属离子与有机配体产生配位键。
这是很多有机金属反应中常见的机理,比如金属催化的有机合成反应。
另一种机制是基于氧化还原反应的形成机制。
在这种机制下,金属离子通过接受或者捐赠电子来与有机物发生反应。
这种反应机制在金属催化的氧化还原反应中经常出现,同时也涉及到电子转移和质子转移等步骤。
2. 金属有机化学反应的步骤金属有机化学反应的步骤通常包括配体的配位、金属间的电子转移、金属间的化学键形成等。
在金属有机化学反应中,有机配体通过与金属离子形成化学键来配位,产生配位化合物。
这一过程可以通过配体置换实验、质子核磁共振等方法来研究。
配体的选择和配体排列方式会对反应活性和选择性产生重要影响。
接下来,金属间的电子转移是一个关键步骤。
这一过程中金属离子可以通过电子交换和电子移动来完成。
电子转移也可以跨越不同金属中心,形成金属间的键。
最后,金属间的化学键形成是整个反应的最终步骤。
金属间的键可以通过配位变化和配体置换等反应来实现。
3. 金属有机化学反应的机理解析对于金属有机化学反应的机理解析通常使用实验和理论计算相结合的方法。
实验可以通过各种技术手段来研究反应的速率、产物和反应过渡态等。
核磁共振、质谱等技术可以用来确定反应物和产物的结构。
同时,通过温度控制、溶剂效应等条件变化可以研究反应的速率和选择性。
理论计算可以通过量子化学方法对反应进行模拟,在原子和分子尺度上研究反应机理。
高考化学中的无机化学重要反应式解析
高考化学中的无机化学重要反应式解析无机化学是化学的重要分支之一,它研究的是无机物质的性质、结构和反应。
在高考化学中,无机化学是一个非常重要的部分,它占据了整个化学考试的一大部分内容。
而无机化学的学习重点之一就是要掌握一些重要的反应式。
本文将针对高考化学中的无机化学重要反应式进行解析和探讨。
一、酸碱反应酸碱反应是无机化学中最基础且最重要的反应之一。
在高考化学中,我们常见的酸碱反应有酸与碱的中和反应,酸与金属的反应等。
1.酸与碱的中和反应酸与碱的中和反应是指酸和碱反应生成盐和水的反应。
其中最典型的就是硫酸与氢氧化钠的中和反应,反应式如下:H2SO4 + 2NaOH → Na2SO4 + 2H2O2.酸与金属的反应酸与金属的反应是指酸和金属反应生成盐和氢气的反应。
其中最常见的就是盐酸与锌的反应,反应式如下:2HCl + Zn → ZnCl2 + H2↑二、氧化还原反应氧化还原反应是无机化学中另一个非常重要的反应类型。
在高考化学中,我们需要重点掌握一些典型的氧化还原反应。
1.金属与非金属氧化物的反应金属与非金属氧化物的反应是指金属与非金属氧化物反应生成盐的反应。
其中最经典的就是铜与硫的反应,反应式如下:Cu + S → Cu2S2.金属与酸的反应金属与酸的反应是指金属与酸反应生成盐和氢气的反应。
这类反应中,盐的配离子和酸中的阳离子相同。
其中最常见的就是铁与盐酸的反应,反应式如下:Fe + 2HCl → FeCl2 + H2↑三、沉淀反应沉淀反应是指两种溶液混合后产生沉淀的反应。
在高考化学中,我们需要掌握一些常见的沉淀反应。
1.银盐的沉淀反应银盐的沉淀反应是指银盐溶液与氯化物溶液混合后产生沉淀的反应。
其中最典型的就是银盐与氯化钠的反应,反应式如下:AgNO3 + NaCl → AgCl↓ + NaNO32.硫酸钙的沉淀反应硫酸钙的沉淀反应是指硫酸钙溶液与硫酸溶液混合后产生沉淀的反应。
其中最常见的就是硫酸钙与硫酸铵的反应,反应式如下:CaCl2 + (NH4)2SO4 → CaSO4↓ + 2NH4Cl总结:无机化学中的重要反应式对于高考化学的学习至关重要,掌握这些反应式有助于我们理解无机化学的基本原理和反应机制。
有机化学中的金属有机化合物和金属催化反应原理
有机化学中的金属有机化合物和金属催化反应原理有机化学是研究碳基化合物的性质和反应的科学,而金属有机化合物和金属催化反应则是有机化学中的重要分支,应用广泛,影响深远。
一、金属有机化合物金属有机化合物指的是含有金属-碳键的化合物,其中金属通常是过渡金属。
这类化合物具有很多特殊的化学性质,例如可以参与金属催化反应,也可以作为有机合成中的试剂。
1. 有机锂化合物有机锂化合物是一类常用的金属有机化合物,由于锂的电负性较低,因此有机锂化合物具有非常强的亲电性。
常见的有机锂化合物包括丁基锂、叔丁基锂等。
有机锂化合物常用于有机合成中的羧酸酯化反应、卤代烃的取代反应等反应中。
2. 有机铜化合物有机铜化合物与有机锂化合物一样具有很强的亲电性,但由于铜的电负性较锂高,因此有机铜化合物通常比有机锂化合物更加稳定。
常见的有机铜化合物包括第一类和第二类有机铜试剂。
有机铜化合物在有机合成中主要用于烯丙基化反应、自由基反应等反应中。
3. 有机铁化合物有机铁化合物是一类特殊的金属有机化合物,其中铁通常是三价的。
常见的有机铁化合物包括费希尔试剂和格氏试剂等。
有机铁化合物在有机合成中常用于羰基化反应、烯烃羰基化反应等反应中。
二、金属催化反应金属催化反应是指在金属催化剂的作用下进行的有机合成反应,通过金属催化剂的引发、传递或者接受中间体上的电子或质子,加速有机物之间的化学反应,并且能够在较温和的条件下实现。
1. 氧化还原反应氧化还原反应是有机合成中常见的反应,而金属催化剂常用于氧化还原反应中。
例如钯、铑、钌等金属常用于氧化还原反应中,例如Suzuki反应、Heck反应等。
金属催化氧化还原反应具有高效、温和、反应通用等优点。
2. 烯丙基化反应烯丙基化反应是有机合成中重要的反应,它广泛用于生物活性物质及金属有机化合物的合成中。
在烯丙基化反应中,常用钯、镍等金属作为催化剂,通过催化剂引发的活化,将烯丙基试剂与底物反应,生成烯丙基化产物。
3. 环合成反应环合成反应是指将一条链状分子合成成为一个环状分子的过程。
亲核水解 亲电水解
亲核水解亲电水解
亲核水解是指通过亲核试剂对溶液中的化合物进行水解反应。
亲核试剂是指能够与碳中的亲电中心结合的碱性或亲核性分子,比如碱金属和碱土金属离子、羰基化合物、亚硫酸盐、胺等。
亲核试剂与化合物之间发生亲核加成反应,将化合物中的某个或多个键断裂,生成新的化合物。
亲电水解是指通过亲电试剂对溶液中的化合物进行水解反应。
亲电试剂是指具有亲电性的分子,能够从其他分子中夺取电子或电子密度较高的区域,比如阳离子、卤素、羧基、酸等。
亲电试剂与化合物之间发生亲电解离反应,将化合物中的某个或多个键断裂,生成新的化合物。
总的来说,亲核水解和亲电水解都是通过不同的试剂对化合物进行水解反应,但在反应机理和反应条件上有所不同。
河北省考研化学复习资料有机化学与无机化学重点反应机理解析
河北省考研化学复习资料有机化学与无机化学重点反应机理解析在河北省考研化学复习中,有机化学和无机化学是两个非常重要的学科领域。
掌握有机化学和无机化学的重点反应机理是化学考研的核心内容之一。
本文将从有机化学和无机化学的角度,对一些重点反应机理进行解析。
一、有机化学重点反应机理解析1. 反应类型分类有机化学中常见的反应类型包括取代反应、消除反应、加成反应、重排反应等。
其中取代反应是有机化学中最为常见的一类反应,它包括亲核取代反应和电子取代反应。
亲核取代反应是指亲核试剂攻击电子不足的位点,将其取代,同时生成新的共价键;电子取代反应是指电子不足的试剂攻击亲电子的位点,将其取代,同样生成新的共价键。
2. 重要反应机理在有机化学中,有一些反应机理是考研中不容忽视的重点内容。
例如,氢化反应是有机化学中重要的加成反应,它可以将烯烃或炔烃转化为烷烃。
氢化反应主要有催化氢化反应和不对称氢化反应两种类型,其中催化氢化反应常常需要使用过渡金属催化剂,而不对称氢化反应可以得到具有手性的产物。
3. 共轭体系与色谱分析共轭体系是有机化学中的重要概念之一,它指的是含有相连的多个共轭键的化合物,可以通过共轭π电子的共享,增加分子的稳定性,影响化合物的光学性质等。
色谱分析是化学分析中常用的一种方法,其中气相色谱和液相色谱是两种常见的色谱技术。
其中气相色谱主要基于化合物在固定相和流动相之间的分配系数来实现分离,而液相色谱则可通过溶剂在固定相上的吸附和洗脱来进行分离。
二、无机化学重点反应机理解析1. 金属氧化还原反应无机化学中最为重要的反应之一是金属氧化还原反应,其本质是金属离子在反应过程中失去或得到电子。
金属的氧化状态通常以“+”号表示,而还原状态则以“-”号表示。
金属氧化还原反应分为红ox反应(有机氧化还原反应)和电ox反应(氧化还原反应)两类,红ox反应是指有机物被氧化代谢得到一种较稳定的原始物质,而电ox反应是指金属与非金属之间的电的相互作用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
关键字 金属有机 配体 亲核 计量
在插入反应中, 有一类反应涉及亲核试剂直接进攻不饱和配位体而不需要亲核试剂 事先与金属配位。已经发现一系列不同的亲核试剂与不饱和配位体的这类反应。这类反 应对计量和催化反应都重要,如它们涉及到由η3-烯丙基和烯烃络合物的有机合成反应 以及 Wacker-Schmidt 反应,水-气平衡反应等催化过程。这些分子间反应不易同分子内 “迁移插入” (后者,亲核试剂必先配位)反应相区分。通过对络合物的配位饱和状态, 取代的难易以及产物立体化学等因素进行分析对判定是分子间还是分子内反应十分有 用。 从下述例子中将会看到有三个因素有利于不饱和配位体直接发生亲核反应, (1)亲 核试剂的活性; (2)起始金属络合物的配位饱和性或这一络合物接纳另一个配位体的惰 性; (3)金属上带有正电荷。多数不饱和配位体都能发生这类反应。常见的不饱和配位 体有一氧化碳、异腈、腈、亚硝基、烯、螯合双烯、π-芳烃、η3-烯丙基等等。多数情 况下,整个反应不发生氧化态的改变,但在η3-烯丙基例子中也会遇到例外。
图 10 反应的机理被认为是亲核的 N-氧化物从外部进攻配位的 CO,遂即假定的中间体分 解,放出 CO2 或第二胺或第三胺[11]。
O M CO + O NR3 M C O NH2R3 M+CO2+R3N
图 11
2.对配位酰基的进攻 许多中性的和负离子酰基络合物似乎对亲核试剂进攻不活泼。但是酰基化合物的氧 化分解能导致酰基容易水解或溶剂解。这在前面氧化诱导烷基迁移反应中作为一种副反 应已经遇到过。在多数情况下假设的中间体酰基阳离子络合对亲核进攻非常敏感,其酰 基的活性宛如活化的酯或酰卤。迄今为止,对酰基络合物的氧化分解进行直接研究的例 子很少,而且酰基阳离子络合物的高度活性在有机合成方面也还没有什么用途,但这可 能是一个很有希望的研究方向。
O M C O +* OH M C OH M H
OH
M + H2O
图7 烷氧离子能生成类似的络合物。如羰基、亚硝基铁(0)阳离子络合物与甲氧离子 反应生成稳定的过渡金属羧酸酯。这里可以看到 CO 被优先进攻,而线型亚硝基配体则 没有发生反应。
PPh3 OC Fe+ PPh3 NO CO O
+ OMe
4.对配位炔烃的亲核进攻 铂(Ⅱ)炔阳离子络合物能加合一系列亲核试剂。Chisholm 和 Clark[12]深入研究了 这些反应,发现还有复杂的后续反应,特别对于端炔络合物。甲醇和原位产生的配位二 取代炔反应得反-σ-乙烯醚络合物:
L2Pt L Fe H 3C
+
R C C +CH4 OCH3
Cl RC L CR AgPF6 CH3OH
1.对 CO 亲核配体的进攻 直接进攻 CO 而不与金属配位的亲核试剂也不少,其中包括格氏试剂、有机锂、氢
第1页
无机化学Ⅱ——金属有机化合物的亲核反应
化物、氢氧化物、胺、N-氧化胺和叠氮离子。从这些分子间进攻所得加成物可以是一些 稳定络合物(例如酰基物)也可以发生分解(如来自 N-氧化胺的衍生物)得到新络合 物。顺势配合物可通过这些加成物的形成而被活化。 1.1 格氏试剂、有机锂和氢化物 烷基和芳基锂是非常强的亲核试剂,它可直接与配位饱和的五羰基铁反应,获得酰 基铁负离子锂:
无机化学Ⅱ——金属有机化合物的亲核反应
金属有机化合物对配体的亲核加成反应
南京大学化学化工学院 031131122 宋晓男
摘要 插入反应是指一种饱和配体同一种不饱和配体相结合形成新配体的过程,它包括分 子内迁移插入和分子间亲核加成。本文对对于化学计量、催化都很重要的亲核加成反应 进行了总结,列举了已发现的重要反应。
+1
5
+
CO
图 18
8.对卡宾和卡拜配位体的亲核进攻 许多基团具有迁移至配位卡宾的倾向性。这种倾向性可导致分子间的配位卡宾的进 攻。直接向配位饱和的带正电荷卡宾配位物的亲核进攻是很容易的。碳负粒子、胺、膦、 硫醇与卡宾的许多反应能够都属于这一范畴。若干这类反应如下式所示,是可逆的。
Me CH2 +N M H2 C N
O
W(CO)6+NaN2
慢
(OC)5W
CN3 Na+
-N2 快
(OC)5W-CONa+
图9 1.5 N-氧化胺 在温和条件下,除去 CO 的一个有趣的有用的方法为下列方程式所示的涉及三甲胺 -N-氧化物的反应[10]:
第4页
无机化学Ⅱ——金属有机化合物的亲核反应
+Fe(CO)5
Me 3NO Me2CO Fe OC CO CO
3.对配位烯烃的亲核进攻 简单的单烯络合物看起来容易遭受强亲核进攻,但这类反应研究得还不多。以羰基 铁烯烃络合物所进行的下述反应为例,当有活化基团存在时,反应是区域选择性,亲核 试剂像 Michael 加成那样进入β-碳。在另外情况下,如钯-烯络合物,进攻部位选择在 位阻较高的烯碳原子上。
H 2C
C Fe(CO)4
+ Na+[CH(CO2Et)2]Pd+ Cl Py 图 13 Cl
Pd+ Py
反应所具有的分子间性质可从产物的立体化学得到证明。丙二酸酯基是外式的 (exo) ,说明碳和钯对配位烯键的加成是反式的。如果是分子内的迁移插入则应有内式 或顺式加成产物。 这一反应的另一特点为亲核试剂直接对烯的进攻, 即使四配位钯 (Ⅱ) 络合物是配位不饱和的。d8 钯(Ⅱ)本身不倾向于五配位以及立体障碍可以解释反应的 分子间性质。中的螯合双烯是非常稳定的,它有阻止烯被置换的倾向。如果是简单的单 烯钯络合物,则烯烃置换反应可成为一种严重的副反应。
第2页
无机化学Ⅱ——金属有机化合物的亲核反应
或其他亲核试剂如氢氧根都可以接受进攻的羰基附近的配位体而发生立体专属性活化。 1.3 水、氢氧化物和烷氧化物 羰基金属可以与水或氢氧根反应。事实上在“Reppe”型催化和水-气平衡反应中就 包含了这样一步反应。 有时可分离出稳定的过渡金属羧酸盐来, 有时这种产物不可分离, 但它们的存在可通过同位素交换推知, 也可从 Fe(CO)5 与 NaOH 反应时有 CO2 生成而证 实。 对不饱和配位体的这种直接亲核进攻可被起始络合物上所带的正电荷所促进。这种 情况可用 H182O 与饱和的六羰基铼、六羰基钨发生同位素 18O 交换的相对速度来说明:
O M C O +H2O* OH O*H MC O*
-H+ +H
+
M-
C
+H+ -H+
M
C
O* +H2O
(O*=18O)
图5 正如所看到的那样,较强的亲和试剂能同中性羰基物反应。氢氧根能进攻饱和的羰 基金属,这是一种广泛而重要的反应。如下式所示,中间体过渡金属羧酸盐失去 CO2 而得到负离子金属化合物:
O Na2+ O -CO2 Na2+ Fe(CO)4 H2O NaOH+Na+ HFe(CO)5 C Fe(CO)4
Fe(CO)5+2NaOH
-H2O
图6
第3页
无机化学Ⅱ——金属有机化合物的亲核反应
Brown 建议失羧反应由于出现一个空配位而得以协助。 前已述及消除 CO2 是均相催 化水-气平衡反应中的关键步骤。在许多场合负离子氢化物的酸性已经很强,足以被过 量的碱脱去质子。整个反应过程导致了对金属的二电子还原。因此 CO2 和碱的水溶液经 常作为金属络合物的还原剂。关于金属 2 电子还原过程一般表示如下:
6.对η3-烯丙基的进攻 对η3-烯丙基末段碳原子的背面亲核进攻可形成相应的π-烯络合物,同时金属也发 生了二电子还原。 络合物中的形式正电荷可促进这种亲核反应。 当进攻试剂是亲核的碳, 则形成 C-C 键时烯丙基会有构型的转化。 下面以具有四种不饱和配位体的钼阳离子络合物为例。反应中,他的π-烯丙基优先被 进攻而得烯配位物,钼也从 Mo(Ⅱ)还原至 Mo(0) :
R C CO RLi+Fe(CO)5 CO CO FeCO Li+ O
图1 这个发生在配位的 CO 上的反应是 Fischer 所发现的[1], 并已成为合成酰基负离子络 合物的一种简便方法。该负离子常以[(Ph3P)2N]+盐而析离纯化。反应是在 Fe(CO)5 能与 游离的 13CO 发生交换的温度下进行的(后者为解离过程,温度为 130℃左右) 。因此这 个反应可以认为是对配体 CO 的直接亲核进攻,当然也可以经由电子转移途径。 格氏试剂也能同羰基金属形成酰基衍生物。强的亲核负离子和羰基物的反应与此类似。 Casey[2]和 Gladysz[3]同意将这个方法用于制备动力学稳定的甲酰基络合物,如:
Re+(CO)6+H2O* W(CO)6+H2O* Re(CO)n(CO*)6-n 无反应
图4 正离子的六羰基来在 25℃和含 18O 的水发生交换,它的半衰期是 30min,二等电子 的中型六羰基钨则 75h 尚未见有交换的痕迹[5][6]。人们认为这种交换是通过水进攻配位 一氧化碳的可逆过程,其一般式为:
R
图 14 产物的反式立体化学说明亲核进攻是分子间的,并且不涉及甲醇与金属事先发生络 合。
5.对配位芳烃的进攻
第6页
无机化学Ⅱ——金属有机化合物的亲核反应
芳烃阳离子络合物特别容易发生分子间的亲核加成。如:
OMe H
MeOMo+ OC CO CO OC CO Mo+ CO
图 15 这种对金属阳离子络合物中的不饱和配体发生的亲核加成是很普遍的。 Davis,Green 和 Mingos 对这类反应进行了评述[13],并提出了预期亲核进攻最有利位置的一些简单规 则。
图 19 Gladusz 曾制得了一个铼卡宾络阳离子可与多种亲核试剂反应[14]:
