第一章金属的晶体结构1
第一章金属的晶体结构 本章重点与难点: ①金属键; ②最常见

第一章金属的晶体结构本章重点与难点:①金属键;②最常见的晶体结构:面心立方结构(fcc)、体心立方结构(bcc)、密排六方结构(hcp);晶向指数和晶面指数;③晶体中存在的缺陷:点缺陷、面缺陷、线缺陷。
内容提要:固体物质的原子是由键结合在一起。
这些键提供了固体的强度和有关电和热的性质。
由于原子间的结合键不同,我们经常将材料分为金属、聚合物和陶瓷三类。
金属的原子之间时依靠金属键结合在一起的。
在结晶固体中,材料的许多性能都与其内部原子排列有关,可将晶体分为7种晶系,14种布拉菲点阵。
金属中最常见的晶体结构有面心立方结构(fcc)、体心立方结构(bcc)、密排六方结构(hcp)结构。
本章还介绍了晶向、晶面的概念及其表示方法(指数),因为这些指数被用来建立晶体结构和材料性质及行为间的关系。
实际的晶体结构中存在着一些缺陷,根据几何形态特征,分为点缺陷、面缺陷、线缺陷。
基本要求:1.建立原子结构的特征,了解影响原子大小的各种因素。
3.建立单位晶胞的概念,以便用来想像原子的排列;在不同晶向和镜面上所存在的长程规则性;在一维、二维和三维空间的堆积密度。
4.熟悉常见晶体中原子的规则排列形式,特别是bcc,fcc以及hcp。
我们看到的面心立方结构,除fcc金属结构外,还有NaCl结构和金刚石立方体结构。
5. 掌握晶向、晶面指数的标定方法。
一般由原点至离原点最近一个结点(u,v,w)的连线来定其指数。
如此放像机定为[u,v,w]。
u,v,w之值必须使互质。
晶面指数微晶面和三轴相交的3个截距系数的倒数,约掉分数和公因数之后所得到的最小整数值。
若给出具体的晶向、镜面时会标注“指数”时,会在三维空间图上画出其位置。
6.认识晶体缺陷的基本类型、基本特征、基本性质。
注意位错线与柏氏矢量,位错线移动方向、晶体滑移方向与外加切应力方向之间的关系。
7 了解位错的应力场和应变能,位错的增殖、塞积与交割。
第一节金属1 金属原子的结构特点金属原子的结构特点是外层电子少,容易失去。
第一章-金属的晶体结构(共118张PPT)可修改全文

B面:
(1) 该面与z轴平行,因此x=1,y=2, z=∞; (2) 1/x=1,1/y=1/2,1/z=0; (3) 最小整数化1/x=2,1/y=1,1/z=0; (4) 〔2 1 0〕
C面:
(1) 该面过原点,必须沿y轴进行移动,因此x= ∞ ,y=-1,z=∞ (2) 1/x=0,1/y=-1,1/z=0; (3) 不需最小整数化;(4) 〔0 1 0〕
晶胞在三维空间的重复构成点阵
〔4〕晶格常数
在晶胞中建立三维坐标体系, 描述出晶胞的形状与大小
晶胞参数- 晶格常数:a、b、c 棱间夹角:α、β、γ
2 晶系与布拉菲点阵
依据点阵参数 的不同特点划分为七种晶系
(1) 三斜晶系
α≠β≠γ≠90° a≠ b≠ c
复杂单胞 底心单斜
(2) 单斜晶系
α=γ=90°≠β a≠ b≠ c
3 原子半径: r 2 a
4 配位数= 12
4
5 致密度= nv/V=(4×3πr3/4)/a3=0.74
γ-Fe(912~1394℃)、Cu、Ni、Al、Ag 等
——塑性较高
面心立方晶胞中原子半径与晶 格常数的关系
a
r 2a 4
(三)密排六方结构〔 h.c.p〕 〔 了解〕
金属:Zn、Mg、Be、α-Ti、α-Co等
具有光泽:吸收了能量从被激发态回到基态时所 产生的幅射;
良好的塑性:在固态金属中,电子云好似是 一种流动的万能胶,把所有的正离子都结合 在一起,所以金属键并不挑选结合对象,也 无方向性。当一块金属的两局部发生相对位 移时,金属正离子始终“浸泡〞在电子云中, 因而仍保持着金属键结合。这样金属便能经 受较大的变形而不断裂。
第一章金属的晶体结构作业答案

第⼀章⾦属的晶体结构作业答案第⼀章⾦属的晶体结构1、试⽤⾦属键的结合⽅式,解释⾦属具有良好的导电性、正的电阻温度系数、导热性、塑性和⾦属光泽等基本特性.答:(1)导电性:在外电场的作⽤下,⾃由电⼦沿电场⽅向作定向运动。
(2)正的电阻温度系数:随着温度升⾼,正离⼦振动的振幅要加⼤,对⾃由电⼦通过的阻碍作⽤也加⼤,即⾦属的电阻是随温度的升⾼⽽增加的。
(3)导热性:⾃由电⼦的运动和正离⼦的振动可以传递热能。
(4) 延展性:⾦属键没有饱和性和⽅向性,经变形不断裂。
(5)⾦属光泽:⾃由电⼦易吸收可见光能量,被激发到较⾼能量级,当跳回到原位时辐射所吸收能量,从⽽使⾦属不透明具有⾦属光泽。
2、填空:1)⾦属常见的晶格类型是⾯⼼⽴⽅、体⼼⽴⽅、密排六⽅。
2)⾦属具有良好的导电性、导热性、塑性和⾦属光泽主要是因为⾦属原⼦具有⾦属键的结合⽅式。
3)物质的原⼦间结合键主要包括⾦属键、离⼦键和共价键三种。
4)⼤部分陶瓷材料的结合键为共价键。
5)⾼分⼦材料的结合键是范德⽡尔键。
6)在⽴⽅晶系中,某晶⾯在x轴上的截距为2,在y轴上的截距为1/2;与z轴平⾏,则该晶⾯指数为(( 140 )).7)在⽴⽅晶格中,各点坐标为:A (1,0,1),B (0,1,1),C (1,1,1/2),D(1/2,1,1/2),那么AB晶向指数为(ī10),OC晶向指数为(221),OD晶向指数为(121)。
8)铜是(⾯⼼)结构的⾦属,它的最密排⾯是(111 )。
9) α-Fe、γ-Fe、Al、Cu、Ni、Cr、V、Mg、Zn中属于体⼼⽴⽅晶格的有(α-Fe 、 Cr、V ),属于⾯⼼⽴⽅晶格的有(γ-Fe、Al、Cu、Ni ),属于密排六⽅晶格的有( Mg、Zn )。
3、判断1)正的电阻温度系数就是指电阻随温度的升⾼⽽增⼤。
(√)2)⾦属具有美丽的⾦属光泽,⽽⾮⾦属则⽆此光泽,这是⾦属与⾮⾦属的根本区别。
(×)3) 晶体中原⼦偏离平衡位置,就会使晶体的能量升⾼,因此能增加晶体的强度。
第一章 金属晶体结构

准晶体的结构像
晶体的原子像
2007-04-17 6
机械工程材料精品课程 机械工程材料精品课程
第一节 金属的晶体结构
三.晶体的描述
1.晶格与晶胞
阵点:将晶体的实际质点(原子、分子)抽象为纯粹的几何点 晶格:描述原子排列方式的几何格架——空间点阵 晶胞:晶格中具有代表性的最小的几何单元。 ——晶格则由晶胞重复堆砌而成。
2007-04-17 14
机械工程材料精品课程 机械工程材料精品课程
第一节 金属的晶体结构
实例
AB
2007-04-17
15
机械工程材料精品课程 机械工程材料精品课程
第一节 金属的晶体结构
想 想 G C O B E x
2007-04-17 16
晶向指数确定?
z H F A
求晶向OA、OB、OC、 EF、EG、EH的晶向指
晶体结构
晶格
晶胞
2007-04-17 7
机械工程材料精品课程 机械工程材料精品课程
第一节 金属的晶体结构
2.晶格特征参数 晶格常数:表示晶胞几何形状、大小的参数。如立方晶胞: 三棱边a、b、c; 三棱边夹角α、β、γ 晶胞所占原子数: 指一个晶胞所占的原子总数 配位数: 指晶体结构中与任何一个原子最近邻且等距离的原子数目 致密度: 晶胞中原子所占体积与晶胞体积之比 配位数和致密度可衡量晶胞中原子排列的紧密程度
金属晶粒内的结构示意图
2007-04-17 26
纯铁的显微组织
奥氏体不锈钢的显微组织
铸铁的显微组织
第二节 实际金属的微观结构
二. 晶体缺陷 1.晶体缺陷的概念 点缺陷 空位、间隙原子、异类原子
《金属学与热处理》崔忠圻(第二版)课后答案完整版
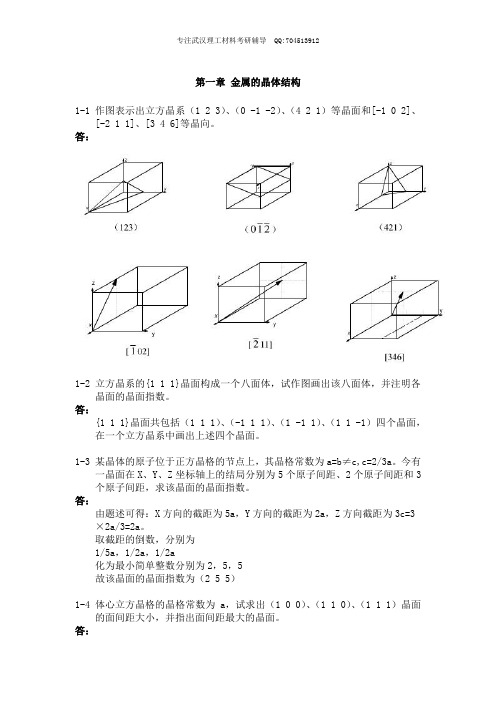
第一章金属的晶体结构1-1 作图表示出立方晶系(1 2 3)、(0 -1 -2)、(4 2 1)等晶面和[-1 0 2]、[-2 1 1]、[3 4 6]等晶向。
答:1-2 立方晶系的{1 1 1}晶面构成一个八面体,试作图画出该八面体,并注明各晶面的晶面指数。
答:{1 1 1}晶面共包括(1 1 1)、(-1 1 1)、(1 -1 1)、(1 1 -1)四个晶面,在一个立方晶系中画出上述四个晶面。
1-3 某晶体的原子位于正方晶格的节点上,其晶格常数为a=b≠c,c=2/3a。
今有一晶面在X、Y、Z坐标轴上的结局分别为5个原子间距、2个原子间距和3个原子间距,求该晶面的晶面指数。
答:由题述可得:X方向的截距为5a,Y方向的截距为2a,Z方向截距为3c=3×2a/3=2a。
取截距的倒数,分别为1/5a,1/2a,1/2a化为最小简单整数分别为2,5,5故该晶面的晶面指数为(2 5 5)1-4 体心立方晶格的晶格常数为a,试求出(1 0 0)、(1 1 0)、(1 1 1)晶面的面间距大小,并指出面间距最大的晶面。
答:H==a/2(1 0 0)==√2a/2H(1 1 0)==√3a/6H(1 1 1)面间距最大的晶面为(1 1 0)1-5 面心立方晶格的晶格常数为a,试求出(1 0 0)、(1 1 0)、(1 1 1)晶面的面间距大小,并指出面间距最大的晶面。
答:==a/2H(1 0 0)H==√2a/4(1 1 0)==√3a/3H(1 1 1)面间距最大的晶面为(1 1 1)注意:体心立方晶格和面心立方晶格晶面间距的计算方法是:1、体心立方晶格晶面间距:当指数和为奇数是H=,当指数和为偶数时H=2、面心立方晶格晶面间距:当指数不全为奇数是H=,当指数全为奇数是H=。
1-6 试从面心立方晶格中绘出体心正方晶胞,并求出它的晶格常数。
答:1-7 证明理想密排六方晶胞中的轴比c/a=1.633。
金属学与热处理第一章 金属的晶体结构

晶体结构特征:
点阵参数: a1=a2=a3=a,
α 1=α 2=α 3=1200
平面轴X1、X2、X3和Z轴的夹角=90 ——四轴坐标系
O
Z轴的单位长度=c,用a、c两个量来度量
点阵参数:α=β=90º, γ=120º; a1=a2=a3≠c, 理想状态:c/a=1.633
第一章 金属的晶体结构
本章教学目的
建立金属晶体结构的理想模型 揭示金属的实际晶体结构
§1-1 金属
一. 金属的特性和概念
1. 特性
金属通常表现出的特性:良好的导电性、导 热性、塑性、金属光泽、不透明。
2. 概念
(1) 传统意义上的概念。 (2) 严格意义上的概念:具有正的电阻温度系 数的物质,即电阻随温度的升高而增加的物质。
晶向─晶体点阵中,由阵点组成的任一直线,代 表晶体空间内的一个方向,称为晶向。 晶面─晶体点阵中,由阵点所组成的任一平面, 代表晶体的原子平面,称为晶面。
1.晶向指数的标定
晶向指数─用数字符号定量地表示晶向,这种数字符 号称为晶向指数。 以晶胞为基础建立三维坐标体系: z C′ O′ A′ c
γ O β α
晶体有各向异性, 非晶体则各向同性。
各向异性:不同方向上的性能有差异。
3.晶体与非晶体的相互转化性
玻璃
长时间保温
金属 极快速凝固
“晶态玻璃”
“金属玻璃”
非晶新材料的发展:光、电、磁、耐蚀 性、高强度等方面的高性能等。
二.晶体学简介
1.晶体结构模型的建立
(1) 假设:原子为固定不动的刚性小球,每个原子 具有相同的环境。
O′
z B′
C′
第一章金属的晶体结构

图2-6密排六方晶胞
第三节 晶体学概念
• • • • • • • 1.3.1 晶胞中的原子数 体心立方: 面心立方: 密排六方: 1.3.2 原子半径 1.3.3 配位数和致密度 配位数:指晶体结构中与任一个原子最近邻且等距离的原 子数目。 • 体心立方晶体8个,面心立方12个,密排六方12个,所以 面心立方和密排六方致密度高 • 致密度分别为0.68、0.74、0.74
图2-5
面心立方晶胞
• (3)密排六方晶胞(close packed lattice hexagonal):密排六方晶体的晶胞如图1.6所示。 • 它是由六个呈长方形的侧面和两个呈正六边形的 底面所组成的一个六方柱体。因此,需要用两个 晶格常数表示,一个是正六边形的边长a,另—个 是柱体的高c。在密排六方晶胞的每个角上和上、 下底面的小心都有一个原子,另外在中间还有三 个原子。因此,密排六方晶格的晶胞中所含的原 子数为:6×1/6×2+2×1/2+3=6个。 • 具有密排六方晶体结构的金属有Mg、Zn、Be、 Cd、α-Ti、α-Co等。
A、B组元组成的固溶体也可表示为A(B), 其中A为溶剂, B为 溶质。例如铜锌合金中锌溶入铜中形成的固溶体一般用α表 示, 亦可表示为Cu(Zn)。
• 固溶体特性:1固溶体成分可以在一定范围内变化, 在相图上表现为一个区域。2固溶体必须保持溶剂 组元的点阵类型。3纯金属结构有哪些类型,固溶 体也应有哪些类型,即固溶体本身没有独立的点 阵类型。4组元的原子尺寸不同会引起的点阵畸变, 原子尺寸相差越大,引起的畸变也越大。
• 1.3.4晶体中原子的排列方式(略) • 1.3.5 晶体结构中的间隙 • 三种典型晶体结构的四面体间隙、八面体间 隙(图1-13,1-14,1-15) • 间隙半径与原子半径之比rB/rA=?(见表1-2) • 可见面心立方结构八面体间隙比体心立方结 构四面体间隙还大,因此溶碳量大的分类 • 1.按溶剂分类 • (1)一次固溶体:以纯金属组元作为溶剂的 固溶体称为一次固溶体,也叫边际固溶体。 • (2)二次固溶体:以化合物为溶剂的固溶体 称二次固溶体,或叫中间固溶体。如电子 化合物、间隙相。 • 有的化合物和化合物之间,也可以相互溶 解而组成固溶体,如Fe3C和Mn3C,TiC和 TiN等。
(完整版)第一章金属的晶体结构

第一章金属的晶体结构1-1. 作图表示立方晶系中的(123),(012),(421)晶面和[102],[211],[346]晶向。
附图1-1 有关晶面及晶向1-2、立方晶系的{111}晶面构成一个八面体,试作图画出该八面体,并注明各晶面的晶面指数。
{111}=(111)+(111)+(111)+(111)(111)与(111)两个晶面指数的数字与顺序完全相同而符号相反,这两个晶面相互平行,相当于用-1乘某一晶面指数中的各个数字。
xy z1-3 (题目见教材)解:x方向截距为5a,y方向截距为2a,z方向截距为3c=3 2a/3=2a。
取截距的倒数,分别为1/5a,1/2a,1/2a化为最小简单整数分别为2,5,5 故该晶面的晶面指数为(2 5 5)1-4 (题目见课件)解:(100)面间距为a/2;(110)面间距为2a/2;(111)面间距为3a/3。
三个晶面中面间距最大的晶面为(110)。
1-5 (题目见课件)解:方法同1-4题1-7 证明理想密排六方晶胞中的轴比c/a=1.633。
证明:理想密排六方晶格配位数为12,即晶胞上底面中心原子与其下面的3个位于晶胞内的原子相切,构成正四面体,如图所示。
则OD=2c,AB=BC=CA=AD=BD=CD=a 因∆ABC 是等边三角形,所以有OC=32CE 因(BC)2=(CE)2+(BE)2则CE=23a ,OC=32×23a =33a又(CD)2=(OC)2+(21c )2,即(CD)2=(33a )2+(21c )2=(a )2因此,ac=38≈1.6331-8解:面心立方八面体间隙半径 r=a/2-2a/4=0.146a , 面心立方原子半径R=2a/4,则a=4R/2,代入上试有CBADEOr=0.146⨯4R/2=0.414R。
(其他的证明类似)1-9 a)设有一刚球模型,球的直径不变,当由面心立方晶格转变为体心立方晶格时,试计算其体积的膨胀?b)经X射线测定,在912℃时γ-Fe的晶格常数为0.3633nm,α-Fe的晶格常数为0.2892nm,当由γ-Fe转变为α-Fe时,试求其体积膨胀? c)分析实际体积膨胀小于理论体积膨胀的原因?解:a)令面心立方晶格与体心立方晶格的体积及晶格常数分别为V面、V体与a面、a体,刚球半径为r,由晶体结构可知,对于面心晶胞有4r=2a面,a面=22r,V面= (a面)3=(22r)3对于体心晶胞有4r=3a体,a体=334r,V体= (a体)3=(334r)3则由面心立方晶胞转变为体心立方晶胞的体积膨胀∆V为∆V=2×V体-V面=2.01r3b)按晶格常数计算实际转变体积膨胀∆V实,有∆V实=2×V体-V面=2×(0.2892)3-(0.3633)3=0.000425 nm3c)实际体积膨胀小于理论体积膨胀的原因在于由γ-Fe转变为α-Fe时,Fe 原子半径发生了变化,原子半径减小了。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
性能(用途)
成分
工艺
组织结构 四面体模型 组织结构不同,性能不同;化学成分不同,性能不同; 加工制造工艺不同,性能不同;成分相同、工艺不同,性能不同
金属和合金在固态下通常为晶体。
1
§1-1 金属 §1-2 金属的晶体结构 §1-3 实际金属的晶体结构
2
§1-1 金属
金属? 具有正的电阻温度系数的物质。 非金属?
α- Co, Cd
密排结构(close-packed crystal structure): fcc 和 hcp
31
课堂作业: 求密排六方结构的致密度。
K
=
nv
=
n
4
3
R3
VV
问题:为什么面心立方和密排立方的配位数和致 密度相同,具有相同的紧密程度,却具有不同的 晶体结构? 原子的堆垛方式
32
a ≠b ≠ c,α≠β≠γ≠90° a ≠ b ≠c,α=γ=90°≠ β a ≠ b ≠c,α=β=γ=90° a = b ≠c,α=β=90°,γ= 120° a = b =c, α=β=γ ≠ 90° a = b ≠c,α=β=γ=90° a = b =c, α=β=γ=90°
15
1、三斜晶系
离子键:一失一得,静电作用(氯化钠)
共价键:相邻原子共用它们的外部价电子,形成稳定的满壳层 (金刚石)
6
三、 结合力与结合能
问题:金属原子为什么排列规则, 并趋于紧密排列?
固态金属中两个原子之间的作用力:
1)正离子与电子的吸引力 2)正离子与正离子、电子与电子的排斥力 “结合力”是吸引力和排斥力的代数和
a b c, 90
c
b
a
简单三斜结构
16
2.单斜晶系
a b c, = = 90
c
a
c
a
b
b
简单单斜结构、底心单斜结构
17
3.正交晶系
a b c, = = = 90
c
c
a b
a b
简单正交结构、底心正交结构、体心正交结构、 面心正交结构
18
4.六方晶系
a = b c, = = 90, = 120
10
B. 理想晶体的晶体学抽象
晶格:描述晶体中原子排列规律的空间格子(空间点阵) 晶胞:完全反映晶体特征的最小几何单元 阵点:代表构成晶体的原子的几何点
11
12
晶胞的表示法
晶格常数或点阵常数 lattice constant
三个棱边的长度a,b,c
轴间夹角α,β,γ表示。
z
c
a
x
结构 原子半径
原子 数
配位数 致密度
常见金属
BCC
r=
3 4 a0
2
8 0.68 α-Fe,, W, Mo,
Nb, V, Cr
FCC
r=
2 4
a0
4
r = a0
HCP
2
6
c0 1.633a0
12 0.74
γ-Fe, Cu, Al, Ag, Pb, Ni
Mg, Zn, Be, α- Ti
12 0.74
结合能:? 吸引能和排斥能的代数和
7
d0 平衡间距或位置 d>d0时,相互吸引 d<d0时,相互排斥 d=d0时,结合力为零
任何对d0偏离,都使势能升高
形成原子团比单个原子能量低 原子周围最近邻的原子数越多 结合能越低 能量越低,状态越稳定
排 斥 力 +F
结合力
o
d0
吸A B
引
力
-F
排斥力
dc
理论抗拉强度 原子间距d
k
每个原子有8个最近邻原 子,配位数为8。
26
(2) 面心立方(fcc ) γ-Fe、 Cu、 Ni 、Al 、Ag等约20种
刚球模型 晶格常数 a=b=c;α=β=γ=90°
质点模型
晶胞原子数模型
N=Ni
Nf 2
Nc 8
晶胞中含有4个原子。
27
原子密排列面是{111}, 密排方向是〈110〉,在 密排方向上原子相切: 原子半径 致密度:
区别
(a)是否具有周期性、对称性 (b)是否长程有序 (c)是否有确定的熔点? (d)是否各向异性
9
二、晶体结构与空间点阵
晶体结构: 晶体中原子(离子、分子)在三维空间有规律的具体排列方式。
A 理想晶体——实际晶体的理想化
三维空间无限延续,无边界 严格按周期性规则排列,是完整的、无缺陷。 原子在其平衡位置静止不动
次外层未填满、最外层先填充电子
易失去最外层电子和次外层电子
过渡族金属的原子间结合力强, 熔点高、强度高
次外层电子也参与结合
5
二、 金属键
金属中自由电子与金属正离子之间构成的键合方式 公有化的自由电子与正离子之间的结合方式
金属的特性:
导电?自由电子沿电场方向 导运热动?自由电子运动、正离子振 正东的电阻温度系数? 不透明、具有金属光泽? 塑性?正离子始终被电子云包围
引力
结合能 排 斥 能
排斥能
EAB 结合能或键能
dc 理论抗拉强度
最大结合力
o 吸A 引 能
ABE
B
吸引能
双原子作用模型
金属原子为什么排列规则,并趋于紧密排列?
原子间距d
8
§1-2 金属的晶体结构
一、晶体的特征
晶体:原子(离子、分子)在三维空间作有规则的周 期性排列的物质。长程有序,各向异性。
非晶体:原子(离子、分子)在三维空间内不规则排 列的物质。短程有序,各向同性。
b
y
13
晶系与布拉菲点阵
14种布拉菲点阵(7个晶系crystal system)
三个晶格常数a、b、c和三个轴间夹角、、 14种点阵类型 布拉菲点阵 七大晶系
14
7个晶系与14种布拉菲点阵
七个晶系
三斜晶系 单斜晶系 正交晶系 六方晶系 菱方晶系 四方晶系 立方晶系
晶格常数;轴(棱边)之间的夹角
一、 金属原子的结构特点
原子
原子核:带正电
质子:正电荷 中子:电中性
核外电子:带负电
金属原子的结构特点: 最外层电子很少,一般为1-2个,最多3个 失去电子形成正离子(正电性元素)
3
K 层 (n = 1)
11个质子 12个中子
L 层 (n = 2)
M 层 (n = 3)
1s22s22p63s1 Na
钠(原子序数为11)原子结构中K、
L和M量子壳层的电子分布状况
4
金属原子的结构特点: 最外层电子很少,一般为1-2个,最多3个 失去电子形成正离子(正电性元素)
非金属元素的原子结构特点: 最外层4-7个元素 得到电子形成负离子(负电性元素)
过渡族金属元素的原子结构特点:(Ti、V、Fe、Mn、Co等) 最外层电子数很少一般为1-2个,最多3个 (同于金属原子的结构特点);
22
最常见的金属晶体结构
(1)体心立方结构 Body-centered cubic (2)面心立方结构 Face-centered cubic (3)密排六方结构 Hexagonal close-packed
体心立方点阵 bcc
面心立方点阵
密排六方点阵
fcc
hcp
23
晶体结构特征的5个参数
1)晶胞中的原子数
c
a
简单六方结构
19
5.菱方晶系
a = b = c, = = 90
a a
a 简单菱方结构
20
6.四方晶系
a = b c, = = = 90
c
c
a a
a a
简单四方结构、体心四方结构
21
7.立方晶系
a = b = c, = = = 90
a
a
a
a a
a a
a a
简单立方结构、 体心立方结构、 面心立方结构
(1) 体心立方(bcc) α-Fe、 Cr、 Mo、 W、 V 、Nb等约30多种
刚球模型 晶格常数 a=b=c;α=β=γ=90°
质点模型
晶胞原子数模型
N=Ni
Nf 2
Nc 8
晶胞中含有2个原子
25
原子密排列面是{110}, 密排方向是〈111〉,在 密排方向上原子相切:
原子半径 致密度:
k
每个原子有12个最近邻 原子,配位数为12。
28
(3) 密排六方(hcp ) Zn 、Mg 、Cd 等
刚球模型
质点模型
晶胞原子数模型
晶格常数
N=N i
Nf 2
+ Nc 6
晶胞中含有6个原子。
a=b≠c;α=β=90°;γ=120°
29
轴比(axial ratio)
30
3种典型的金属晶体结构参数小结
N=Ni
Nf 2
Nc 8
立方晶系
2)点阵常数a,c 3)原子半径 r
N=N i
Nf 2
+ Nc 6
六方晶系
4)配位数 5)致密度
K
=
nv
=
ห้องสมุดไป่ตู้
n
4
3
R3
VV
晶体中原子排列的紧密程度是反映晶体结构特征的一个重要因素
配位数:指晶体结构中,与任一原子最近邻并且等距离的原子数
致密度:晶胞中原子所占的体积分数
24
