设计实验 乙二胺水杨醛Schiff碱
实验项目卡--水杨醛乙二胺希夫碱的合成
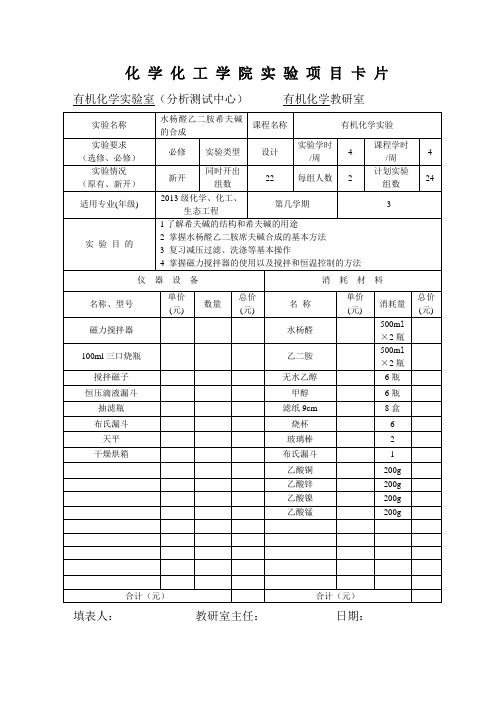
有机化学实验室(分析测试中心)有机化学教研室
实验名称
水杨醛乙二胺希夫碱的合成
课程名称
有机化学实验
实验要求
(选修、必修)
必修
实验类型
设计
实验学时/周
4
课程学时
/周
4
实验情况
(原有、新开)
新开
同时开出组数
22
每组人数2Fra bibliotek计划实验组数
24
适用专业(年级)
2013级化学、化工、生态工程
500ml×2瓶
搅拌磁子
无水乙醇
6瓶
恒压滴液漏斗
甲醇
6瓶
抽滤瓶
滤纸9cm
8盒
布氏漏斗
烧杯
6
天平
玻璃棒
2
干燥烘箱
布氏漏斗
1
乙酸铜
200g
乙酸锌
200g
乙酸镍
200g
乙酸锰
200g
合计(元)
合计(元)
填表人:教研室主任:日期:
第几学期
3
实验目的
1了解希夫碱的结构和希夫碱的用途
2掌握水杨醛乙二胺席夫碱合成的基本方法
3复习减压过滤、洗涤等基本操作
4掌握磁力搅拌器的使用以及搅拌和恒温控制的方法
仪器设备
消耗材料
名称、型号
单价
(元)
数量
总价
(元)
名称
单价
(元)
消耗量
总价
(元)
磁力搅拌器
水杨醛
500ml×2瓶
100ml三口烧瓶
乙二胺
双核乙二胺水杨醛Schiff碱Cu(II)配合物的合成及晶体结构

o th d a o r i a in e vr n n. ca e r c o d n t n i me t l o o
Ke r s: c i a e; r sa sr cu e c mp e y wo d S h f b s c t l t t r ; o lx y u
JANG G a g q ’ I u n — i ( eate t f hm sy G i o nvri , uyn 50 5 C ia D pr n o e ir, uz uU iesy G iag50 2 , hn ) m C t h t
Abta tA wl os-k opr I) o pe a enpeae yc ri tn r ci fe yeeim n ai l dhd s c: i goel ecpe (I cm l hsbe rprd b o dn i e t no t lnda ies c a eye r d i x ao a o h l y l
D。 . 0 g c , =1 7 6 / m3 =1 3 . 2, R = .53 w 2 012 ; 10 8 I 004 ,R = .52 结构分 析表 明 , 配合物
中存 在两种 截然 不 同的 c u
(I 配位 模式 ,u 1 离子采取 四方平面构型 ,u 2 离子却为扭 曲八面体几何构 型。 I) C() C () 关键词 : 夫碱 ; 席 晶体结构 ; 配合物
重金属离子捕集剂水杨醛双Schiff碱的合成及应用

S hf 碱 配体 的合成 路线 见 图 1 ci f 。
多新 的方 法 , 如螯合 沉 淀 法 、 剂 萃取 法 、 溶 天然 沸 石 吸 附一 离 子交 换法 、 腐殖 酸 类 பைடு நூலகம் 附法 、 聚 糖类 吸 附 法 、 壳
微生 物 吸附法 及纳米 材料 催化 还原 法等 。 螯合 沉淀 法 , 因其能 克服传 统化学 沉 淀法 的不 足 , 操作 简单 , 已成 为重 金 属 废 水 处理 研 究 的热 点 。作 者 在此 以 2 6吡 啶二 甲酸 、 二胺 及 水 杨醛 等 为 原 料合 ,一 乙
C 什 等 ) 行 螯 合 反 应 , 成 了 稳 定 的 絮 状 沉 淀 , 而 r 进 生 从 可 以去 除废水 中的重金 属离 子 。
图 1 配 体 的 合 成 路 线
Fi .1 S nt e i o e o he l n g y h t c r ut f t i ga d
合反 应 。 结 果表 明 , 体 化 合 物 Ⅱ能 与 重 金 属 离子 生成 稳 定 性 较 高 且 不 溶 于 水 的 螯 合 物 , 以去 除 废 水 中 的 重 金 属 离 配 可
子。
关 键 词 : , 一 啶 二 甲酸 ; 杨 醛 ; c if ; 2 6吡 水 S hf 碱 重金 属 离 子 中 图分 类 号 : 2 . 2 O 6 6 3 文献标识码 : A 文 章 编 号 : 6 2 4 5 2 1 ) 5 0 7 — 0 1 7 —5 2 ( 0 1 0 — 0 4 3
测仪 。
1 2 方 法 .
仪 ; ruyVX 3 0型 核 磁 共 振 仪 ( 0 Hz , r Mec r 0 3 0M ) Vai -
目前 , 去除水 中重 金属 离子 的方法 很 多 , 统 的有 传
水杨醛Schiff碱及其金属配合物的合成

水杨醛Schiff碱及其金属配合物的合成摘要】水杨醛Schiff碱及其金属配合物在目前各学科的相关研究领域的应用已经得到广泛关注。
而对于合成的水杨醛Schiff碱及其金属配合物的合成而言,一般可以用红外、紫外以及荧光光谱等来实施光谱分析,用以确定其合成的是否为想要得到的目标产物。
【关键词】Schiff碱金属配合物合成1.有关 Schiff 碱及其金属配合物的概述Schiff碱是一种含有亚胺、甲亚胺特性基团(-RC=N-)的有机化合物,一般由胺和活性羰基缩合而成的。
Schiff碱的C=N键的长度在0.124~0.128nm之间,其偶极矩约为0.90D。
与此同时,schiff碱有顺(Z)-、反(E)-两种主要的构型。
而存在其结构中的亚胺基属于极活泼的基团,能够和氰氢酸发生反应形成α-氨基酸,与丙二酸二乙酯反应生生成β-氨基酸还可以与格利雅试剂发生反应生成胺的衍生物,还可以水解作用生成醛或酮和胺。
伴随着生物科学以及化学科学的的不断发展和进步,Schiff碱及其金属配合物的应用已经在医学、催化、分析化学中得到了普遍和广泛的应用。
在医学中,Schiff碱能够用在抑菌、杀菌、抗病毒等;而在催化领域中,Schiff碱在一些具有催化作用的配合物的作用下可以作为催化剂进行相应的应用;对于有关的分析领域而言,Schiff碱能够作为一种非良好的配体用来对金属离子进行鉴定同时还可以对金属离子做一定的定量分析在此基础上分析出其具体含量的多少。
Schiff碱以及金属配合物具有的生物活性已经得到了很大的重视,尤其是在医学研究领域中的抗菌、抗肿瘤、抗氧化等方面。
为了找出高效低毒的药物,我们合成了大量的、不同类型的Schiff碱及其金属配合物对其生物活性进行了研究。
由于在Schiff碱中有C=N键的存在,其轨道上的N原子是含有孤对电子的,可见其具有相当重要的化学和生物学价值。
单纯的schiff碱的水溶性是比较差的,而其水溶性的高低直接影响到的是schiff碱在在具体应用领域中的应用。
双水杨醛缩乙二胺Schiff_碱
双水杨醛缩乙二胺Schiff 碱及其钴(Ⅱ)配合物的合成与表征摘要:本实验以水杨醛、乙二胺、硝酸镍为原料,采用加热、回流等方法合成了席夫碱配体及其Ni(Ⅱ)配合物。
并采用红外光谱、EDTA直接滴定法、测定熔点等途径对化合物进行表征。
关键词:水杨醛;乙二胺;席夫碱;氯化钴;红外光谱水杨醛及其衍生物是重要的有机合成中间体。
由水杨醛及其衍生物与胺类化合物反应生成的席夫碱与其金属配位生成的金属配合物在医药、催化、分析化学、腐蚀和光致变色领域有着重要应用,因而受到人们的广泛关注。
本文对回流条件下双水杨醛缩乙二胺Schiff 碱及其钴(Ⅱ)配合物的合成进行了研究,并对其进行表征。
一、实验部分(一)主要仪器和药品药品:水杨醛、乙二胺、95%乙醇、85%乙醇、无水乙醇、2mol/L HCl溶液、Co·6H2O。
仪器:天平、红外光谱仪、熔点仪、毛细管圆底烧瓶、磁力搅拌器、球形冷凝管、布氏漏斗、温度计、酸式滴定管(50mL)、锥形瓶、烧杯。
材料:滤瓶、pH试纸反应物参数:名称乙二胺水杨醛氯化钴西佛碱分子量60.1 122 238 268.1g/mol密度g/ml 0.9000 1.1656 1.92(二)实验原理1.双水杨醛缩乙二胺Schiff碱及其镍(Ⅱ)配合物的合成Schiff碱的合成是涉及到加成、重排、消去等过程的一种缩合反应。
反应物的立体结构及电子效应在合成中起着重要作用,其反应机理如下图:本实验采用水杨醛和乙二胺在75℃的条件下用回流法制备相应的Schiff碱,反应方程式如下所示:席夫碱基团通过碳氧双键(-C=N-)上的氮原子与相邻的具有孤对电子的氧(O)、硫(S)、磷(P)原子作为给体与金属原子配对,所以氮原子相邻位置存在这类原子的Schiff碱往往具有高配位能力。
(三)实验装置图(四)实验内容1.Schiff 碱配体及其镍(Ⅱ)配合物的合成实验步骤现象记录(1)Schiff 碱配体的合成在装有回流冷凝管和搅拌器的圆底烧瓶中加入6ml水杨醛和30ml无水乙醇,开动搅拌器搅拌。
席夫碱实验学生实验报告(3篇)

第1篇一、实验目的1. 了解席夫碱的基本概念、性质及其应用;2. 掌握席夫碱的合成方法;3. 学习并掌握实验操作技能,提高实验能力。
二、实验原理席夫碱(Schiff base)是一种含有亚胺或甲亚胺特性基团(RCN)的有机化合物,通常由胺和活性羰基缩合而成。
席夫碱具有优良液晶特性,在有机合成、催化、分析化学等领域有广泛应用。
席夫碱的合成通常采用醛或酮与胺的缩合反应。
在本实验中,以邻氨基苯甲酸和苯甲醛为原料,通过席夫碱缩合反应合成席夫碱。
三、实验仪器与试剂1. 仪器:试管、烧杯、酒精灯、石棉网、玻璃棒、抽滤装置、干燥器、电子天平、红外光谱仪等。
2. 试剂:邻氨基苯甲酸、苯甲醛、无水乙醇、浓硫酸、氢氧化钠、碳酸钠、氯化钠等。
四、实验步骤1. 原料称量:准确称取0.1g邻氨基苯甲酸和0.1g苯甲醛,置于试管中。
2. 反应液的配制:向试管中加入5mL无水乙醇,用玻璃棒搅拌溶解。
3. 缩合反应:将试管置于石棉网上,用酒精灯加热至回流状态,保持回流30分钟。
4. 冷却:将反应液冷却至室温,加入少量碳酸钠中和溶液中的酸性物质。
5. 抽滤:将反应液过滤,滤液用氯化钠饱和,静置分层。
6. 收集产物:将滤液倒入烧杯中,加入少量氢氧化钠,使溶液呈碱性,静置析出固体。
7. 干燥:将固体产物用滤纸过滤,晾干后置于干燥器中保存。
8. 红外光谱分析:对产物进行红外光谱分析,确定产物结构。
五、实验结果与分析1. 实验结果:产物为白色固体,熔点为180~182℃。
2. 红外光谱分析:产物在3280cm^-1、1650cm^-1、1590cm^-1、1540cm^-1、1450cm^-1、1360cm^-1、1290cm^-1、1120cm^-1、1000cm^-1等处有特征吸收峰,与席夫碱的结构特征相符。
3. 结论:通过本实验,成功合成了席夫碱,并对产物进行了红外光谱分析,确定了产物结构。
六、实验讨论1. 在实验过程中,控制好反应温度和回流时间对产物的收率和纯度有很大影响。
设计实验 希夫碱
实验方案实验设备及药品:实验设备:集热式恒温加热磁力搅拌器,150mL三口(圆底)烧瓶,滴液漏斗,冷凝管,酸式滴定管,锥形瓶,烧杯,250mL容量瓶,25mL移液管。
药品:水杨醛(A.R),乙二胺(A.R),无水乙醇(A.R),醋酸锌Zn(OAc)2·2H2O(A.R),浓硝酸,HCl(1:1),ZnO(A.R,基准试剂),NH3·H2O(1:1),20%六次甲基四胺溶液,二甲酚橙指示剂,乙二胺四乙酸二钠(A.R)。
一、希夫碱配体及其配合物的制备:1.水杨醛双缩乙二胺希夫碱配体(Salen)的合成在三口(圆底)烧瓶中加入11mL水杨醛和50mL无水乙醇,搅拌均匀,2分钟后缓慢加入3.2mL乙二胺和10mL无水乙醇的混合液,开始滴加乙二胺即有黄色不溶物产生,随着乙二胺的加入不溶物大量生成,将温度升至50℃回流反应1h。
冷却至室温抽滤,无水乙醇洗涤数次。
60℃下干燥,得大量黄色晶体。
2.制备salenZn希夫碱金属配合物准确称取0.2681g双水杨醛缩乙二胺于三口(圆底)烧瓶,加入50mL无水乙醇,搅拌溶解,得黄色透明溶液。
配制0.2192g醋酸锌20mL的无水乙醇溶液,缓慢加入到希夫碱配体中并将温度升至60℃加热回流1h。
反应完毕后冷却至室温过滤。
将滤渣在60℃下干燥,得黄色粉尘状产物。
二、希夫碱及其配合物的表征1.用熔点仪测定希夫碱及其配合物的熔点。
2.将希夫碱及其配合物用KBr压片法在红外光谱仪上进行红外光谱分析。
3.准确称取三份1~2g的试样放入250ml锥形瓶中,加入少量去离子水及几滴浓硝酸,在通风橱中加热煮沸数分钟,将Zn2+释放出来,继续加热数分钟,除去多余的硝酸。
加入约20mL 去离子水,2~3滴二甲酚橙指示剂,先加NH3·H2O(1:1)至溶液由黄色刚变橙色(不能多加),然后滴加20%六次甲基四胺至溶液呈稳定的紫红色后再多加3mL,用EDTA标准溶液(用ZnO基准物标定)滴定至溶液由紫红色变为亮黄色,即为终点。
乙二胺水杨醛双Schiff碱Cr(Ⅲ)配合物的合成与表征
, 、
化活性 , 甚至表 现 出与生命 现象 相关 的化学模 拟 , 具 有
2
+
: = = ] 罟 N
Cr ”
△
.
CI
1 实 验
1 . 1 试剂 与仪器
体, 即配体 乙二胺 水 杨醛 双 S c h i f f 碱 。m. P .1 2 7 ~
> 1 2 8℃( 文献值 L 8 ]1 2 7 ~1 2 8℃) 。 /
关键词 : 乙二 胺 ; 水杨醛 ; 双S c h i f f 碱; 配合 物 ; 表 征
中 图分 类 号 : 0 6 2 6 . 3 2
文 献标 识码 : A
文章 编 号 : 1 6 7 2 —5 4 2 5 ( 2 0 1 3 ) 0 2 -0 0 5 8 -0 3
近年来 , 水杨 醛双 S c h i f f 碱 及其 配合物 在催化 剂 、 医药 、 农药 、 缓蚀剂 、 新材料 、 有机合成、 分 析化 学 等领
水杨 醛和 乙二胺在 乙醇 溶液 中反应 得 到亮 黄色 晶
基金项 目: 湖北 科 技 学院 科 研 项 目( KY1 o 0 4 8 ) 收 稿 日期 : 2 0 1 2 一l O 一2 O
作者简介 : 李艳 ( 1 9 7 6 一) , 女, 湖j 通城人, 剐教授. 主要从事有机合 成的研 究, E - ma i l : l i y a n 7 5 0 6 0 6 @y a h o o . c o m。 a r t 。
2 h后 , 将 反应 混 合 物放 人 冰 盐 浴 中 冷却 , 抽滤 , 得 到
淡黄 色 固体 , 即乙二胺 水杨 醛双 S c h i f f 碱C r ( Ⅲ) 配合
水杨醛缩乙二胺席夫碱及金属配合物的合成
水杨醛缩乙二胺希夫碱及金属配合物的合成一实验目的1 掌握水杨醛缩乙二胺席夫碱碱合成的基本原理和方法。
2 复习回流、重结晶、热过滤、洗涤等基本操作方法。
3掌握磁力搅拌器的使用方法。
二实验原理水杨醛及其衍生物是重要的有机合成中间体。
由水杨醛及其衍生物与胺类化合物反应生成的希夫碱与其金属配位生成的金属配合物在医药、催化、分析化学、腐蚀和光致变色领域有着重要应用,因而受到人们的广泛关注。
本文对回流条件下双水杨醛缩乙二胺Schiff 碱及金属铜(Ⅱ)配合物的合成进行了研究。
席夫碱碱的合成是涉及到加成、重排、消去等过程的一种缩合反应。
反应物的立体结构及电子效应在合成中起着重要作用,其反应机理如下图:本实验采用水杨醛和乙二胺在50℃的条件下用回流法制备相应的Schiff碱配体L,反应方程式如下:希夫碱基团通过碳氧双键(-C=N-)上的氮原子与相邻的具有孤对电子的氧(O)、硫(S)、磷(P)原子作为给体与金属原子配对,所以氮原子相邻位置存在这类原子的Schiff碱往往具有高配位能力。
M2+为金属离子(M2+分别为Cu2+、Zn2+、Ni2+、Mn2+、Ni2+等离子)二仪器和药品1 仪器100mL三口烧瓶恒压滴液漏斗磁力搅拌器玻璃塞抽滤瓶烧杯2 药品水杨醛(相对分子质量122.12,密度1.17g/cm³乙二胺(相对分子质量60.10,密度0.90g/cm³无水乙醇乙酸铜、硝酸钴、乙酸锰、乙酸锌、硝酸锌、氯化镍三实验步骤1 希夫碱配体(L)的合成步骤移取5.2mL(0.05mol)的水杨醛与15 mL的无水乙醇溶于三口瓶中,再量取1.8mL(0.025mol)的乙二胺与10mL的无水乙醇于烧杯中搅拌溶解。
将三口瓶固定在搅拌器上,开启仪器,将乙二胺的无水乙醇溶液逐滴滴加到三口瓶中,恒温55℃反应1小时。
反应结束。
抽滤得黄色的固体,干燥称重并计算产率。
反应装置图如下:乙二胺的无水乙醇溶液2 希夫碱配体(L)与金属离子(M2+)的反应步骤称取1.34g(0.005mol)配体L,与20 mL的无水乙醇混合溶解于三口瓶中,在称取金属盐,若为乙酸铜时质量为1g(0.005mol)。
乙二胺水杨醛双Schiff碱Cr(Ⅲ)配合物的合成与表征
万方数据万方数据万方数据乙二胺水杨醛双Schiff碱Cr(Ⅲ)配合物的合成与表征作者:李艳, 李军喜, 陆兰青, LI Yan, LI Jun-xi, LU Lan-qing作者单位:李艳,李军喜,LI Yan,LI Jun-xi(湖北科技学院核技术与化学生物学院,湖北咸宁,437100), 陆兰青,LU Lan-qing(咸宁高中,湖北咸宁,437000)刊名:化学与生物工程英文刊名:Chemistry & Bioengineering年,卷(期):2013,30(2)1.罗勤慧;沈孟长配位化学 19872.孟庆金;戴安邦配位化学的创始与现代化 19993.Desai M N;Chauhan P O;Shah N Schiff bases derived from chloroanlines as corrosion inhibitors of zinc in sulfuric acid solutions 1995(02)4.Iolio A B;Gennaro A C;Vianello E E Electrochemical reduction of Schiff bases ligands H2 salen and H2 salophen1997(13-14)5.Bastos B R M;Moreira J C;Farias P A M Adsorptive stripping voltammetric behaviour of UO2 (Ⅱ) complexed with the Schiff base N,N'-ethylenebis(salicylidenimine) in aqueous 4-(2-hydroxyethyl)-1-piperazine ethanesulfonic acid medium [外文期刊] 2000(1-2)6.Ma H;Chen S;Niu L Studies on electrochemical behavior of copper in aerated NaBr solutions with Schiff base2001(05)7.赵建章;赵冰;徐蔚青Schiff碱N,N'-双水杨醛缩-1,6-己二胺的光致变色光谱研究[期刊论文]-高等学校化学学报 2001(06)8.陈玉红;丁克强;王庆飞席夫碱应用研究新进展[期刊论文]-河北师范大学学报(自然科学版) 2003(01)9.竹学友;俞志刚;刘洲亚一种新型席夫碱及其铜配合物的合成与抑菌活性的研究[期刊论文]-化学与生物工程 2008(04)本文链接:/Periodical_hbhg201302014.aspx。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验步骤
1.双水杨醛缩乙二胺的合成
在装有回流冷凝管和搅拌器的圆底烧瓶中加入0.01mol (1.2213g)水杨醛和60 mL 85%乙醇,开动搅拌器搅拌,溶解 后滴加0.005(0.6012g)mol乙二胺,加毕后加热至75℃回流 1 h,冷却到室温,将析出的淡黄色固体滤出,用乙醇洗涤,烘 干得双水杨醛缩乙二胺,计算产率。
EDTA滴定
由黄色变为紫红色
滴定金属离子
Ni2+含量的计算式:
Ni2+(g) = MV×58.69
其中: M — EDTA的浓度(mol/L) V — EDTA的耗用量(mL) 58.69 — Ni的摩尔质量(g/mol)
5.不同条件对席夫碱合成的影响
研究时间对合成席夫碱的影响
在装有回流冷凝管和搅拌器的圆底烧瓶中加入 0.01mol (1.2213g)水杨醛和60 mL 85%乙醇,开 动搅拌器搅拌,溶解后滴加0.005 mol ( 0.6012g)乙 二胺,加毕后加热至75℃回流1 h,冷却到室温,将 析出的淡黄色固体滤出,用乙醇洗涤,烘干得双水杨 醛缩乙二胺,计算产率。
双水杨醛缩乙二胺Schiff 碱 及其镍(Ⅱ)配合物的合成与表征
组员:洪诚毅(040802121) 曾志媛(040802114) 游振威(040802103) 黄冬(040802124) 方菲(040802127)
1.席夫碱及配合物的合成
实验原理
Schiff碱的合成是涉及到加成、重排、消去等过程的 一种缩合反应。反应物的立体结构及电子效应在合成中起 着重要作用,其反应机理如下图:
Ni(NO3)2 ·6H2O
实验原理
金属配合物的表征
(1)金属配合物的稳定性受很多因素的影响,通常可以用加热或 改变溶液的酸碱性来破坏;
(2)游离出来的Ni离子在pH=10,以紫脲酸铵为指示剂用EDTA直 接滴定,由此可计算出Ni的量;
(3)用熔点仪或毛细管加热测定配体及其配合物的熔点;
(4)用红外光谱仪测定配体席夫碱及其配合物的红外光谱图。
选择3个实验时间进行比较: 30min、60min、 90min。
研究温度对合成席夫碱的影响
在装有回流冷凝管和搅拌器的圆底烧瓶中加入 0.01mol (1.2213g)水杨醛和60 mL 85%乙醇,开 动搅拌器搅拌,溶解后滴加0.005 mol ( 0.6012g)乙 二胺,加毕后加热至75℃回流1 h,冷却到室温,将 析出的淡黄色固体滤出,用乙醇洗涤,烘干得双水杨 醛缩乙二胺,计算产率。
实验原理
Schiff碱本身不太稳定,其稳定性决定于它们的结 构,若一CH=CH一双键能和一CH=N一双键共轭,则 这类物质极稳定。因此,带有苯环的醛及其衍生物与单 胺、二胺、多甘醇二胺等缩合而成的各种芳香族Schiff 碱都是稳定的。
实验原理
Schiff碱配合物的合成 A.直接合成法
直接合成法是一种简单,易行的方法。它是将醛、胺与金属盐按 一定物质的量比,直接混合反应而合成Schiff碱金属配合物。此法产 率高,简便快速,缺点是容易发生副反应而使产品中混有杂质,使产 品在纯化时有一定的困难。一般为了减少副反应的发生,可采用分步 合成法。 B.分步合成法
▪ 把电表调至零按升温按钮,数分钟后初熔灯先亮, 然后出现终熔读数显示,按初熔按钮可知初熔读数, 记录初、终熔温度;
▪ 按下降温按钮,使之降至室温,换一根新的熔点管, 重复上面的操作;
▪ 关闭电源。
Schiff碱的熔点测定操作步骤同配合物
表2 各物质熔点的测定
序号
物质
1
2
水杨醛缩乙二胺
镍(Ⅱ)配合物
选择3个实验温度进行比较: 60 ℃、 75 ℃、 90 ℃ 。
研究pH不同对产率影响
镍(Ⅱ)配合物熔点的测定
▪ 插上电源插头,稳定20min,通过拨盘设定起始温度, 再按起始温度按钮,输入此温度,此时预置灯亮, 选择升温速率把波段开关旋至所需位置;
▪ 将研细的配合物在表面皿上堆成小堆→取料,配合 物的高度为2-3mm;
▪ 当预置灯熄灭时 ,可插入装有样品的毛细管,此时 初熔灯熄灭;
2.镍(Ⅱ)配合物的合成
称取配体3.22g(0.012mol)溶于30 mL 95%乙醇中,搅拌加 热,在65°C下滴加3.52g(0.0121mol ) Ni(NO3)2·6H2O的20mL 95%乙醇,溶液逐渐变为红色,滴完后,继续回流1 h,冷却即有沉 淀析出,抽滤并用少量蒸馏水及乙醇洗涤数次,在70℃干燥得到 配合物,计算产率。
表1 配合物的合成数据记录
项目
物质
1
2
3
4
双水杨醛 缩乙二胺 的合成
镍(Ⅱ) 配合物的
合成
水杨醛
___ g
乙二胺 席夫碱配体
___ g ___ g
Ni(NO3)2·6H2O 席夫碱配体
___ g
___ g
配合物
___ g
产率
__ %
产率
__ %
2.席夫碱及配合物的熔点测定
实验装置图
图-2 熔点仪
主要仪器和药品
药品:水杨醛、乙二胺、95%乙醇、85% 乙醇、无水乙醇、Ni(NO3)2·6H2O。
仪器:天平、红外光谱仪(KBr压片)、 红外灯、 玛瑙研钵、熔点仪、圆底烧瓶、 磁力搅拌器、球形冷凝管、抽滤瓶、布氏 漏斗、温度计、酸式滴定管(50mL)、锥 形瓶、烧杯、pH试纸。
实验装置图
分步合成法按两步进行。 第一步先由醛和胺缩合反应得到Schiff碱配体; 第二步Schiff碱配体与金属盐反应而得到配合物。分步合成法合 成的Schiff碱金属配合物,一般都有较高的产率,产品相对比较纯净。 所以,目前多采用该方法。
实验原理
我们的实验采用分步合成法,先用水杨醛和乙二胺在70-80℃的 条件下用回流法制备Schiff碱,再用合成的配体与Ni(NO3)2·6H2O在 65℃下继续回流合成配合物。 反应方程式如下:
3.红外光谱
将样品用KBr压片
↓
在红外光谱仪上记录400-4000 cm-1 范围的红外光谱图
4.滴定金属离子
取0.5g样品于250mL锥形瓶
少量去离子水
5-6d浓硝酸
△煮沸数分钟 使Ni2+释放出来 继续△H3-NH4Cl缓冲溶液 调节pH=10左右 1-2d紫脲酸铵
