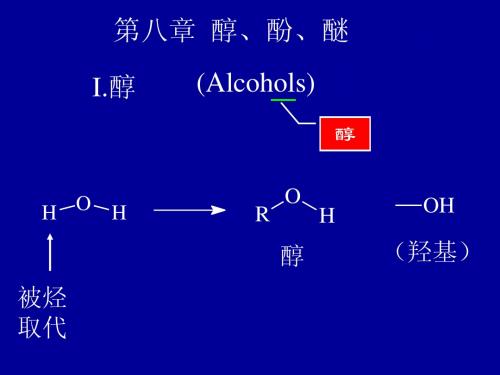
第八章 醇酚醚
合集下载
08第八章醇酚醚-chy
1.2.1.2 氢键对溶解度的影响
O H H
R OH
相似
★ C3 以下无限溶解
R O H R O H R O H
形成氢键
n – 丁醇 n – 戊醇
8g / 100g 水 2g / 100g 水
∵ 随烷基的增大, 占的比例小
相似相溶原理
1.3 醇的反应 极性键的断裂
H R C H O H
酸性、酯化
78.5 ℃
-44.5 ℃ 256 ℃
十三烷
184
235.4 ℃
1. 醇比烷 bp 高的多
2. 随 M 的增大,Δbp → 0
bp
ROH RH
C 原子数
bp
CH3CH2CH2CH2OH
CH3 CH3 CH3 CH3 CH CH2 CH3 C CH3
C2H5OH CH2 OH CH2 OH CH2 OH CH CH2 OH OH
H H C OH OH
H 4 IO
HCOH + H O + NH3 + H COOH + CO2 2
断开的地方加羟基
H HO C NH2 OH
∵
HO C O
OH
脱H2O
HC O H + H2O
HC O + NH3 OH
CO2 + H2O
II. 酚 (Phenols)
OH
CH2OH
酚
醇
1 结构、命名(书中例子 p141) 、性质 1 命名:
CH3 CH3-C-CH2+OH2 CH3
-H2O
CH3 CH3-C +CH2 ( 。 +) 1 C CH3
CH3 CH3-C +CH2 CH3 。 1 C+
第八章醇酚醚

C-O键断裂 取代或消除
碱性
孤对电子
1. 氧孤对电子导致的化学性质——Lewis碱
①溶于强酸
ROH 浓H2SO4 ROH H
应用: 钼羊盐
稀释或受热
ROH
▪除去烷烃或卤代烃中的少量醇 ▪区分醇与烷烃、卤代烃
②与金属离子的络合
MgCl2•6ROH CaCl2•4ROH
结晶醇 (溶于水不溶于有机溶剂)
第八章:醇、酚、醚
一. 醇的分类与命名
1. 分类
①按羟基所连碳原子的类型分:
10 伯醇( RCH2OH ): CH3CH2OH
20 仲醇( R CH OH ): CH 3CHCH 2CH 3
OH
R'
OH
R
30 叔醇( R' C OH ):
R''
(CH3)3COH
②按羟基所连的烃基分:
饱和醇:
CH3CH2OH (CH3)3COH
不饱和醇:CH2=CHCH2OH
CH3C≡ CCH2OH
芳香醇:
CH OH 2
OH OH
CH OH 2
③按羟基的数目分:
一元醇C:H3CH2CH2OH
OH
二元醇:H2C CH CH3 OH OH
OH OH
三元醇:H2C CH CH 2 OH OH OH
2. 命名
①普通命名法
CH3CH2CH2OH 正丙醇
R C OH
*源自格式试剂
H3C C O + R MgX 干醚
H
H3C C OMgX H R
H2O
*源自羰基碳
R
*源自格式试剂
H
C CH3 OH
3. 醛、酮还原制醇
第八章醇酚醚

己酮)氧化成酮,丙酮被还原成异丙醇,这一反应称为欧芬脑尔 (Oppenauer,R.V)氧化法,其逆反应称为麦尔外因-彭道夫(MeerweinPonndorf)还原。
O R2CHOH + CH3CCH3
Al(OCMe3)3 欧芬脑尔氧化法
麦尔外因-彭道夫还原
OH R2CH=O + CH3CHCH3
反应方向的控制
减压蒸餾
-H2SO4
CH3OSO2OCH3 硫酸二甲酯
C2H5OH NaOH
甲基化反应
C2H5OCH3 + CH3OSO3Na + H2O
2oROH , 3oROH在硫酸作用下消除。
五 氧化反应
ROH
氧化剂 反应条件
产物
氧化剂
氧化剂
RCH2OH
RCHO
RCOOH
O
氧化剂
R2CHOH
RC R
O
H+
氧化剂
反应机理
C OH C OH
OH
CO
OH
C O I O-
O
OH
HO HO
I
OH O-
O
-2H2O
I = +7
-H2O
C=O + C=O + IO3-
I = +5
邻二醇被高碘酸氧化的分析
OH OH
OH
OH OH
OH
OH OH
?
OH
(CH3)3C
OH
OH
OH
-羟基酸、 -二酮、 -氨基酮、1-氨基2-羟基化合物也能发生类似的反应。
100%
Br
3oROH 、大多数2oROH和空阻大 的 1oROH按SN1机理进行反应。
O R2CHOH + CH3CCH3
Al(OCMe3)3 欧芬脑尔氧化法
麦尔外因-彭道夫还原
OH R2CH=O + CH3CHCH3
反应方向的控制
减压蒸餾
-H2SO4
CH3OSO2OCH3 硫酸二甲酯
C2H5OH NaOH
甲基化反应
C2H5OCH3 + CH3OSO3Na + H2O
2oROH , 3oROH在硫酸作用下消除。
五 氧化反应
ROH
氧化剂 反应条件
产物
氧化剂
氧化剂
RCH2OH
RCHO
RCOOH
O
氧化剂
R2CHOH
RC R
O
H+
氧化剂
反应机理
C OH C OH
OH
CO
OH
C O I O-
O
OH
HO HO
I
OH O-
O
-2H2O
I = +7
-H2O
C=O + C=O + IO3-
I = +5
邻二醇被高碘酸氧化的分析
OH OH
OH
OH OH
OH
OH OH
?
OH
(CH3)3C
OH
OH
OH
-羟基酸、 -二酮、 -氨基酮、1-氨基2-羟基化合物也能发生类似的反应。
100%
Br
3oROH 、大多数2oROH和空阻大 的 1oROH按SN1机理进行反应。
【课件】第八章醇酚醚10-11学年1PPT

酸性序: H2O > R-OH > HC≡CH > NH3 > R-H 碱性序:OH- < RO- < HC≡C- < NH2- < R-
Li、K等碱金属和Mg、Ca、Ba等碱土金属也能和 C1 ~ C8的醇类反应,生成相应的醇的金属化合物
问题:比较CH3CH2CH2OH、
(CH3)2CHOH及(CH3)3COH与 Na反应的活性以及相应醇钠的 碱性大小
问题:氯化钙能用作干燥剂,是因为它能与水形成 CaCl2 ·6H2O。能否用氯化钙来干燥醇类?
某些醇具有特殊的
香味,多用来配制 香精。如苯乙醇具 有玫瑰香气
8.1.4 醇的化学性质
氧化反应
H CC H
形成氢键 形成金羊盐
酸性(被金属取代)
O
H
取代反应 脱水反应
1. 与活泼金属反应——似水
H—O-H + Na ——> Na OH + H2 (反应激烈) R—O-H + Na ——> RO Na + H2 (反应和缓)
2、由于醇分子与水分子之间能形成氢键,三个碳的醇和叔丁醇 能与水混溶。
从丁醇开始,在水中的溶解度随相对分子量的增加而减小。
R
O HH O
H
R
O HH O
H
R
O HH O
H
醇与水之间形成的氢键
3、醇合物 醇与水的另一相似之处:能形成象水合物那 样的醇合物,称为结晶醇。如:
MgCl2 ·6CH3OH
CaCl2 ·4CH3OH
或: Al2O3,250 ℃
+ H2O
Lewis酸如Al2O3,也能催化醇的脱水反应。
醇的脱水是质子化的醇作为脱水物的单分子消除反应(E1)。
Li、K等碱金属和Mg、Ca、Ba等碱土金属也能和 C1 ~ C8的醇类反应,生成相应的醇的金属化合物
问题:比较CH3CH2CH2OH、
(CH3)2CHOH及(CH3)3COH与 Na反应的活性以及相应醇钠的 碱性大小
问题:氯化钙能用作干燥剂,是因为它能与水形成 CaCl2 ·6H2O。能否用氯化钙来干燥醇类?
某些醇具有特殊的
香味,多用来配制 香精。如苯乙醇具 有玫瑰香气
8.1.4 醇的化学性质
氧化反应
H CC H
形成氢键 形成金羊盐
酸性(被金属取代)
O
H
取代反应 脱水反应
1. 与活泼金属反应——似水
H—O-H + Na ——> Na OH + H2 (反应激烈) R—O-H + Na ——> RO Na + H2 (反应和缓)
2、由于醇分子与水分子之间能形成氢键,三个碳的醇和叔丁醇 能与水混溶。
从丁醇开始,在水中的溶解度随相对分子量的增加而减小。
R
O HH O
H
R
O HH O
H
R
O HH O
H
醇与水之间形成的氢键
3、醇合物 醇与水的另一相似之处:能形成象水合物那 样的醇合物,称为结晶醇。如:
MgCl2 ·6CH3OH
CaCl2 ·4CH3OH
或: Al2O3,250 ℃
+ H2O
Lewis酸如Al2O3,也能催化醇的脱水反应。
醇的脱水是质子化的醇作为脱水物的单分子消除反应(E1)。
醇酚醚
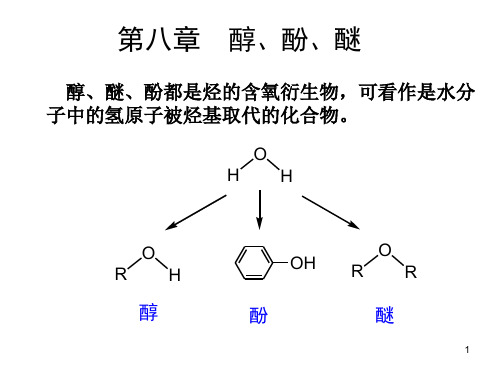
-H2O
85%H3PO4 80oC
CH3 H3C C CH CH3 CH3 OH2
+
CH3 H3C C CH CH3 + CH3
CH3 H3C C CH CH3 + CH3
-H
+
CH3 CH3 H3C C C CH3 + H2C C CH CH3 CH3 CH3 80% 20%
20
5 氧化或脱氢反应
酚的结构中有苯环和羟 基,所以酚表现出这两个官 能团的一些特征的化学性质, 能团的一些特征的化学性质, 如苯环的亲电取代反应, 如苯环的亲电取代反应,羟 基的酸性等。 基的酸性等。
O H
另一方面,由于羟基和苯环直接相连, 另一方面,由于羟基和苯环直接相连,这类化合物具 有一些独特的化学性质, 键难于断裂, 有一些独特的化学性质,如 C-O 键难于断裂,容易被氧 化等。 化等。
RONO2 + H2O
10
CH2 OH CH OH + 3HNO3 CH2 OH
H2SO4
CH2 ONO2 CH ONO2 + H2O CH2 ONO2
三硝酸甘油酯
ROH + HOSO2OH
ROSO2OH + H2O
硫酸烷基酯
ROH + ROSO2OH
ROSO2OR + H2O
硫酸二烷基酯
11
OH R OH + HO P OH O
30
1 酚羟基的酸性
OH + NaOH ONa + H2O
ONa + HCl
OH + NaCl
酸性大小顺序: RCOOH > H2CO3 >苯酚 >H2O > R-OH
85%H3PO4 80oC
CH3 H3C C CH CH3 CH3 OH2
+
CH3 H3C C CH CH3 + CH3
CH3 H3C C CH CH3 + CH3
-H
+
CH3 CH3 H3C C C CH3 + H2C C CH CH3 CH3 CH3 80% 20%
20
5 氧化或脱氢反应
酚的结构中有苯环和羟 基,所以酚表现出这两个官 能团的一些特征的化学性质, 能团的一些特征的化学性质, 如苯环的亲电取代反应, 如苯环的亲电取代反应,羟 基的酸性等。 基的酸性等。
O H
另一方面,由于羟基和苯环直接相连, 另一方面,由于羟基和苯环直接相连,这类化合物具 有一些独特的化学性质, 键难于断裂, 有一些独特的化学性质,如 C-O 键难于断裂,容易被氧 化等。 化等。
RONO2 + H2O
10
CH2 OH CH OH + 3HNO3 CH2 OH
H2SO4
CH2 ONO2 CH ONO2 + H2O CH2 ONO2
三硝酸甘油酯
ROH + HOSO2OH
ROSO2OH + H2O
硫酸烷基酯
ROH + ROSO2OH
ROSO2OR + H2O
硫酸二烷基酯
11
OH R OH + HO P OH O
30
1 酚羟基的酸性
OH + NaOH ONa + H2O
ONa + HCl
OH + NaCl
酸性大小顺序: RCOOH > H2CO3 >苯酚 >H2O > R-OH
高教版 有机化学 第八章 醇 酚 醚

C2H5ONa+H2
(C 2H 5O)2Mg+H 2
6CH 3CHCH 3 + 2 Al OH
[HgCl2或 AlCl3]
[(CH 3)2CHO] 3Al + 3 H 2 异丙 醇 铝
7
说明 R—OH H—OH 1)醇与金属反应比水与金属反应缓和一些。 2)醇(如甲醇的pKa=16) 的酸性比水的酸性 (pKa=15.4)稍弱,故醇不能使石蕊变红。和氢氧化钠 的作用也很难,是一个可逆反应。
OH OH Ph C C CH3 Ph CH3 Ph CH3 C C Ph CH3
+ H3O
Ph CH3 C C
O
Ph CH3
+ H3O O
25
O + H3O OH OH
Ph Ph OH OH + H 3O
O Ph Ph
26
5 欧芬脑尔(Oppenauer, R.V.)氧化
OH CH R1 R2 Al[OC(CH3)3]3 CH3COCH3 R1 O C OH
36
酚的命名
OH OH OH
Me CH3
间甲酚
CH3
C(CH3)3
对甲酚
3-甲基-4-叔丁基苯酚
O2N HO
OH
Cl H3CO
OH
HO
CO2H 对羟基苯甲酸
4-硝基间苯二酚 or 4-硝基-1,3-苯二酚
6-甲氧基-7-氯-2-萘酚 or 6-甲氧基-7-氯--萘酚
or 4-羟基苯甲酸
37
二、酚的物理性质
13
3)、与SOCl2、PCl3、PBr3、PCl5的反应
SOCl2
RCl + SO2 + HCl RX + H3PO3 (Br2 / P, I2 / P) RCl + POCl3
第八章醇酚醚
一. 醇
醇的分类
1、按烃基结构分为
饱和醇 CH3CH2CH2CH2OH 不饱和醇 CH2 脂环醇 芳香醇
OH
CH2OH
丁醇 CHCH2OH 烯丙醇 环戊醇 苯甲醇
2、按醇分子中所含羟基的数目分为
一元醇 二元醇
CH3 OH CH2 CH2
甲醇 乙二醇 丙三醇
多元醇 CH2 CH CH2
OH OH OH
OH OH CHO SO 3H COOH OH
对羟基苯磺酸
邻羟基苯甲醛
对羟基苯甲酸
三、酚的制备 1. 磺酸盐碱熔法
SO3Na
ONa
NaOH >300℃ (融 熔)
H+
OH
2. 氯苯水解法
O Na NaOH , 400℃
Cl
H+
OH
200atm
氯苯难以发生亲核取代,当卤原子的邻对 位有吸电子基团时,水解反应容易进行。
(二) 乙醇(CH3CH2OH) 俗称“酒精”
(三) 丙三醇(CH2OH—CHOH—CH2OH) 又称“甘油”
CH2 ONO2 CH CH2 ONO2 ONO2
阿尔弗里德.伯恩纳德 .诺贝尔(Alfred Bernhard Nobel) 诺贝尔的一生中 ,仅在英国申请 的发明专利就有 355项之多。
CH3CH3OH
Cu
250~350 ℃
CH3CHO + H2
CH3CCH3 + H2 O
CH3 CHCH3 OH
Cu
500 ℃ , 0.3 MPa
叔醇:分子中没有α-H,不发生脱氢反应。
三、几种重要的醇 (一) 甲醇(CH3OH)
又称“木醇”, 毒性大,误服10ml可致失明,误服30ml可致死亡 。
第八章醇、酚、醚消除反应
甲醇的分子结构
H
::
H H
C O
sp3
H
二、醇的物理性质和光学性质
1.物理性质 低级一元醇:C1-C4无色流动液体,比水轻。
C5-C11油状液体, C12以上无色蜡状固体。 甲醇、乙醇、丙醇都带有酒味. 丁醇开始到十一醇有不愉快的气味. 二元醇和多元醇:是具有甜味液体,故乙二醇俗
称甘醇,丙三醇俗称甘油.
[O]
[O]
1°ROH
RCHO
RCOOH
[O]
2°ROH
RCOR’
等。
3°ROH 因无 α - H,难以被氧化,若在强烈条件下氧化,碳链将断裂。
CH3CH2CH2CH2OH K2Cr2O7 / dil. H2SO4 CH3CH2CH2CHO (50%)
CH3CH(CH2)3CH3 OH
K2Cr2O7 / dil. H2SO4
结晶醇: 低级醇和一些无机盐类(MgCl2,CaCl2,CuSO4等) 形成结晶状的分子化合物, 如:MgCl2.6CH3OH,CaCl2.4C2H5OH等。 结晶醇不溶于有机溶剂而溶于水,可使醇与 其他有机物分开或从反应物中除去醇类 如:乙醚中的少量乙醇,加入 CaCl2便可除去.
2.光谱性质 IR:-OH未缔合的3640-3610cm-1有尖峰;
可用来区别一元醇和邻二醇或邻多醇ch2ohch2ohcuoh2ch2och2ocu可溶性洛合物降兰色h2o2与高碘酸或四乙酸铅反应二醇可被高碘酸四乙酸铅氧化生成相应的羰基化合物反应是定量的每分裂一组邻二醇结构消耗一个分子hio4因此根据hio4的消耗量可以推知分子中有几组邻二醇结构可用agno3来检测邻二羟基结构rchohrchohio4rchorchoiooohohrchorchoio3h2o白agio3io3agno3四乙酸铅作氧化剂rchchrch3coo4pbohohrchhcrch3coo2pbch3coohoo被hio4氧化断键除邻二醇外还有羰基醇
第八章 醇酚醚1
H H O H R O H H O H R O H H O
醇与水分子间氢键缔合
自正丁醇开始,随着烃基的增大,在水中的溶解度降 低,癸醇以上的醇几乎不溶于水。
21
多元醇分子中含有两个以上的羟基,可以形成更 多的氢键,所以分子中所含羟基越多,沸点越高, 在水中的溶解度也越大。
例:乙二醇 沸点:197℃ 甘油(丙三醇) 沸点:290℃。 低级醇能和一些无机盐类(MgCl2,CaCl2,CuSO4等) 形成结晶状的分子化合物,称为结晶醇。 CaCl2· 4CH3OH CaCl2· 4C2H5O H MgCl2· 6CH3OH MgCl2· 6C2H5OH
3o 醇 、烯丙醇、苄醇 室温下反应液立即混浊、分层; 2o醇 1o醇 2 ~ 5 min. 反应液混浊、分层; 加热,反应液混浊、分层;
31
Lucas试剂(无水ZnCl2与浓HCl配制的溶液)鉴别六 个碳以下的伯、仲、叔醇(烯丙式醇)
现象
R3C-OH 烯丙式醇 R2CHOH R3C-Cl Lucas试剂 立即浑浊
CH2Cl2 + H2O CH3Cl 225C 加压 OH HC OH OH H2O 165C 加压 OH H2C OH H2O O H C H O H C OH
9
(三)命名:
1.普通命名法:
适用于结构简单的醇,在醇前加烃基名称,称为“某醇”
CH3CH2OH CH3 2CHOH CH3 3COH
22
醇类物质不能用氯化钙、氯化镁做干燥剂。
(二)光谱性质
IR:-OH 未缔合时在3650-3500 cm-1有尖峰
缔合时在3500-3200 cm-1宽峰
C-O 吸收峰在1260-1000 cm-1 (1060-1030 cm-1
醇与水分子间氢键缔合
自正丁醇开始,随着烃基的增大,在水中的溶解度降 低,癸醇以上的醇几乎不溶于水。
21
多元醇分子中含有两个以上的羟基,可以形成更 多的氢键,所以分子中所含羟基越多,沸点越高, 在水中的溶解度也越大。
例:乙二醇 沸点:197℃ 甘油(丙三醇) 沸点:290℃。 低级醇能和一些无机盐类(MgCl2,CaCl2,CuSO4等) 形成结晶状的分子化合物,称为结晶醇。 CaCl2· 4CH3OH CaCl2· 4C2H5O H MgCl2· 6CH3OH MgCl2· 6C2H5OH
3o 醇 、烯丙醇、苄醇 室温下反应液立即混浊、分层; 2o醇 1o醇 2 ~ 5 min. 反应液混浊、分层; 加热,反应液混浊、分层;
31
Lucas试剂(无水ZnCl2与浓HCl配制的溶液)鉴别六 个碳以下的伯、仲、叔醇(烯丙式醇)
现象
R3C-OH 烯丙式醇 R2CHOH R3C-Cl Lucas试剂 立即浑浊
CH2Cl2 + H2O CH3Cl 225C 加压 OH HC OH OH H2O 165C 加压 OH H2C OH H2O O H C H O H C OH
9
(三)命名:
1.普通命名法:
适用于结构简单的醇,在醇前加烃基名称,称为“某醇”
CH3CH2OH CH3 2CHOH CH3 3COH
22
醇类物质不能用氯化钙、氯化镁做干燥剂。
(二)光谱性质
IR:-OH 未缔合时在3650-3500 cm-1有尖峰
缔合时在3500-3200 cm-1宽峰
C-O 吸收峰在1260-1000 cm-1 (1060-1030 cm-1
有机化学第8章 醇、酚、醚
8.11.3过氧化物的生成
醚对氧化剂比较稳定,但是,遇空气长期接触,却能被空气中 的氧逐渐氧化生成过氧化物。一般认为氧化是首先发生在 -C-H键上,然后再转变成结构更为复杂的过氧化物。
■另外,氧上电子云密度降低,使O-H键极性增加,酚羟基中H的
酸性增加。 共轭的结果使得:
1.酚羟基氢易于以质子的形式离去使酚显酸性;
2.苯环上的电子云密度增高易于进行亲电取代反应。
8.5.2命名
8.6酚的物理性质(自学)
8.7酚的化学性质
酚中羟基与苯环形成大的p—π共轭体系,由于氧的给电子共轭
醚键对强酸不稳定,遇强酸会发生醚键断裂,但HCl、HBr断裂
较难,需要催化剂;使醚键断裂最有效的试剂是浓的氢碘酸(HI)。 醚键的断裂是醚在HI中,先形成洋盐,然后,I-再作为亲核试 剂进攻-C而发生醚键断裂。 醚键断裂的顺序:30烷基>20烷基>10烷基>芳烃基
I-有两种进攻方向,但从电子效应和空间效应两方面看,都是
I-进攻甲基碳有利。所以,在混醚断键时,总是先从碳链较 小的一端断裂。如果 HI过量,则生成的醇可进一步生成碘代烃。
芳香混醚与浓HI作用时,总是断裂烷氧键,生成酚和碘代烷。
总结:
◆反应活性:HI>HBr>HCl ◆伯烷基醚按SN2机制断裂, ◆叔烷基醚按SN1机制断裂, ◆芳基烷基醚总是烷氧键断裂
碱性溶液中与烃基化剂(硫酸二甲酯、卤代烃等)作用生成。
羧酸与醇在酸催化下可以成酯,由于酚羟基中的氧与苯环发 生了p_π共轭其反应活性减小,与羧酸难于成酯。但可与活 性较大的酰基化试剂酰氯或酸酐成酯。
8.7.2芳环上的亲电取代反应
8.7.2.1卤代反应
反应很灵敏,很稀的苯酚溶液就能与溴水生成沉 淀。故此反应可用作苯酚的鉴别和定量测定。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
OH OH
OH OH
HO
OH
1,2-苯二酚 (邻苯二酚)
1,3-苯二酚 (间苯二酚)
1,4-苯二酚 (间苯二酚)
3.三元酚命名 命名时以苯三酚为母体,三个酚羟 基间的位置用阿拉伯数字或连、偏、对称等字表示。 例如:
OH
OH
OH
OH
OH OH
OH
HO OH
1,2,3-苯三酚 (连苯三酚)
1,2,4-苯三酚 (偏苯三酚)
甘油可与新配制的氢氧化铜反应,生成一种深蓝色 的溶液。此反应可以鉴别具有邻二醇结构的化合物。
CH2 CH CH2
OH OH OH Cu(OH)2
CH2 CH CH2
O O OH Cu 2H2O
甘油
甘油铜(深蓝色)
(四)苯甲醇(
CH2OH
)
苯甲醇又称苄醇,具有微弱的麻醉作用,既能镇 痛又能防腐。
(五)山梨醇和甘露醇
课堂互动
护理工作中常用浓度为70%~75%的酒精 作外用消毒剂,为什么说70%~75%的酒精
杀菌效果好于其他浓度的酒精?
(三)丙三醇(
CH2
CH
CH2
OH OH OH 丙三醇俗称甘油 ,有较强的吸湿性,可作助溶
)
剂能增加药物的溶解度。 临床上常用甘油栓或0.55的甘油水溶液(开塞
露)来灌肠润滑并刺激肠壁,软化大便,治疗便秘。
苯二酚有邻、间、对三种同分异构体,它们的结构
简式分别为:
OH
OH OH
OH
OH
OH
邻苯二酚
间苯二酚
对苯二酚
(四)乙醚
乙醚( CH3CH2OCH2CH3 )是具有特殊气味的无色液
体,极易挥发和着火,失火时不能用水扑灭。使用乙 醚时要特别小心。
乙醚具有麻醉作用,在外科手术中是使用较早的 麻醉剂之一。
本章小结
硬化、肝炎、脂肪肝、血中胆固醇过高等症。
案例
1918年西班牙流感肆虐欧洲
请问
1.“来苏儿”属于哪类有机物?指出其官能团。 2. 说出“来苏儿”的成分,写出其结构式。
第二节
酚和醚
一、酚和醚的结构、分类和命名
(一)酚的结构
酚:芳香烃分子中苯环上的氢原子被羟基取代后 生成的化合物。
酚的官能团: ‒OH 羟基又称酚羟基。
CH 2 OH
甘油
CH 2 ONO2 甘油三硝酸酯
酯化反应:醇与酸在强酸(如浓硫酸)催化下生成 酯和水的反应。
2.醇与无机含氧酸的酯化反应 人体内软骨中的硫酸
甘油三硝酸酯又称硝 酸甘油,稀释后制成0.3% 的硝酸甘油片剂,舌下给 药,可缓解冠状动脉狭窄 引起的心绞痛。
软骨素就含有硫酸酯结构; 生物体内广泛存在着磷酸 酯,例如组成细胞的重要 成分DNA、RNA和磷脂都具 有磷酸酯结构。
2. 与三氯化铁的显色反应
凡是具有烯醇式结构的
化合物都能与三氯化铁发生显色反应。
OH C C 烯醇式结构
OH H
2. 与三氯化铁的显色反应
苯酚和间-苯二酚 与 三 氯 化 铁 反 应
紫色
邻-苯二酚和对-苯二酚
绿色
甲酚
蓝色
3. 苯酚与溴水反应 鉴别。
OH
生成白色沉淀,常用于酚类的
OH Br + 3Br 2 Br Br + 3HBr
例如:
OH
OH CH3
苯酚
邻甲酚
(二)酚的分类和命名
1.一元酚命名 以苯酚为母体,编号从苯环上连有酚 羟基的碳原子开始,也可以用邻、间、对表示取代基与 酚羟基间的位置。例如:
OH
OH CH3
OH CH3
CH3
2-甲酚 (邻甲酚)
3-甲酚 (间甲酚)
4-甲酚 (对甲酚)
2.二元酚命名 命名时以苯二酚为母体,两个酚羟 基间的位置用阿拉伯数字或邻、间、对等字表示。例 如:
医用化学
第八章
醇、酚和醚
教学内容
01
第一节
醇
02
第二节
酚和醚
学习目标
1.掌握醇、酚的主要化学性质。 2.熟悉醇、酚和醚的结构及常见的醇、酚和醚 在医学上的应用。 3.了解醇和酚的分类及简单命名法。
案例
2009年7月的一天,郑州某司机无证、醉酒驾驶、
连撞11人,酿成3死8伤的重大事故;2011年5月的一天, 在北京发生一起交通事故;经乙醇检验,司机每百毫 升血液中乙醇含量为243.04mg,已构成醉酒驾车。 2013年8月的一天,广州某司机醉酒驾驶奔驰汽车飙车, 超速行驶,致3人死亡4人受伤。这些案件引起了恶劣 的社会影响,由于酒驾引发的一件件惨案给我们敲响 了警钟。
(二)甲酚
有邻、间、对三种同分异构体,结构简式分别为:
OH邻甲酚
间甲酚
对甲酚
甲酚杀菌能力比苯酚强,是常用的外用消毒剂和防 腐剂。
甲酚配成47%~53%的肥皂溶液称为甲酚皂溶液, 或煤酚皂溶液,俗称“来苏儿”。
课堂互动
不小心把“来苏儿”沾 到皮肤上如何处理?
(三)苯二酚
(二)主要化学性质
1.与活泼金属的反应
2CH3CH2OH+ 2Na
2 CH3CH2ONa+ H2
乙醇钠 乙醇钠溶液呈碱性,遇酚酞其溶液变红色。
CH3CH2ONa + H2O
CH3CH2OH+ NaOH
2.醇与无机含氧酸的酯化反应
CH 2 OH CH OH + 3HO NO2
硝酸
H 2 SO4
CH 2 ONO 2 CH ONO2 + 3H2O
例如:
CH3 CH3 CH CH2OH
2-甲基-1-丙醇
CH3 CH CH2 CH3 OH
2-丁醇
CH3 CH OH
CH CH3
CH3
3-甲基-2-丁醇
二、醇的性质
(一)物理性质
常温常压下,C1~C4的低级醇为无色透明、 易挥发的液体,具有酒味,易溶于水。 但随着碳原子数的增多,溶解度逐渐降低, 从C7以上的醇基本不溶于水,溶于丙酮和乙醚 等有机溶剂。
命名
主要化 学性质
常见的 醇酚醚
结构 通式
醇: R-OH 酚: Ar-OH Ar-CH2-OH 醚: (Ar)R-O-R(Ar) 酚:酚羟基 —OH 醇:醇羟基 —OH
官能团
醚:醚键
C-O-C
分类
醇 酚 醚
醇:1.脂肪醇、脂环醇和芳香醇 2.伯醇、仲醇和叔醇 3.一元醇和多元醇 酚:一元酚、二元酚和多元酚 醚:单醚和混醚,又分饱和醚、不饱和醚、芳香醚 醇:普通命名法和系统命名法 酚:以酚为母体,确定取代基位置命名 醚:单醚称“某醚”,混醚根据烃基不同称“某某醚” 醇:1.与活泼金属的反应 2.与无机含氧酸的酯化反应 3.氧化反应 酚:1.弱酸性 2.与三氯化铁的显色反应 3.与溴水反应 4.氧化反应 醇:甲醇 乙醇 丙三醇 苯甲醇 山梨醇和甘露醇 环己六醇 酚:苯酚 甲酚 苯二酚 醚:乙醚
氧化,所以常带有不同程度的红色或暗红色。 酚能与水分子形成氢键,微溶于水,能溶于 乙醇、乙醚、苯等有机溶剂。
(二)主要化学性质
1. 弱酸性
OH + NaOH ONa + H2O
现象:浑浊液逐渐变澄清
ONa + CO2 + H2O OH + NaHCO 3
现象:澄清液又变浑浊
鉴别酚与有机酸
酚有弱酸性能和碱性较强的Na2CO3反应, 而不能和NaHCO3反应,所以可用NaHCO3鉴别。
CH3-CH2-O-CH2-CH3 乙醚
O
二苯醚
例如: 混醚:命名时较小的烃基 的名称放在前面,较大的 烃基的名称放在后面,芳 香烃基的名称放在脂肪烃 基的前面,然后再加上 “醚”字。 CH3-O-CH2-CH3 甲乙醚
O CH3
苯甲醚
二、酚的性质
(一)物理性质
酚具有特殊的气味,有毒,对皮肤有腐 蚀作用。纯净的酚无色,但由于酚易被空气
二者是同分异构体,又名己六醇。
CH2 CH OH OH
CH CH OH OH
CH
CH2
OH OH
临床上用20%甘露醇溶液作组织脱水药,渗 透性利尿药。 山梨醇和50%的高渗葡萄糖溶液主要用于脑 水肿和急性肺水肿,效果不如甘露醇。
HO
OH OH
(六)环己六醇 ( HO
HO OH
)
环己六醇又称肌醇、肌糖。主要用于治疗肝
R
C
乙醛
H
[O]
R
COOH
乙酸
三、常见的醇在医学上的应用
(一)甲醇(CH3OH)
甲醇是假酒的主要成分,摄入少量就可引起中毒, 误饮10ml即可失明、误饮30ml即死亡。
(二)乙醇(CH3CH2OH)
药用酒精 B=95% 消毒酒精 B=70%~75%
医学工作 中的酒精
擦浴酒精 B=25%~50% 按摩酒精 B=40%~50%
1,3,5-苯三酚 (对称苯三酚)
(三)醚的结构、分类和命名
1.醚的结构 两个烃基通过一个氧原子连接起来的
化合物称为醚。
醚的结构通式:(Ar)R-O-R(Ar) 醚的官能团: 例如: CH3OCH3 甲醚 苯甲醚
O CH3
C O C
醚键
2. 醚的分类和命名 例如:
单醚:与氧原子相连的两 个烃基相同的醚。命名时 写出烃基名称,称为“某 醚”。烃基是烷基时, “二”字省略,是芳香烃 基保留“二”字。
官能团:‒OH 羟基又称醇羟基。
例如:
OH
CH3-CH2-OH
CH2OH
(二)醇的分类
按羟基所连 的烃基分 脂肪醇 CH3OH 脂环醇 伯醇 按羟基所连 碳原子分 按羟基的 数目分
OH OH
HO
OH
1,2-苯二酚 (邻苯二酚)
1,3-苯二酚 (间苯二酚)
1,4-苯二酚 (间苯二酚)
3.三元酚命名 命名时以苯三酚为母体,三个酚羟 基间的位置用阿拉伯数字或连、偏、对称等字表示。 例如:
OH
OH
OH
OH
OH OH
OH
HO OH
1,2,3-苯三酚 (连苯三酚)
1,2,4-苯三酚 (偏苯三酚)
甘油可与新配制的氢氧化铜反应,生成一种深蓝色 的溶液。此反应可以鉴别具有邻二醇结构的化合物。
CH2 CH CH2
OH OH OH Cu(OH)2
CH2 CH CH2
O O OH Cu 2H2O
甘油
甘油铜(深蓝色)
(四)苯甲醇(
CH2OH
)
苯甲醇又称苄醇,具有微弱的麻醉作用,既能镇 痛又能防腐。
(五)山梨醇和甘露醇
课堂互动
护理工作中常用浓度为70%~75%的酒精 作外用消毒剂,为什么说70%~75%的酒精
杀菌效果好于其他浓度的酒精?
(三)丙三醇(
CH2
CH
CH2
OH OH OH 丙三醇俗称甘油 ,有较强的吸湿性,可作助溶
)
剂能增加药物的溶解度。 临床上常用甘油栓或0.55的甘油水溶液(开塞
露)来灌肠润滑并刺激肠壁,软化大便,治疗便秘。
苯二酚有邻、间、对三种同分异构体,它们的结构
简式分别为:
OH
OH OH
OH
OH
OH
邻苯二酚
间苯二酚
对苯二酚
(四)乙醚
乙醚( CH3CH2OCH2CH3 )是具有特殊气味的无色液
体,极易挥发和着火,失火时不能用水扑灭。使用乙 醚时要特别小心。
乙醚具有麻醉作用,在外科手术中是使用较早的 麻醉剂之一。
本章小结
硬化、肝炎、脂肪肝、血中胆固醇过高等症。
案例
1918年西班牙流感肆虐欧洲
请问
1.“来苏儿”属于哪类有机物?指出其官能团。 2. 说出“来苏儿”的成分,写出其结构式。
第二节
酚和醚
一、酚和醚的结构、分类和命名
(一)酚的结构
酚:芳香烃分子中苯环上的氢原子被羟基取代后 生成的化合物。
酚的官能团: ‒OH 羟基又称酚羟基。
CH 2 OH
甘油
CH 2 ONO2 甘油三硝酸酯
酯化反应:醇与酸在强酸(如浓硫酸)催化下生成 酯和水的反应。
2.醇与无机含氧酸的酯化反应 人体内软骨中的硫酸
甘油三硝酸酯又称硝 酸甘油,稀释后制成0.3% 的硝酸甘油片剂,舌下给 药,可缓解冠状动脉狭窄 引起的心绞痛。
软骨素就含有硫酸酯结构; 生物体内广泛存在着磷酸 酯,例如组成细胞的重要 成分DNA、RNA和磷脂都具 有磷酸酯结构。
2. 与三氯化铁的显色反应
凡是具有烯醇式结构的
化合物都能与三氯化铁发生显色反应。
OH C C 烯醇式结构
OH H
2. 与三氯化铁的显色反应
苯酚和间-苯二酚 与 三 氯 化 铁 反 应
紫色
邻-苯二酚和对-苯二酚
绿色
甲酚
蓝色
3. 苯酚与溴水反应 鉴别。
OH
生成白色沉淀,常用于酚类的
OH Br + 3Br 2 Br Br + 3HBr
例如:
OH
OH CH3
苯酚
邻甲酚
(二)酚的分类和命名
1.一元酚命名 以苯酚为母体,编号从苯环上连有酚 羟基的碳原子开始,也可以用邻、间、对表示取代基与 酚羟基间的位置。例如:
OH
OH CH3
OH CH3
CH3
2-甲酚 (邻甲酚)
3-甲酚 (间甲酚)
4-甲酚 (对甲酚)
2.二元酚命名 命名时以苯二酚为母体,两个酚羟 基间的位置用阿拉伯数字或邻、间、对等字表示。例 如:
医用化学
第八章
醇、酚和醚
教学内容
01
第一节
醇
02
第二节
酚和醚
学习目标
1.掌握醇、酚的主要化学性质。 2.熟悉醇、酚和醚的结构及常见的醇、酚和醚 在医学上的应用。 3.了解醇和酚的分类及简单命名法。
案例
2009年7月的一天,郑州某司机无证、醉酒驾驶、
连撞11人,酿成3死8伤的重大事故;2011年5月的一天, 在北京发生一起交通事故;经乙醇检验,司机每百毫 升血液中乙醇含量为243.04mg,已构成醉酒驾车。 2013年8月的一天,广州某司机醉酒驾驶奔驰汽车飙车, 超速行驶,致3人死亡4人受伤。这些案件引起了恶劣 的社会影响,由于酒驾引发的一件件惨案给我们敲响 了警钟。
(二)甲酚
有邻、间、对三种同分异构体,结构简式分别为:
OH邻甲酚
间甲酚
对甲酚
甲酚杀菌能力比苯酚强,是常用的外用消毒剂和防 腐剂。
甲酚配成47%~53%的肥皂溶液称为甲酚皂溶液, 或煤酚皂溶液,俗称“来苏儿”。
课堂互动
不小心把“来苏儿”沾 到皮肤上如何处理?
(三)苯二酚
(二)主要化学性质
1.与活泼金属的反应
2CH3CH2OH+ 2Na
2 CH3CH2ONa+ H2
乙醇钠 乙醇钠溶液呈碱性,遇酚酞其溶液变红色。
CH3CH2ONa + H2O
CH3CH2OH+ NaOH
2.醇与无机含氧酸的酯化反应
CH 2 OH CH OH + 3HO NO2
硝酸
H 2 SO4
CH 2 ONO 2 CH ONO2 + 3H2O
例如:
CH3 CH3 CH CH2OH
2-甲基-1-丙醇
CH3 CH CH2 CH3 OH
2-丁醇
CH3 CH OH
CH CH3
CH3
3-甲基-2-丁醇
二、醇的性质
(一)物理性质
常温常压下,C1~C4的低级醇为无色透明、 易挥发的液体,具有酒味,易溶于水。 但随着碳原子数的增多,溶解度逐渐降低, 从C7以上的醇基本不溶于水,溶于丙酮和乙醚 等有机溶剂。
命名
主要化 学性质
常见的 醇酚醚
结构 通式
醇: R-OH 酚: Ar-OH Ar-CH2-OH 醚: (Ar)R-O-R(Ar) 酚:酚羟基 —OH 醇:醇羟基 —OH
官能团
醚:醚键
C-O-C
分类
醇 酚 醚
醇:1.脂肪醇、脂环醇和芳香醇 2.伯醇、仲醇和叔醇 3.一元醇和多元醇 酚:一元酚、二元酚和多元酚 醚:单醚和混醚,又分饱和醚、不饱和醚、芳香醚 醇:普通命名法和系统命名法 酚:以酚为母体,确定取代基位置命名 醚:单醚称“某醚”,混醚根据烃基不同称“某某醚” 醇:1.与活泼金属的反应 2.与无机含氧酸的酯化反应 3.氧化反应 酚:1.弱酸性 2.与三氯化铁的显色反应 3.与溴水反应 4.氧化反应 醇:甲醇 乙醇 丙三醇 苯甲醇 山梨醇和甘露醇 环己六醇 酚:苯酚 甲酚 苯二酚 醚:乙醚
氧化,所以常带有不同程度的红色或暗红色。 酚能与水分子形成氢键,微溶于水,能溶于 乙醇、乙醚、苯等有机溶剂。
(二)主要化学性质
1. 弱酸性
OH + NaOH ONa + H2O
现象:浑浊液逐渐变澄清
ONa + CO2 + H2O OH + NaHCO 3
现象:澄清液又变浑浊
鉴别酚与有机酸
酚有弱酸性能和碱性较强的Na2CO3反应, 而不能和NaHCO3反应,所以可用NaHCO3鉴别。
CH3-CH2-O-CH2-CH3 乙醚
O
二苯醚
例如: 混醚:命名时较小的烃基 的名称放在前面,较大的 烃基的名称放在后面,芳 香烃基的名称放在脂肪烃 基的前面,然后再加上 “醚”字。 CH3-O-CH2-CH3 甲乙醚
O CH3
苯甲醚
二、酚的性质
(一)物理性质
酚具有特殊的气味,有毒,对皮肤有腐 蚀作用。纯净的酚无色,但由于酚易被空气
二者是同分异构体,又名己六醇。
CH2 CH OH OH
CH CH OH OH
CH
CH2
OH OH
临床上用20%甘露醇溶液作组织脱水药,渗 透性利尿药。 山梨醇和50%的高渗葡萄糖溶液主要用于脑 水肿和急性肺水肿,效果不如甘露醇。
HO
OH OH
(六)环己六醇 ( HO
HO OH
)
环己六醇又称肌醇、肌糖。主要用于治疗肝
R
C
乙醛
H
[O]
R
COOH
乙酸
三、常见的醇在医学上的应用
(一)甲醇(CH3OH)
甲醇是假酒的主要成分,摄入少量就可引起中毒, 误饮10ml即可失明、误饮30ml即死亡。
(二)乙醇(CH3CH2OH)
药用酒精 B=95% 消毒酒精 B=70%~75%
医学工作 中的酒精
擦浴酒精 B=25%~50% 按摩酒精 B=40%~50%
1,3,5-苯三酚 (对称苯三酚)
(三)醚的结构、分类和命名
1.醚的结构 两个烃基通过一个氧原子连接起来的
化合物称为醚。
醚的结构通式:(Ar)R-O-R(Ar) 醚的官能团: 例如: CH3OCH3 甲醚 苯甲醚
O CH3
C O C
醚键
2. 醚的分类和命名 例如:
单醚:与氧原子相连的两 个烃基相同的醚。命名时 写出烃基名称,称为“某 醚”。烃基是烷基时, “二”字省略,是芳香烃 基保留“二”字。
官能团:‒OH 羟基又称醇羟基。
例如:
OH
CH3-CH2-OH
CH2OH
(二)醇的分类
按羟基所连 的烃基分 脂肪醇 CH3OH 脂环醇 伯醇 按羟基所连 碳原子分 按羟基的 数目分
