8.2.2内部审核
质量管理基础知识

质量管理基础知识1.质量:一组固有特性满足要求的程度。
固有特性(产品、过程或体系与要求有关的固有特性)特性赋予特性要求:指明示的、通常隐含的或必须履行的需求或期望。
质量具有广义性、时效性和相对性。
2.质量管理:在质量方面指挥和控制组织的协调的活动。
全面质量管理(TQM):以质量为中心,以全员参与为基础,目的在于通过让顾客满意和本组织所有者、员工、供方、合作伙伴或相关方受益而达到长期成功的一种管理途径。
质量管理发展的三个阶段:质量检验阶段,统计质量控制阶段、全面质量管理阶段。
3. 顾客4. PDCA循环(戴明环):是由计划(plan)----实施(do)----检查(check)----处置(action)4个要素构成的一个循环的持续改进的工作方法。
特点:完整的循环,逐步上升的循环,大中套小的循环5.质量管理的八项原则:①以顾客为关注焦点组织依存于其顾客。
因此,组织应理解顾客当前的和未来的需求,满足顾客要求并争取超越顾客期望。
组织所需采取的活动:1、全面了解顾客的需求和期望,包括当前的和未来的;2、确保组织的各项目标,包括质量目标能体现顾客的需求和期望。
3、确保顾客的需求和期望在整个组织中得到沟通。
4、满足顾客要求并争取超越顾客的期望。
5、测量顾客的满意程度并采取相应的活动和措施。
6、处理好与顾客的关系,力求顾客满意。
7、确保兼顾其他相关方的利益,使组织得到全面、持续的发展。
②领导作用领导者建立组织统一的宗旨及方向。
他们应当创造并保持使员工能充分参与实现组织目标的内部环境。
最高管理者应采取的措施:1、考虑所有相关方的需求和期望。
2、为本组织的未来描绘清晰的远景,制定质量方针和质量目标。
3、在整个组织及各级、各层次制定富有挑战性的目标。
4、在组织各级创造并坚持一种共同的价值观,并树立职业道德榜样,形成企业的精神和企业文化。
5、使全体员工工作在一个比较宽松、和谐的环境之中,建立信任,消除忧虑。
6、为员工提供所需的资源、培训及在职责范围内的自主权。
ISO13485审核重点

ISO13485审核重点(一)
当顾客抱怨没有采取预防和(或)纠正措施, 则其理由应予以批准(见5.5.1)并记录。 如果国家或地区法规要求通告符合规定报告 准则的不良事件,组织应建立告知行政主管部 门的形成文件的程序。
ISO13485审核重点(一)
7 产品实现 7.1 产品实现的策划 --组织应在产品实现全过程中,建立风险管 理的形成文件的要求。应保持风险管理引起的 记录 --风险管理的有关措施的文件化、实施
ISO13485审核重点(一)
7.2 与顾客有关的过程 7.2.1 与产品有关要求的确认 7.2.2 与产品有关要求的评审 7.2.3 顾客沟通 --忠告性通知
ISO13485审核重点(一)
--作为设计和开发确认活动的一部分,如国家或 地区的法规要求(见注2),组织应实施医疗 器械临床评价和(或)性能评价。 注1:如果医疗器械只能在使用现场进行组装 和安装后进行确认,则该医疗器械直到正式转 交给顾客后才可认为是完成交付。 注2:为了临床评价和(或)性能评价提供医 疗器械,不认为是交付。 7.3.7设计和开发更改的控制
ISO13485审核重点(一)
7.3 设计和开发 7.3.1 设计和开发的策划 --组织应建立设计和开发的形成文件的程序 7.3.2 设计和开发的输入 --风险管理的输出 --应对这些输入进行评审,以确保输入是充分与 适宜的,并经批准
Leabharlann ISO13485审核重点(一)
7.3.3 设计和开发的输出 --应保持设计和开发输出的记录。 --设计和开发输出的记录可包括规范、制造程序 、工程图纸、工程或研究历程记录。 7.3.4 设计和开发的评审 7.3.5 设计和开发的验证 7.3.6 设计和开发的确认
内审计划、内审记录及内审报告

审核目的:检查质量管理体系运行的有效性和符合性,通过纠正与预防措施进一步提高质量管理体系的适宜性和有效性,持续改进公司总体绩效。
审核范围:公司产品、活动和服务涉及的所有部门、人员、场所和过程。
依据标准/程序要求:GB/T19001-2022 标准;公司质量管理体系文件;国家、行业及地方有关的法律法规、标准及其他相关文件。
内审组长:内审员:审核日程表2022- 12-25时间08:30-09:0009:00-12:0013:30-17:30审核地点/活动/过程/要素首次会议管理层: 1.2/4.1/4.2.1/4.2.2/5.1/5.2/5.3/5.4/5.5/5.6/6.1/8.1/8.2.2/8.5.1综合部: 5.4.1/5.5.1/4.2.3/4.2.4/6.2/7.4/8.2.2/8.5.12022- 13:30-17:3008:30-12:0013:30-15:30生产技术部:5.4.1/5.5.1/6.3/6.4/7.1/7.3/7.5继续审核生产技术部:7.6/8.2.3/8.2.4/8.3/8.4/8.5.2/8.5.3营销部:5.4.1/5.5.1/7.2/8.2.1审核员全员日期1、检查公司 QMS 质量管理体系运行的符合性、有效性;2、评价公司各主要业务流程的运营管理效率及改进点。
1、公司质量管理体系覆盖的所有范围。
2、公司所有职能部门。
1、公司质量质量管理体系文件、管理制度及主要业务流程。
2、GB/T19001-2022 质量质量管理体系要求;3、国家、行业和地方法律法规、国家标准及其他要求。
内审组长:内审员:涵盖 GB/T19001-2022 质量管理体系全条款。
从审核结果来看,公司质量管理体系已基本建立,运行三个多月来切实可行有效,各部门主要业务流程已基本成型,流程执行意识有所加强。
经过抽样检查,共发现 1 个不符合项,具体情况详见《内审不符合报告》。
各部门的质量管理体系文件应有专人管理,各过程运转都要求建立和保留客观的记录证据,而在我们的审核中发现营销部的质量手册、程叙文件无法找到,不少部门都没有受控文件清单;记录不完整(例如:营销部的部份表格该记录的,没有记录,该审批的没有审批)或者未做记录现象较多,如综合部组织过新员工入职培训但无相应的培训记录。
内审检查表

内审检查表编号:
记录人:第页共页
内审检查表编号:
记录人:第页共页
内审检查表编号:
记录人:第页共页
内审检查表编号:
记录人:第页共页
内审检查表编号:
记录人:第页共页
内审检查表编号:
记录人:第页共页
内审检查表编号:
长史、参军,此悉贞良死节之臣,愿陛下亲之、信之,则汉室之隆,可计日而待也。
先帝知臣谨慎,故临崩寄臣以大事也。
受命以来,夙夜忧叹,恐托付不效,以伤先帝之明;故五月渡泸,深入不毛。
今南方已定,兵甲已足,当奖率三军,北定中原,庶竭驽钝,攘除奸凶,兴复汉室,还于旧都。
此臣所以报先帝而忠陛下之职分也。
至于斟酌损益,进尽忠言,则攸之、祎、允之任也。
愿陛下托臣以讨贼兴复之效,不效,则治臣之罪,以告先帝之灵。
若无兴德之言,则责攸之、祎、允等之慢,以彰其咎;陛下亦宜自谋,以咨诹善道,察纳雅言,深追先帝遗诏。
臣不胜受恩感激。
今当远离,临表涕零,不知所言。
ISO9000内审员试题答案

内部审核员复习题姓名:单位:年月日一:讨论及思考1、9000标准覆盖有哪四类通用产品?各有何特点?硬件、软件、效劳、流程性材料。
1)硬件:有形、形状固定、可计数。
2)软件:无形、由信息组成,需要载体。
3)效劳:无形、在及顾客的接触时完成的活动。
4)流程性材料:有形、形态和形状多样,可计量。
2、9000族标准中的4个核心标准的名称及适用范围是什么?1〕9000 质量管理体系根底和术语:根底理论2〕9001质量管理体系要求:审核依据;选用的组织强制执行3〕9004 质量管理体系业绩改良指南:改良指南4〕19011 质量和〔或〕环境管理体系审核指南:内、外部审核管理3、什么是管理评审?谁参加?谁主持?评审什么?1〕管理评审是组织战略筹划活动之一,是组织高层领导对质量管理体系决策性质量筹划活动,是最高管理者的任务之一,是对照质量方针和质量目标,定期和系统的评价质量管理体系的适宜性、充分性、有效性和效率。
2)公司的高层领导、管理层和内审员参加。
3)公司的最高管理者主持。
4)评审内容:对照质量方针和质量目标,定期和系统的评价质量管理体系的适宜性、充分性、有效性和效率。
4、简述质量管理的八项原那么。
1)以顾客为关注焦点2)领导作用3)全员参及4)过程方法5)管理的系统方法6)持续改良7)基于事实的决策方法8)及供方互利的关系5、制定质量方针和质量目标的根本要求是什么?质量方针的根本要求:1)及组织的宗旨相适应2)包括对满足要求和持续改良有效性的承诺3)提供制定和评审质量目标的框架4)在组织内得到沟通和理解5)在持续适宜性方面得到评审质量目标的根本要求:1)应在组织的相关职能和层次上建立质量目标2)包括满足产品要求所需的内容3)应是可测量、可考核的4)应及质量方针保持一致,能通过目标实现方针6、应对哪些人规定其职责和权限?所有员工都应被赋予相应的职责和权限,从而使他们为实现质量目标做出奉献。
7、管理者代表职责是什么?由谁担任?职责:1)确保质量管理体系所需的过程得到建立、实施和保持。
IT内审检查表
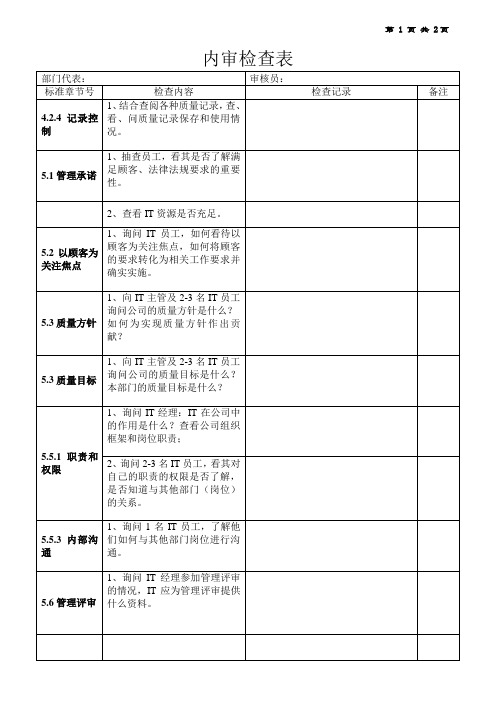
1、询问1名IT员工,了解他们如何与其他部门岗位进行沟通。
5.6管理评审
1、询问IT经理参加管理评审的情况,IT应为管理评审提供什么资料。
标准章节号
检查内容
检查记录
备注
6.2人力资源
1.询问IT主管,公司是如何开展IT服务的。
确认:
a、需求是否明确。
b、是否所有对质量有影响的人员都纳入培训之中。
5.3质量方针
1、向IT主管及2-3名IT员工询问公司的质量方针是什么?
如何为实现质量方针作出贡献?
5.3质量目标
1、向IT主管及2-3名I标是什么?
5.5.1职责和权限
1、询问IT经理:IT在公司中的作用是什么?查看公司组织框架和岗位职责;
2、询问2-3名IT员工,看其对自己的职责的权限是否了解,是否知道与其他部门(岗位)的关系。
2、现场检查工作环境管理的有效性。
8.2.2内部审核
1、询问是否定期接受内部质量体系审核?如何对待?
2、查阅最近1次内审时发现的不合格项报告以及纠正措施的实施与验证记录。
8.5改进
1、询问参加改进、纠正及预防措施的情况
编制/日期:
审批/日期:
内审检查表
部门代表:
审核员:
标准章节号
检查内容
检查记录
备注
4.2.4记录控制
1、结合查阅各种质量记录,查、看、问质量记录保存和使用情况。
5.1管理承诺
1、抽查员工,看其是否了解满足顾客、法律法规要求的重要性。
2、查看IT资源是否充足。
5.2以顾客为关注焦点
1、询问IT员工,如何看待以顾客为关注焦点,如何将顾客的要求转化为相关工作要求并确实实施。
最新CCAA-QMS国家注册审核员考试大纲
C C A A-Q M S国家注册审核员考试大纲CCAA QMS国家注册审核员考试大纲3.基础知识部分的考试范围和内容3.1 范围a. 注册准则2.3.1 个人素质b. 注册准则2.4.1.2 质量管理体系c. 注册准则2.4.1.3 法律法规3.2 内容3.2.1 GB/T 19001—2008标准(以下序号以GB/T 19001—2008标准的条款号为序)理解本条款中列出的内容0 引言a. 影响组织质量管理体系的设计和实施的6个因素b. 标准的目的、用途、质量管理体系要求与产品要求的关系c. 过程方法、PDCA的含义d. GB/T 19001与GB/T 19004标准的关系e. GB/T 19001标准与其他管理体系标准的相容性1 范围a. GB/T 19001-2008标准的适用范围b.遵守法律与符合标准的关系,满足产品要求应包含的几项内容c.标准中,术语“产品”适用的范围2 应用:标准要求的通用性、“删减”的原则3 引用标准:GB/T 19001-2008标准4 质量管理体系4.1总要求a. 建立、实施、保持质量管理体系并持续改进有效性的总体思路b. 外包过程的含义、识别和控制要求及影响对外包过程控制的类型和程度的3个因素c. 外包过程和7.4的关系4.2文件要求a. 质量管理体系文件类型b. 质量手册必须包括的内容c. 文件控制的目的和重要性,文件控制包括的七个方面的内容d. 记录与文件的关系及控制要求,记录的作用5 管理职责5.1管理承诺的内容和证据5.2以顾客为关注焦点的体现,与7.2.1条款、8.2.1条款的关系5.3质量方针的制定要求和管理要求a. 质量方针应包括的两个承诺、一个框架b. 质量方针的管理要求及与质量目标的关系5.4策划的控制要点a. 质量管理体系策划与标准4.1条款和质量目标的关系b. 质量目标应包括的内容,质量目标的管理要求c. 质量管理体系策划的内容与要求5.5职责权限和沟通a. 内部沟通的内容、目的、方法和措施5.6管理评审a. 管理评审的目的与要求b. 管理评审输入、输出内容6 资源管理6.1需要确定和提供资源的两个方面6.2人力资源a. 考虑的四个方面的因素,对人员具备能力能够胜任的要求b. 直接或间接地影响产品要求符合性的人员的范围c. 满足人员能力要求的措施及其评价,记录的要求6.3对基础设置控制的范围和要求6.4对工作环境所涉及的对象、范围、要求和内容7 产品实现7.1产品实现策划a. 产品实现策划的对象、范围及4项内容b. 质量策划和质量计划的理解7.2与顾客有关的过程a. 产品要求包括的4个方面,交付后活动的内容b. 产品要求评审的目的、对象、时机、方法和内容c. 组织与顾客沟通的安排与控制7.3设计和开发a. 产品设计和开发策划应确定的内容b. 产品设计输入与设计输出包括的内容,设计输入与输出的关系c. 产品设计评审、设计验证、设计确认的内涵、区别和方法(可单独或以任意组合的方式进行并记录)d. 产品设计更改的控制要点7.4采购a. 对供方评价和选择的要求,评价的方法b. 评价、选择和再评价供方的准则c. 采购过程的控制要求d. 对采购信息的基本要求,采购信息的内容应充分和适宜e. 适当时应采购信息应包括的三个方面的要求的具体含义f. 采购产品的验证7.5生产和服务提供a. 生产和服务提供的策划及其控制的对象、范围和要点b. 交付后活动的类型c. 过程确认的目的、对象和要求d. 标识的三种形式和作用及其区别e. 顾客财产识别、控制的范围及控制要求f. 产品防护涉及的对象、内容、要求与方式7.6 监视和测量设备的控制a. 监视和测量活动的区别,监视和测量的范围,校准和检定(验证)的关系b. 对测量设备的控制要求c. 发现设备部符合要求时,组织应该采取的措施d. 校准和验证(检定)结果的记录要求e. 对用于监视和测试的计算机软件的确认要求8 测量、分析和改进8.1总则a. 对监视、测试、分析和改进过程策划的要求、范围和目的b. 对包括统计技术在内的适用方法的确定要求8.2顾客满意a. “顾客满意”的概念及识别和获取的要求b. 对“顾客满意”的信息获取、利用的要求c. 获取“顾客满意”的信息的方法8.2.2内部审核a. 内部审核的时机、目的、作用及实施要求b. 审核方案的策划要求c. 编制形成文件的程序的要求及程序文件的内容d. 审核的独立性和公正性要求,审核员的选择e. 纠正和纠正措施要求及跟踪活动要求8.2.3过程的监视和测量过程监视和测量的目的、对象、内容、方法及要求8.2.4产品的监视和测量a. 产品监视和测量的目的、对象、时机和记录的要求b. 向顾客放行产品和交付服务的要求8.3不合格品控制a. 对不合格品控制和处置的目的和要求b. 编制形成文件的程序的要求c. 纠正后再验证的要求8.4数据分析数据分析的目的、输入和输出的要求8.5改进a. 持续改进的概念,持续改进的方法和活动b. 纠正、纠正措施和预防措施的目的和要求3.2.2 GB/T 19000—2008标准理解、质量管理工具相关知识1 八项质量管理原则a. 八项质量管理原则的含义b. 八项质量管理原则在GB/T 19001—2008标准中的体现和应用2 质量管理体系基础重点理解以下基础:a.质量管理体系要求和产品要求的区别和相互关系b.过程方法c. 文件的价值d. 持续改进e.统计技术的作用3 术语和定义了解GB/T 19000-2008标准中的所有术语和定义。
质量管理体系审核中常见的不符合项
质量管理体系审核中常见的不符合项1、质量手册(标准条款4.2.2)(1)各部门执行的文件与手册的规定不一致。
(2)质量手册未包括或引用形成文件的程序。
(3)对标准的剪裁不合理。
(4)质量手册不是最高管理者签发。
(5)质量手册不能完整反映该组织的性质特点。
(6)程序文件中规定的控制和操作方法与现行的运用不一致。
(7)程序文件与质量手册不协调一致。
(8)质量手册的发布、修改、管理比较混乱不能保证最新有效版本在现场使用2、文件控制(标准条款4.2.3)(1)程序没涉及失效文件的控制。
(2)外来文件、发外文件未列人控制范围。
(3)电子媒体和其他形式的文件未受控。
(4)发布的文件无批准人。
(5)不能识别文件的修订状态。
(6)未标识保存的作废文件。
(7)外来文件没有办理识别性的手续。
(8)未对文件进行定期评审。
(9)文件的发放没有控制,随便复制。
(10)保管不善,不能迅速出示文件。
(11)文件更改记录没有或不适当。
(12)文件被非授权人复制或更改。
(13)现场使用的文件不是有效版本,或有效版本与作废版本并存。
3、记录控制(标准条款4.2.4)(1)供方的质量记录未纳人控制范围。
(2)未规定电子媒体形式的质量记录控制方法。
(3)质量记录保存环境不符合要求。
(4)质量记录未规定标识、贮存、保护、保存期、处置的方法。
(5)质量记录填写不全,质量记录上无记录者签名。
二、管理职责(标准条款:5)1、管理承诺(标准条款5.1)(1)最高管理者不知道对管理承诺应提供哪些证据。
(2)组织成员对质量方针、质量目标各有各的理解。
(3)资源配置不足,检验人员素质差,内审人员未经培训。
2、以顾客为关注焦点(标准条款5.2)(1)拿不出文件证实顾客的要求已得到确定。
3、质量方针(标准条款5.3)(1)质量方针空洞,体现不出企业特色,与质量目标的关系不明确。
(2)下级人员不清楚质量方针。
(3)拿不出对质量方针的评审证据。
(4)有的部门也制订了质量方针。
内审检查表表填写范例
Q3/8.2.2—03 审核检查表编号:
Q3/8.2.2--03 审核检查表编号:
Q3/8.2.2--03审核检查表编号:
3 / 27
Q3/8.2.2--03审核检查表编号:
Q3/8.2.2--03审核检查表编号:
5 / 27
Q3/8.2.2--03审核检查表序号
Q3/8.2.2--03审核检查表序号
7 / 27
Q3/8.2.2--03审核检查表序号
Q3/8.2.2--03审核检查表序号
9 / 27
Q3/8.2.2--03审核检查表序号
Q3/8.2.2--03审核检查表序号
11 / 27
Q3/8.2.2--03审核检查表序号
Q3/8.2.2--03审核检查表序号
13 / 27
Q3/8.2.2--03审核检查表序号
Q3/8.2.2-03审核检查表序号
15 / 27
Q3/8.2.2-03审核检查表序号
Q3/8.2.2--03审核检查表序号
17 / 27
Q3/8.2.2--03审核检查表序号
Q3/8.2.2--03审核检查表序号
19 / 27
Q3/8.2.2--03审核检查表序号
Q3/8.2.2--03审核检查表序号
21 / 27
Q3/8.2.2--03审核检查表序号
Q3/8.2.2--03审核检查表序号
23 / 27
Q3/8.2.2--03审核检查表序号
Q3/8.2.2--03审核检查表序号
25 / 27
Q3/8.2.2--03审核检查表序号
27 / 27。
质量管理体系审核中常见的不符合项
质量管理体系审核中常见的不符合项1、质量手册(标准条款4。
2.2)(1)各部门执行的文件与手册的规定不一致。
(2)质量手册未包括或引用形成文件的程序.(3)对标准的剪裁不合理.(4)质量手册不是最高管理者签发。
(5)质量手册不能完整反映该组织的性质特点.(6)程序文件中规定的控制和操作方法与现行的运用不一致。
(7)程序文件与质量手册不协调一致.(8)质量手册的发布、修改、管理比较混乱不能保证最新有效版本在现场使用2、文件控制(标准条款4.2。
3)(1)程序没涉及失效文件的控制。
(2)外来文件、发外文件未列人控制范围.(3)电子媒体和其他形式的文件未受控。
(4)发布的文件无批准人。
(5)不能识别文件的修订状态。
(6)未标识保存的作废文件.(7)外来文件没有办理识别性的手续。
(8)未对文件进行定期评审。
(9)文件的发放没有控制,随便复制.(10)保管不善,不能迅速出示文件.(11)文件更改记录没有或不适当.(12)文件被非授权人复制或更改。
(13)现场使用的文件不是有效版本,或有效版本与作废版本并存。
3、记录控制(标准条款4。
2。
4)(1)供方的质量记录未纳人控制范围.(2)未规定电子媒体形式的质量记录控制方法. (3)质量记录保存环境不符合要求。
(4)质量记录未规定标识、贮存、保护、保存期、处置的方法.(5)质量记录填写不全,质量记录上无记录者签名.二、管理职责(标准条款:5)1、管理承诺(标准条款5。
1)(1)最高管理者不知道对管理承诺应提供哪些证据。
(2)组织成员对质量方针、质量目标各有各的理解。
(3)资源配置不足,检验人员素质差,内审人员未经培训。
2、以顾客为关注焦点(标准条款5。
2)(1)拿不出文件证实顾客的要求已得到确定.3、质量方针(标准条款5。
3)(1)质量方针空洞,体现不出企业特色,与质量目标的关系不明确。
(2)下级人员不清楚质量方针。
(3)拿不出对质量方针的评审证据。
(4)有的部门也制订了质量方针.4、质量目标(标准条款5。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1.目的:审核质量体系的符合性、有效性,采取纠正措施,使体系正常运行。
2.范围:本程序适用于内部质量体系审核(以下简称“内审”)。
3 职责
3.1品管部组织内部质量体系审核。
3.2各部门配合内审工作。
4 程序
4.1内部的策划
4.1.1建立内审员队伍。
从各部门抽出骨干,进行内审员培训(或委外培训),培训考试合格,取得内审员证
书后,方可作为内审员,由管理者代表根据实际情况任命的内审员,方有资格参加内审。
4.1.2制定年度内审计划。
品管部每年年初编制《年度内审计划》,有管理者代表批准后付诸实施,以确定质量
体系是否符合ISO9001:2008版标准的要求,是否得到有效的实施和保持。
审核计划的制定应考虑:所涉及对象的现状、重要性及其影响,以往审核的结果,
对各个部门所开展的质量活动每年进行至少一次内审,同时覆盖部门负责的主要活动(过
程),并规定审核采用的方法。
4.2审核准备
(1)每次审核前由品管部根据生产过程和区域的状况和重要性以及以往审核的结果,
策划审核方案,确定组长、内审员,由品管部编制《内审计划》,报管理者代表
批准,计划中应根据审核活动的实际情况和重要性来安排日程计划,计划应包括:
①审核的目的和范围; ②审核的依据; ③审核的性质;
④审核组成员名单; ⑤审核日期; ⑥审核日程安排。
(2)审核组应有较强的独立工作能力,确定内审员时,一定要考虑该内审员不应审核
自己的工作。
(3)品管部将《审核计划》发至各受审核部门。
(4)内审员根据《审核计划》编制《检查表》,报管理者代表审核。
4.3内审的实施
(1)审核组长主持首次会议,向被审核部门负责人简要说明审核目的、范围、方法和
审核组成员组成等内容,并请受审部门安排一名联络员。
山东诺捷智能装备有限公司
程 序 文 件
编号:SDNJ/CX-8.2.2-11
第A版 第0次修改
文件名称 内部审核控制程序
共2页 第1页
(2)内审员按《检查表》通过查、问、看等形式收集客观证据,并作好记录。
(3)在内审过程中发现不合格项,由内审员报审核组分析后确认,内审员负责编制《不
合格报告》,陈述不合格事实,并注明违反标准哪一条款,内审员在开具不合格
报告时应确保审核过程的客观性和公正性。
(4)被审核部门负责人确认不合格事实并签名。
(5)当内审员与被审核部门意见不一致时,报管理者代表仲裁。
(6)审核组完成审核后召开末次会议,审核组长根据《不合格项分布表》说明不合格
项的数量和分布,按重要程度宣读不合格报告,要求各责任部门尽快分析原因并
制定纠正和预防措施加以实施,并对这次审核结果得出结论性意见。
(7)对于暂时不能构成不合格项,但有潜在趋势,内审员应开出观察项,提交责任部
门注意并采取措施。
4.4品管部负责编制《内部质量体系审核报告》其内容包括:
① 审核目的和范围; ② 审核组组成;
③ 审核时间; ④ 审核依据;
⑤ 审核概况和不合格项分布状况; ⑥ 审核组对质量体系运行的评价;
⑦ 审核报告的发放范围。
4.5纠正和纠正措施实施
被审核部门应限期整改不合格项,并做到举一反三,整改中遇到困难,应请求管理
者代表帮助解决。
4.6纠正和纠正措施跟踪验证
审核组应对纠正措施实施情况进行跟踪,有问题及时向管理者代表反映,纠正和纠
正措施完成后,内审员应进行验证。
4.7年终由品管部对年度内审情况,进行一次总的分析,编写,年度内核报告。
4.8内审的频次
一般情况下,每年不少于1次集中式审核,当出现特殊情况时可以增加审核次数。
如:发生重大质量问题,影响较大的顾客投诉,组织结构发生重大变化,第三方认证前,
都可临时增加审核频次。
4.9内审报告要提交管理评审。
4.10品管部保存内审记录。
5.相关记录:6.1检查表 6.2不合格报告。
山东诺捷智能装备有限公司
程 序 文 件
编号SDNJ/CX-8.2.2-11
第A版 第0次修改
文件名称 内部审核控制程序
共2页 第2页
