沙门氏菌分离流程
沙门氏菌的分离与鉴定
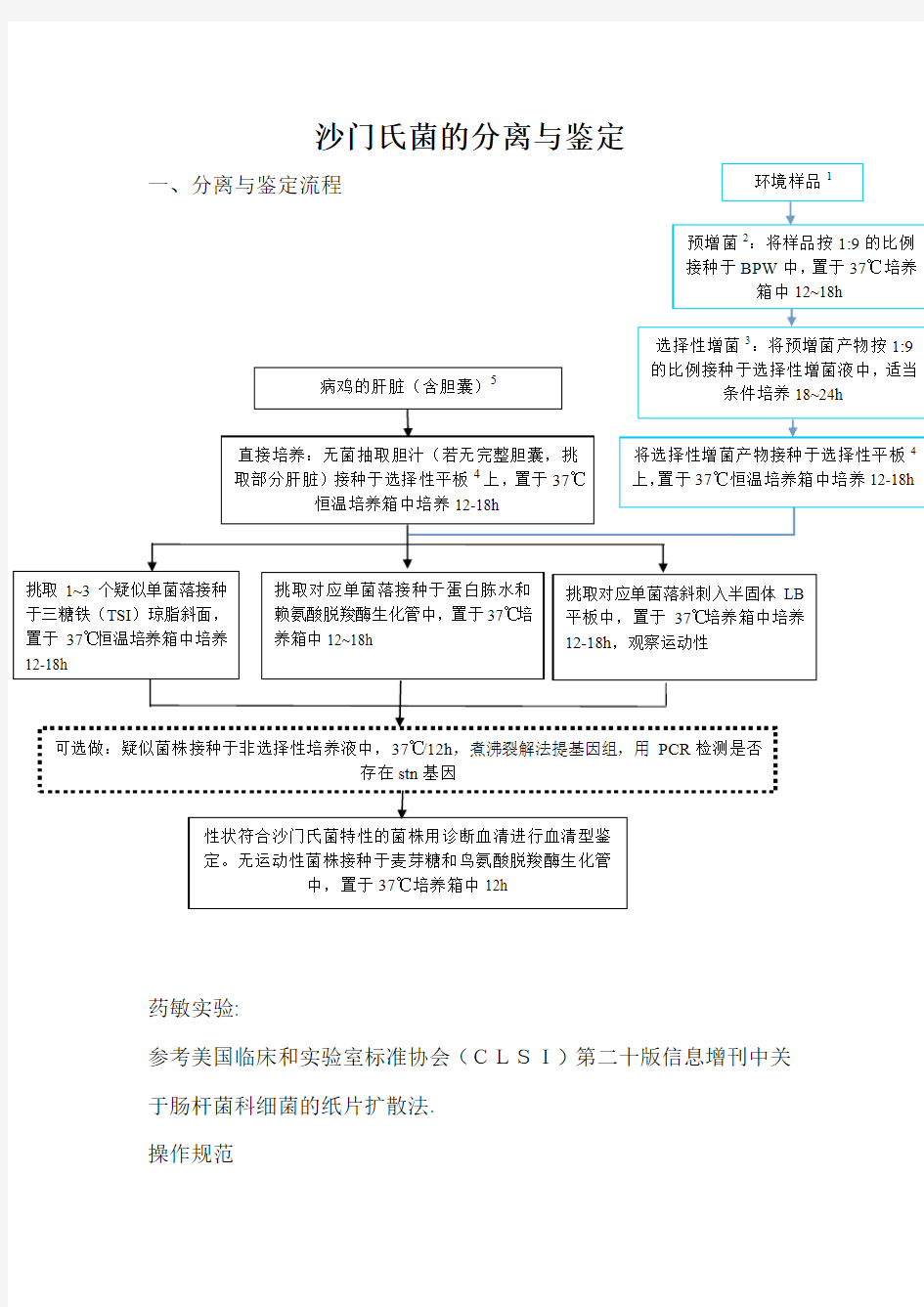
一、分离与鉴定流程
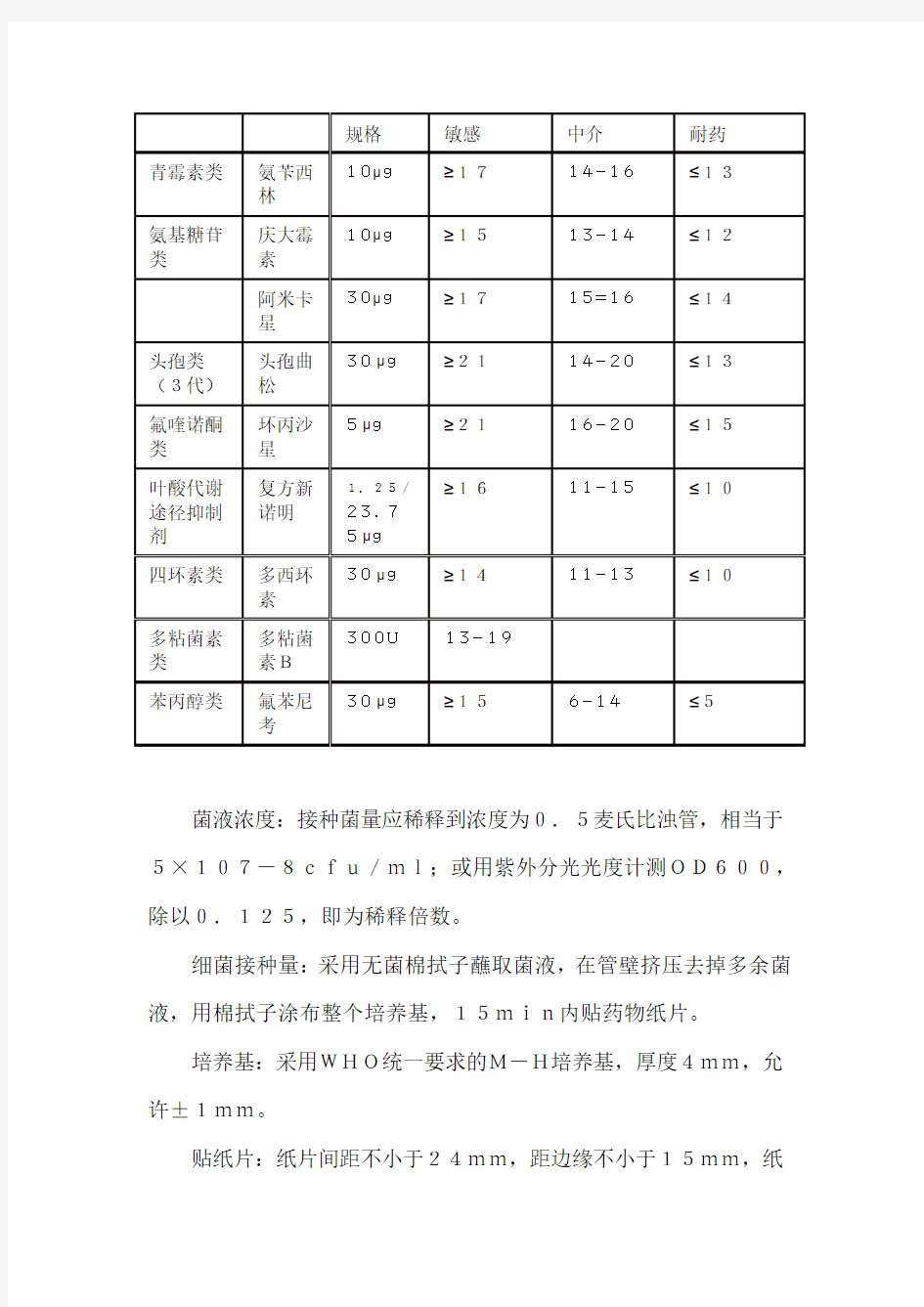
药敏实验:
参考美国临床和实验室标准协会(CLSI)第二十版信息增刊中关于肠杆菌科细菌的纸片扩散法. 操作规范
直接培养:无菌抽取胆汁(若无完整胆囊,挑
取部分肝脏)接种于选择性平板4
上,置于37℃
恒温培养箱中培养12-18h
挑取对应单菌落接种于蛋白胨水和赖氨酸脱羧酶生化管中,置于37℃培养箱中12~18h
挑取对应单菌落斜刺入半固体LB 平板中,置于37℃培养箱中培养12-18h ,观察运动性
可选做:疑似菌株接种于非选择性培养液中,37℃/12h ,煮沸裂解法提基因组,用PCR 检测是否
存在stn 基因
性状符合沙门氏菌特性的菌株用诊断血清进行血清型鉴定。无运动性菌株接种于麦芽糖和鸟氨酸脱羧酶生化管
中,置于37℃培养箱中12h
病鸡的肝脏(含胆囊)5
挑取1~3个疑似单菌落接种于三糖铁(TSI )琼脂斜面,置于37℃恒温培养箱中培养12-18h 环境样品1
预增菌2:将样品按1:9的比例
接种于BPW 中,置于37℃培养
箱中12~18h 选择性增菌3:将预增菌产物按1:9的比例接种于选择性增菌液中,适当
条件培养18~24h 将选择性增菌产物接种于选择性平板4上,置于37℃恒温培养箱中培养12-18h
规格敏感中介耐药
青霉素类氨苄西
林
10μg≥1714-16≤13
氨基糖苷类庆大霉
素
10μg≥1513-14≤12
阿米卡
星
30μg≥1715=16≤14
头孢类(3代)头孢曲
松
30μg≥2114-20≤13
氟喹诺酮类环丙沙
星
5μg≥2116-20≤15
叶酸代谢途径抑制剂复方新
诺明
1.25/
23.7
5μg
≥1611-15≤10
四环素类多西环
素
30μg≥1411-13≤10
多粘菌素类多粘菌
素B
300U13-19
苯丙醇类氟苯尼
考
30μg≥156-14≤5
菌液浓度:接种菌量应稀释到浓度为0.5麦氏比浊管,相当于5×107-8cfu/ml;或用紫外分光光度计测OD600,除以0.125,即为稀释倍数。
细菌接种量:采用无菌棉拭子蘸取菌液,在管壁挤压去掉多余菌液,用棉拭子涂布整个培养基,15min内贴药物纸片。
培养基:采用WHO统一要求的M-H培养基,厚度4mm,允许±1mm。
贴纸片:纸片间距不小于24mm,距边缘不小于15mm,纸
片接触培养基后不应再移动。
观察结果:35℃培养18-24h,测量结果。
沙门氏菌的检验
沙门氏菌得检验 食品学院14食品质量与安全1班 刘文敏柳基炜卫杰恒温紫君 2 2 2 2 摘要:本实验采用GB/T4789。4-2010得检测方法测定鸡场中得沙门氏菌、通过本实验学习沙门氏菌得检测方法与技术,了解沙门氏菌得一些生化特性;本实验先用显色培养基找出可疑菌落,再做生化试验找出可疑得典型性得沙门氏菌,再通过血清学试验最终确定就是否为沙门氏菌属。 关键词:沙门氏菌接种生化试验血清学鉴定 前言 沙门氏菌病就是公共卫生学中具有重要意义得人畜共患病种之一,其病原沙门氏菌属于肠道细菌科。沙门氏菌就是一个统称,泛指 2000多种有紧密连系得细菌,包括引起食物中毒,导致胃肠炎、伤寒与副伤寒得细菌。虽然只有少数人因沙门氏菌而患病,但就是,在世界范围内得细菌性食物中毒事件中,由沙门氏菌引起得占大多数。因此,采用科学、合理得方法检验食品中沙门氏菌,已经成为了人们最关心得问题之一[1]。国标法(GB4789。4-2010)就是目前中国规定得食品中沙门氏菌得标准检测方法,也就是基层实验室普遍采用得检测方法,它根据沙门氏菌得生长特点与生化特性,采取前增菌、增菌、分离、生化试验与血清学鉴定5个步骤进行[2]。 1材料与方法 1、1实验材料 1、1.1仪器设备 均质器、三角烧瓶、平皿、玻璃棒、接种棒 恒温培养箱:36℃±1℃,42℃±1℃ 吸管:1 mL(具 0.01 mL刻度)、10mL(具0、1mL刻度或微量移液器及吸头 电子天平PL602-S,梅特勒—托利多仪器(上海)有限公司; 手提式不锈钢压力蒸汽灭菌锅SYQ—DSX-280B,上海申安医疗器械厂 1。1。2试剂药品
鸡肠、靛基质试剂、沙门氏菌O与H诊断血清、API20E生化试剂盒或VITEKGNI 生化鉴定卡 1.1。3培养基 蛋白胨水(BPW)、四硫磺酸钠煌绿(TTB)、亚硒酸盐胱氨酸(SC)增菌液、亚硫酸铋(BS)琼脂、HE琼脂、三糖铁琼脂、蛋白胨水、尿素琼脂、氰化钾、氰化钾对照、赖氨酸脱羧酶、赖氨酸脱羧酶对照、甘露醇、山梨醇、β—D半乳糖苷(ONPG)培养基 1、2 实验方法 1.2。1培养基得制备 1、2。1.1培养基得配制步骤 蛋白胨水(BPW):称取蛋白胨10g、氯化钠5g、磷酸氢二钠9g、磷酸二氢钠1.5g、蒸馏水1000ml,将各成分加入蒸馏水中,搅混均匀,静置约 10 min,煮沸溶解,调节pH,高压灭菌 121℃,15min。分装10瓶,每瓶90ml 四硫磺酸钠煌绿(TTB):高压灭菌 121 ℃,15 min灭菌冷却后至30℃,每100ml 基础培养液加碘液2ml,煌绿液1ml 1。2.1、2配制培养基得注意事项 (1)按照说明书上得用量进行换算,称取准确分量得合成培养基粉末; (2)加热煮沸溶解培养基时,留意锅内水位得变化,水位下降可再添加适量得水,以免水分蒸发过多,导致后面分装不够量; (3)往试管中放小导管时,注意处理气泡、 1。2。2 沙门氏菌群检测 1、2.2.1沙门氏菌检测程序
油砂
选修课期末论文 课程:非常规油气资源开发理论与技术 论文题目:油砂分布与开采的相关问题研究分析 10级勘查技术与工程专业一班 1400100102 李阳
油砂分布与开采的相关问题研究分析 一、非常规油气资源的前景 世界范围内的非常规资源蕴藏十分丰富,非常规油产量超过7500×104t∕a,非常规天然气超过1800×108m3∕a。近年来非常规油气资源的勘探开发,已经使人们认识到了它对未来世界资源格局的影响。作为非常规油气资源的主要来源,在世界能源供给中起着巨大作用。 我国非常规油气资源也比较丰富,油页岩、油砂、煤层气和天然气水合物等开发潜力巨大。与世界非常规油气资源研究与利用相比,我国在非常规油资源的研究和开发方面相对比较滞后,对油砂矿的资源潜力研究与评价技术、开采技术及综合利用技术研究得比较少,有待进一步的加大科研投入。 油砂及其利用前景 油砂是一种非常规性含原油的砂状矿藏,由砂、沥青、矿物质、黏土和水以相互结合的方式构成,是地壳表层的碎屑物或岩石与其中所含的水和沥青形成的混合物的统称。不同地区油砂矿的组成不同,沥青是其主要成分,含量可占到1%~20%,砂和粘土占80% ~85%,水占3% ~6%。又称“沥青砂”、“稠油砂”、“重油砂”或“焦油砂”。 其中的沥青经过焦化、蒸馏、催化转换、加氢处理等复杂的工艺环节被从油砂中提取出来后,可产生类似天然石油的“合成原油”。用油砂生产合成石油的第一步,是将其中的沥青与砂、矿物质、黏土以及水分进行分离。然后在分选厂,
通过加热过程,将漂浮在大型分离池表面的沥青加工成各种石油产品。 油砂的特点:1、通常含有80%~90%的无机质(砂、矿物等)、3%~6%的水和6%~20%的沥青。油砂沥青是烃类和非烃类有机物质,是稠粘的半固体2、沥青流动性极差,一般不能以打井开采原油、稠油的方法来获取油砂沥青。3、油砂中的沥青大部分溶于有机溶剂,而有别于油页岩中有机质不能溶于有机溶剂。 4、油砂中的沥青多来自降解作用,正构石蜡族烃达到了几乎耗尽的程度,因此饱和馏分中没有或几乎没有正构石蜡族烃。 油砂资源分布广泛,根据美国地质调查局的相关数据表明,世界油砂油可开采资源量为6510亿桶,约占世界石油资源可开采总量的32%,开发潜力巨大。如果全部开发利用,大概可使世界消费上百年。 由于其开采成本较高,起初并不被人们所重视,但随着油价的飙升与油砂开采技术的革新,油砂越来越吸引投资者的目光。随着世界经济对烃类需求的不断上升,未来能源的巨大缺口在很大程度上要依靠包括油砂在内的非常规油气资源来弥补。目前,对于油砂资源的研究和开发,世界各国均在加速进行,其占世界烃类能源的比重在不断增加,在今后的能源结构中起着至关重要的作用,勘探前景巨大,综合利用前景广泛。
第三节 奈瑟菌属
第三节奈瑟菌属(Neisseria) 致病菌脑膜炎奈瑟菌(N. meningitides) 淋病奈瑟菌(N. gonorrhoeae) 一、脑膜炎奈瑟菌(N. meningitides) (一)生物学性状形态与染色肾形,G-双球菌,有荚膜,菌毛培养特性专性需氧,培养基:巧克力培养基,5%CO2 菌落:光滑,透明,不溶血 1.抵抗力对干燥,热力,消毒剂均敏感 (二)致病性致病物质荚膜:菌毛:内毒素:主要致病物质 1.所致疾病流脑,人是其唯一易感宿主三种临床类型:普通型,爆发型,慢性败血病型 (三)免疫性:以体液免疫为主 (四)微生物学检查法标本采集涂片染色镜检分离培养与鉴定快速诊断法 (五)防治原则流脑荚膜多糖疫苗,治疗首选青霉素G :1云南大学药学院(昆明650091);2云南沃森生物技术有限公司(昆明6501l8 为制备四价脑膜炎球菌疫苗的需要2005 A群脑膜炎球菌多糖结合物的免疫原性研究上海生物制品研究所朱为2002 脑膜炎奈瑟菌(Neisseria meningitides)感染是细菌性脑膜炎的常见病因,按荚膜多糖可将其分成12个血清群,其中A、B 和C 群感染占所有感染者的90%。全球由脑膜炎球菌引起的脑膜炎发病率在30-50万,病死率约10%,有相当一部分儿童因脑膜炎球菌严重感染而发生致聋等永久后遗症。在我国,A群脑膜炎球菌是主要致病菌群,95%的病例由A群引起。80 年代以来,我国进行了A群脑膜炎球菌荚膜多糖疫苗的大面积接种,有效地控制了发病率。该荚膜多糖是N-乙酰-3-O-乙酰甘露糖胺磷酸盐的线形共聚物,属T细胞非依赖性(TI)抗原,具有中等免疫原性和年龄相关的保护力,不能诱导免疫记忆。现已证实它对2岁以上儿童和成人在短期内有效,但随时间延续保护力下降,尤其在幼龄儿童中。因此有必要改进现有疫苗,提高其对各年龄组(包括婴儿)的免疫效果。近期的研究集中在开发多糖结合疫苗,即将多糖共价结合到蛋白质上,使其转化为T细胞依赖性(TD)抗原,以增强免疫原性和诱导免疫记忆。本文报道将! 群脑膜炎球菌多糖共价结合到精制破伤风类毒素(TT)上制备结合物,观察其在小鼠中的免疫原性。 A+C群脑膜炎球菌多糖一DT结合疫苗与多糖疫苗诱导的抗多糖抗体间的功能活性差异[英]2004 多糖蛋白结合疫苗对预防由一些有荚膜细菌(包括b型流感杆菌、肺炎球菌和C群脑膜炎球菌)引起的侵袭性疾病高度有效。与未结合多糖疫苗相比,多糖一蛋白结合疫苗能在婴幼儿体内诱导更高浓度的血清抗荚膜抗体。而且,结合疫苗诱导的抗体亲和力更高,补体介导的杀菌活性更强。 。在限定剂量时,多糖疫苗诱导的血清抗荚膜抗体预防C群脑膜炎球菌感染婴鼠发生菌血症的效力弱于结合疫苗。结合疫苗组的抗C群抗体的亲和力指数高于多糖疫苗组。两种疫苗在成人中诱导的抗荚膜抗体的功能活性差异,意味着各自激活了不同的B细胞群。 (兰州生物制品研究所崔萱林2001 流行性脑脊髓膜炎是由脑膜炎球菌(Meningococcus)引起的细菌性脑膜炎(简称流脑),发病急,病死率高,且在各年龄组中都可发生,15岁以下儿童发病占75%以上。脑膜炎球菌根据荚膜多糖的结构可分为12个血清群,其中A、B、c群引发的流脑占90%以上。流脑的流行具有菌群漂移特点,如美国在1945年以前为A群流行,1960年以后以B群为主,1967年以后转为C群流行。我国以A群菌流行为主,B群和C群菌有少量病例,约占lO%左右。因此预防流脑的重点应是A、B、C群流脑球菌引起的疾病。由于流脑菌群的漂移现象,国外多采用多价多糖疫苗用于预防流行性脑脊髓膜炎,目前所使用的主要为A+C群二价疫苗(B群多糖对人体无效,主要研制外膜蛋白为基础的疫苗),其次为A、C、Y及WI35四价疫苗,其它相关菌群引起的流脑病例已少见。国内目前主要使用A群流脑多糖疫苗,自80年代初使用至今效果很好;对于其它菌群的预防.目前尚未有疫苗出现,因此我们研制了A+C群流脑多糖疫苗,即在现有的A群流脑多糖疫苗中加入C群流脑多糖抗原,形成二价疫苗以预防A、C群流脑球菌引起的脑脊髓膜炎。 A+C群脑膜炎球菌多糖疫苗的制造和检定均按照WHO(生物制品规程》的要求进行,C群流脑多糖原液的主要制造过程借鉴A群流脑多糖原液的生产工艺,在多糖纯化步骤另采用澄清过滤、苯酚抽提控制多糖浓度等措施,使得C群多糖原液的蛋白质和核酸含量符合要求。A群流脑多糖原液为选用的本所常规生产的原液制品。由于多糖原液在制备过程中未进行专门的除类毒素工艺,因而在原液检定中采用鲎试剂法对类毒素含量进行测定,以确保疫苗的安全性。 2岁以下年龄组儿童在接种A+C群脑膜炎球菌多糖疫苗一个月后,虽然同组儿童的免前及免后的血清杀菌抗体滴度有显著差.但血清4倍阳转率较大年龄组儿童低,而且免后血清中的杀菌抗体滴度的整体水平也相对较低。提示低年龄组儿童对多糖疫苗的免疫应答水平较高年龄组儿童低,有关该疫苗人体接种后的安全性和免疫持久性的结果将另文报告。 A群脑膜炎球菌多糖疫苗自80年代在我国研制成功并广泛接种以来效果明显。我国A群带菌率和发病率大幅度下降,预防效果达90%以上。至今在我国引起流脑的脑膜炎球菌仍以A群为主,同时B群和C群的病例也开始出现。欧美国家主要流行菌群由A群转为B群和c群的事实。提示我们在A群脑膜炎被控制之后要防止B群和C群变迁。 1994年法国由法国巴斯德梅里厄血清疫苗研究所(PasteurMerreux)提供生产的A+C群脑膜炎球菌多糖疫苗,申请在我国注册,中国药品生物制品检定所与河南省卫生防疫站协作,在河南省新县进行了人群安全性与免疫原性的现场考核,现将结果报告如下该疫苗较安全,免疫原性较强,且更具免疫持久性。2000 A群脑膜炎球菌多糖结合疫苗的研制2000杨丽华 (长春生物制品研究所,长春130062)李风祥(中国药品生物制品检定所, 本试验制备的A群脑膜炎球菌多糖结合疫苗的理化特性及免疫特性与国内外文献报道结果一致。制备的结合疫苗可诱导出高水平的保护性A群脑膜炎球菌多糖抗体和TT抗体。结合疫苗具有很好的免疫原性和安全性。制备工艺稳定,重复性好,可批量生产。本试验为进一步临床评价结合疫苗的人群免疫效果提供了实验基础。本试验选用Tr作为载体蛋白,因为这种蛋白目前已经标准化,作为载体蛋白的同时兼有预防伤风感染的作用,而用TT蛋白对于已经建立起的免疫程序和“自然”免疫并不产生干扰 A群脑膜炎球菌多糖结合疫苗的制备熊慧玲成都生物制品研究所 预防A群脑膜炎球菌引起的脑脊髓膜炎,我国目前采用A群脑膜炎球菌多糖疫苗,而疫苗接种后,小于1岁的婴儿,即使加强接种产生的抗体只能维持1年,1~1.5岁半的婴幼儿,加强后只能维持2年,1.5~2岁的幼儿,接种1针维持不到1年_l1 。wHO指出,按目前的免疫程序,婴儿在出生后5年内至少需要免疫接种4次才可提供中度抗体水平一。说明A群脑膜炎球菌多糖疫苗在婴幼儿中,尤其在2岁以下,免疫原性低,即使产生抗体,抗体水平也不能长久保持。因而提高疫苗免疫原性,使它能对各年龄组,尤其2岁以下婴幼儿提供高水平的长期保护作用,有特别重要的意义。b型流感嗜血杆菌结合疫苗的成功研制和应用给我们以深刻的启示。和流感嗜血杆菌荚膜多糖一样,A群脑膜炎球菌多糖为半抗原,为非T细胞依赖性抗原,当与蛋白结合后,可转化为T细胞依赖性抗原,可刺激机体产生高水平的保护抗体,重复接种有记忆抗体产生因此,我们进行了A群脑膜球菌多糖结合疫苗的研制,并对经中国药品生物制品检定所检定合格的连续3批 2003 流行性脑脊髓膜炎(流脑)被发现并确认已有l00多年.尽管对此病已有有效的预防和治疗措施,但它仍是一种急性传染病.而且病死率高、继续威胁着人类,尤其是儿童的身体健康。我国目前使用的预防制品是A群脑膜炎球菌多糖疫苗,该疫苗对4岁以上儿童有很好免疫效果,对幼儿免疫效果较差,保护时问较短。而脑膜炎球菌多糖与一种蛋白载体连接构成结合疫苗.可增强其对幼儿的免疫回忆反应,提高预防效果?。卫生部成都生物制品研究所已研制成功“A群脑膜炎球菌多糖结合疫苗”,并由中国药品生物制品检定所、卫生部成都生物制品研究所、江苏省疾病预防控制中心联合于2002年l0月~2003年1月在江苏省射阳县进行的“A群脑膜炎球菌多糖结合疫苗临床研究”已圆满结束。现将婴幼儿接种A群脑膜炎球菌多糖结合疫苗的安全性报告如下本次临床试验表明,3~4月婴幼儿接种A群脑膜炎球菌多糖结合疫苗具有良好的安全性,但由于该疫苗首次应用于人群,在大规模推广接种前,仍需对其安全性进一步进行观察 C群脑膜炎球菌结合疫苗的质量控制与生产的科学挑战2004 世界卫生组织(WHO)生物制品标准化专家委员会于1976年通过了脑膜炎球菌多糖疫苗的建议,并于1978年和1981年进行了修订。在临床研究中,疫苗的有效率至少达9O% ,证明其在疫苗接种计划中高度有效。然而,不能在幼婴中诱生保护性应答或免疫记忆制约了其在英国婴儿免疫接种计划中的应用。随着b型流感杆菌(Hib)结合疫苗的成功引入,C群脑膜炎球菌(MenC)荚膜多糖结合疫苗的研究取得了显著的进展。临床对照试验已证实它们在所有年龄组中均可诱生针对MenC多糖的保护性水平的抗体,并且作为T细胞依赖性抗原,能诱导免疫记忆和抗荚膜抗体的亲和力成熟。英国引入MenC结合疫苗后,证实该疫苗可提供保护性免疫。WHO已经制定了有关这些新疫苗生产和检定的建议。 脑膜炎球菌是细菌性脑膜炎和败血病的重要病原。根据荚膜多糖在化学和血清学上的不同,脑膜炎球菌可分为若干群,其中A、B、C、Y、Wl35群对人致病。A群在
油砂的传统开采方法及新技术展望
(一)、油砂的开采方法 最近几年, 油砂开发技术的进步不断推进着油砂工业的发展, 并已经取得了巨大的进步。主要有以下几方面: 用巨型卡车和铲车开采油砂, 增加了开采的灵活性, 同时降低了成本; 用水力运输管道系统代替了传送带系统, 使油砂达到管输要求, 并简化了把沥青和砂分离开来的萃取过程; 在萃取阶段, 降低了加工的温度; 采用固化或合成残渣的技术, 加快了大面积残渣池的治理, 并在努力研究一种覆盖技术来处理残渣。 目前,油砂开采方式有两种,一类是露天开采,适用于埋深小于75m,厚度大于3m,另一类是井下开采,适用于埋深大于75m的矿层。针对莫尔图克矿一层埋深较浅(0-46m),因此采用露天开采。 露天开采程序上分为采矿和萃取两个部分,主要用于开采埋藏较浅的近地表油砂,具有回收率高、效率高、安全的特点。露天开采所需的设备及费用、油砂油采收率较其他方法好,技术上较为成熟,在加拿大及委内瑞拉等都已形成大规模工业开采。多年来,油砂的露天开采技术已经取得的重要进步如下: 采矿过程主要分为以下几个部分: ?用卡车和铲车除去盖层; ?用电动或水力铲车挖出油砂; ?把油砂从矿场运送到压碎机; ?把油砂加工碾碎; ?将油砂混合成砂浆; ?用离心泵和管线(常称为水力输送)把油砂从矿区运送到萃取区域。
图1-1 采矿过程示意图 (二)、油砂的萃取分离 1、油砂的分离工艺步骤 采矿设备和某些采矿操作是油砂工业所独有的, 现在这一操作主要受到下一分离过程的限制;而萃取过程也是沥青损失最大的过程, 因此, 必须综合考虑采矿和萃取两个步骤。 在过去的15 年里, 水力传输已经代替了其他的设备。从矿石浆中萃取沥青由两个步骤组成: 步骤一: 分离初级分离器( primary separat io nvessel) 中的沥青泡沫, 其中含60% 沥青, 30%水, 10% 微固体。 步骤二: 稀释发泡处理(见图2-1) : 提取沥青, 尽可能排除水和固体。如今, 实现此过程主要有两种方法: 最初的石脑油溶剂处理过程需要斜板分离器 ( inclined plate separators) 和离心分离机除去残余固体和水; 新的石蜡溶剂处理过程需要沉降容器, 但是由于不用离心分离机, 可以得到较纯净的产品。 图2-1 萃取过程示意图 ( 1) 初级分离 初级分离器是一个巨大、昂贵、固定不易移动的装置。运行条件必须稳定, 对矿石等级、温度、进料速度和其他因素的微小变化非常敏感。35℃以上的温度条件需要大量的能量, 占一桶合成原油能量消耗的40%。此过程还需要加入添加剂, 将pH值控制在8.5 左右。
沙门氏菌检验
沙门氏菌的检验 1.目的 规范沙门氏菌检测方法,使产品检验有据可依。 2.消毒灭菌要求 微生物检测用的玻璃仪器、金属用具及培养基、被污染和接种的培养物等,必须经灭菌后方能使用。 注:本实验采用湿热灭菌法,吸管、培养皿、培养基等盖好塞子并包好瓶口在高压灭菌锅中按要求的温度和压力灭菌,一般是121℃()下灭菌20min。 3.原理 沙门氏菌的检验分四个连续阶段: 4.操作步骤 准备工作 配制实验所需的缓冲蛋白胨水、亚硒酸盐胱氨酸培养基(无需灭菌)、HE培养基、三糖铁培养基等,并将准备好的均质杯、吸管、培养皿、大试管等一起灭菌。 前增菌 在无菌环境下,称取25g待检样品放入盛有225ml灭菌好的缓冲蛋白胨水中,然后放到36±1℃的恒温培养箱内进行前增菌4-6h; 增菌 在无菌环境下,用灭菌好的吸管吸取10ml前增菌液接种与100ml亚硒酸盐胱氨酸培养基中进行二次增菌,恒温培养箱36±1℃,培养18-24h; 分离培养 将增菌培养液摇匀,以无菌操作,用直径3mm的接种环挑取一环,划线于表面无凝结水的BS和SS琼脂平板各一个,于36±1℃培养18-24h。观察各个平板上有无典型或可疑沙门氏菌属的菌落。如无典型或可疑菌落,应再继续培养24±2h。然后观察培养的平板(黄色的菌落是大肠杆菌;蓝绿色或蓝色,产硫化氢,菌落中心黑色或几乎全黑色为可疑沙门氏菌)。 沙门氏菌属各亚属在其他选择性琼脂平板的菌落特征 生化实验 用灭菌好的接种针在培养平板上挑取可疑的沙门氏菌单菌落,接种到三糖铁培养基上,恒温培养箱36±1℃,培养18-24h; 典型沙门氏菌培养物斜面显红色(碱性),底端显黄色(酸性),有气体产生,形成硫化氢(琼脂变黑)。 三糖铁培养基变化表 肠杆菌科各属在三糖铁琼脂内的反应结果
铸造实用工艺流程
消失模铸造工艺流程 一、工艺流程示意图 二、工艺流程 模样生产工艺流程图 铸件 清砂(抛丸机)、 打磨浇冒口 上涂料 烘干 粘接 发泡膜 浇注及 冷却 埋箱 造型 落砂 铸件 热处理 铸件成品 EPS EPMMA STMMA 预热 → 加料、搅拌 → 抽真空 → 喷水雾 → 停止抽真空 → 出料 → 干燥 → 料仓 珠粒 可发性 预发泡 发泡成型 干燥 筛分 熟化 闭模 → 预热模具 → 加料 → 合模 → 发泡成型 → 冷却 → 脱模 浇冒 口 组合 落砂斗 → 水平振动筛 → 型砂冷却 → 提升机 → 磁选、除尘 → 储砂斗 零件图 铸件图 模样图 模具 图 模具 EPS 珠粒 预发泡 熟化 成型 冷却 出模 干燥 模样组合 检验 新砂、旧砂、覆塑料膜密封砂箱、置浇口杯
(一)预发泡: 预发泡目的:为了获得低密度、表面光洁、质量优良的泡沫模样。 流程:预热→ 加料、搅拌→ 抽真空→ 喷水雾→ 停止抽真空→ 出料→ 干燥→ 料仓、熟化 EPS预发温度100~105℃;STMMA预发温度105~115℃;EPMMA预发温度120~130℃。进入预发机的加热蒸汽压力在0.15~0.20MPa范围调节。 说明: ①间歇式蒸汽预发泡机必须满足加热均匀(蒸汽与珠粒接触)筒体内 温度在90~130℃范围容易调节和控制。搅拌要充分、均匀,筒体底部和侧壁要有刮板,防止珠粒因过热而粘壁,搅拌速度可调。筒体底部冷凝水的排除要畅通,否则影响预发泡效果。 ②加热蒸汽压力可调并稳定,且蒸汽中不能夹带水分。 ③出料要干净,每批发泡后,筒体内残留的料要吹扫干净。 熟化:把预发泡珠放置几小时以上,让空气进入珠粒内,使珠粒变得干燥有弹性,变形后又能复原的过程。熟化时间一般为10~24h,熟化时间不能太长否则发泡剂损失太多影响发泡成型质量。 (二)成形发泡的工艺过程为: 闭模→ 预热模具→ 加料→ 合模→ 发泡成型→ 冷却→ 脱模→ 模样熟化 要点:珠粒均匀填满模具,模具必须预热到100℃,水蒸气温度一般在120℃左右,压力为0.15MPa。 模样熟化:将模样置入50~70℃的烘干室强制干燥5~6h,可达到在室温下自然熟化2天的效果。 (三)模样的粘合 对复杂的模样往往不能整体发泡成形,而分块制造,最后需要将各块粘合成整体。另外,模样与浇冒口系统组成模样组,也需要粘合工序。粘合工序一般是采用粘结剂来完成的。目前国内使用的消失模铸造用的粘结剂可分为热熔胶型、水溶型和有机溶剂型粘胶。 粘接剂要求:
MTO烯烃分离装置操作规程
目录 第一部分工艺技术规程 3 1 装置说明 3 2 工艺指标31 第二部分开工程序39 1 开工准备39 2 开工统筹图40 3 开工操作程序40 第三部分正常操作程序69 1 操作注意事项69 2 正常操作程序69 3 正常切换操作程序70 4 关键部位取样操作程序及注意事项71 第四部分停工程序73 1 停工准备73 2 停工统筹图73 3 停工操作程序73 第五部分设备操作规程97 第六部分故障处理程序135 第七部分仪表控制系统操作规程143 1 DCS系统概述143 2 主要仪表控制回路说明145 3 装置联锁逻辑控制说明156 第八部分安全生产及环境保护167 第九部分附录和相关文件177 1 附录177 2 相关文件204
第—部分工艺技术规程 1烯烃分离装置说明 1.1装置简介 神达化工烯烃项目烯烃分离装置采用中石化LPEC专利技术,包括烯烃分离单元和烯烃罐区单元,由中国石化洛阳工程公司进行详细工程设计。烯烃分离单元占地面积255×110m2,烯烃罐区占地面积150×111m2。烯烃分离单元采用LPEC前脱乙烷后加氢、丙烷洗工艺技术,由LPEC进行工艺包、基础工程设计和进行详细工程设设计。此工艺与常规乙烯分离工艺主要区别有:此工艺无深冷分离系统、无乙烯制冷系统。 装置2012年11月动工建设,2014年4月30日装置中交,年运行时间为8000h。装置每年生产300kt/a乙烯和300kt/a丙烯。混合C4产品量为99kt/a,小时产量为12.36t。液相的C5以上产品量为26kt/a,小时产量为3.267t。燃料气的产量为4.9kt/a,小时产量6.172t。 装置设计寿命为二十年,设计操作弹性为70%~120%(以每小时生产的产品计算)。 装置连续运行周期为36个月。 装置设计加工处理来自MTO装置的产品气进料54475kg/h,进料中的乙烯/丙烯(E/P比)的范围是从0.8~1.2。 工况1:额定工况,E/P=0.8 工况2:设计工况,E/P=1.0 工况3:额定工况,E/P=1.2 1.2工艺原理 传统的乙烯、丙烯的制取路线是通过石脑油裂解生产,其缺点是过分依赖石油。由甲醇制乙烯、丙烯等低碳烯烃(Methanol-to-Olefin,简称MTO)是最有希望替代石脑油为原料制烯烃的工艺路线,目前工艺技术开发已趋于成熟。甲醇制烯烃技术的工业化,开辟了由煤炭或天然气经气化生产基础有机化工原料的新工艺路线,有利于改变传统煤化工的产品格局,是实现煤化工向石油化工延伸发展的有效途径。 神华包头煤制烯烃项目烯烃分离装置采用美国Cbi-Lummus专利技术,包括烯烃分离单元 和烯烃罐区单元。烯烃分离单元采用Lummus前脱丙烷后加氢、丙烷洗工艺技术,此工艺 与常规乙烯分离工艺相比较简单,主要区别有:此工艺无前冷系统;无乙烯制冷系统。 MTO工艺由甲醇转化烯烃单元和轻烯烃回收单元组成,本装置为烯烃回收单元,采用的是美国Lummus的乙烯分离技术。来自甲醇制烯烃装置的产品气进入烯烃分离装置,首先经 过四级压缩、酸性气体脱除、洗涤和干燥后,进入高低压脱丙烷塔进行分离。高压脱丙烷塔顶物流经产品气四段压缩后送至脱甲烷塔,塔顶产品主要是甲烷,经冷箱后得到燃料气。 塔底物流送至脱丁烷塔,得到C5以上产品和混合C4产品。脱甲烷塔底物流送至脱乙烷塔进行C2和C3分离,塔顶C2经过乙炔转化后进入乙烯精馏塔塔,塔顶产品即为聚合级乙烯产 品。塔底C3进入丙烯精馏塔,塔顶流股便是聚合级丙烯。聚合级的乙烯和丙烯产品分别送入PE装置和PP装置。 1.3工艺流程说明
加拿大油砂开采脱砂工艺简述
加拿大油砂开采脱砂工艺简述 油砂从矿场开采完成后,重要的是对油砂进行分离处理。加拿大油砂分离处理工艺经过20多年的研究和实践,形成了以热水/表面活性剂洗油法、有机溶剂提取法和干溜法为主的油砂分离方法。 在分离方法的选择上主要考虑油砂特点、性质以及成本和环保等方面因素,本着优先选择热水/表面活性剂洗油法,然后再考虑干溜法、有机溶剂提取法。 (一)热水/表面活性剂洗油法 1、工作原理 通过热碱的作用,改变砂子表面润湿性,使砂子表面更加亲水,实现砂与吸附在上面的沥青分离,分离后的原油上浮进入碱液中,而油砂沉降在下部,以达到分离的目的。表面活性剂的目的是降低油水界面张力,增强油的乳化能力,促使油砂与油的分离。;表面活性剂还可产生协同效应,降低界面张力,提高洗油效率。 该方法适合油砂性质比较好,沙粒表面有水膜,表面润湿性为亲水的油砂。 2、工艺流程 油砂经过传送系统运输到分离中心,在反应器中加入热碱活性剂,在一定温度(一般为80摄氏度)下化学剂与油砂相互作用形成砂浆,原油乳化脱落;然后进入分离器将油砂与液体、油分离。砂子通过输送系统再返回矿场掩埋或在专门地方存放;分离油再经过破乳、提取分离,得到原油与分离出的液体,回收的液体通过补充可以重复利用。
(二)有机溶剂萃取法 1、工作原理 主要是根据物质的相似相容原理来实现油砂分离。即:采用石脑油或甲苯/酒精混合物,在室温状态下,溶剂与油砂混合搅拌,油砂溶解到溶剂中,然后进行蒸馏,实现油砂分离。 这种方法是洗油效率高,溶剂可重复利用。 2、工艺流程 粉碎油砂进入离心分离前加入溶剂萃取,通过分离后,干净砂子回填或堆放在指定地点,混合物进行蒸馏,产生的溶剂回收再利用,分离出的油进行精炼。 (三)干馏法 (1)工作原理 采用250摄氏度以上高温进行裂解,经过高温处理后,沥青的质量得到很大改变,分子质量变小,胶质减少,高温处理过程中产生轻质油。 该方法适合地表干燥油砂资源的开发利用。 (2)工艺流程 油砂进行粉碎,通过送料系统进入干馏炉高温燃烧,然后进入洗涤塔洗涤、分离塔进行分离,产生的副产品天然气可补充燃烧。
烯烃_链烷烃分离工艺进展
现代化工 MODERN CHEMICAL INDUSTRY 2000 Vol.20 No.11 P.21-24 烯烃/链烷烃分离工艺进展 邝生鲁 奚强 朱成诚 摘要 当前开发的烯烃/链烷烃分离技术有物理吸收法、化学吸收法、吸收分离法、萃取蒸馏法及膜分离法。其中最有发展前途的是利用π-配合作用的化学吸收法,现已有工业化装置。将蒸馏与吸附相结合的复合分离技术,是烯烃/链烷烃分离技术的发展方向之一。 关键词 烯烃/链烷烃分离,化学吸收,π-配合物, 吸附分离,膜分离,萃取蒸馏Recent developments of olefin/paraffin separation technology KUANG Shenglu, XI Qiang, ZHU Chengcheng (Wuhan Institute of Chemical Technology, 430074) Abstract A number of olefin/paraffin separation technologies have been developed today. They include physical absorption, chemical absorption, absorption separation, extractive distillation and membrane separation. The most promising appears to chemical absorption by π-complexation. There are already some commercialized plants. One of the developing trends for olefin/paraffin separation is the composite separation technology combining distillation with absorption. Key words olefin/paraffin separation, chemical absorption, π-complexation, absorption separation, membrane separation, extractive distillation 第一作者:邝生鲁,男,1938年生,大学,教授,从事精细化工、应用电化学等方面研究。 邝生鲁(武汉化工学院,430074) 奚强(武汉化工学院,430074) 朱成诚(武汉化工学院,430074) 参考文献 1,Humphrey J L,Seibert A F.Separations Technologies Advances and Priorities. New York:Department of Energy Report 12920-1.1991.25~40 2,Fatemizadeh A,Nolley E.Ethylene Recovery from Polyethylene Plant Vent Streams.Presented at the National AIChE Meeting.Orlando,FL,1990.1~20 3,Eldridge R B.Ind Eng Chem Res.1993,32:2208~2212
大肠杆菌和沙门氏菌的分离鉴定方案
大肠杆菌和沙门氏菌的分离鉴定方案 实验原理: 1、大肠杆菌的性质: 大肠杆菌是G--无芽孢直杆菌,在大多数培养基上表现出不同的特性。在麦康凯琼脂平板上是凸起光滑湿润的粉红菌落,革兰氏染色镜检为红色短杆菌。三糖铁琼脂上的反应为斜面和底部都变黄,产气,不产生硫化氢。生化特性为发酵葡萄糖、乳糖、甘露醇、麦芽糖,不发酵蔗糖。MR试验,吲哚试验为阳性,VP试验为阴性,不产生H2S,不能利用枸椽酸盐。半固体中沿穿刺线向四周生长。 2、沙门氏杆菌的性质: 沙门氏杆菌是G-直杆菌。在麦康凯平板上为细小半透明、圆形、无色小菌落,三糖铁斜面下层变黄色,上层仍为红色,穿刺处为变黑产生H2S。能发酵葡萄糖产酸产气,能利用枸椽酸盐,不发酵乳糖不利用蔗糖肌醇,MR阳性,VP阴性,不产吲哚,不分解尿素。 实验材料: 含有大肠杆菌和沙门氏菌的猪肝脏、培养基(琼脂平板培养基、三糖铁琼脂斜面培养基、麦康凯琼脂、生化培养基、SC)、器械(剪刀、记号笔、接种环、酒精灯、显微镜、试管、玻片、培养皿)、药品(消毒酒精、结晶紫、碘液、酸酒精、品红、松柏油) 实验内容及操作程序: 一、培养基制备: 制备普通琼脂培养基、麦康凯平板、SC增菌培养基、生化培养基,制备方法见附1.二、标本制备: (1)取新鲜猪肝脏一小块,火焰表面消毒。 (2)用浸过消毒液的剪刀剪开一个小口于消过毒的猪肝脏。 (3)用接种环在剪开的肝脏小口沾取肝脏液,分别画线于麦康凯培养基和接种于SC中,37°C恒温培养24小时。 三、细菌分离培养: (1)取出培养了24小时的麦康凯平板。挑选麦康凯平板上的凸起光滑湿润的粉红菌落染色镜检,看是否为红色短杆菌,若是,即疑似为大肠杆菌,则取其接种于另一麦康凯平板,37°C 恒温培养24小时。 (2)取出培养了24小时的SC增菌培养基,染色镜检,看是否有疑似沙门氏菌,有则取其中细菌画线接种于麦康凯平板上,37°C恒温培养24小时。 四、细菌的鉴定纯化: (1)检查疑似大肠杆菌的培养基是否长满了粉红色菌落,染色镜检。并取其分别接种于生化培养基上(葡萄糖、乳糖、麦芽糖、甘露醇、蔗糖、肌醇、枸椽酸盐、尿素、MR、VP、H2S),并做穿刺实验于三糖铁上。37°C恒温培养24小时后观察结果。若实验结果满足预期效果,则可判定为大肠杆菌,则将其接种于普通琼脂培养基上传代培养。 (2)检查疑似沙门氏菌的平板上是否长满细菌,染色镜检,看是否满足于沙门氏菌的染色特性。并取其接种于生化培养基上,并作穿刺实验于三糖铁上,37°C恒温培养24小时后观察结果,若结果满足于沙门氏菌的生化特性,则可判定为沙门氏菌,则将其接种于普通琼脂培养基上传代培养。
铸造工艺流程
消失模铸造工艺流程 一、工艺流程示意图 r A EPS EPMMA 预热T加料、搅拌T抽真空T喷水雾T停止抽真空T出料T干燥T料仓闭模T预热模具T加料T合模T发泡成型T冷却T脱模 新砂、旧砂、覆塑料膜密封砂箱、置浇口杯 落砂斗T水平振动筛T型砂冷却T提升机T磁选、除尘T储砂斗 二、工艺流程模样生产工艺流程图 STMMA 干上 { 抛 丸 机 ? 打 磨 浇 冒 口 却浇 珠 粒 可 发 性 铸 件 成 品砂件
(一)预发泡:预发泡目的:为了获得低密度、表面光洁、质量优良的泡沫模样。 流程:预热f加料、搅拌f抽真空f喷水雾f停止抽真空f 出料f干燥f料仓、熟化 EPS预发温度100~105C;STMMA 预发温度105~115°C;EPMMA 预发温度120~130C。进入预发机的加热蒸汽压力在0.15~0.20MPa范围调节。 说明: ①间歇式蒸汽预发泡机必须满足加热均匀(蒸汽与珠粒接触)筒体内温度在90~130C 范围容易调节和控制。搅拌要充分、均匀,筒体底部和侧壁要有刮板,防止珠粒因过热而粘壁,搅拌速度可调。筒体底部冷凝水的排除要畅通,否则影响预发泡效果。 ②加热蒸汽压力可调并稳定,且蒸汽中不能夹带水分。 ③出料要干净,每批发泡后,筒体内残留的料要吹扫干净。熟化:把预发泡珠放置几 小时以上,让空气进入珠粒内,使珠粒变得干 燥有弹性,变形后又能复原的过程。熟化时间一般为10~24h,熟化时间不能太长否则发泡剂损失太多影响发泡成型质量。 (二)成形发泡的工艺过程为: 闭模f预热模具f加料f合模f发泡成型f冷却f脱模 f 模样熟化 要点:珠粒均匀填满模具,模具必须预热到100C,水蒸气温度一般在 120C左右,压力为0.15MPa。 模样熟化:将模样置入50~70C的烘干室强制干燥5~6h可达到在室温下自然熟化2 天的效果。 (三)模样的粘合对复杂的模样往往不能整体发泡成形,而分块制造,最后需要将各块粘 合成整体。另外,模样与浇冒口系统组成模样组,也需要粘合工序。粘合工序一般是采用粘结剂来完成的。目前国内使用的消失模铸造用的粘结剂可分为热熔胶型、水溶型和有机溶剂型粘胶。 粘接剂要求: ①足够的粘接强度,大于100MPa。 ②快干性好,最好能在1h 内干燥,并具有一定的粘接强度,不致在加工或搬运过程中损坏模样。
神华包头煤化工分公司全厂工艺方块流程图说明
SHENHUA GROUP 神华包头煤化工分公司全厂工艺方块流程图说明 一、各装置的进料说明: 1、原料煤的进料量为六台磨煤机进料量的总和; 121FIC150+121FIC250+121FIC350+121FIC450+121FIC550+121FIC650 2、净化装置的进料量为变换两系列的进料量之和;146FI101+146FI201 3、硫回收的进料量为低温甲醇洗至硫回收的酸性气流量;FI1038 4、硫磺产品为包装后的固体硫磺量;暂时无数据 5、甲醇装置的进料量为低温甲醇洗至甲醇装置的合成气量;151FI116 6、甲醇罐区的进料量为甲醇装置稳定塔至甲醇罐区的MTO级甲醇量;151FIC111 7、甲醇制烯烃装置的进料量为进MTO装置的MTO级甲醇量;FI1401B 8、烯烃分离装置的进料量为MTO装置的产品气量;FI 2114 9、烯烃分离装置至烯烃罐区的乙烯量为乙烯精馏塔送至乙烯罐的流量;FC660 10、烯烃分离装置至烯烃罐区的丙烯量为丙烯精馏塔送至丙烯罐的流量;FC650 11、烯烃分离装置至烯烃罐区的C4量为脱丁烷塔顶送至混合C4罐的流量;FC656 12、烯烃分离装置至烯烃罐区的C5量为脱丁烷塔底送至C5罐的流量;FC659 13、副产品C5为C5罐送至装车栈台的量;FI-105 14、副产品C4为混合C4罐送至装车栈台的量;FI-104 15、聚丙烯装置的进料量为丙烯脱气塔C-2008的进料量;FI-2008-1 16、聚乙烯装置的进料量为乙烯中间换热器E-2105的进料量;FI-2001-1 17、聚丙烯装置至聚丙烯包装仓库的进料量为挤压造粒机的负荷;暂时无数据(石化盈科联系霍尼韦尔下装数据) 18、聚乙烯装置至聚乙烯包装仓库的进料量为挤压造粒机的负荷;暂时无数据(石化盈科联系霍尼韦尔下装数据) 19、聚丙烯产品为仓储中心聚丙烯颗粒的包装量;暂时无数据
沙门氏菌的检验
沙门氏菌的检验 食品学院14食品质量与安全1班 刘文敏柳基炜卫杰恒温紫君 摘要:本实验采用GB/的检测方法测定鸡场中的沙门氏菌。通过本实验学习沙门氏菌的检测方法和技术,了解沙门氏菌的一些生化特性;本实验先用显色培养基找出可疑菌落,再做生化试验找出可疑的典型性的沙门氏菌,再通过血清学试验最终确定是否为沙门氏菌属。 关键词:沙门氏菌接种生化试验血清学鉴定 前言 沙门氏菌病是公共卫生学中具有重要意义的人畜共患病种之一,其病原沙门氏菌属于肠道细菌科。沙门氏菌是一个统称,泛指 2000 多种有紧密连系的细菌,包括引起食物中毒,导致胃肠炎、伤寒和副伤寒的细菌。虽然只有少数人因沙门氏菌而患病,但是,在世界范围内的细菌性食物中毒事件中,由沙门氏菌引起的占大多数。因此,采用科学、合理的方法检验食品中沙门氏菌,已经成为了人们最关心的问题之一[1]。国标法是目前中国规定的食品中沙门氏菌的标准检测方法,也是基层实验室普遍采用的检测方法,它根据沙门氏菌的生长特点和生化特性,采取前增菌、增菌、分离、生化试验和血清学鉴定5个步骤进行[2]。 1材料与方法 实验材料 均质器、三角烧瓶、平皿、玻璃棒、接种棒 恒温培养箱:36℃±1℃,42℃±1℃ 吸管:1 mL(具 mL刻度)、10mL(具刻度或微量移液器及吸头 电子天平PL602-S,梅特勒-托利多仪器(上海)有限公司; 手提式不锈钢压力蒸汽灭菌锅SYQ-DSX-280B,上海申安医疗器械厂 试剂药品 鸡肠、靛基质试剂、沙门氏菌O和H诊断血清、API20E生化试剂盒或VITEKGNI生化鉴定卡
培养基 蛋白胨水(BPW)、四硫磺酸钠煌绿(TTB)、亚硒酸盐胱氨酸(SC)增菌液、亚硫酸铋(BS)琼脂、HE琼脂、三糖铁琼脂、蛋白胨水、尿素琼脂、氰化钾、氰化钾对照、赖氨酸脱羧酶、赖氨酸脱羧酶对照、甘露醇、山梨醇、β-D半乳糖苷(ONPG)培养基 实验方法 培养基的制备 培养基的配制步骤 蛋白胨水(BPW):称取蛋白胨10g、氯化钠5g、磷酸氢二钠9g、磷酸二氢钠、蒸馏水1000ml,将各成分加入蒸馏水中,搅混均匀,静置约 10 min,煮沸溶解,调节 pH,高压灭菌 121 ℃,15 min。分装10瓶,每瓶90ml 四硫磺酸钠煌绿(TTB):高压灭菌 121 ℃,15 min灭菌冷却后至30℃,每100ml基础培养液加碘液2ml,煌绿液1ml 配制培养基的注意事项 (1)按照说明书上的用量进行换算,称取准确分量的合成培养基粉末; (2)加热煮沸溶解培养基时,留意锅内水位的变化,水位下降可再添加适量的水,以免水分蒸发过多,导致后面分装不够量; (3)往试管中放小导管时,注意处理气泡。 沙门氏菌群检测 2沙门氏菌检测操作步骤 前增菌 称取 10 g(mL)样品放入盛有 90 mL BPW的无菌均质杯中,以 8 000 r/min~10 000 r/min 均质1 min~2 min,或置于盛有90 mL BPW的无菌均质袋中,用拍击式均质器拍打 1 min~2 min。使用均质袋,可直接进行培养,于 36 ℃±1 ℃培养8 h~18h。 増菌 轻轻摇动培养过的样品混合物,移取 1 mL,转种于10mL TTB 内,于42℃±1℃培养18h~24h。同时,另取1mL,转种于10mL SC内,于36℃±1℃培养18 h~24h。 分离
沙门氏菌的检验
沙门氏菌的检验 2.2 恒温培养箱:36 ℃±1 ℃,42 ℃±1 ℃。 2.3 均质器。 2.4 振荡器。 2.5天平:感量0.1 g。 2.6 无菌锥形瓶:容量500 mL,250 mL。 2.7 无菌吸管:1 mL(具0.01 mL 刻度)、10 mL(具0.1 mL 刻度)或微量移液器及吸头。 2.8 无菌培养皿:直径90 mm。 2.9 无菌试管:3 mm×50 mm、10 mm×75 mm。 2.10 无菌毛细管。 2.11 pH 计或pH 比色管或精密pH 试纸。 3 培养基和试剂 3.1 缓冲蛋白胨水(BPW):见附录A 中A.1。 3.2 四硫磺酸钠煌绿(TTB)增菌液:见附录A 中A.2。 3.3 亚硒酸盐胱氨酸(SC)增菌液:见附录A 中A.3。 3.4 亚硫酸铋(BS)琼脂:见附录A 中A.4。 3.5 HE 琼脂:见附录A 中A.5。 3.6 木糖赖氨酸脱氧胆盐(XLD)琼脂:见附录A 中A.6。 3.8 三糖铁(TSI)琼脂:见附录A 中A.7。 3.9 蛋白胨水、靛基质试剂:见附录A 中A.8。 3.10 尿素琼脂(pH 7.2):见附录A 中A.9。 3.11 氰化钾(KCN)培养基:见附录A 中A.10。 3.12 赖氨酸脱羧酶试验培养基:见附录A 中A.11。 3.13 糖发酵管:见附录A 中A.12。 3.14 邻硝基酚β-D 半乳糖苷(ONPG)培养基:见附录A 中A.13。 3.15 半固体琼脂:见附录A 中A.14。 3.16 丙二酸钠培养基:见附录A 中A.15。 1 前增菌 称取25 g(mL)样品放入盛有225 mL BPW 的无菌均质杯中,以8 000 r/min~10 000 r/min 均质 1 min~ 2 min,或置于盛有225 mL BPW 的无菌均质袋中,用拍击式均质器拍打1 min~2 min。 2 增菌 轻轻摇动培养过的样品混合物,移取1 mL,转种于10 mL TTB 内,于42 ℃±1 ℃培养18 h~24h。同时,另取1 mL,转种于10 mL SC 内,于36 ℃±1 ℃培养18 h~24 h。 3 分离 分别用接种环取增菌液1 环,划线接种于一个BS 琼脂平板和一个XLD 琼脂平板(或HE 琼脂平板或沙门氏菌属显色培养基平板)。于36 ℃±1 ℃分别培养18 h~24 h (XLD 琼脂平板、
